不同劑量重組人生長激素治療對特發性矮小癥患兒身高、體重以及血清IGF-1和IGFBP-3表達的影響
郭艷艷,蔣成霞,姚 蘭,黃 煒
目前,在我國特發性矮小癥(ISS)的發病率約為3%,且呈逐年上升的趨勢,嚴重影響患兒的個性、自尊自信、認知發育能力和社交能力[1]。導致ISS的原因復雜,臨床應詳細詢問病史、進行全面體格檢查,并合理的選擇實驗室及特殊檢查,進行全面分析,從而做出診斷[2]。血清胰島素樣生長因子-1(IGF-1)和胰島素樣生長因子結合蛋白-3(IGFBP-3)隨年齡增長和發育而增高,且與營養、骨代謝等因素密切相關,是針對身材矮小兒童常用的特殊檢查指標[3]。重組人生長激素(r-hGH)是目前治療ISS的主要藥物,推薦劑量為0.1~0.2 U/(kg·d),但是劑量選擇尚無統一標準,選擇有效、安全的劑量方案具有重要的臨床意義[4]。因此,本研究觀察大劑量與小劑量r-hGH在ISS治療中的應用情況,現將研究結果報告如下。
1 資料與方法
1.1一般資料 回顧性分析2014年3月—2018年4月宜賓市第二人民醫院58例ISS患兒的臨床資料。①納入標準:所有患兒符合《諸福棠實用兒科學》中關于ISS的診斷標準[5];年齡6~12歲;就診前1個月無糖皮質激素、內分泌、免疫、抗生素治療史;患兒家屬均知情同意并簽署知情同意書。②排除標準:存在先天性畸形、染色體異常、宮內發育遲緩等疾病者;有明確全身性、營養性、消耗性或器質性疾病者;有嚴重心理、情感障礙疾病或攝食異常者;臨床資料不全者。按照r-hGH的應用劑量不同分為大劑量組31例和小劑量組27例。其中大劑量組男17例,女14例;年齡6~12(8.17±1.83)歲;青春Tanner分期:Ⅰ期20例,Ⅱ期11例。小劑量組男14例,女13例;年齡6~12(8.21±1.85)歲;青春Tanner分期:Ⅰ期18例,Ⅱ期9例。2組的性別、年齡、青春Tanner分期等一般資料比較差異無統計學意義(P>0.05),具有可比性。
1.2方法 2組均予以指導合理飲食以及補充鈣劑、維生素、微量元素等基礎營養治療。大劑量組在此基礎上予以r-hGH(長春金賽藥業股份有限公司,國藥準字:S10980102)0.2 U/(kg·d)每晚睡前皮下注射,注射部位取臍周、大腿中部前外側面,每次注射應更換注射點,持續治療12個月。小劑量組則將r-hGH劑量調整為0.1 U/(kg·d)每晚睡前皮下注射,其余同大劑量組。
1.3觀察指標 所有患兒通過電話、復診等方式隨訪12個月。于治療前及治療12個月后測定2組的身高、體重,并計算生長速度(GV)、身高標準差積分(Ht SDS),GV=(治療后身高-治療前身高)/間隔時間×12,Ht SDS=(實測身高值-同齡兒童身高的均值)/同齡兒童身高的標準差。于治療前及治療12個月后采集清晨空腹靜脈血6 ml,離心分離血清;采用西門子IMMULITE 2000-全自動化學發光免疫分析儀及配套試劑盒檢測血清IGF-1、IGFBP-3水平;采用羅氏cobas e 601電化學發光儀及配套試劑盒檢測血清骨代謝相關指標:Ⅰ型前膠原氨基端前肽(PⅠNP)、骨堿性磷酸酶(BAP)、Ⅰ型膠原交聯羧基末端肽(β-CTX)水平差異。觀察2組治療過程中的不良反應發生情況。
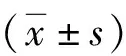
2 結果
2.1生長情況相關指標比較 治療前,2組身高、體重、GV、Ht SDS比較差異均無統計學意義(P>0.05)。治療后,2組身高、體重、GV、Ht SDS均較治療前明顯升高,且大劑量組明顯高于小劑量組(P<0.05)。見表1。
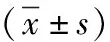
表1 2組ISS患兒治療前后身高、體重、GV、Ht SDS比較
注:ISS為特發性矮小癥,GV為生長速度,Ht SDS為身高標準差積分;與治療前比較,aP<0.05;與小劑量組比較,cP<0.05
2.2血清IGF-1、IGFBP-3水平比較 治療前,2組血清IGF-1、IGFBP-3水平比較差異均無統計學意義(P>0.05)。治療后,2組血清IGF-1、IGFBP-3水平均較治療前明顯升高,且大劑量組明顯高于小劑量組(P<0.05)。見表2。
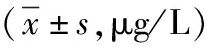
表2 2組ISS患兒治療前后血清IGF-1、IGFBP-3水平比較
注:ISS為特發性矮小癥,IGF-1為胰島素樣生長因子-1,IGFBP-3為胰島素樣生長因子結合蛋白-3;與治療前比較,aP<0.05;與小劑量組比較,cP<0.05
2.3骨代謝相關指標比較 治療前,2組血清PⅠNP、BAP、β-CTX水平比較差異均無統計學意義(P>0.05)。治療后,2組血清PⅠNP、BAP水平均較治療前明顯升高,且大劑量組高于小劑量組(P<0.05);2組血清β-CTX水平均較治療前明顯降低,且大劑量組明顯低于小劑量組(P<0.05)。見表3。
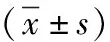
表3 2組ISS患兒治療前后血清PⅠNP、BAP、β-CTX水平比較
注:ISS為特發性矮小癥,PⅠNP為Ⅰ型前膠原氨基端前肽,BAP為骨堿性磷酸酶,β-CTX為Ⅰ型膠原交聯羧基末端肽;與治療前比較,aP<0.05;與小劑量組比較,cP<0.05
2.4不良反應發生情況比較 2組總不良反應發生率比較差異無統計學意義(P>0.05)。見表4。

表4 2組ISS患兒不良反應發生情況比較[例(%)]
注:ISS為特發性矮小癥
3 討論
ISS是指患兒身高較同種族、同年齡、同性別正常兒童平均身高低2個標準差,并排除先天性、器質性、內分泌系統疾病、染色體病、慢性系統性疾病、營養心理疾病等已明確病因導致的生長障礙[6]。ISS是一個排他性、描述性的分類,并不是一種特定的臨床診斷,故是小兒生長落后最常見的類型,約占矮小兒童的60%~80%[7]。
生長激素是由人垂體前葉分泌的具有促進除神經組織外其他組織生長、蛋白質合成、脂肪分解、微量元素吸收及抑制葡糖糖利用等作用的蛋白質激素[8]。r-hGH具有與內源性生長激素相似的作用,于2003年6月經美國FDA批準用于ISS的治療,國內外研究均已證實,r-hGH治療ISS安全、有效[9-11]。但目前臨床應用r-hGH劑量范圍較大,常用劑量是0.1~0.2 U/(kg·d),劑量選擇尚無統一標準,且不同劑量療效存在差異[12-13],故選擇有效、安全的用藥劑量具有重要臨床價值。本研究對58例r-hGH治療ISS患兒的臨床資料進行回顧性分析,發現治療12個月后,2組身高、體重、GV、Ht SDS均較治療前明顯升高,且大劑量組明顯高于小劑量組,表明r-hGH的促生長效應呈劑量依賴性,大劑量r-hGH促生長效果更優。
生長激素由垂體前葉合成、分泌,受生長激素釋放激素和生長抑素的雙重控制[14]。生長激素可直接作用于干骺端生長板上的軟骨細胞前體,促進細胞分化[15]。亦可通過生長激素-IGF-1軸對骨骼生長發揮調節作用,生長激素與肝臟等靶器官上的生長激素受體結合,合成IGF-1,IGF-1與IGFBP-3、酸不穩定亞單位形成三元復合物,進入血液循環,結合長骨骨干末端生長板軟骨細胞上的IGF-1受體,促進細胞分裂增殖[16-17]。本研究結果發現,治療12個月后,2組血清IGF-1、IGFBP-3水平均較治療前明顯升高,且大劑量組明顯高于小劑量組;顯示大劑量r-hGH對ISS患兒血清IGF-1、IGFBP-3水平的改善作用優于小劑量r-hGH,更有利于促進患兒骨骼的生長。本研究對ISS患兒的骨代謝指標分析也發現,治療12個月后,2組血清PⅠNP、BAP水平均較治療前明顯升高,且大劑量組明顯高于小劑量組;2組血清β-CTX水平均較治療前明顯降低,且大劑量組明顯低于小劑量組;顯示r-hGH治療ISS有助于加快患兒骨形成及骨吸收速度,促使機體呈高轉換狀態,骨形成大于骨吸收,骨量累積,從而有效促進骨骼生長,且大劑量r-hGH促進生長效果更為顯著。此外,本研究還顯示,2組總不良反應發生率比較差異無統計學意義;表明相較于0.1 U/(kg·d)r-hGH,0.2 U/(kg·d)r-hGH治療ISS并未增加不良反應發生率,且不良反應皆在可控范圍內,安全性良好。
綜上所述,0.2 U/(kg·d)r-hGH可有效促進ISS患兒生長,改善患兒血清IGF-1、IGFBP-3水平和骨代謝,效果優于0.1 U/(kg·d)r-hGH,且安全性良好。

