基于證據推理和模型認知的《酚》教學案例
麥達勤

一、教學現狀分析
目前《苯酚》教學主要有以下做法:其一是老師讓學生自主設計實驗,后讓學生在探究中獲取苯酚性質。其二是老師引導學生分析簡單苯酚的結構,然后快速進入苯酚的實驗,從實驗中得到苯酚的性質。教學上缺乏對苯酚結構的深入分析、宏微結合層層遞進的證據推理,沒有凸顯苯酚在有機物教學中的獨特作用,學生未能有效建構有機物認知模型。
二、教學思想與創新點
其一,在教學過程中抓住宏微結合的認識方式,基于球棍模型實物及圖像,分析有機物微觀結構,不斷滲透微粒動態觀。其二,借助實驗激發學生興趣,同時為學生提供有機物性質描述或推理的證據素材。其三,教學過程關注有機物分子結構分析模型的建構。
三、教學目標
1.通過觀察苯酚樣品及相關實驗,能夠有序說出苯酚的主要物理性質。
2.通過分析苯酚的結構特點,及與乙醇和苯進行比較預測苯酚的性質,再通過事實驗證預測是否正確。
3.感受基團之間的相互影響,基于甲苯和苯的性質對比,對苯酚和苯的性質進行遷移,再次豐富“結構決定性質、性質反映結構”的學科思想。
四、教學流程
五、教學實錄
環節一苯酚的物理性質
【引導】請同學們觀察試劑瓶的苯酚,歸納苯酚的物理性質(顏色、狀態、氣味)。
【設疑】乙醇與水任意比例互溶,苯難溶于水,苯酚在溶解性上有什么特點呢?
【演示實驗】如下表。
【回顧課本】閱讀課本P52,了解苯酚的溶解度。
環節二苯酚的結構及性質預測
【學生活動】請完成下表,并說出你預測苯酚化學反應中斷鍵位置的依據。
【學生】苯環上的C-H可斷開,依據是苯可以斷C-H;C-O和O-H鍵可斷開,依據是乙醇可斷開C-O和O-H鍵可斷開;苯環中碳碳鍵可斷開,依據是苯可以跟氫氣加成,斷大π鍵。
【過渡】在學習甲苯的性質時,我們對比甲烷和甲苯的性質,發現苯環可以使甲基更活潑,甲基更容易發生反應,那苯酚的羥基和苯環也會互相影響嗎?
環節三認識苯酚的酸性,了解苯環對羥基的影響
【引導】剛才我們在預測斷鍵位置時,苯酚的O—H鍵可斷開,苯環可能對O—H鍵有影響,苯酚能與氫氧化鈉反應嗎?請完成以下實驗。
【小結】當-OH與苯環相連時,電離出H+,說明苯酚有酸性。
【思考】設計實驗比較鹽酸和苯酚溶液酸性的強弱?
【思考】設計實驗比較苯酚和碳酸的酸性的強弱?
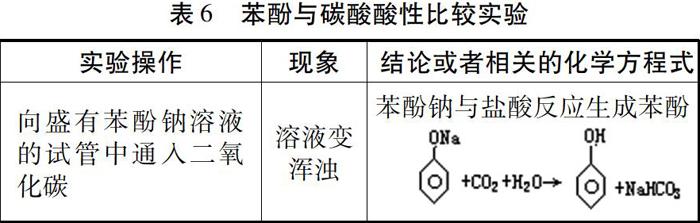
【學生問題】苯酚鈉溶液與二氧化碳反應,是生成碳酸鈉還是碳酸氫鈉。
【關鍵突破】往苯酚的乳濁液中加入碳酸鈉溶液,乳濁液變澄清,說明苯酚和碳酸鈉不能大量共存,這兩種產物不可能同時出現,所以苯酚鈉溶液與二氧化碳反應,是生成碳酸氫鈉。
【小結】酸性:鹽酸>苯酚>碳酸
【思考】同樣是含有羥基,乙醇水溶液呈中性,而苯酚水溶液呈弱酸性,為什么?
【師生討論分析】對比苯酚和乙醇分子的結構,其不同點在于苯酚分子的羥基與苯環相連,而乙醇分子的羥基與乙基相連。苯酚的羥基受苯環的影響,苯環使O-H共價鍵更易斷開,電離出H+,使苯酚顯酸性。
環節四認識苯酚的取代反應,了解羥基對苯環的影響
【過渡】苯環對-OH的影響使O-H的共價鍵更容易斷開,那么-OH對苯環有影響嗎?
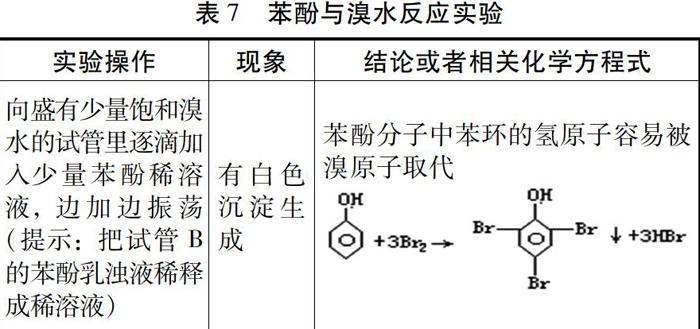
【實驗】苯酚和濃溴水的反應,如下表。
【小結】苯酚與濃溴水反應生成的三溴苯酚是一種難溶于水但易溶于有機溶劑的固體
【思考】苯酚與溴的取代反應、苯與溴的取代反應相比,那個反應更容易進行?為什么?
【用途】苯酚與溴的反應很靈敏,可用于苯酚的定性檢驗和定量測定。
環節五了解苯酚的特性
【用途】苯酚的定性檢驗還可以利用苯酚的顯色反應:苯酚遇FeCl3溶液,溶液呈紫色。
六、教學效果與反思
1.突出重點,不面面俱到;有所為,有所不為
本節課重點是突破苯酚的化學性質。有關苯酚、鹽酸、碳酸、碳酸氫根的酸性強弱的比較,若讓學生設計自主探究實驗,難度太大,會沖淡了本節課的主題,可以在復習課再展開。
2.利用“實驗和實物模型”突破重點
本節課是比較典型的元素化合物課,通過觀察苯酚外觀,開展相關實驗等活動獲得宏觀反應事實的認識;通過書寫化學或離子方程式獲得符號表征;運用理論模型獲得微觀認識。
3.注重學習方法的梳理和指導
其一,學習有機物的一般程序:結構——性質——用途。其二,有機化學的基本思維方法:“結構決定性質,性質反映結構”是有機化學的核心思維方法;“類比遷移、歸納推理”是自然科學的基本思維方法。
4.注重學生化學核心素養的培養
教學中融入化學學科核心觀念,注重學生宏觀辨識與微觀探析、證據推理與模型認知等學科核心素養的培養,促進學生建構有機化合物微觀—宏觀、孤立—系統、靜態—動態的認識方式。
責任編輯 徐國堅

