脫泛素酶OTUD7B調控腫瘤微環境和腫瘤進程的分子機制*
林丹丹, 申 陽, 解 欣, 2, 史建紅△
(1河北大學附屬醫院實驗中心, 河北省腫瘤放化療機制與規程研究重點實驗室, 2河北大學醫學院, 河北 保定 071000)
泛素化(ubiquitination)是一種蛋白質翻譯后修飾過程,泛素(ubiquitin)以共價連接的方式形成多聚泛素鏈并結合到靶蛋白賴氨酸(lysine,K)殘基上,該過程由泛素激活酶(ubiquitin-activating enzymes,UBE,E1)、泛素結合酶(ubiquitin-conjugating enzymes,UCE,E2)和泛素連接酶(ubiquitin ligases,E3)順序激活[1]。經典的泛素化調節方式是通過泛素-蛋白酶體系統(ubiquitin-proteasome system,UPS)介導蛋白質降解而實現對靶蛋白含量的精確調控[2-3]。隨著人們對泛素化認識的不斷深入,除了UPS介導的蛋白質降解和更新外,泛素化還可通過非降解機制調節細胞功能,如K63-和M1 (Met1)-多聚泛素鏈可形成細胞內反應的平臺,參與激酶活化和細胞內信號轉導[4-5]。泛素化是一個可逆的動態過程,受到E3和脫泛素酶(deubiquitinase,DUB)的共同調節[6]。OTUD7B(OTU domain-containing 7B)是一種多功能脫泛素酶,介導K11-、K48-和K63-多聚泛素鏈解離,在生長發育、免疫應答和惡性腫瘤等生理病理過程中發揮重要作用。
1 OTUD7B與脫泛素調節
1.1OTUD7B的基因結構和特點 OTUD7B是OTU脫泛素酶超家族成員。通過晶體結構分析發現,OUT超家族蛋白在氨基酸序列上與其他類的脫泛素化酶有較大差異,該家族蛋白核心區域由2個螺旋結構和5個β-折疊組成。不同的OTU 家族成員其OTU結構域大小不同,但均已被證實具有脫泛素酶活性[7-8]。OTU家族的共同結構特點為:含有OTU結構域、泛素相關(ubiquitin-associated,UBA)結構域、Npl4鋅指(Npl4 zinc finger)結構域和 A20樣鋅指(A20-like zinc finger)結構域。
OTUD7B的分子結構包括 UBA、OTU、cytadhesin P30/P32和A20樣鋅指結構域,見圖1。現已知UBA結構域不直接影響OTUD7B的脫泛素酶活性,但可介導K63-多聚泛素鏈解離,影響NF-κB信號通路[9];OTU結構域發揮主要的DUB活性[10];cytadhesin P30/P32結構域參與細胞黏附;A20樣鋅指結構域參與泛素鏈結合。
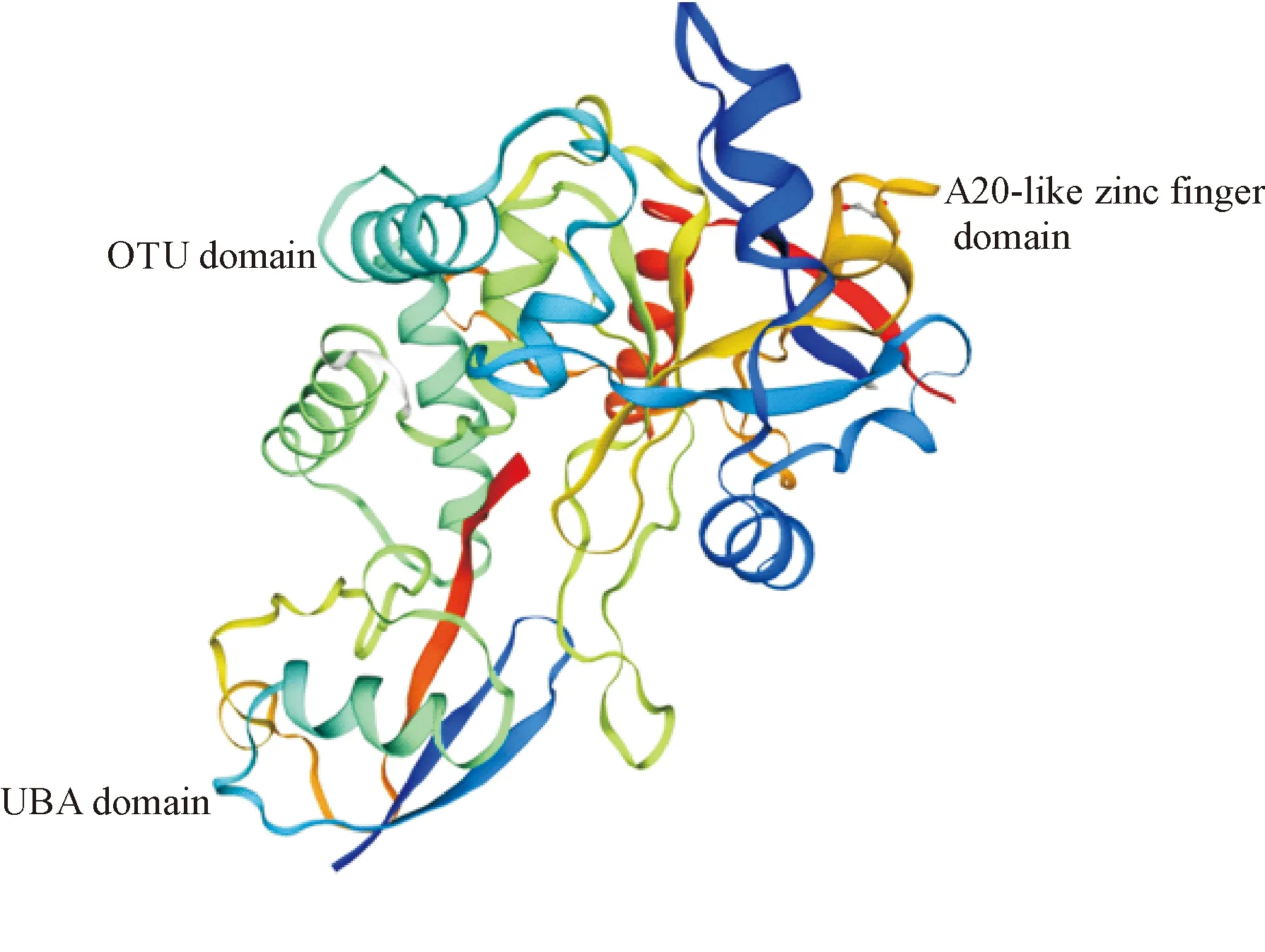
Figure 1.The structure of OTUD7B.
圖1 OTUD7B分子結構示意圖
1.2OTUD7B催化K11-、K48-和K63-多聚泛素鏈水解 根據泛素連接方式不同,多聚泛素鏈共有8種類型:K6-、K11-、K27-、K29-、K33-、K48-、K63-和M1-多聚泛素鏈。K48-泛素化主要介導靶蛋白通過UPS降解,調節細胞內蛋白質的穩定性;K63-泛素鏈通過非降解機制介導細胞內信號傳遞;K11-多聚泛素鏈的功能研究目前尚不十分清楚。體外實驗證實,OTUD7B可特異性靶向K11-多聚泛素鏈,催化K11-脫泛素化過程[11]。晶體結構分析顯示,K11-泛素鏈可結合OTUD7B的酶催化S1位點OTUD7B[12]。OTUD7B通過調節HIF-1α分子K11-脫泛素化,抑制缺氧誘導因子1α(hypoxia-inducible factor-1α,HIF-1α)通過UPS非依賴途徑降解[13]。OTUD7B也可與UBE2S/E2-EPF和UBE2C/UbcH10共同調節有絲分裂后期促進復合體(anaphase-promoting complex,APC/C)的K11-多聚泛素鏈的脫泛素化和泛素化過程,影響其穩定性,參與細胞周期調控和內質網相關降解(endoplasmic reticulum-associated degradation,ERAD)[14-17],見圖2。
盡管體外實驗和晶體實驗數據顯示,與其他7種泛素鏈相比,OTUD7B更容易結合并水解K11-多聚泛素鏈,一些細胞實驗證實OTUD7B也可靶向細胞內蛋白的K48-和K63-多聚泛素鏈,促進靶蛋白脫泛素化并調節細胞信號轉導[18]。OTUD7B還可直接作用于E3連接酶,催化腫瘤壞死因子受體相關因子3(tumor necrosis factor receptor-associated factor 3,TRAF3)的K48-多聚泛素鏈解離,抑制TRAF3通過UPS降解[10]。在低氧條件下,OTUD7B可以誘導TRAF6分子K63-脫泛素化,調節NF-κB活化。TNFα可刺激OTUD7B募集到TNFR并催化K63-多聚泛素鏈與RIP解離[18]。OTUD7B也可以使GβL發生K63-脫泛素化,促進哺乳動物雷帕霉素靶蛋白(mammalian target of rapamycin, mTOR)復合體2(mTOR complex 2, mTORC2)的穩態和活性[19],見圖2。
2 OTUD7B與腫瘤的發生發展
2.1OTUD7B誘導乳腺癌增殖和耐藥 OTUD7B在不同腫瘤中的作用不盡相同。OTUD7B在乳腺癌中高表達,并被證實與乳腺癌高侵襲性相關[20]。OTUD7B可催化乳腺癌細胞的表皮生長因子受體(epidermal growth factor receptor,EGFR)脫泛素化,抑制EGFR通過UPS降解,促進乳腺癌細胞增殖和存活[20]。在三陰性乳腺癌(triple-negative breast can-cer,TNBC)中,OTUD7B可通過負調節NF-κB-Lin軸,導致微小RNA(microRNA,miRNA,miR)let-7介導的caspase-3下調,促進乳腺癌高侵襲性和紫杉醇耐藥[21]。
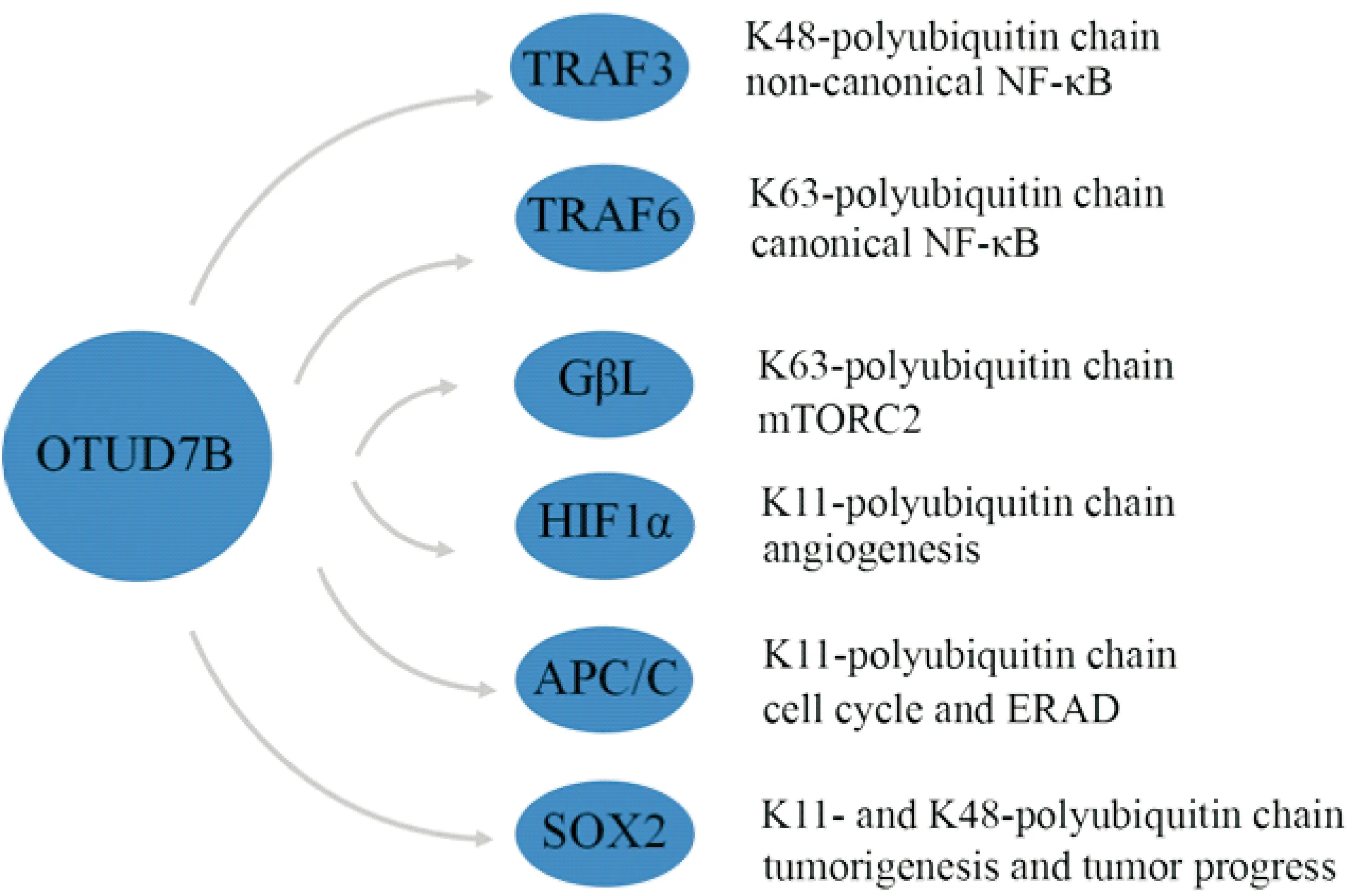
Figure 2.OTUD7B catalyzes deubiquitination.
圖2 OTUD7B催化的脫泛素化過程
2.2OTUD7B在肝癌中的作用 與乳腺癌不同,在肝細胞癌(hepatocellular carcinoma,HCC)的研究發現,OTUD7B在HCC的表達水平明顯低于癌旁肝組織。OTUD7B水平越低的肝癌患者,其腫瘤越大、臨床分期越高、組織分化程度往往較低并伴有淋巴結轉移,血管侵襲能力增加,伴有早期復發,預后較差[22]。OTUD7B可通過誘導上皮-間充質轉化,抑制肝癌細胞的遷移和侵襲[23]。
2.3OTUD7B與肺癌 OTUD7B在肺癌中的表達和作用機制目前仍不十分清楚。有研究顯示,OTUD7B抑制H157非小細胞肺癌細胞株的NF-κB核轉位發揮抑癌作用,參與紫杉醇和MEK抑制劑U0126聯合作用誘導的H157細胞死亡[24]。OTUD7B基因敲除小鼠用KRAS誘導的自發性肺癌發生率顯著下降[19]。OTUD7B在肺腺癌組織中高表達,OTUD7B表達水平與肺癌的不良預后呈正相關[25]。
2.4OTUD7B與其他腫瘤 OTUD7B在其他腫瘤中的作用尚未明確,但有研究表明,OTUD7B通過其脫泛素化修飾,調節性別決定區Y框蛋白2(sex determining region Y-box 2,SOX2)的穩定性[26]。SOX2在乳腺癌、肺癌、胃腸道腫瘤、皮膚腫瘤、前列腺癌、中樞神經系統等多種類型腫瘤中表達均上調,參與腫瘤生長、轉移等過程,與不良預后及化療耐藥相關,因此,OTUD7B可能通過調節SOX2的穩定性調控多種類型腫瘤進程[27]。
3 OTUD7B對腫瘤功能的調控
3.1促進腫瘤生長和轉移 EGFR信號活化過程往往伴隨一些E3泛素酶,如CBL,迅速結合活化的EGFR并介導EGFR通過UPS降解,從而快速終止EGFR信號的持續活化[28]。OTUD7B通過其OTU結構域催化EGFR脫泛素化,抑制EGFR降解,促進EGFR下游分子持續活化[20]。在宮頸癌HeLa細胞和乳腺癌MDA-MB-468細胞中,EGF刺激OTUD7B與EFGR結合并抑制EGFR泛素化降解,增強乳腺癌細胞增殖和遷移,促進腫瘤的生長和侵襲[20]。
胰島素樣生長因子受體(insuline-like growth factor receptor,IGFR)激活下游磷脂酰肌醇3-激酶(phosphatidylinositol 3-kinase,PI3K)-絲氨酸/蘇氨酸蛋白激酶(protein kinase B,PKB,即AKT) 1-mTOR通路和MAPK通路,調節腫瘤細胞增殖、凋亡和存活。IGFR泛素化和脫泛素化的動態平衡對IGF信號途徑的觸發和終止調節也至關重要[29]。肺腺癌組織中,OTUD7B和IGFR表達呈正相關[25],提示OTUD7B可能是調節IGFR信號通路的一種重要分子,其分子作用機制尚待進一步研究。
轉錄因子SOX2主要經Shh、Wnt、成纖維細胞生長因子受體(fibroblast growth factor receptors,FGFR)和轉化生長因子β(transforming growth factor beta,TGF-β)信號通路活化,誘導下游促細胞存活、生長、增殖基因的轉錄[30]。泛素連接酶和脫泛素酶共同調節SOX2的穩定性,從而影響腫瘤干細胞的特性,促進多種腫瘤的生長、侵襲和轉移能力,影響預后轉歸[26]。
3.2促進腫瘤發生 mTOR是細胞生長和多條代謝途徑調節的關鍵分子。mTOR可形成2種復合物:mTORC1和mTORC2[31-32]。mTORC1對雷帕霉素敏感,能磷酸化S6K1和4E-BP1促進蛋白質翻譯[33];mTORC2主要響應細胞外生長因子信號通路,如PI3K信號。OTUD7B通過靶向mTORC1和mTORC2共有成分GβL分子K63-多聚泛素鏈,催化GβL脫泛素化,引發mTORC1解離,促進mTORC2形成,激活下游Akt信號,促進腫瘤發生[19]。
3.3細胞周期的調節 細胞分裂增殖的過程中,APC/C作為一種E3連接酶,促進有絲分裂細胞周期蛋白的降解,調節周期依賴性蛋白激酶(cyclin-dependent kinase,CDK)活性,控制細胞周期依賴性鈣振蕩(cell cycle-dependent calcium oscillation)[15, 34]。OTUD7B可拮抗APC/C的泛素化作用,催化K11-多聚泛素鏈解離,抑制APC/C介導的有絲分裂進程和微核形成,抑制腫瘤細胞增殖[16]。
4 OTUD7B調節腫瘤微環境
4.1經典NF-KB信號影響腫瘤發生發展 泛素化和脫泛素化調控在NF-κB信號激活的多個環節中發揮調節作用[4, 35-37]。非小細胞肺癌細胞株H157中,OTUD7B抑制NF-κB核轉位,降低IL-8和ICAM-1表達。耐藥基因DJ-1結合OTUD7B并抑制其脫泛素酶活性[24]。在缺氧條件下,OTUD7B可抑制RelA磷酸化和TRAF6泛素化,抑制NF-κB核轉位,減少缺血再灌注反應中的炎癥和損傷[38]。TNF-α誘導HEK293細胞和人臍靜脈血管內皮細胞中OTUD7B表達,OTUD7B通過其OTU結構域催化K48-和K63-脫泛素化,負反饋抑制TNFα誘導的IKK活化、IκBα磷酸化降解和NF-κB核轉位[18]。
4.2非經典NF-κB信號調節免疫反應 與經典NF-κB不同,非經典NF-κB信號途徑主要調節免疫系統功能[39]。非經典NF-κB激活主要表現為抑制性蛋白的降解:非激活狀態下,TRAF3與TRAF2-cIAP1/2形成E3復合體,降解非經典NF-κB途徑關鍵激酶——NF-κB誘導激酶(NF-κB-inducing kinase,NIK);信號激活時,TRAF3等抑制性蛋白被泛素化降解,NIK的抑制解除,NIK活化并向下傳遞細胞信號[37]。OTUD7B可通過其N-端UBA結構域結合TRAF3并催化其K48-脫泛素化,抑制TRAF3進入UPS降解途徑[10]。OTUD7B基因敲除的小鼠中,B淋巴細胞發生抗原超應答,小腸黏膜淋巴濾泡增生,對腸道細菌Citrobacterrodentium的防御能力增強[10]。OTUD7B通過調節TRAF3穩定性參與機體免疫調節,有望成為針對黏膜免疫治療和非經典NF-κB信號相關疾病治療的新靶點。
4.3調節腫瘤血管新生 惡性實體腫瘤的生長過程面臨著氧氣和營養需求不斷增長和供應不足的矛盾。當供氧不足時,HIF-1α亞基泛素化降解受到抑制,其細胞內蛋白水平迅速升高,啟動新的轉錄調控程序上調各種促血管新生因子的表達,促進細胞存活,加速腫瘤新生血管形成[40-41]。OTUD7B可結合HIF-1α并促進其K11-脫泛素化,維持HIF-1α蛋白穩定性,影響 HIF-1α介導的基因轉錄[13]。盡管HIF-1α和HIF-2α在基因序列上有很多相似性,但在組織分布和功能特性上有著明顯的差異[42]。OTUD7B并不能直接調節HIF-2α蛋白水平,而是通過調控其上游轉錄因子E2F1的脫泛素化,維持E2F1穩定性,間接調控HIF-2α基因轉錄[43]。
4.4T細胞免疫反應和T細胞功能的調節 T細胞在抗感染和抗腫瘤免疫反應中發揮重要作用。外界抗原通過T細胞受體(T-cell receptor,TCR)激活初始T細胞(naive T cells),啟動T細胞分化[44]。在TCR與配體結合活化后,OTUD7B可迅速募集到TCR信號核心分子酪氨酸激酶Zap70上并使其發生脫泛素化,從而抑制Zap70泛素化,阻止負性調節的磷酸酶Sts1和Sts2與Zap70相互作用,促進Zap70磷酸化和TCR信號轉導,從而促進T細胞活化和T細胞介導的免疫反應和自身免疫反應[45]。
5 總結
OTUD7B是一種重要的脫泛素酶,通過靶向K11-、K48-和K63-連接的多聚泛素鏈,特異性調控底物蛋白的泛素化水平,參與細胞增殖、炎癥反應、腫瘤血管生成和抗腫瘤免疫等多種信號轉導途徑的調節(表1),在肺癌、乳腺癌和肝癌等惡性腫瘤發生發展中發揮重要作用。OTUD7B的表達模式和作用機制受到局部細胞和組織內環境的影響,深入認識OTUD7B調控細胞生物學行為的分子機理,尋找其影響惡性腫瘤進程的組織特異性機制,有助于揭示惡性腫瘤泛素化調節的內在規律,為開發靶向OTUD7B的抗腫瘤治療藥物提供有力的線索和依據。
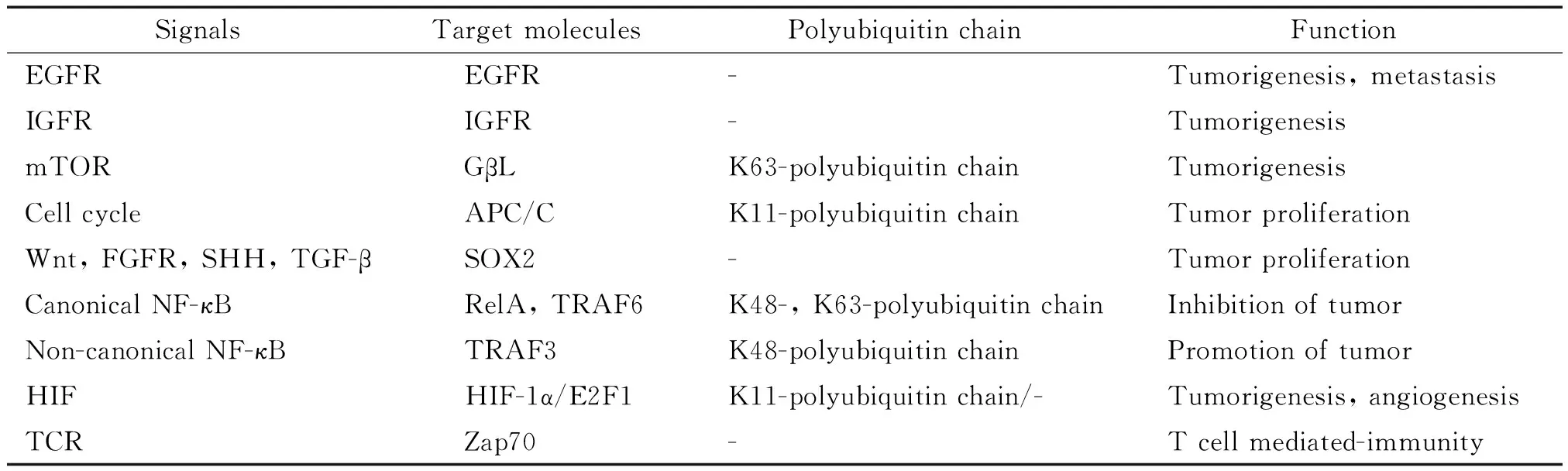
表1 OTUD7B介導的腫瘤相關信號通路

