連續胸椎旁神經阻滯對乳腺癌術后疼痛綜合征的影響*
靳紅緒 張同軍 孫學飛 張 華 王福朝 呂東海 姚長青 王忠義
(河北省衡水市哈勵遜國際和平醫院麻醉科,衡水053000)
乳腺癌術后疼痛綜合征(post-mastectomy pain syndrome, PMPS)是發生于乳腺癌術后的一種慢性神經病理性疼痛,指繼發于手術急性疼痛之后,在胸部、腋窩、上臂及肩部出現的慢性疼痛,并且超過3 個月以上[1,2]。PMPS 是乳腺癌根治術后的主要并發癥之一,其發病率高達20%~52%[3~5],PMPS 可持續數年,嚴重影響了病人術后的生活質量,增加了病人的經濟負擔并帶來一系列嚴重的社會問題[6]。有研究認為有效地治療乳腺癌術后急性疼痛可以很大程度上預防PMPS 的發生[7]。近年來,隨著超聲引導技術在區域麻醉中的逐步普及,胸椎旁神經阻滯(thoracic paravertebral block, TPVB)逐漸應用于乳腺癌根治術中及術后鎮痛中。本研究通過將超聲引導下連續胸椎旁神經阻滯應用于乳腺癌切除術病人圍術期鎮痛,評價其對術后PMPS 的影響,旨在為預防乳腺癌切除術病人PMPS和術后疼痛治療提供新的思路和方法。
方 法
1.一般資料
本研究方案經哈勵遜國際和平醫院醫學倫理委員會批準,所有病人均簽署知情同意書。選擇2015年1 月至2017 年3 月,在本院擬行單側乳腺癌根治術的女性病人206 例,年齡32 ~76 歲,體質量指數 (BMI) 17.3 ~34.5 kg/m2, ASA 分級Ⅰ或Ⅱ級。采用計算機隨機數字表法,將其隨機分為兩組:連續胸椎旁神經阻滯聯合全麻組(PG 組)和單純全麻組 (GA 組)。8 例因術后失聯未能完成隨訪而被剔除,完成全部受試及隨訪共198 例,PC 組102例,PA 組 96 例。
排除標準:慢性疼痛病史及長期服用鎮痛藥物者;穿刺部位存在感染;嚴重脊柱畸形或有開胸手術史者;酰胺類局麻藥過敏史;心、腦、肝、腎等重要臟器功能不全;凝血功能障礙;精神和神經系統疾患;術后發生感染及二次手術者。
2.方法
所有病人常規禁飲禁食,無術前用藥。入室后開放外周靜脈通路,常規監測心率 (HR)、脈搏血氧飽和度 (SpO2)、心電圖 (ECG)、呼氣末二氧化碳 (PETCO2)和腦電雙頻譜指數 (BIS)。GA 組行常規全麻誘導:依次靜脈注射咪達唑侖0.03 mg/kg,芬太尼3 μg/kg,丙泊酚1.5 mg/kg 及順式阿曲庫銨0.15 mg/kg。喉罩置入成功后連接麻醉機行機械控制通氣。PG 組首先在超聲(Terason 3000 +二維超聲顯像儀,25 mm 高頻線陣探頭,頻率6 ~13 MHz)引導下行術側肋間入路T3椎旁神經阻滯并置管。取側臥位,患側在上,觸摸確定骨性標志并標記擬穿刺節段上下的棘突,定位T3椎間隙,常規消毒鋪巾,將探頭在T3水平旁矢狀切面沿肋間上下移動探頭掃查,將探頭放置在兩根肋骨之間,避開肋骨在超聲下可見橫突、肋橫突韌帶和胸膜,橫突和其外側與胸膜圍成的空間即為胸椎旁間隙。采用18 G Touchy 穿刺針在探頭外側進針,進針過程保持穿刺針在超聲影像中全程可見,針尖抵達肋橫突韌帶,嘗試推注2 ml 生理鹽水,確認針尖所在位置,緩慢進針突破肋橫突韌帶,回抽無血和腦脊液后注射0.5%的鹽酸羅哌卡因20 ml,可見壁層胸膜因藥物注入向下受壓,椎旁間隙擴張,即可確認針尖到達理想部位。注藥完畢后退出針芯向胸椎旁間隙置入導管約3 cm,皮下隧道妥善固定導管。測定阻滯平面(以痛覺或溫度覺減退范圍不小于T2-T5為阻滯成功),阻滯失敗的剔除實驗組。起效15 min 后開始全麻誘導,方法同GA 組。麻醉維持兩組均以1%丙泊酚靜脈靶控輸注(效應室濃度2 ~3 μg/ml),間斷靜注芬太尼,術中維持BIS 值在45 ~60 之間。若切皮后HR、MAP 明顯升高,每次追加芬太尼0.15 μg /kg,維持病人HR、MAP 波動范圍在基礎值的±20%內,必要時酌情給予去甲腎上腺素或烏拉地爾。縫皮時停止輸注丙泊酚,病人蘇醒后拔出喉罩送麻醉恢復室 (PACU) 繼續觀察。
GA 組采用病人自控靜脈鎮痛 (patient controlled intravenous analgesia, PCIA):舒芬太尼 2 μg/kg +地佐辛0.3 mg/kg +阿扎司瓊30 mg +生理鹽水至250 ml,背景輸注劑量 5.0 ml/h,PCA 劑量 3.0 ml,鎖定時間15 min。PG 組病人采用連續胸椎旁神經自控鎮痛 (patient controlled thoracic paravertebral analgesia,PCPA):0.2%羅哌卡因250 ml,背景劑量5.0 ml/h,PCA 3.0 ml,鎖定時間15 min。術后疼痛管理的目標是確保病人術后 NRS<4 分,當 NRS ≥ 4 分時則給予地佐辛5 mg 靜脈注射進行補救鎮痛。
3.觀察指標
記錄術中芬太尼和丙泊酚的用量、術后48 h 鎮痛泵有效按壓次數、補救鎮痛例數、鎮痛滿意率情況(若病人術后NRS<3 分認為術后鎮痛滿意)。記錄術后嗜睡、惡心嘔吐 (PONV) 和尿潴留等不良反應發生情況。隨訪并復查術后3、6、12 個月時病人PMPS 的發生情況。PMPS 的診斷可參照文獻[8]及國際疼痛學會的標準,從疼痛部位、疼痛性質和疼痛時間三個方面評估:疼痛部位多位于術側腋窩、上肢及肩部受損神經所支配的區域,主要為前胸,其次是腋窩、手臂;疼痛性質多為麻木、電擊痛、燒灼痛、針刺痛,并可出現與幻肢痛類似的乳房幻覺痛;疼痛可在術后即刻出現,一般長達2個月以上,多呈間歇性發作。使用NPS 量表[9]進行神經病理性疼痛的篩查,包含相關癥狀、疼痛特征、痛覺過敏及蟻走感4 個方面共10 個問題,每個問題記1 分,總分4 分以上即可診斷為PMPS。
4.統計學分析
采用SPSS 22.0 統計學軟件進行處理。正態分布的計量資料采用均數±標準差±SD)表示,組間比較采用獨立樣本t檢驗,偏態分布可采用Mann-Whitney U 檢驗;計數資料組間比較采用X2檢驗。P<0.05 為差異有統計學意義。
結 果
1.兩組病人一般情況和圍術期資料的比較
本研究起始共納入206 例乳腺癌病人,8 例因術后失聯未能完成隨訪而被剔除。完成全部受試及隨 訪 的 198 例 病 人,PG 組 102 例,GA 組 96 例。兩組病人年齡、BMI、ASA 分級、手術時間、術中失血量等一般情況差異均無統計學意義(P>0.05)。PG 組術中丙泊酚用量和芬太尼用量明顯少于GA組(P<0.05,見表 1)。
表1 兩組病人一般情況和圍術期資料的比較±SD)Table1 Comparison of general information and perioperative data between groups ±SD)
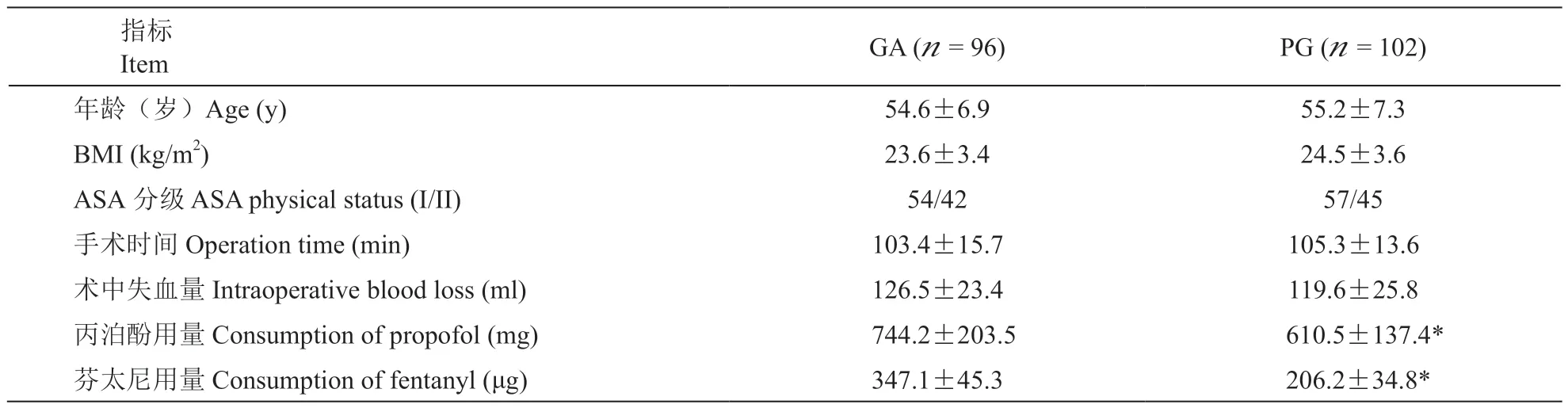
表1 兩組病人一般情況和圍術期資料的比較±SD)Table1 Comparison of general information and perioperative data between groups ±SD)
*P < 0.05,與 GA 組比較;*P < 0.05, compared with group GA.
GA (n = 96) PG (n = 102)年齡(歲)Age (y) 54.6±6.9 55.2±7.3 BMI (kg/m2) 23.6±3.4 24.5±3.6 ASA 分級 ASA physical status (I/II) 54/42 57/45手術時間 Operation time (min) 103.4±15.7 105.3±13.6術中失血量 Intraoperative blood loss (ml) 126.5±23.4 119.6±25.8丙泊酚用量 Consumption of propofol (mg) 744.2±203.5 610.5±137.4*芬太尼用量 Consumption of fentanyl (μg) 347.1±45.3 206.2±34.8*指標Item
2.兩組病人術后鎮痛情況的比較
PG 組術后48 h 內鎮痛泵有效按壓次數、補救鎮痛例數均顯著少于GA 組,術后鎮痛滿意率顯著高于GA 組(P<0.05,見表2)。PG 組病人術后嗜睡、PONV及尿潴留等不良反應的發生率分別為0(0 例)、2.9%(3 例)和 0(0 例),明顯低于 GA 組的13.5%(13 例)、27.1%(26 例)、和10.4%(10 例)(P<0.05)。
表2 兩組病人術后鎮痛情況的比較±SD)Table2 Comparison of postoperative analgesia between groups (±SD)

表2 兩組病人術后鎮痛情況的比較±SD)Table2 Comparison of postoperative analgesia between groups (±SD)
*P<0.05,與 GA 組比較;*P<0.05, compared with group GA.
鎮痛滿意率(%)Satisfaction rate of analgesia GA 96 14.6±5.6 9 (9.4) 78.5 PG 102 2.5±1.2 * 2 (2.0) * 95.1*組別Group例數Cases有效按壓次數(次)Effective compression times (time)補救鎮痛例數 [n (%)]Remedy for analgesia
3.兩組病人術后PMPS 發生情況的比較
PG 組病人術后3、6、12 個月PMPS 的發病率明顯低于 GA 組(P<0.05,見表3)。

表 3 兩組病人術后PMPS 發生情況的比較[n (%)]Table 3 Comparison of postoperative incidence of PMPS between groups [n (%)]
討 論
乳腺癌術后病人常常經歷中度以上的急性疼痛,這是由于手術操作導致乳腺周圍組織和胸壁神經損傷,痛覺信號經傳導通路到達相應的腦皮質區域產生痛覺。乳腺癌術后的急性疼痛若控制不佳,可引起外周傷害性感受器持續受到刺激,促使損傷組織產生炎性介質和致痛因子,形成外周敏化,繼而使脊髓背角神經元發生可塑性改變,產生中樞敏化和PMPS 的發生[10]。PMPS 的病因和機制尚不完全明確,影響因素很多,涉及圍術期的各個階段,目前主要觀點是乳房切除術后對肋間神經的損傷引起的肋間神經痛,同時手術類型,尤其是全腋窩淋巴結清掃、放療、化療、年齡、術后急性疼痛的管理等均是引起PMPS 的重要危險因素[11]。其中,術后急性疼痛的嚴重程度是導致術后疼痛慢性化重要風險因素,因此,通過直接降低風險因素或間接控制敏感因素來阻止術后急性疼痛向PMPS 轉化,從而降低PMPS 的發病率,改善病人預后。
PMPS 屬于慢性神經病理性疼痛,而慢性疼痛的發生發展與急性期疼痛的管理有關,最常見的慢性疼痛是由急性術后疼痛管理不當引起的。Borghi等[12]研究發現,圍手術期積極有效地控制疼痛可以顯著降低PMPS 的發病率。近年來,以區域神經阻滯為代表的多模式鎮痛技術受到了臨床的廣泛推崇,并成為多模式鎮痛的重要手段。超聲引導下TPVB 通過局麻藥直接作用于肋間神經、脊神經后支、脊膜返支和胸交感神經鏈,阻滯該側的運動、感覺和交感神經,單點阻滯局麻藥可上下擴散產生4 ~5 個節段的感覺阻滯,且對血流動力學影響輕微[13]。Karmakar 等[14]將TPVB 應用于乳腺癌根治病人的術中鎮痛,發現其只是減低了慢性疼痛的疼痛強度,并沒有降低術后慢性疼痛的發生率。本研究結果與其不盡相同,可能與本研究選取的局麻藥劑量和濃度不同,穿刺針的入路等有所不同,造成的肋間神經阻的范圍不同。此外,選擇的PMPS 評估標準不同,也會造成預測和診斷PMPS 的效度和靈敏度不同。本研究采用超聲可視下將穿刺針尖準確引導至胸椎旁間隙并置入導管,使鎮痛貫穿整個術中和術后,術中芬太尼的使用量大為減少,術后鎮痛泵按壓次數和術后補救鎮痛的需求例數明顯少于對照組,鎮痛滿意率較對照組亦明顯升高。本研究使用NPS 量表進行術后神經病理性疼痛的篩查,病人術后3、6、12 個月時PMPS 的發生率較對照組顯著降低。本研究提示超聲引導下TPVB 對乳腺癌手術病人的術后急性疼痛和乳腺癌術后疼痛綜合征均具有較好的臨床效果。
PMPS 發生的確切機制仍未完全清楚,現有研究認為與手術部位神經損傷、神經可塑性改變、持續炎癥反應以及下行傳導通路的改變有關[1]。手術創傷導致炎癥反應,交感神經末梢釋放大量炎癥介質,神經元內神經遞質及離子通道和受體表達水平發生改變,進一步增加傷害性感受神經元對傳入信號的敏感性,產生外周敏化,放大傳入的疼痛信號。隨著疼痛信號在脊髓表達的增強,通過影響抑制性中間神經元的功能甚至促進抑制性神經元凋亡,使得抑制性神經元功能缺失,導致中樞敏化。本研究采用胸椎旁神經阻滯降低乳腺癌病人PMPS 的發生率,其機制可能與預先鎮痛可以有效減輕外周神經感受器的傷害性刺激,阻斷信號傳導通路及炎性反應,從而避免外周和中樞敏化的產生,抑制神經元可塑性變化[15]。
綜上所述,超聲引導下連續胸椎旁神經阻滯鎮痛用于乳腺癌根治術病人效果確切,不良反應發生少,可有效減少乳腺癌根治術病人PMPS 的發生率,其發生機制還有待進一步研究和探索。

