鹽酸賽庚啶在Caco-2細胞中吸收轉運的研究
金永華,劉健,劉卉芳,李文娟,童煥,王湛博,楊勇,吳玉林
(1.中國藥科大學基礎醫學與臨床藥學學院,江蘇南京211198;2.中國藥科大學新藥安全評價研究中心,江蘇南京211198)
體內生物等效(bioequivalence,BE)是證明仿制藥和原研藥等效的“金標準”,但人體等效性試驗費用高、耗時長且采用健康志愿者,面臨倫理學問題。如何采用體外方法代替人體等效性試驗是制藥界和藥品監管機構一直努力探索的問題[1-2]。考慮到溶出度、溶解性和腸道內的滲透性是影響常釋口服制劑在體內吸收速度和程度的3個主要因素,Amidon等[3]于1995年提出生物藥劑學分類系統(biopharmaceuticsclassificationsystem,BCS)的概念,根據溶解度和滲透性將藥物分為4類,即BCS1類,高溶解性-高滲透性;BCS2類,低溶解性-高滲透性;BCS3類,高溶解性-低滲透性;BCS4類,低溶解性-低滲透性。美國食品藥品監督管理局(FDA)[4]、歐洲藥品管理局(EMA)[5]、世界衛生組織(WHO)[6]等監管機構分別出臺了基于生物藥劑學系統分類(BCS)豁免的指導原則。2016年原國家食品藥品監督管理總局發布了《人體生物等效性試驗豁免指導原則》[7],明確指出對于BCS1類和3類的藥物,只要處方中的其他輔料成分不顯著影響API的吸收,則不必證明該藥物在體內生物利用度和生物等效的可能性,即生物等效性豁免。對于通透性的研究可以采用單層人工培養上皮細胞的方法,Caco-2方法簡單、易行、成本低廉,常用于研究藥物的滲透性。
鹽酸賽庚啶片為藥品審評中心(CDE)公布的豁免名單草案中明確豁免BE的品種,但正式公布豁免名單時卻將其剔除。本實驗通過建立Caco-2細胞模型,研究鹽酸賽庚啶在小腸上皮細胞的攝取、跨膜轉運及外排作用,闡明鹽酸賽庚啶的吸收機制,為其能否生物豁免提供依據。
1 材料與方法
1.1 試劑和儀器 對照品:賽庚啶 (委托方提供);法莫替丁(中國食品藥品檢定研究院,批號:100305-201304);普萘洛爾 (Sigma-Aldrich,批號:BCBV9430);地高辛(TokyoChemicalIndustry,批號:MERKG-DL);沙丁胺醇(中國食品藥品檢定研究院,批號:100204-201103);甲苯磺丁脲(Sigma-Aldrich,批號:BCBV8457)。
材料和試劑:Caco-2細胞株(中國科學上海生命科學院細胞庫,批號:HTB-37);MEM培養基(Gibco,批號:C11095500BT);胎牛血清(BI,批號:04-001-1ACS);HBSS 溶 液 (Hyclone,批 號:SH30030.02);雙 抗(Hyclone,批號:SV30010);0.25%胰酶(Gibco,批號:25200-072);丙酮酸鈉(Gibco,批號:11360-070);非必需氨基酸(Gibco,批號:11140-050);L-谷氨酰胺(Gibco,批號:25030-081);依克立達(TargetMol,批號:T2657);4-羥乙基哌嗪乙磺酸(HEPES,Sigma-Aldrich,批號:H4034);氯化鈉(西隴科學,批號:180329);氯化鉀(上海凌峰,批號:20170111);十二水合磷酸氫二鈉(西隴科學,批號:171220);磷酸二氫鉀(上海凌峰,批號:20170122);熒光黃二鉀鹽(Sigma-Aldrich,批號:L0144);RIPA細胞裂解液(碧云天,批號:P0013K)。甲醇、乙腈為色譜純,購自Merck公司,其他溶劑和試劑均為分析純或以上。
儀器和耗材:Millicell小室(Merck,型號:MCRP24H48);細胞培養板(Sunub,型號:TCP-24);離心機(Dragonlab,型號:DM0412);數顯恒溫水浴鍋(DFS,型號:HH-4);細胞培養箱(Thermo,型號:3111);生物安全柜(Thermo,型號:1384);多功能酶標儀(En-Spire,型號:2300);生物倒置顯微鏡(Olympus,型號:CKX31);跨膜電阻儀(Millicell-ERS)。
1.2 Caco-2細胞模型的建立和評價 Caco-2細胞以1×105/cm2的密度接種于Millicell懸掛式培養小室中,于接種后的第21天使用Millicell-ERS跨膜電阻儀測定Caco-2細胞的跨膜電阻值。檢測Caco-2細胞滲透性:測定300μmol·L-1熒光黃AP-BL側的通透性。
1.3 熒光黃表觀滲透系數的測定 稱取適量熒光黃溶于二甲基亞砜(DMSO)中,配成300mmol·L-1母液,臨用前用Hanks平衡鹽溶液(HBSS)稀釋至300μmol·L-1工作液,用于測定Caco-2細胞致密性。后逐級稀釋熒光黃儲備液配制成1000、500、100、50、10、5nmol·L-1,線性回歸計算標準曲線。熒光黃的測定采用PerkinElmer多功能酶標儀,激發波長425nm,發射波長528nm,通過標準曲線計算熒光黃透過率。
1.4 給藥液與接收液的配制 供試品和對照品分別稱取適量,溶于DMSO配成100mmol·L-1儲備液,臨用前稀釋。Elacridar配制成50mmol·L-1母液,臨用前稀釋,具體配制方法見表1。

表1 溶液配置方法
1.5 轉運試驗 生長在Millicell培養小室中的細胞培養23d時,選取細胞電阻值大于300Ω的小室進行藥物轉運實驗。棄去小室培養基,用已預熱的轉運緩沖液將細胞清洗3遍,第三次加入后置于培養箱中溫孵20min。對于AP-BL:分別于AP側加入200μL頂端給藥液,于BL側加入1000μL基底端接收液;BL-AP:分別于AP側加入200μL頂端接收液,于BL側加入1000μL基底端給藥液。將培養板置于37℃,5%CO2和95%相對濕度條件下孵育,分別收集接收側在60、90和120min的溶液100 μL,同時補加100μL空白接收液,其中120min膜兩側均取樣100μL,用于計算回收率。
起始給藥液即為T0樣品,取完樣后吸棄細胞板內剩余的溶液,加入終止液200μL裂解細胞,輕輕震搖5min后收集細胞裂解液。
1.6 樣品分析
1.6.1 HBSS緩沖液中賽庚啶的檢測 液相色譜-串聯質譜(LC-MS/MS)檢測條件:色譜柱為Poroshell120 PhenylHexyl(2.7 μm,50mm×2.1mm);柱溫為 35 ℃;流動相A:0.1%甲酸的水溶液(V/V),流動相B:甲醇;梯度洗脫:0.0~0.6min 為 10%B,0.6~1.0min 為 10%B→80%B,1.0~3.0min 為 80%B,3.10~4.0min 為 10%B;運行時間:4.0min;流速為 0.3mL·min-1;進樣量為 5.0 μL。采用MRM模式;離子化方式為電噴霧離子化;離子極性為正離子;離子化電壓為5500V;溫度為500℃;氣簾氣為15psi;霧化氣為25psi;渦輪氣為25psi。賽庚啶和內標的MRM質譜檢測參數見表2。前處理方法:精密移取20μL樣品于1.5mLEP管中,加入10μL內標溶液,混勻,再加入180μL甲醇,渦旋混勻,20000g,4 ℃,離心 5min,取 80 μL上清液與80μL純化水,混勻后進樣。

表2 賽庚啶的質譜檢測參數
1.6.2 HBSS緩沖液中法莫替丁、普萘洛爾和地高辛的檢測 法莫替丁的LC-MS/MS檢測條件:色譜柱為 ZorbaxSB-C8,(3.5 μm,150mm×4.6mm);柱溫為40℃;流動相 A:0.1%甲酸的水溶液(V/V),流動相 B:甲醇;等度洗脫:0.0~3.5min 為 40%B;運行時間:3.5min;流速為 0.8mL·min-1;進樣量為5.0μL。離子檢測方式為多重反應監測;離子化方式為電噴霧離子化;離子極性為正離子;離子化電壓為5000V;溫度為450℃;氣簾氣為28psi;霧化氣為55psi;渦輪氣為50psi。法莫替丁和內標的MRM質譜檢測參數見表3。

表3 法莫替丁的質譜檢測參數
普萘洛爾的LC-MS/MS檢測條件:色譜柱為Poroshell120PhenylHexyl,(2.7 μm,50mm×2.1mm);柱溫為35℃;流動相A:0.1%甲酸的水溶液(V/V),流動相 B:甲醇;梯度洗脫:0.0~0.8min 為 20%B,0.8~1.1min 為 20%B→70%B,1.1~2.0min 為 70%B,2.10~3.5min 為 20%B;運行時間:3.5min;流速為 0.5 mL·min-1;進樣量為5.0μL。離子檢測方式為多重反應監測;離子化方式為電噴霧離子化;離子極性為正離子;離子化電壓為5000V;溫度為450℃;氣簾氣為28psi;霧化氣為55psi;渦輪氣為50psi。普萘洛爾和內標的MRM質譜檢測參數見表4。
地高辛的LC-MS/MS檢測條件:色譜柱為Poroshell120PhenylHexyl(2.7 μm,50mm×2.1mm);柱溫為35℃;流動相A:0.1%甲酸的水溶液(V/V),流動相 B:甲醇;梯度洗脫:0.0~0.8min 為 20%B,0.8~1.1min 為 20%B→70%B,1.1~2.0min 為 70%B,2.10~3.5min 為 20%B;運行時間:3.5min;流速為 0.5 mL·min-1;進樣量為5.0μL。離子檢測方式為多重反應監測;離子化方式為電噴霧離子化;離子極性為正離子;離子化電壓為-4500V;溫度為550℃;氣簾氣為20psi;霧化氣為50psi;渦輪氣為60psi。地高辛和內標的MRM質譜檢測參數見表5。
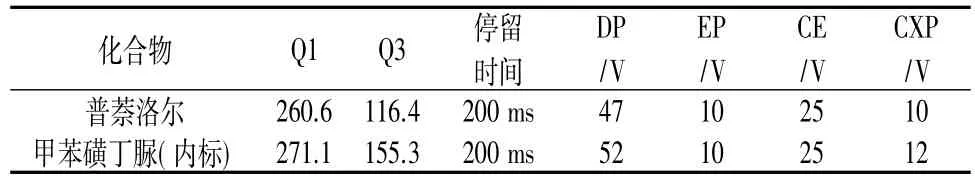
表4 普萘洛爾的質譜檢測參數
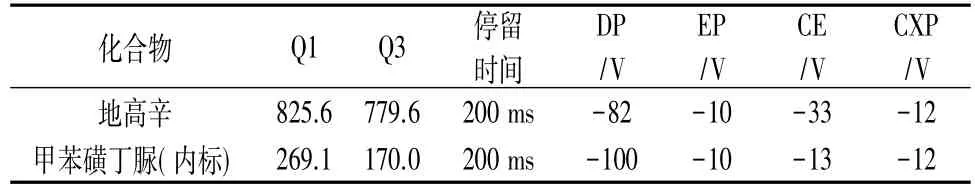
表5 地高辛的質譜檢測參數
法莫替丁樣品的前處理方法:取30μL樣品加入150μL內標工作液(沙丁胺醇),渦旋5min,20000g,4℃離心10min,取上清液100μL與100 μL水混合,渦旋10min,LC/MS/MS分析。
普萘洛爾和地高辛樣品的前處理方法:取30μL樣品加入270μL內標工作液(甲苯磺丁脲),渦旋5 min,20000g,4 ℃離心 10min,取上清液 100 μL 與100μL水混合,渦旋10min,LC/MS/MS分析。
1.7 數據計算 采用如下公式計算表觀滲透系數(Papp,cm·s-1),外排率以及回收率。
Papp=
熒光黃透過到基底端的百分率用以下公式計算:
RFUApical和RFUBasolaterd分別是熒光黃在頂端和基底端的相對熒光強度。VApical和VBasolaterd分別是頂端和基底端的上樣體積(分別為0.2mL和1mL)。
2 結果
2.1 賽庚啶HBSS緩沖液中方法學驗證 選擇性:在該試驗條件下,賽庚啶的出峰時間為2.21min,內標甲苯磺丁脲的出峰時間為2.09min。空白樣本、賽庚啶以及內標的選擇性色譜圖見圖1。
殘留:在標準曲線最高濃度點(ULOQ)后,進樣空白樣本,未見空白樣本中有殘留干擾。
標準曲線:以待測物峰面積和內標峰面積的比值對待測物濃度作權重回歸計算,選1/c2為權重因子得出標準曲線方程,鹽酸賽庚啶:Y=0.000924X+0.00223,r=0.9959(n=8)。表明鹽酸賽庚啶在 10~5000nmol·L-1內線性關系良好。鹽酸賽庚啶LLOQ為10nmol·L-1,準確度為 93.3% ~ 104.0%,RSD 為4.0%。
稀釋效應:超限樣品(1000nmol·L-1)稀釋10倍后進樣分析,結果,樣品準確度在 101.5%~107.2%之間,RSD 在 2.1%~15.0%之間。
準確度和精密度:制備濃度為30、200、4000 nmol·L-1的樣品,考察準確度和精密度,結果準確度在 104.6%~107.0%之間,精密度在 6.1%~8.2%。2.2 Caco-2細胞單層生長過程中跨膜電阻值的變化及熒光黃的測定 Caco-2細胞接種到小室后,TEER值隨著接種的時間逐漸增大,到第3周時TEER值增長緩慢。第21天測定各小室的TEER值,均已超過300Ω·cm2。隨機抽取6個小室進行熒光黃測定,熒光黃的透過率均小于2.5%左右,表明本實驗中Caco-2細胞單層模型的致密性良好。2.3 對照品法莫替丁、普萘洛爾和地高辛細胞單層的滲透性結果 Caco-2細胞單層致密連接形成后,法莫替丁(50μmoL·L-1)、普萘洛爾(50 μmoL·L-1)的細胞單層滲透性結果見表6。地高辛的外排實驗結果見表7。
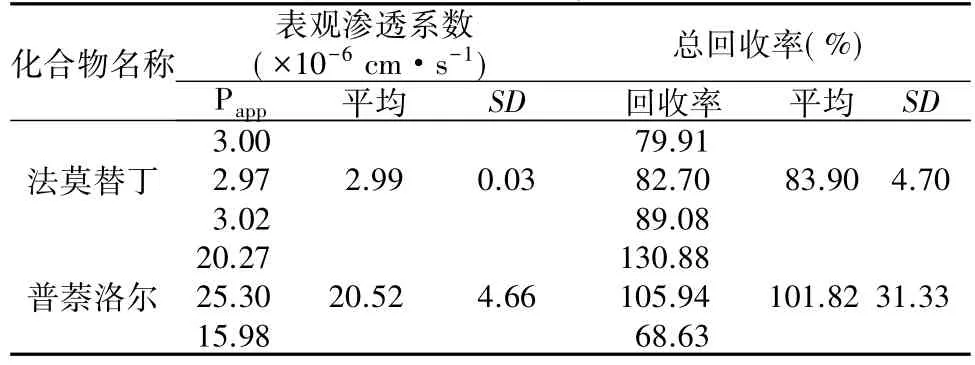
表6 法莫替丁和普萘洛爾滲透性實驗結果
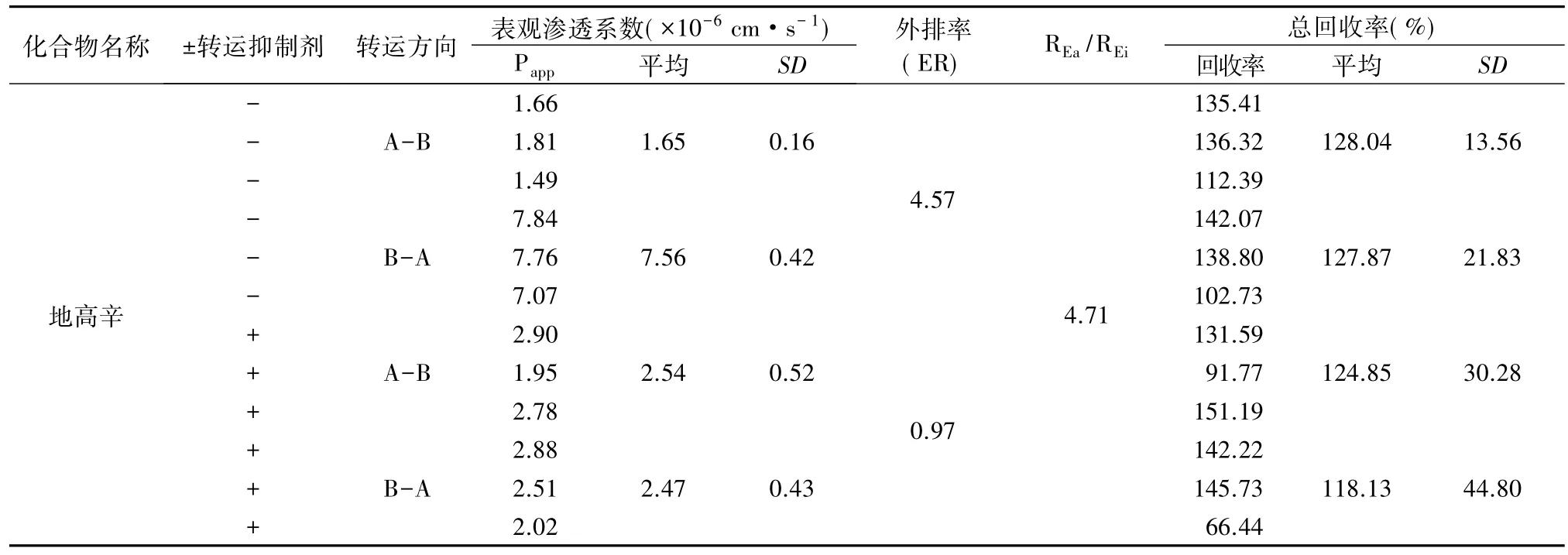
表7 地高辛的外排實驗結果
作為低滲的對照藥,法莫替丁的平均表觀滲透系數[Papp(A-B)]為 2.99×10-6cm·s-1;作為高滲的對照藥,普萘洛爾的平均表觀滲透系數[Papp(AB)]為20.52×10-6cm·s-1(見表6)。作為外排轉運的對照藥,不加抑制劑時,地高辛的平均表觀滲透系數 Papp(A-B)和 Papp(B-A)值分別為 1.65×10-6cm·s-1和7.56×10-6cm·s-1,外排率為4.57;加入抑制劑時,地高辛的平均表觀滲透系數Papp(A-B)和Papp(B-A)值分別為 2.54×10-6cm·s-1和 2.47×10-6cm·s-1,外排率為0.97(見表7)。對照藥的溶液回收率為 68.32% ~124.35%,總回收率為 83.90% ~128.04%。因此本研究所采用的Caco-2細胞展示出合格的功能特性。
2.4 賽庚啶雙向滲透性結果 Caco-2細胞單層致密連接形成后,鹽酸賽庚啶(5、10和 20 μmoL·L-1)的細胞單層滲透性結果見表2。
在給藥濃度為5、10和20μmoL·L-1及不含抑制劑的條件下,鹽酸賽庚啶在A-B方向的平均表觀滲透系數分別為 6.36×10-6、6.14×10-6、23.1×10-6cm·s-1。在B-A方向的平均表觀滲透系數分別為16.7×10-6、18.16×10-6、29×10-6cm·s-1,外排率REa,分別為 2.63、2.96、1.26。在給藥濃度 5、10 和20μmoL·L-1及含抑制劑的條件下,鹽酸賽庚啶在A-B方向的平均表觀滲透系數分別為7.74×10-6、15.06×10-6、26.96×10-6cm·s-1。在 B-A 方向的平均表觀滲透系數分別為 14.03×10-6、18.51×10-6、21.3×10-6cm·s-1。外排率 REi分別為 1.81、1.23、0.79。鹽酸賽庚啶Caco-2細胞中表現出較好的滲透性,同時可能存在外排轉運現象,為外排轉運體的底物。實驗結果見表8。
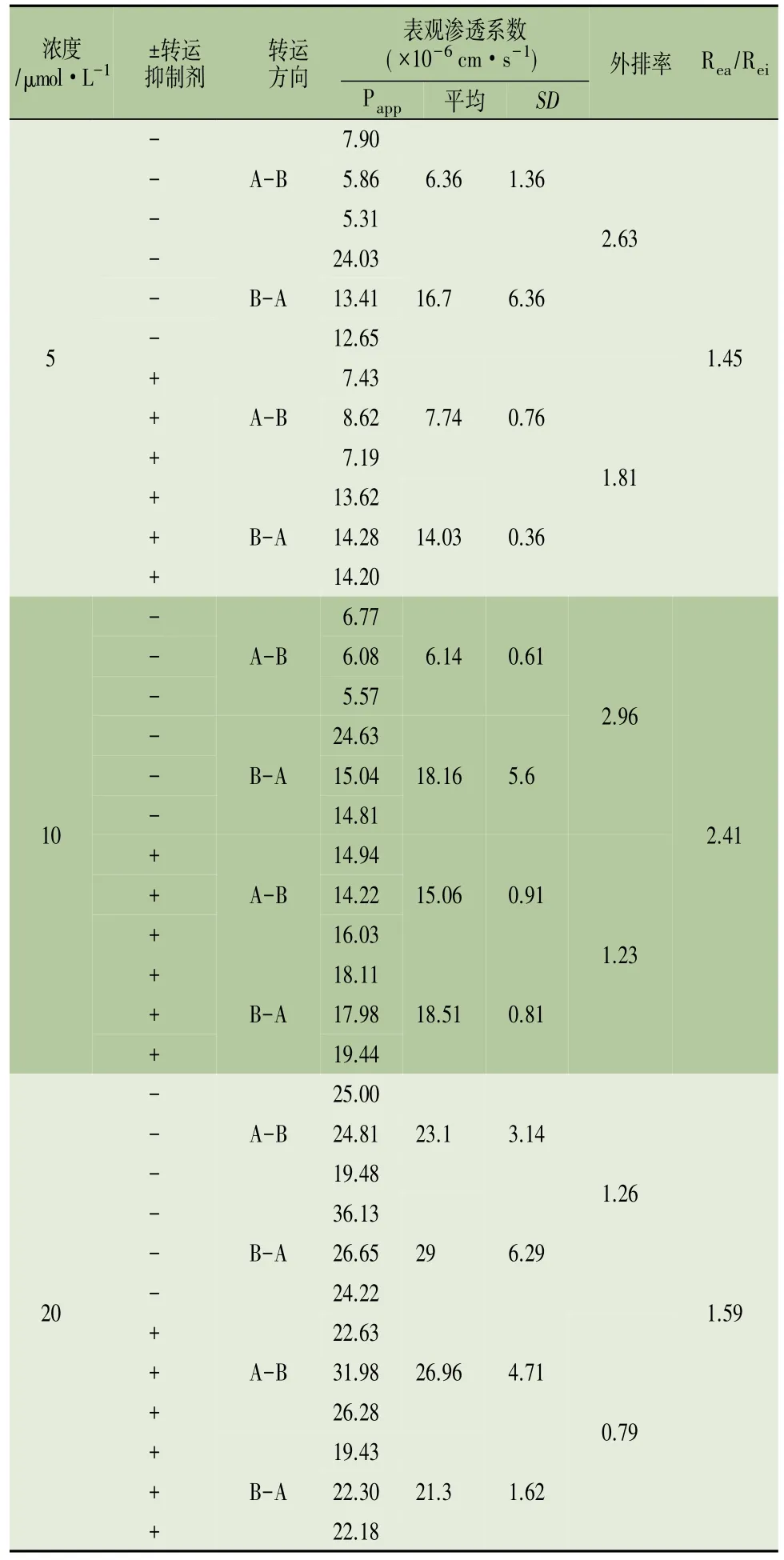
表8 賽庚啶滲透性及外排實驗結果
3 討論
鹽酸賽庚啶片為CDE公布的豁免名單草案中明確豁免BE的品種,但正式公布豁免名單時卻將其剔除。溶解性試驗中已明確鹽酸賽庚啶為高溶解性物質,對于滲透性的考察,高濃度(20μmoL·L-1)表現出高滲透性,當濃度為5、10μmoL·L-1時,滲透系數較20μmoL·L-1下降,同時外排率大于2,存在外排現象。本實驗采用依克立達作為外排轉運體抑制劑,依克立達為P-糖蛋白(P-gp)和乳腺癌耐藥蛋白(BCRP)轉運體底物,加入依克立達后,外排率降低,說明鹽酸賽庚啶可能是P-gp和BCRP轉運體底物。而采用Caco-2方法進行滲透性研究僅適用于被動轉運的藥物(藥物的外排率應小于2)[8]。從鹽酸賽庚啶的滲透性結果可以看出,滲透隨藥物濃度的變化而變化,且與轉運方向有關。推測未將鹽酸賽庚啶作為BE豁免品種可能與其在Caco-2細胞中存在主動轉運現象有關。

