促性腺激素釋放激素拮抗劑的固定方案與靈活方案在新鮮胚胎移植周期中的妊娠結局比較
蔡麗思 歐建平 邢衛杰 蔡柳洪 李濤 陶欣

【摘要】目的比較促性腺激素釋放激素拮抗劑(GnRH-ant)的固定方案和靈活方案在不同年齡組患者中行體外受精/單精子胞漿內注射一胚胎移植(IVF/ICSI-ET)新鮮胚胎移植周期的妊娠結局。方法收集采用GnRH-ant方案進行IVF/ICSI-ET者的臨床資料,共納入1 321個周期,根據患者采用的GnRH-ant方案分為固定方案組(1014個周期)及靈活方案組(307個周期),比較固定方案組和靈活方案組患者的基本資料、促排卵情況、新鮮移植周期的妊娠結局差異,并根據女方年齡分為<35歲、35~39歲、)40歲,分別比較新鮮周期中不同年齡者行固定方案與靈活方案的妊娠結局差異。最后進行二元Logistic回歸分析,分析固定方案組與靈活方案組間的臨床妊娠率差異。結果固定方案組和靈活方案組的生化妊娠率、臨床妊娠率和種植率比較差異均無統計學意義(P均>0.05)。固定方案組的獲卵數、成熟卵子數和優質胚胎數均多于靈活方案組(P均<0.05)。新鮮周期中年齡<35歲者,固定方案組的Go總用量低于靈活方案組、HCG注射日雌二醇水平高于靈活方案組、獲卵數亦多于靈活方案組(P均<0.05)。二元Logistic回歸分析顯示年齡(校正后OR=0.961,95%C10.927一0.996,P=0.033)和移植胚胎數(校正后OR=1.756,95%CI 1.167一2.642,P=0.012)是臨床妊娠率的影響因素,而選擇固定方案或靈活方案對臨床妊娠率無影響(P>0.05)。結論GnRH-ant固定方案和靈活方案的妊娠結局相近。與靈活方案相比,GnRH-ant固定方案組的促排卵時間縮短,獲卵數、成熟卵子數和優質胚胎數增加。
【關鍵詞】促性腺激素釋放激素拮抗劑;體外受精-胚胎移植;輔助生殖技術
促性腺激素釋放激素拮抗劑(GnRH-ant)能與垂體GnRH受體結合,有效阻斷內源性GnRH作用,迅速降低血清中卵泡刺激素(FSH)、黃體生成素(LH)水平。GnRH-ant無GnRH激動劑(GnRH-a)的一過性作用,且停藥后48 h即解除對垂體的抑制作用。有研究發現,GnRH-ant方案能夠有效縮短總治療時間和減少促性腺激素(Gn)用量,且可降低卵巢過度刺激綜合征(OHSS)發生率[1]。目前臨床最常用的促排卵方案是在促排卵第5日或第6日添加GnRH-ant,即固定方案。但為了減少GnRH-ant的用量,Kolibianankis等[2]和Escudero等[3]提出了靈活方案,即當優勢卵泡直徑≥14mm或優勢卵泡直徑≥12mm且雌二醇>300pg/ml時添加GnRH-ant。目前在GnRH-ant固定方案和靈活方案的選擇方面仍存在一定爭議。Hamdine等[4]研究顯示,早期添加GnRH-ant可減少早發性LH峰的出現,從而避免過早排卵和減少卵泡黃素化,降低周期取消率。蘇靜等[5]研究顯示,靈活方案的妊娠結局并不劣于固定方案,且在減少GnRH-ant使用時間和用量方面存在明顯的優勢。本研究旨在比較GnRH-ant固定方案和靈活方案在新鮮移植周期的促排卵效果和臨床妊娠結局,現報告如下。
對象與方法
一、研究對象
收集2015年12月至2018年5月在本中心采用GnRH-ant方案進行體外受精/單精子胞漿內注射一胚胎移植(IVF/ICSI-ET)者的臨床資料。所有夫婦均已簽署知情同意書,本研究獲中山大學附屬第三醫院醫學倫理委員會批準。納入標準:①夫婦雙方有IVF/ICSI-ET的指征;②采用GnRH-ant方案進行IVF/ICSI助孕;③均有可利用胚胎并在新鮮周期移植。排除標準:①有影響胚胎著床的因素,如子宮黏膜下肌瘤、宮腔粘連、子宮解剖結構異常等;②合并自身免疫性疾病或其他內分泌及代謝性疾病;③染色體異常需行胚胎植人前基因診斷的患者。
二、治療方案
1.GnRH-ant固定方案
在月經周期第2一3日開始使用Gn,即重組FSH(rFSH,普麗康或果納芬),啟動劑量75-300U,根據患者的年齡、BMI、竇卵泡數而定。同時監測血清性激素水平(LH、雌二醇、孕酮)和卵泡發育情況。在啟動后第5日或第6日添加GnRH-ant(思則凱)。當有2個或2個以上優勢卵泡直徑≥18mm時,用5000~10 000 U人絨毛膜促性腺激素(HCG)或250 wg重組HCG(艾澤)扳機。若患者有OHSS發生高風險,則采用雙扳機,即0.1mg GnRH-a(達菲林)聯合2 000 U HCG.扳機后34~36h取卵。
2.GnRH-ant靈活方案
啟動時間和劑量參考固定方案,在優勢卵泡直徑≥14mm或優勢卵泡直徑≥12mm且雌二醇>300pg/ml時添加GnRH-ant。其他性激素和卵泡監測、扳機時機同固定方案。
3.胚胎移植和驗孕
取卵后第3日或第5日在B超引導下進行胚胎移植。移植后12~14d查血清β-HCG陽性即為生化妊娠。移植后5周行陰道B超,B超下見孕囊即為臨床妊娠。種植率為孕囊數除以移植胚胎數。黃體支持一直持續到孕10周。
三、研究方法
根據患者采用的GnRH-ant方案分為固定方案組及靈活方案組,比較2組患者的基本資料、促排卵情況、妊娠結局差異,并根據女方年齡分為<35歲、35一39歲、≥40歲3個亞組,分別比較新鮮周期中不同年齡患者行固定方案與靈活方案的妊娠結局差異。
四、統計學處理
采用SPSS 21.0進行數據統計和分析。服從正態分布的計量資料以x1s表示,2組間比較采用獨立樣本t檢驗;不服從正態分布的計量資料以中位數(四分位數間距)表示,組間比較采用非參數檢驗。計數資料以率表示,組間比較采用χ2檢驗。為了控制混雜因素,進行了二元Logistic回歸分析,納入了年齡、Gn啟動劑量、Gn總用量、促排時間、HCG注射日子宮內膜厚度、獲卵數、移植胚胎數以及方案的選擇,分析固定方案組與靈活方案組間的臨床妊娠率差異。P<0.05為差異有統計學意義。
結果
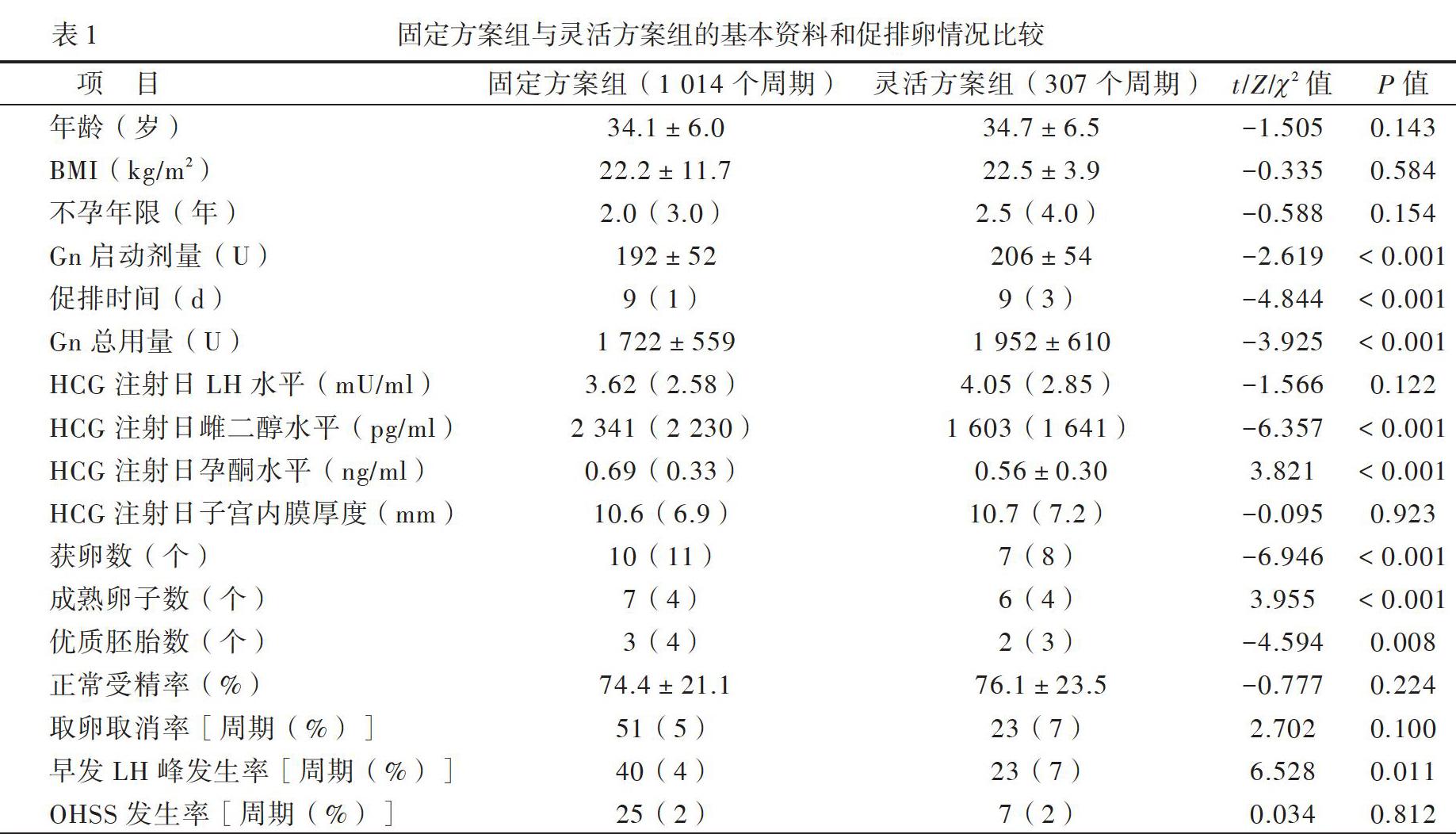
一、固定方案組與靈活方案組的基本資料和促排卵情況比較
共納入1321個周期,其中1014個周期使用GnRH-ant固定方案,307個周期使用GnRH-ant靈活方案。2組患者的年齡、BMI、不孕年限比較差異均無統計學意義(P均>0.05)。與靈活方案組相比,固定方案組的Gn啟動劑量及總用量均較低、促排卵時間較短(P均<0.05)。2組患者HCG注射日LH水平和子宮內膜厚度相近(P均>0.05),但固定方案組的HCG注射日雌二醇和孕酮水平均高于靈活方案組(P均<0.05)。固定方案組的獲卵數、成熟卵子數和優質胚胎數均多于靈活方案組(P均<0.05),2組間正常受精率和取卵取消率比較差異均無統計學意義(P均>0.05),見表1。
二、固定方案組與靈活方案組的妊娠結局比較
共560個周期進行了新鮮周期移植,其中439個周期為GnRH-ant固定方案,121個周期為GnRH-ant靈活方案。固定方案組共移植826枚胚胎,其中移植第3日胚胎(D3)719枚、囊胚107枚,種植233枚(28.2%);靈活方案組共移植217枚胚胎,其中移植D3 184枚、囊胚33枚,種植56枚(25.8%)。2組的胚胎移植種類(χ2=0.751,P=0.386)及種植率(χ2=0.495,P=0.482)比較差異均無統計學意義。2組周期的移植胚胎數、生化妊娠率、臨床妊娠率和種植率比較差異亦均無統計學意義(P均>0.05),見表2。
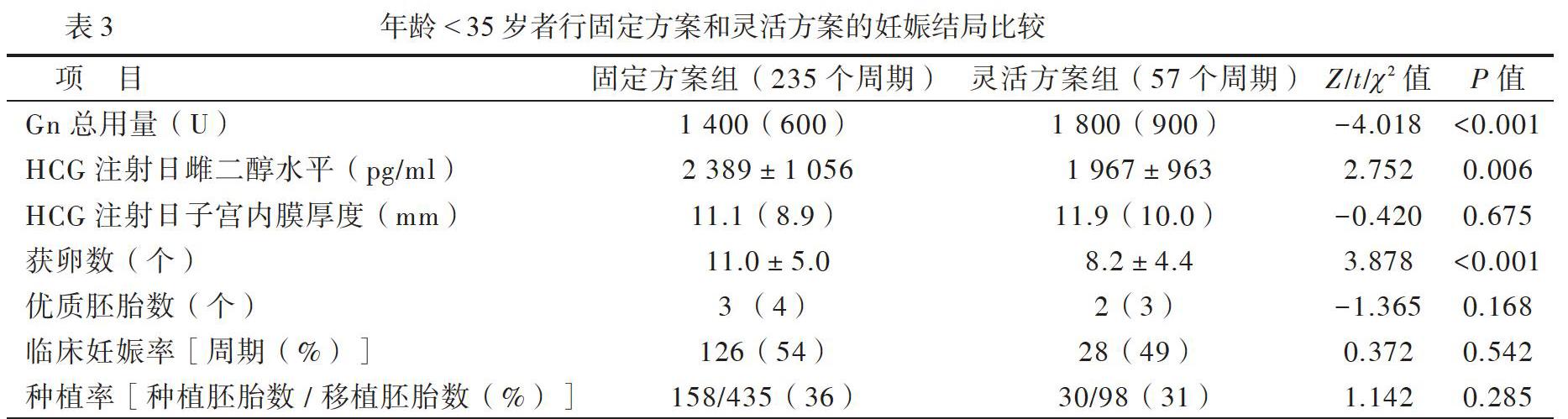
2.年齡35~39歲者行固定方案和靈活方案的妊娠結局比較
對于年齡35~39歲者,固定方案組與靈活方案組的妊娠結局各項指標比較差異均無統計學意義(P均>0.05),見表4。
3.年齡≥40歲者行固定方案和靈活方案的妊娠結局比較
對于年齡≥40歲者,固定方案組與靈活方案組的妊娠結局各項指標比較差異均無統計學意義(P均>0.05),見表5。
四、二元Logistic回歸分析結果
為了控制混雜因素,進行了二元Logistic回歸分析,納入了年齡、Gn啟動劑量、Gn總用量、HCG注射日子宮內膜厚度、獲卵數、移植胚胎數以及方案的選擇等因素,結果顯示年齡越小、移植胚胎數越多,臨床妊娠率越高(P均<0.05).在校正了其他因素后,選擇固定方案或靈活方案對臨床妊娠率無影響(P>0.05),見表6。
討論
一般認為,各種促排卵方案的制定必須在保證一定數量的卵泡發育的同時抑制內源性的LH峰。最早用于抑制LH峰的藥物是GnRH-a,但其可產生激發(一過性升高)效應,需要等待受體的耗竭和脫敏,還可能過度抑制垂體。在上世紀90年代,GnRH-ant開始在輔助生殖領域用于抑制LH峰的產生[6]。GnRH-ant可以與垂體上的GnRH受體競爭性結合,即時產生抑制LH的作用,與GnRH-a相比具有使用方便、促排卵時間短、無一過性升高效應的優點,且其抑制作用呈劑量依賴性,停藥后48h即解除對垂體的抑制作用,GnRH-ant方案還可以降低OHSS的發生[7]。然而,關于何時添加GnRH-ant仍存在爭議。一項大樣本多中心的回顧性研究納入了27000個采用GnRH-ant方案的IVF周期,探究添加GnRH-ant的最佳時機,結果顯示在第5日或第6日添加GnRH-ant所獲得的臨床妊娠率是最高的,而當雌二醇水平過低(<300pg/ml)或過高(>1100pg/ml)時添加GnRH-ant均會明顯降低臨床妊娠率[8]。目前GnRH-ant方案主要有固定方案和靈活方案。固定方案即在促排卵第5日或第6日添加GnRH-ant 、而靈活方案即當優勢卵泡直徑≥14mm或優勢卵泡直徑≥12mm且雌二醇>300pg/ml時添加GnRH-ant。
一項隨機對照研究納入了146個IVF周期,其中72個周期在促排第6日開始添加GnRH-ant 、74個周期在優勢卵泡直徑>14mm時添加GnRH-ant,其余條件保持一致,觀察2組的促排卵效果和臨床結局,結果顯示2組的獲卵數、繼續妊娠率、流產率、種植率均相近,且無早發LH峰的發生[2]。有學者對11個比較GnRH-ant固定方案和靈活方案的臨床研究進行薈萃分析,其中包括4項隨機對照研究,結果表明固定方案組的臨床妊娠率較高,尤其是高于靈活方案組中啟動第8日才添加GnRH-ant者,但靈活方案組能明顯減少Gn和GnRH-ant用量,所有納入的研究均無早發LH峰的出現,可能與納入研究的樣本量較小有關[9]。本研究顯示,固定方案組和靈活方案組的妊娠結局無統計學差異。而二元Logistic回歸分析也進一步證實,年齡和移植胚胎數是臨床妊娠率的影響因素,而固定方案和靈活方案的選擇并不影響臨床妊娠率。
另一方面,LH峰的出現由排卵前優勢卵泡分泌的雌二醇正反饋誘發,是促進卵泡最后成熟、恢復卵母細胞減數分裂的關鍵。但控制性超促排卵是抑制多卵泡發育的過程,超生理水平的雌二醇易誘發過早內源性LH峰的產生。而早發LH峰的出現可抑制顆粒細胞增殖,卵泡閉鎖,排卵前卵泡黃素化,影響子宮內膜的容受性,導致周期取消率增加[10]。因此,促排卵過程中抑制內源性LH,防止早發LH峰的發生十分重要。然而,歐湘紅等[11]回顧性分析了108例行IVF-ET的高齡患者,比較GnRH-ant固定方案和靈活方案的促排卵效果,結果發現,對于高齡患者,應用GnRH-ant固定方案會導致卵泡中期過低的LH水平,影響卵母細胞和胚胎質量,而靈活方案組GnRH-ant的用量減少、使用時間縮短,獲得更多的優質胚胎,減輕患者經濟負擔。近年有學者提出要在GnRH-ant固定方案中反向添加LH[12]。本研究顯示,雖然靈活方案組的Gn總用量明顯減少,但其HCG注射日LH水平、早發LH峰發生率和取卵取消率略高于固定方案。2015年的專家共識也提出GnRH-ant靈活方案可能導致早發LH峰的發生[13]。
本研究中固定方案在增加獲卵數、成熟卵子數和優質胚胎數方面優于靈活方案。可能有以下幾點原因:第一,本研究為回顧性研究,不可避免存在選擇偏倚,而且無法確定因果關系。第二,一般在臨床工作中,若患者本身為慢反應人群,醫生則傾向于推后數日再添加GnRH-ant,無形中延長了促排卵時間。而高齡患者往往因卵巢儲備低,促排卵過程中容易呈現慢反應,所以醫生傾向于采用靈活方案。雖然本研究中固定方案組和靈活方案組年齡比較差異無統計學意義,但靈活方案組年齡略高。第三,對于年齡≥40歲者,靈活方案組的獲卵數、優質胚胎數和種植率略低于固定方案組,可能也正是因為患者本身為慢反應,所以才采用靈活方案。因此還需要更多的隨機對照研究確定方案的選擇與妊娠結局之間的關系。
綜上所述,GnRH-ant固定方案和靈活方案的妊娠結局相近,與靈活方案相比,GnRH-ant固定方案組的促排卵時間減少,獲卵數、成熟卵子數和優質胚胎數增加。由于本研究為回顧性研究,因此仍需要前瞻性的隨機對照研究來明確方案的選擇與妊娠結局的關系。
參考文獻
[1]Bodri D,Vernaeve V,Guillen JJ,Vidal R,Figueras F,CollO.Comparison between a GnRH antagonist and a CnRH agonistflare-up protocol in oocyte donors:a randomized clinical trial.Hum Reprod,2006,21(9):2246-2251.
[2]Kolibianakis EM,Venetis CA,Kalogeropoulou L,PapanikolaouE,Tarlatzis BC.Fixed versus flexible gonadotropin-releasinghormone antagonist administration in in vitro fertilization:a ran-domized controlled trial.Fertil Steril,2011,95(2):558-562.
[3]Escudero E,Bosch E,Crespo J,Simbn C,Remohi J,Pellicer A.Comparison of two different starting multiple dose gonadotropin-releasing hormone antagonist protocols in a selected group of invitro fertilization-embryo transfer patients.Fertil Steril,2004,81(3):562-566.
[4]Hamdine 0,Broekmans FJ,Eijkemans MJ,Lambalk CB,Fauser BC,Laven JS,Macklon NS:CETRO trial study group.Early initiation of gonadotropin-releasing hormone antagonisttreatment results in a more stable endocrine milieu during themid-and late-follicular phases:a randomized controlled trialcomparing gonadotropin-releasing hormone antagonist initiationon cycle day 2 or 6.Fertil Steril,2013,100(3):867-874.
[5]蘇靜,薛惠英,張繼躍,仲紀祥,邱峰龍.3種拮抗劑方案在PCOS患者行IVF治療中的臨床應用價值分析.現代中西醫結合雜志,2018,27(26):2940-2943.
[6]游澤山,李國裸.面向21世紀的胎兒醫學.新醫學,2001,32(12):711-713.
[7]朱潔茹,歐建平,邢衛杰,陶欣,蔡柳洪,李濤,孫麗,林慧.GnRH激動劑長方案與GnRH拮抗劑方案在不同年齡組、不同反應人群中的新鮮周期臨床結局比較.中山大學學報(醫學科學版),2017,38(5):738-745.
[8]Lyttle Schumacher BM,Mersereau JE,Steiner AZ.Cycle day,estrogen level,and lead follicle size:analysis of 27,790 invitro fertilization cycles to determine optimal start criteria forgonadotropin-releasing hormone antagonist.Fertil Steril,2018,109(4):633-637.
[9]Al-Inany H,Aboulghar MA,Mansour RT,Serour GI.Optimizing GnRH antagonist administration:meta-analysis offixed versus flexible protocol.Reprod Biomed Online,2005,10(5):567-570.
[10]葉虹.再論促黃體生成素峰.生殖醫學雜志,2010,19(z1):3-5.
[11]歐湘紅,陳雷寧,王保平,陳海霞,李瑾,劉怡憧,靖濤.在低卵巢儲備患者中靈活的促性腺激素拮抗劑方案優于標準拮抗劑方案.生殖與避孕,2015,35(9):601-605.
[12]He W,Lin H,LV J,Wen Y, Cai L.The impact of luteinizinghormone supplementation in gonadotropin-releasing hormoneantagonist cycles:a retrospective cohort study.Gynecol Endo-crinol,2018,34(6):513-517.
[13]喬杰,馬彩虹,劉嘉茵,馬翔,李尚為,楊業洲,張波,臘曉琳,王曉紅,輔助生殖促排卵藥物治療專家共識.生殖與避孕,2015,35(4):211-223.
(收稿日期:2019-02-01)
(本文編輯:林燕薇)
DOI:10.3969/j.issn.0253-9802.2019.05.015
作者單位:510630 廣州,中山大學附屬第三醫院生殖醫學中心
通信作者,陶欣,E-mail:doctort@163.com

