卵巢移位術后增敏化療聯合放療對宮頸癌患者圍絕經期癥狀、性激素及卵巢功能的影響
莫文杰 羅傳文 黃金漢 徐 升 唐 浩 賴 琳
(湖北省恩施土家族苗族自治州中心醫院腫瘤放療中心,恩施州 445000,電子郵箱:zmhllhfl@sina.com)
近年來,宮頸癌已成為婦科最常見的惡性腫瘤,其發病率僅次于乳腺癌和結直腸癌,每年新發病例近50萬,死亡病例近27萬[1]。目前,宮頸癌發病呈年輕化趨勢。對于早期宮頸癌患者,如何在治療疾病的同時有效保留卵巢功能和生育能力是臨床上極為關注的問題之一。卵巢作為機體重要的性激素分泌器官,盆腔的放射治療會損害其功能,嚴重影響年輕患者的生活質量[2]。因此,為了使放療不影響患者卵巢的功能,臨床上常采用卵巢移位手術將卵巢移出放射野[3]。本文探討卵巢移位術后增敏化療聯合放療對宮頸癌患者圍絕經期癥狀、血清卵泡刺激素(follicle-stimulating hormone,FSH)、雌二醇及黃體生成素(luteinizing hormone,LH)及卵巢功能的影響,現報告如下。
1 資料與方法
1.1 臨床資料 回顧性分析我院2015年1月至2016年10月收治的105例行卵巢移位術后ⅠB1~ⅡA2期宮頸癌患者的臨床資料。納入標準:(1)經病理活檢證實為宮頸鱗狀細胞癌,根據2009年國際婦產科協會臨床分期標準[3]診斷為早期宮頸癌;(2)行卵巢移位手術,移位卵巢距離髂總動脈分叉2 cm以上;(3)年齡<45歲。排除標準:(1)既往接受過盆腔放療及化療者;(2)發生癌轉移者;(3)藥物過敏者;(4)嚴重腎功能衰竭患者;(5)妊娠或哺乳期婦女;(6)資料不全或不配合者。所有患者術后均給予增敏化療,其中59例患者(觀察組)術后病理結果提示存在腫瘤浸潤深肌層、宮旁或陰道切緣陽性、淋巴結轉移、分化程度低、脈管癌栓陽性等高危因素,術后聯合放療,其余46例患者(對照組)術后未聯合放療。觀察組年齡27~44(33.1±2.4)歲,疾病分期ⅠB1期24例,ⅠB2期14例,ⅡA1期13例,ⅡA2期8例。對照組25~44(32.7±2.8)歲,疾病分期ⅠB1期19例,ⅠB2期11例,ⅡA1期10例,ⅡA2期6例。兩組患者的疾病分期、年齡等資料比較,差異均無統計學意義(均P>0.05),具有可比性。本研究通過本院醫學倫理委員會批準,所有患者及家屬知情同意。
1.2 治療方法 (1)手術治療:所有患者在評估卵巢狀態后行腹腔鏡下或開腹宮頸癌根治術及卵巢移位術。術中鉗斷卵巢固有韌帶,游離一側或雙側卵巢動靜脈,游離長度為10~12 cm,采用0.9%氯化鈉溶液紗布包裹輸卵管切除側卵巢,待卵巢移位準備完畢后行行子宮切除術+盆腔淋巴結清掃術;然后繼續游離卵巢動靜脈,游離長度為15 cm,將已包裹卵巢向右上方旋轉,沿結腸側溝腹膜外間隙上行后穿過后腹膜,刺穿腹膜后進入腹腔內,將其固定于脾下緣水平,骨盆漏斗韌帶固定腹膜數針,盡量避免固定于放射治療照射區內,確認無血管阻塞,避免卵巢動靜脈扭轉。(2)觀察組術后進行同步放化療:采用瓦里安直線加速器進行外照射治療,總劑量為45~50 Gy,分25次完成,5次/周;采用銥源后裝腔內治療機進行腔內近距離照射,治療總劑量為20 Gy,分4次完成,2次/周;同時給予同步化療,順鉑30 mg/m2靜脈滴注,1次/周,共5次。(3)對照組術后單純行放射治療,放療外照射方法及腔內近距離照射方法同觀察組。
1.3 觀察指標 (1)比較兩組患者圍絕經期癥狀:治療后6個月對患者進行隨訪,根據Kupperman絕經指數(Kupperman menopause index,KMI)[4]判斷患者術后圍絕經期癥狀,KMI 評分表共包含13種癥狀,即潮熱汗出、感覺障礙、失眠、易激動、抑郁疑心、眩暈、疲乏、骨關節痛、頭痛、心悸、皮膚蟻走感、性生活下降和泌尿系感染,嚴重程度分4個等級,其中0分為無該項癥狀,1分、2分、3分分別視為輕、中、重度癥狀。計算總分時,潮熱出汗癥狀加權分為4分,感覺異常、失眠、易激動、性生活異常及泌尿系統感染癥狀加權分為2分,其余的癥狀加權分為1分,KMI評分≥15分則診斷為出現圍絕經期癥狀。(2)比較兩組患者卵巢功能保留情況:治療后6個月根據KMI評分和血清FSH值判斷卵巢功能,FSH值<10 mIU/ml為卵巢功能正常,FSH值在10~40 mIU/ml且出現圍絕經期癥狀為卵巢功能衰退,FSH值>40 mIU/ml為卵巢功能喪失。(3)于治療前和治療后6個月采用放射免疫法患者的FSH、雌二醇及LH水平。
1.4 統計學分析 采用SPSS 19.0軟件進行統計學分析。符合正態分布的計量資料以(x±s)表示,比較采用t檢驗;計數資料以例數和百分比表示,比較采用χ2檢驗。以P<0.05為差異有統計學意義。
2 結 果
2.1 治療后兩組患者圍絕經期癥狀發生情況比較 治療后6個月,對照組和觀察組分別有4例(8.70%)和30例(50.85%)患者出現圍絕經期癥狀,對照組圍絕經期癥狀發生率低于觀察組(χ2=20.975,P<0.001)。
2.2 治療前后兩組患者FSH、雌二醇、LH水平比較 治療前,兩組患者FSH、雌二醇、LH水平比較,差異均無統計學意義(均P>0.05)。治療后,觀察組FSH和LH水平均高于治療前及對照組水平,雌二醇水平低于治療前及對照組水平(均P<0.05)。見表1。
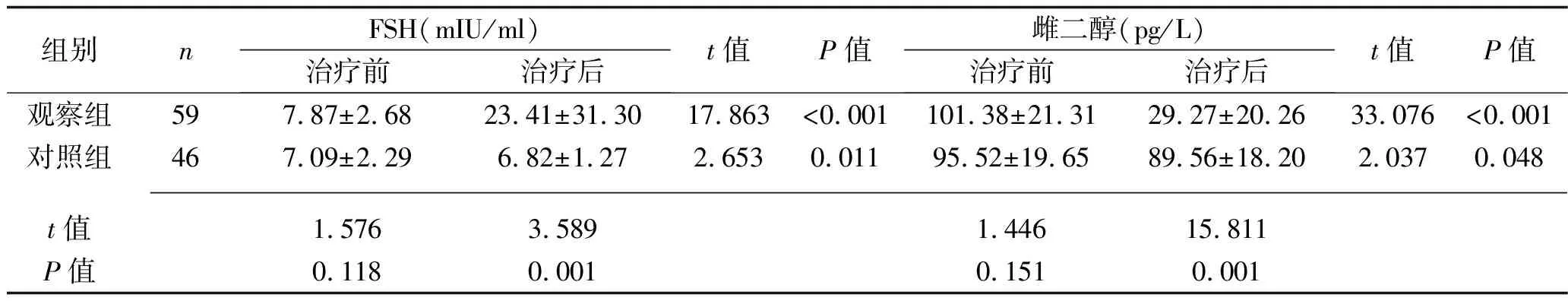
表1 治療前后兩組患者FSH、雌二醇、LH水平比較(x±s)

組別nLH(mIU/ml)治療前治療后t值P值觀察組597.51±2.8246.09±16.2726.838<0.001對照組468.04±2.577.43±1.762.0190.049 t值0.99316.026P值0.3230.001
2.3 治療后兩組患者卵巢功能保留情況比較 觀察組患者卵巢功能正常率低于對照組,卵巢功能衰退率及卵巢功能喪失率均高于對照組(均P<0.05)。見表2。

表2 兩組患者卵巢功能保留情況比較[n(%)]
3 討 論
宮頸癌作為婦科最常見的生殖系統惡性腫瘤,其發病率及死亡率較高,且發病呈年輕化趨勢[5]。目前宮頸癌的發病機制尚不清楚,可能是多因素作用的結果,與分娩次數、病毒感染、性行為及其他行為和生物學因素等均有關[6]。
治療宮頸癌的主要手段是放射治療和手術切除。而近年來,增敏化療聯合放療的臨床效果得到了肯定,其作用機制之一是化療藥物對放療有增敏作用,能夠顯著縮小腫瘤體積,降低宮頸癌遠處轉移率,從而提高放療療效[7]。目前,放射治療幾乎應用于三分之二癌癥患者的治療中,但術后輔助放射治療對卵巢功能影響較大。經常輻照可導致年輕宮頸癌患者出現卵巢衰竭等遠期不良后果。放射劑量達到250~300 cGy時患者卵巢功能可永久喪失,甚至可能導致終生不孕。治療腫瘤的同時需改善患者的生活質量是目前宮頸癌的治療原則,既要盡量徹底地切除腫瘤以減少復發和轉移,同時還要考慮患者的生理和心理是否受到影響。因此,對于年輕的早期宮頸癌患者應該盡可能地保留卵巢,以維持其體內的正常內分泌功能,減少由激素水平下降所帶來的神經系統、內分泌系統及心血管系統的并發癥。對此,有學者提出對于早期年輕宮頸癌患者,可采取卵巢移位術后行放射治療,以減小卵巢照射量,防止放射治療導致卵巢功能損害,從而保護卵巢功能[8]。卵巢移位術是通過卵巢移位并固定于盆腔外的腹腔,從而降低術后放療對卵巢功能的損害[9]。
FSH由垂體分泌,對促進卵子成熟和排卵具有重要影響,其水平的變化能直接反映卵巢功能狀態變化[10]。LH是一種由腺垂體嗜堿粒細胞分泌的激素,與FSH合稱為促性腺激素,兩者可協同調節女性月經周期,并影響雌激素分泌[11]。雌二醇由卵巢黃體分泌,其主要作用為增進和調節性器官的正常發育及維持子宮內膜形態,而高強度放射治療對卵巢功能的傷害會明顯降低雌二醇的分泌[12]。本研究結果顯示,治療后,觀察組FSH和LH水平均高于治療前及對照組水平,雌二醇水平低于治療前及對照組水平(均P<0.05),提示卵巢移位后行增敏化療聯合放療可影響卵巢內分泌功能,使血清性激素水平異常。此外,兩組均有患者出現卵巢功能衰退或喪失,而觀察組患者卵巢功能正常率低于對照組,卵巢功能衰退率及卵巢功能喪失率均高于對照組(P<0.05),且圍絕經期癥狀發生率高于對照組(P<0.05)。提示在卵巢移位手術后行聯合放療的患者卵巢功能均有一定程度下降,而術后行增敏化療聯合放療對卵巢功能影響更大,患者卵巢功能衰退更為明顯,說明盆腔放化療可能是影響卵巢功能的主要原因。值得注意的是,卵巢移位手術本身即有可能導致卵巢功能衰退,因此應嚴格控制手術指征,謹慎選擇行卵巢移位手術的對象。術中觸及腫大淋巴結或前哨淋巴結陽性、腫瘤直徑超過4 cm、宮頸活檢發現脈管內癌栓等,均提示術后聯合放療可能性大,如有合并以上高危因素的年輕患者,應積極行卵巢移位手術。
綜上所述,與術后單純放療比較,卵巢移位術后行增敏化療聯合放療的患者圍絕經期癥狀發生率更高,血清性激素水平紊亂及卵巢功能減退更為明顯。

