9例感染后繼發性機化性肺炎患者的臨床分析
金如月,劉秀明,朱佳榮,李進霞,張 紅
(寧夏醫科大學總醫院呼吸與危重癥學科,銀川 750000)
繼發性機化性肺炎(secondary organizing pneumonia,SOP)是原因明確的一類機化性肺炎(organizing pneumonia,OP),常見的引起SOP的病因包括感染(細菌、病毒、支原體等)、結締組織疾病、藥物(胺碘酮、博來霉素等)、放射線、器官移植等。其中感染后SOP最為常見。感染后SOP主要指經抗感染治療后,病原微生物得到清除, 但持續的炎性反應導致肺泡腔內纖維蛋白滲出。臨床上通常抗感染治療無效,易被誤診為肺炎、肺癌等,造成病情延誤及醫療資源的浪費。感染后SOP的確診往往需要組織病理學依據,臨床診斷過程中由于原發疾病的混淆,診斷相對困難。本文分析本院收治的9例感染后SOP患者的臨床特點,以期提高對此病的認識,現報道如下。
1 資料與方法
1.1一般資料 選取2017年1月至2018年1月本院呼吸與危重癥醫學科確診的9例感染后SOP患者,其中男3例,女6例,年齡50~68歲,平均(59±24)歲。9例患者中1例合并有高血壓病、1例合并有食道癌術后、1例合并房顫。
1.2方法 所有患者根據肺部感染病原學培養結果選用敏感抗生素治療2~3周,復查胸部CT并經組織病理學確診OP。所有患病均給予糖皮質激素治療,激素治療后1~3個月隨訪肺部影像學。
2 結 果
2.1臨床表現 癥狀:咳嗽9例,發熱8例,進行性加重的呼吸困難5例,咯血1例,伴有食欲減退7例、體質量下降6例。體格檢查:肺部體格檢查濕啰音9例,Velcro啰音7例。
2.2實驗室檢查 9例患者均存在Ⅰ型呼吸衰竭;8例血沉均升高,且大于或等于20 mm/h,1例血沉正常;9例患者的血腫瘤標志物如癌胚抗原(CEA)、糖類抗原(CA)125、CA199、神經元特異烯醇化酶(NSE)、細胞角蛋白19片段均正常;9例患者風濕免疫指標篩查均正常。
2.3病原學檢查 2例患者痰培養提示金黃色葡萄球菌,1例痰培養提示銅綠假單胞菌,1例甲型流感病毒(H1N1)陽性,1例痰培養提示白色念珠菌,1例患者痰培養示副流感嗜血菌,1例痰及肺泡灌洗液培養提示煙曲霉,2例無明確病原菌。
2.4胸部影像學 以單肺或雙肺多發的斑片滲出影3例,實變影3例,磨玻璃影1例,蜂窩影1例,空洞病變1例,其中有2例并發胸腔積液。
2.5電子支氣管鏡檢查 支氣管檢查過程中7例患者鏡下表現氣管腔黏膜充血,2例患者鏡下表現病灶管腔黏膜慢性病變,見圖1。
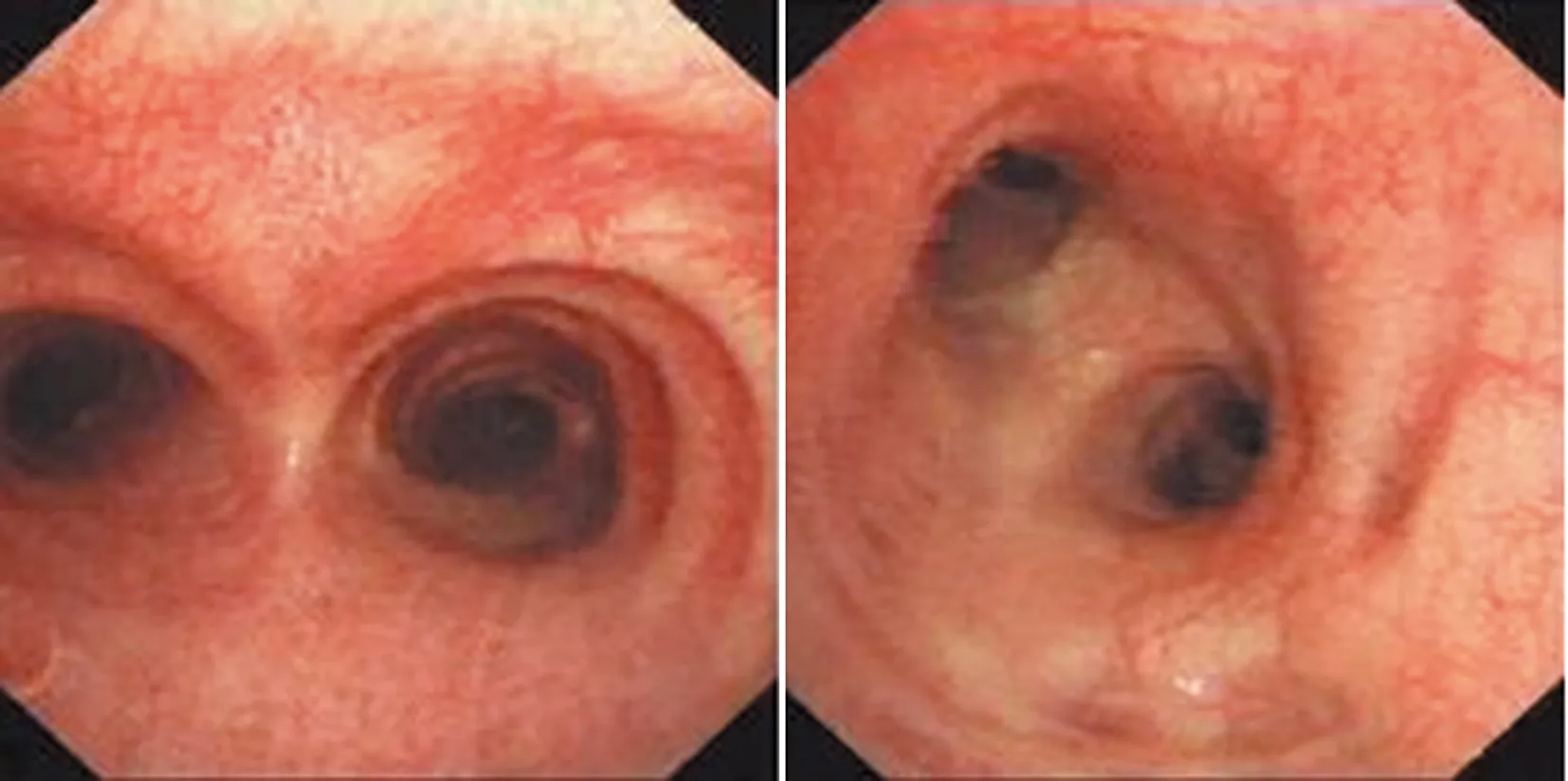
圖1 支氣管鏡檢查
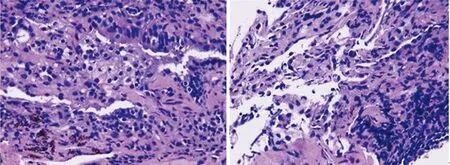
圖2 病理學檢查
2.6病理學檢查 9例患者中4例行經支氣管鏡肺活檢(TBLB),4例CT或B超引導下行經皮肺穿刺活檢,1例行胸腔鏡活檢,病理均提示:肺泡腔內可見纖維素性滲出物,部分滲出性纖維素周圍纖維母細胞包繞形成機化,肺間質內可見大量中性粒細胞、淋巴細胞,少量嗜酸性粒細胞浸潤,符合OP,見圖2。
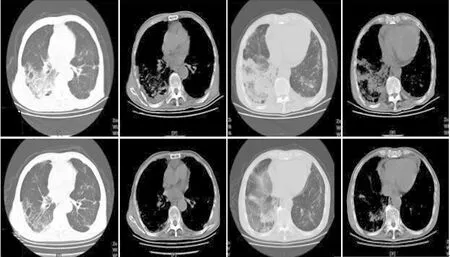
圖3典型病例胸部CT表現
2.7療效觀察 患者抗感染治療3周后的胸部CT以右肺滲出、實變為主,所有患者經臨床確診后,均給予糖皮質激素治療(激素劑量根據0.75 mg/kg使用),1周后復查CT提示病灶吸收達50%的有2例,半月后病灶吸收達50%有4例,1月后病灶吸收達50%有5例,3月后復查7例患者病灶吸收達50%,見圖3。
3 討 論
OP是指肺泡、肺泡管及細支氣管被疏松的纖維結締組織充填的一種疾病,根據病因是否明確,分為原發性OP(COP)和SOP。近年來,COP已逐漸為臨床醫師所認識,被歸為特發性間質性肺炎[1]。繼發于感染、藥物、結締組織病和吸入等因素所致的原因明確的OP稱為SOP[2]。但SOP并未得到足夠重視,檢索近20年SOP病例,導致SOP的原因最多見于結締組織疾病(如皮肌炎等),其次為放療、化療、感染等,關于感染后SOP報道很少,國外研究相對較多的是病毒感染,如H1N1、B型流感病毒等,3項相關報道中的患者均發生了嚴重的呼吸衰竭,部分患者甚至因此而死亡[3-5]。而國內關于感染后SOP病例報道有2例,1例是鮑曼不動桿菌感染,1例為大腸埃希菌感染,此兩項報道患者經積極治療均好轉[6-7]。我國近年來多次出現各種亞型的H1N1流行,但在流感病毒感染后SOP方面缺乏相關研究。
本研究顯示SOP多發生于中老年,男女發病無明顯區別。臨床多表現為發熱、咳嗽、進行性加重的呼吸困難,以咯血為首發癥狀,伴有乏力、消瘦等全身不適超過50%。VASU等[8]研究了33例OP病例(COP 18例、SOP 15例),發現SOP患者發熱更常見(73%),其次是干咳、呼吸困難,與本研究結果一致。此外,VASU等[8]研究發現SOP患者中肺部Velcro啰音最常見。本研究顯示9例SOP患者體檢中均有肺部啰音,其中有7例系典型的Velcro音。
OP的影像學特點為五多一少,即多形態、多發性、多變性、多復發性、多雙肺受累,少蜂窩肺。最常見的表現為雙肺多發的斑片狀實變影,另可見結節影、網狀、結節狀,較少見的空洞、反暈輪征、胸腔積液等[9],但國內無SOP的影像學表現特點的報道。DRAKOPANAGIOTAKIS等[10]研究發現COP和SOP在影像學方面無明顯差別,VASU等[8]研究發現SOP患者容易出現胸腔積液(60%)。而國內兩篇細菌感染后的SOP報道中,影像學表現以雙肺片狀實變影為主,可見支氣管充氣征,但未見病灶的游走性及多變性。本研究9例患者中,以單肺或雙肺多發的斑片滲出影、實變影3例,磨玻璃影及蜂窩肺2例,空洞病變1例;其中并發胸腔積液2例,此結果與國內相關報道結果一致,而國外研究易出現胸腔積液,與本研究結果存在一定差異。
OP的診斷依賴于臨床放射學特征和典型的病理學,感染后SOP的診斷主要依靠病原學、影像學特點、抗感染或抗真菌治療無效、排除其他已知原因(如結締組織疾病、腫瘤、藥物、器官移植等),且典型病理提示由斑片狀的肉芽組織構成的松散的栓子充填于肺泡和呼吸性細支氣管內[11]。本研究中9例SOP患者中有7例病原學明確為細菌、病毒、真菌感染,2例病原學未明。根據病原學結果選用敏感抗生素治療后,病變無吸收,后經肺組織活檢證實為OP,且排除了其他導致OP的常見病因。因此,對臨床中有明確病原體感染,在積極給予針對性治療后,患者仍出現發熱、干咳伴進行性呼吸困難等表現,且肺部影像學提示原發病灶無吸收或增多,在排除了已知病因后,需考慮OP可能。
大部分OP患者接受激素治療后臨床和影像學改變可完全消失[12],但激素減量或過早停藥病情會復發。本研究中9例患者根據病原學抗感染治療無效,病理確診后均開始加用激素治療,1周后復查影像學病灶吸收達50%的有2例,半個月后病灶吸收達50%有4例,1個月后病灶吸收達50%有5例,3個月后復查7例患者病灶吸收達50%。其中有1例患者治療1周復查病灶明顯吸收,但院外自行停藥,病灶復發。本病對腎上腺皮質激素反應良好,且早期使用治療效果更佳。
綜上所述,SOP患者臨床表現主要以發熱、咳嗽伴進行性加重的呼吸困難為主,均存在低氧血癥,胸部影像學主要表現為多發斑片狀滲出、實變,可伴胸腔積液,可獲取組織病理學加以診斷,治療應及時給予糖皮質激素。

