負載光敏劑D-甘露糖修飾膠束的制備及其在靶向光動力治療中的應用
蔡 穎,王勝濤,魏 朋,張 權,尹 健*
(1.江南大學 糖化學與生物技術教育部重點實驗室,江蘇 無錫 214122;2.江南大學 生物工程學院,江蘇 無錫 214122)
光動力療法(Photodynamic Therapy,PDT)是治療腫瘤疾病的一種非侵入性新技術[1-2]。這種治療策略主要依賴于單線態氧(1O2)的產生[3]:當低暗毒性光敏藥物在腫瘤組織區域富集后,向腫瘤部位給予特定波長的光照,光敏藥物吸收特定波長的光躍遷至激發態;此時處于激發態的光敏藥物會將能量傳遞給周圍腫瘤組織和細胞中的基態氧,產生活性很強的單線態氧,單線態氧和相鄰的生物大分子發生氧化反應,產生細胞毒性作用進而導致細胞受損和死亡[4-5]。
目前,用于光動力療法的光敏劑種類已經被廣泛開發,主要包括卟啉、二氫卟酚、酞菁、氟硼二吡咯(簡稱BODIPY)等[6-7]。這些光敏劑具有高熒光量子產率、高光穩定性、良好化學穩定性和易于化學修飾等性質,但其在水中溶解性較差,而且缺乏對腫瘤細胞的靶向性[8-9],因此嚴重制約了其在光動力療法臨床上的應用。近年來,已有許多報道利用新型靶向輸送系統在改善光敏劑性能方面取得了很大的進步,但仍需進一步開發安全高效的新型輸送載體材料用于靶向光動力治療研究。
膠束是一類藥物輸送系統。具有良好生物相容性的兩親性大分子能在水中自組裝形成膠束[10]。對疏水性的光敏劑進行親水性修飾,或以包載的形式構建成具有光敏特性的膠束,可以滿足光動力治療的要求。同時,由于腫瘤區域增強滲透與滯留(EPR)效應[11]的存在,通過構建適宜粒徑的具光敏特性的膠束可以實現很好的被動靶向作用,進一步提高光動力治療的效率,減少對正常細胞的毒副作用。但僅依靠EPR 作用不足以實現對癌細胞選擇性光動力治療;通常采用對光敏劑修飾靶向性分子或用具有靶向性的膠束包載光敏劑的方式,實現靶向光動力治療的目的。由于癌組織區域細胞的特殊的生長性質,其會在細胞膜表面過度表達多種靶向受體;而一些功能性靶向分子,例如透明質酸[12]、抗體[13]、多肽[14]、葉酸[15]等,能特異型識別這些受體,所以表面修飾有靶向分子的膠束能被癌細胞通過受體介導識別方式大量攝取,從而達到靶向輸送光敏劑進行光動力治療的目的,降低光動力治療對正常細胞的毒性。
甘露糖作為一類靶向性小分子已被應用于靶向藥物輸送的研究中[16]。近年來,已有研究表明修飾有甘露糖的納米載體能夠特異性識別甘露糖受體[17],而達到靶向給藥的目的;但利用甘露糖的靶向作用,實現選擇性光動力治療的研究鮮有報道。本文以D-甘露糖修飾的兩親性β-環糊精(β-CD)制備膠束,另外合成金剛烷(Ad)修飾的BODIPY 光敏劑分子,利用β-CD 與Ad 之間主客體識別[18]原理制備高負載光敏劑的膠束,考察其理化性質和光動力治療性能。以表面甘露糖受體高表達的人乳腺癌細胞MDA-MB-231 作為細胞模型,考察了負載光敏劑聚合物膠束通過甘露糖受體識別作用被MDA-MB-231 癌細胞攝入并用于靶向光動力治療的性能。
1 材料與方法
1.1 主要試劑
1-金剛烷甲酸(99%)、2-(2-氨基乙氧基)乙醇(99%)、對甲苯磺酰氯(TsCl,99%)、2,4-二甲基吡咯(97%)、N-碘代丁二酰亞胺(NIS,99%)、2,3-二氯-5,6-二氰基-1,4-苯醌(DDQ,98%)、對甲基苯磺酸(98%)、三氟甲磺酸三甲基硅酯(TMSOTf,99%)、3-(4,5-二甲基-2-噻唑基)-2,5-二苯基-2H-四氮唑鎓溴化物(MTT,98%)、(+)-L-抗壞血酸鈉(99%)、五水硫酸銅(CuSO4·5H2O,98%)、炔丙醇(99%)均于百靈威科技有限公司購買;9,10-蒽基-雙(亞甲基)二丙二酸(ABDA)、4’,6-二脒基-2’-苯基吲哚(DAPI)購于sigma 試劑有限公司;D-甘露糖(D-Mannose,分析純)、β-環糊精(β-CD,98%)購于國藥集團化學試劑有限公司。
1.2 主要儀器
AVANCE 400M 型核磁共振儀,德國Bruker 公司生產;熒光分光光度計,美國Agilent 公司生產;Nano ZS 動態光散射儀(DLS),英國Malvern 公司生產;UV-3 900 紫外可見分光光度計,日本日立公司生產;JEM-2 100 透射電子顯微鏡(TEM),日本電子株式會社生產;激光共聚焦顯微鏡(CLSM),日本尼康株式會社生產;Enspire 多標記檢測系統,美國PerkinElmer 公司生產。
1.3 D-甘露糖修飾的兩親性β-CD(C3-CDMan7)與光敏劑BTA 的合成
D-甘露糖修飾的丙酰化環糊精分子C3-CDMan7的化學合成方法參照文獻[19]。共價鍵連金剛烷(Ad)的BODIPY 光敏劑分子(BTA)的合成方法參照文獻[20]。
1.4 負載光敏劑BTA 膠束(BTA@C3-CD-Man7)的制備
采用透析凍干法制備高負載光敏劑膠束BTA@C3-CD-Man7。準確稱取C3-CD-Man7(150 mg,41.44 μmol)和光敏劑BTA(12 mg,7.75 μmol);用3 mL DMSO 溶解C3-CD-Man7,室溫下攪拌2 h,制得溶液①;另用3 mL DMSO 溶解BTA,室溫下攪拌2 h,制得溶液②。然后將溶液②加入溶液①,再在室溫下攪拌2 h,獲得混合溶液。再向上述混合溶液中,緩慢滴加20 mL DD H2O,并于室溫下攪拌30 min。然后將制備的BTA@C3-CD-Man7溶液轉移到透析袋(MW 2 000)中透析2 d,每6 h 換一次水,除去DMSO。冷凍干燥所獲澄清綠色溶液,獲得BTA@C3-CD-Man7粉末。
1.5 膠束的TEM 與DLS 表征
對于TEM 樣品的制備,分別稱取C3-CD-Man7和BTA@C3-CD-Man7并配制兩種膠束的水溶液(1 mg/mL);各取50 μL 上述溶液,滴加于電鏡銅網上,并對膠束C3-CD-Man7的銅網用磷鎢酸復染處理,待兩種TEM 樣品晾干后,于電鏡下進行觀察。對于DLS 樣品的制備,分別配制濃度為200 μg/mL C3-CD-Man7和BTA@C3-CD-Man7的10%胎牛血清培養液,并各取上述溶液1 mL,通過DLS 在25°C 條件下測定其流體力學直徑。
1.6 BTA@C3-CD-Man7中BTA 含量的測定
BTA@C3-CD-Man7中負載光敏劑BTA 的質量百分比通過紫外可見分光光度計(UV-3 900)進行準確測定。分別配制光敏劑BTA 的DMSO 溶液(1 mg/mL)和BTA@C3-CD-Man7的DMSO 溶液(1 mg/mL)待用。稱取BTA 固體粉末,并配制濃度為5、10、15、20、25、30 μg/mL 的系列溶液,利用紫外可見分光光度計對BTA 在300~800 nm 波段內進行全波長掃描,測定其在最大吸收665 nm 處的吸光度。以吸光度A 與質量濃度c 作圖,制作光敏劑BTA 的標準工作曲線,計算出BTA 的質量濃度與吸光度之間的線性關系,進而測定BTA@C3-CD-Man7中BTA 的百分含量。
1.7 BTA@C3-CD-Man7產單線態氧性能的測定
單線態氧捕獲劑ABDA 能被氧化導致熒光強度降低,從而表征負載光敏劑的膠束產單線態氧的性能[21]。準確稱取兩份1 mg ABDA,分別用DMSO、DD H2O 溶解,配制成兩種1 mg/mL 母液待用;再配制1 mg/mL BTA@C3-CD-Man7水溶液。通過熒光分光光度計測定,選取終質量濃度為0.5 μg/mL 的ABDA 溶液為宜。然后分別配制四種溶液:0.5 μg/mL ABDA 的水溶液、0.5 μg/mL ABDA 的DMSO 溶液,0.5 μg/mL ABDA+0.04 mg/mL BTA@C3-CD-Man7的水溶液和其DMSO 溶液。用LED 光源(665 nm,20 mW/cm2)分別對上述溶液進行10、20、30、40 min照射,在激發波長為380 nm 的條件下,分別測定上述各溶液在熒光波段(390~500 nm)處的熒光光譜。
1.8 甘露糖受體介導的細胞內吞
將人乳腺癌細胞MDA-MB-231 接種于細胞培養皿內,置于37 ℃、5% CO2的培養箱孵育24 h,使其貼壁生長。加入含有BTA@C3-CD-Man7(160 μg/mL)的培養液繼續培養24 h。棄去培養液,用pH 7.4磷酸鹽緩沖液(PBS)清洗2 次。將癌細胞用4.0% 甲醛在室溫下固定15 min 后,移除甲醛溶液,1 mL PBS 清洗2 次,再用4’,6-二脒基-2’-苯基吲哚(DAPI,1 μg/mL)對細胞核進行染色15 min[22],最后用PBS 溶液清洗2 次。利用激光共聚焦顯微鏡(CLSM)觀察BTA@C3-CD-Man7在細胞內部的分布狀態(激發波長:408/561 nm;發射波長:417~477/570~1 000 nm)。
1.9 小分子甘露糖競爭性實驗
與上述細胞攝取實驗相似,先將MDA-MB-231癌細胞接種于細胞培養皿內,讓其貼壁生長24 h。然后再加入含過量小分子甘露糖的新鮮培養液繼續于孵育箱中培養4 h。移除舊的培養基,加入含有BTA@C3-CD-Man7(160 μg/mL)的培養液繼續培養24 h。棄去培養液,用pH 7.4 的磷酸鹽緩沖液(PBS)清洗2 次。對細胞樣依次經4.0%甲醛固定,DAPI 染色15 min,PBS 緩沖液清洗處理。最后,利用激光共聚焦顯微鏡(CLSM)觀察BTA@C3-CD-Man7被癌細胞吸收的情況(激發波長:408/561 nm;發射波長:417~477/570~1 000 nm)。
2.0 細胞毒性評價
采用MTT 法對空白膠束和負載光敏劑膠束的光暗細胞毒性進行評價[23]。將人乳腺癌細胞MDAMB-231 種植于96 孔板內,每孔約10 000 個細胞。在37 ℃、5% CO2的培養箱中孵育細胞24 h 后,加入含BTA@C3-CD-Man7或C3-CD-Man7的10%胎牛血清培養基,確定體系中所含光敏劑BTA 的質量濃度為20 μg/mL,繼續于孵育箱中培養一段時間。待24 h 后,分別進行665 nm LED 光源照射30 min和黑暗環境處理后,移除培養液,用pH 7.4 的PBS緩沖溶液清洗2 次,每孔中加入100 μL MTT 培養液(0.5 mg/mL)繼續培養4 h。移除每個孔內MTT 培養液,再加入100 μL DMSO,振蕩10 min,用多功能酶標儀測量490 nm 處各孔的吸光值(OD),計算細胞存活率。
2 結果與分析
2.1 BTA@C3-CD-Man7的設計制備及其光動力治療策略
通過β-CD 和金剛烷超分子識別作用將甘露糖功能化β-CD 固定到光敏劑納米聚集體表面,從而制備了表面甘露糖功能修飾的光敏劑納米粒子[20]。然而由于上述研究的納米粒子在水溶液中的長期穩定性較差,因此需要進一步開發具有高穩定性的負載光敏劑輸送載體材料。為了實現這一目標,本研究希望通過C3-CD-Man7自組裝形成膠束,同時包載BTA 進入膠束的疏水性空腔,從而提高負載BTA 膠束的穩定性,并將其應用于靶向光動力治療的研究中。
通過透析凍干法制得新型負載光敏劑膠束BTA@C3-CD-Man7,并將其應用于靶向光動力治療人乳腺癌細胞MDA-MB-231 的研究中。如圖1 所示,將所獲具有靶向作用的BTA@C3-CD-Man7與MDA-MB-231 癌細胞共培養。利用甘露糖受體識別介導光敏劑BTA 被癌細胞內吞,并在665 nm LED燈照射下誘導胞質內的基態氧產生單線態氧,進而氧化殺傷癌細胞;這里細胞中基態氧主要以三線態氧(3O2)形式存在。
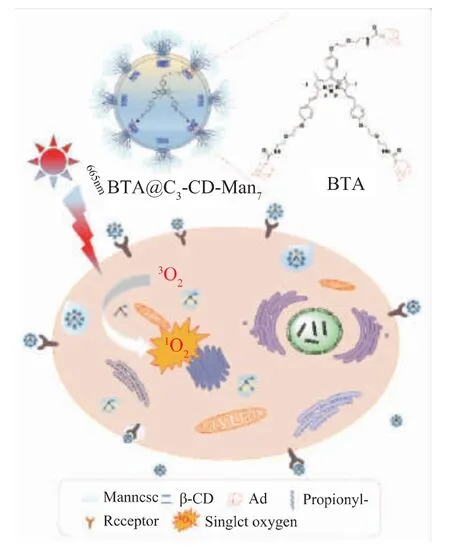
圖1 BTA@C3-CD-Man7的結構及其應用于靶向光動力治療的示意Fig.1 Schematic illustration of BTA@C3-CD-Man7for targeted PDT
2.2 膠束的DLS 與TEM 表征
優良的兩親性納米載體需具有良好的結構外形和穩定性。通過TEM 觀察膠束的形貌和粒徑,用DLS 測定膠束的水合粒徑分布以及一段時間內在生物溶劑中的穩定性,結果見圖2。根據TEM 與DLS 的結果,空白膠束C3-CD-Man7在負載光敏劑BTA 后,平均粒徑明顯增大。由于在溶液中膠束表面會形成水合層,其流體力學粒徑明顯大于TEM測得的真實粒徑,對比空白膠束的TEM 和DLS 的結果可知,其由TEM 測得真實直徑30 nm 左右變為DLS 測得的流體力學直徑110 nm 左右(圖2(a)和圖2(c));負載光敏劑膠束BTA@C3-CD-Man7也呈現類似的結果(圖2(b))。而圖2(c)則表示兩種膠束的動態光散射實驗結果,其中C3-CD-Man7的PDI 值 為0.210,BTA@C3-CD-Man7的PDI 值 為0.291,這表明兩者均一性較好。另外,選取3 d 來考察空白膠束C3-CD-Man7以及負載光敏劑膠束BTA@C3-CD-Man7在含10%胎牛血清的培養基中穩定性,一般3 d 是藥劑在生物體內循環作用的時間;從圖2(d)中則可以看出,在培養基中兩種膠束流體力學直徑波動較小,在這段時間內膠束的整體結構較穩定,滿足光動力治療的要求。
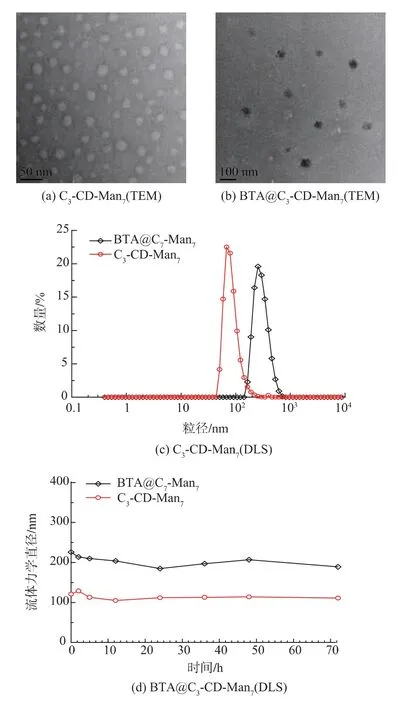
圖2 C3-CD-Man7和BTA@C3-CD-Man7的透射電鏡照片,水溶液中的流體力學直徑分布圖以及在10%胎牛血清培養基中的長期穩定性Fig.2 TEM images,hydrodynamic size distributions in water and long-term colloidal stability in culture medium with 10% FBS of the micelles
2.3 BTA@C3-CD-Man7中BTA 含量的測定
膠束僅作為輸送載體,介導光敏劑在腫瘤組織中富集并用于光動力治療時需明確光敏劑的量。通過紫外分光光度計分別測定一系列濃度下光敏劑BTA 在最大吸收665 nm 處的最大吸光度,制定出BTA 的標準工作曲線,從而表征BTA 濃度與吸光度之間的線性關系。結果如圖3 所示:從圖3(a)中可以明顯看出不同濃度下BTA 在665 nm 處均有最大吸光度;進而繪制其標準工作曲線,見圖3(b)。這一實驗結果表明光敏劑的濃度與其最大吸收處的吸光度兩者之間具有良好的線性關系。根據朗伯比爾定律科:
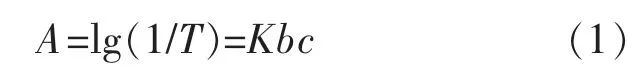
式中:A 為吸光度;T 為透射比;b 為吸收層厚度;c為吸光物質的質量濃度;K 為吸光系數,只與物質本身性質相關。光敏劑BTA 的吸光系數K 為0.048 6。
根據上述測定方法,取負載光敏劑膠束BTA@C3-CD-Man7加入1 mL DMSO 中破壞膠束,測定其吸光度,即可知道膠束中光敏劑BTA 濃度與吸光度之間的關系。通過計算,可知負載光敏劑膠束BTA@C3-CD-Man7中BTA 的質量百分比為14%。另外,本文對末端未共價鍵連金剛烷的BODIPY 光敏劑,按上述相同的方法制備另一種載光敏劑膠束,并對其確切的包載量進行測定。結果發現其包載率僅為5%左右,這些結果表明由于β-CD 與金剛烷之間的超分子識別作用,由C3-CDMan7自組裝形成膠束包載BTA 的能力明顯增強。
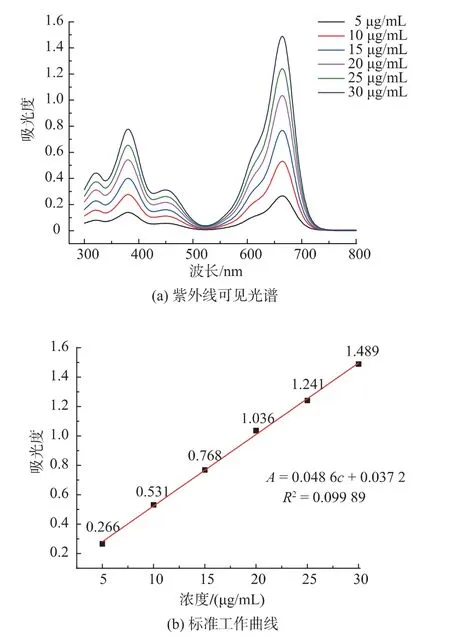
圖3 B TA 的紫外可見光譜圖和標準工作曲線Fig.3 UV -vis spectrum andthe standard curve of photosensitizer BTA in DMSO
2.4 BTA@C3-CD-Man7產單線態氧的研究
光敏劑產單線態氧(1O2)的能力是衡量其光動力治療效果的重要指標。光敏劑在特定波長的光照下產生的單線態氧能將其捕獲劑ABDA 氧化,進而導致ABDA 在其特征吸收光帶(390~500 nm)處熒光強度降低,通過這種方式間接地表征單線態氧的產生。
實驗結果如圖4 所示:在有機溶劑DMSO 中在光照條件下下不斷產生有單線態氧(1O2)產生,而ABDA 捕獲1O2后導致結構改變,熒光猝滅,熒光強度下降,通過連續階段的光照,ABDA 的熒光強度不斷的降低(圖4(a));而在去離子水中,即便給予長時間光照,也不能產生單線態氧,故而單線態氧捕獲劑ABDA 的熒光強度不變(圖4(b))。這一現象主要是由于BTA@C3-CD-Man7在兩種溶劑中存在形式的不同引起:其在DMSO 中以分子狀態存在,而在水中則以膠束的形式存在。
以上實驗證明BTA@C3-CD-Man7以分子狀態存在時能夠在近紅外光照射下不斷產生單線態氧,滿足光動力治療殺傷癌細胞的條件。為了考察溶劑因素對實驗結果的影響,另做兩組空白對照實驗驗證:①ABDA 的水溶液在連續光照下熒光光譜;②ABDA 的DMSO 溶液在連續光照下熒光光譜。結果表明了單線態氧捕獲劑ABDA 在水相或油相中穩定,熒光強度不會改變,也證實了上述實驗中ABDA熒光強度的改變僅是光敏劑在起作用。
2.5 甘露糖受體介導的細胞內吞
利用激光共聚焦顯微鏡(CLSM),考察BTA@C3-CD-Man7經甘露糖受體介導被人乳腺癌細胞MDA-MB-231 內吞的性能,研究甘露糖的靶向作用。BTA@C3-CD-Man7與MDA-MB-231 癌細胞在5% CO2的孵育箱中共培養24 h 后,依次用4%甲醛固定,1 μg/mL DAPI 染色,pH 7.4 PBS 溶液清洗保存,然后使用激光共聚焦顯微鏡觀察。結果見圖5,癌細胞的細胞核經過DAPI 染色而呈現藍色,光敏劑BTA 呈現紅色熒光,通過兩者疊加圖,可以明顯地看到BTA 被內吞進入細胞。
由于甘露糖受體介導的細胞內吞,負載光敏劑膠束BTA@C3-CD-Man7具有良好的靶向性。將BTA@C3-CD-Man7與人乳腺癌細胞MDA-MB-231共培養24 h 后,在癌細胞內有大量紅色熒光,這些紅色熒光是由于BTA@C3-CD-Man7被內吞入細胞后解組裝釋放BTA 分子所產生的(圖5(a))。而通過提前用過量的小分子甘露糖對癌細胞表面的甘露糖受體進行競爭性實驗,發現膠束靶向內吞受阻和光敏劑BTA 的內吞量減少,表現為細胞內紅色熒光強度明顯降低(圖5(b))。上述靶向性細胞攝取實驗和小分子甘露糖競爭性實驗充分證實了甘露糖分子具有良好的靶向作用,也表明了負載光敏劑膠束BTA@C3-CD-Man7能夠靶向識別乳腺癌細胞MDA-MB-231 表面的甘露糖受體,并通過受體識別內吞的方式進入癌細胞內,實現了良好的靶向輸送光敏藥物的目的。
2.6 光動力治療的細胞評價
細胞水平上的光動力治療效果,作為衡量光敏劑用于光動力療法的必要指標。利用激光共聚焦顯微鏡(CLSM),研究BTA@C3-CD-Man7被內吞進入癌細胞的情況,進而在光動力治療后對人乳腺癌細胞MDA-MB-231 進行細胞形態觀察、評價。
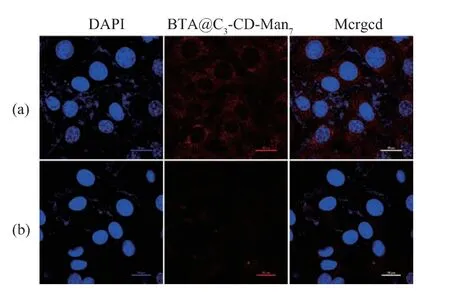
圖5 BTA@C3-CD-Man7(160 μg/mL)與癌細胞MDAMB-231 共培養24 h 后分別在無甘露糖環境和有小分子甘露糖競爭下的激光共聚焦顯微鏡圖Fig.5 CLSM images of MDA -MB -231 cancer cells incubated for 24 h with BTA@C3-CD-Man7(160 μg/mL)as indicated
結果如圖6 所示:在不對癌細胞給予LED(665 nm,20 mW/cm2)燈照射的條件下,光敏劑不會產生單線態氧而殺傷細胞,此時細胞形態飽滿,細胞核圓潤,可以清晰地看見細胞整體外形(圖6(a));而當對癌細胞給予LED 光照30 min 時,光敏劑BTA將能量轉移給胞質中的基態氧而產生單線態氧(1O2),進而殺傷癌細胞,表現為細胞整體形態萎縮,細胞明顯變小,細胞核也嚴重蜷縮變小,出現明顯的光動力治療效果(圖6(b))。
實驗通過CLSM 直接觀察到MDA-MB-231 癌細胞在黑暗環境和給予光照條件下,癌細胞大小與形態以及細胞核大小與形態均出現明顯差異。表明BTA@C3-CD-Man7在體外細胞水平上有明顯的光動力治療效果,初步滿足光敏劑用于光動力治療的要求。
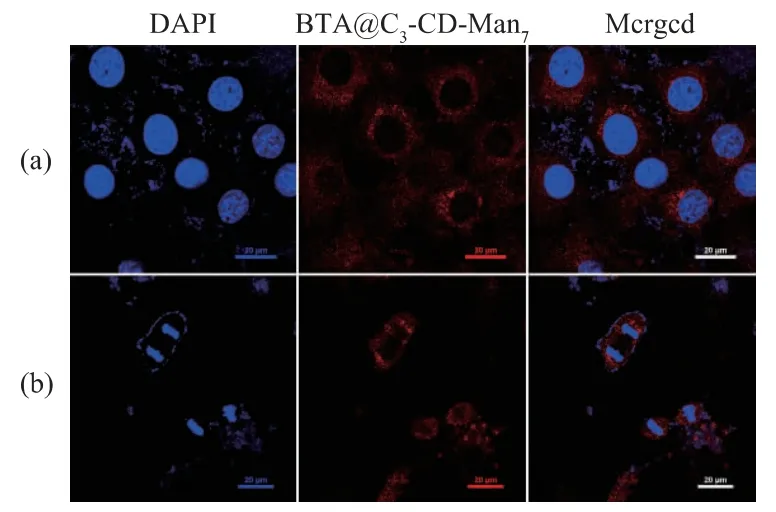
圖6 B TA@C3-CD-Man77(160 μg/mL)與癌細胞MDAMB-231 共培養24 h 后在黑暗環境或665 nm LED燈光照30 min 條件下的激光共聚焦顯微鏡圖Fig.6 CLSM images about PDT of MDA -MB -231 cancer cells incubated with BTA@C3-CD-Man7(160 μg/mL)for 24 h followed
2.7 細胞毒性評價
用于光動力治療的光敏劑應具有低的暗毒性,以及高的光動力治療性能[24]。實驗采用MTT 法分別考察空白膠束C3-CD-Man7和負載光敏劑BTA 膠束BTA@C3-CD-Man7分別在黑暗和665 nm LED燈光照30 min 條件下對人乳腺癌細胞MDA-MB-231 的毒性,實驗結果見圖7。
由圖7a 可知,隨C3-CD-Man7和BTA@C3-CDMan7劑量的增加,在不給予LED 燈光照的黑暗條件下,MDA-MB-231 癌細胞存活率略有降低;當膠束的質量濃度達到200 μg/mL(此時BTA@C3-CDMan7中BTA 的質量濃度約為25 μg/mL)時,細胞存活率仍大于90%。這表明C3-CD-Man7具有良好的生物相容性,是一種優良的靶向輸送載體;而且BTA@C3-CD-Man7表現為低暗毒性,滿足光敏劑低暗毒性的條件。而由圖7(b)可知,將甘露糖受體過度表達的人乳腺癌細胞MDA-MB-231 分別與相同劑量的兩種膠束共同孵育后,在665 nm LED 光照條件下,癌細胞存活率表現出明顯差異;孵育有BTA@C3-CD-Man7的癌細胞存活率大大降低,當其濃度達到200 μg/mL 時,細胞存活率僅為7%,表現出極高的光療效果;而LED 燈光照對孵育有C3-CD-Man7的癌細胞幾乎無毒副作用。
由于BTA@C3-CD-Man7能通過甘露糖受體介導的內吞作用將光敏劑BTA 輸送進入癌細胞內,在特定波長(665 nm)光照下,BTA 能大量誘導單線態氧的產生,進而殺傷癌細胞,表現出優良的光動力治療性能。因此,BTA@C3-CD-Man7是一種優良的光動力治療材料,可以靶向性地光動力治療人乳腺癌MDA-MB-231 細胞。
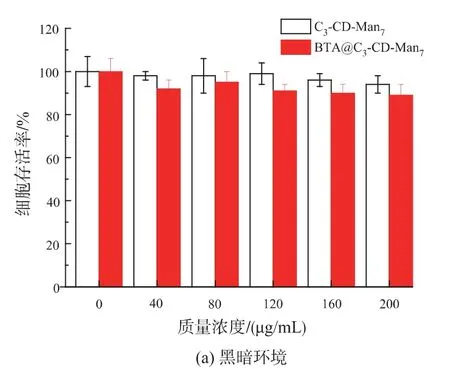
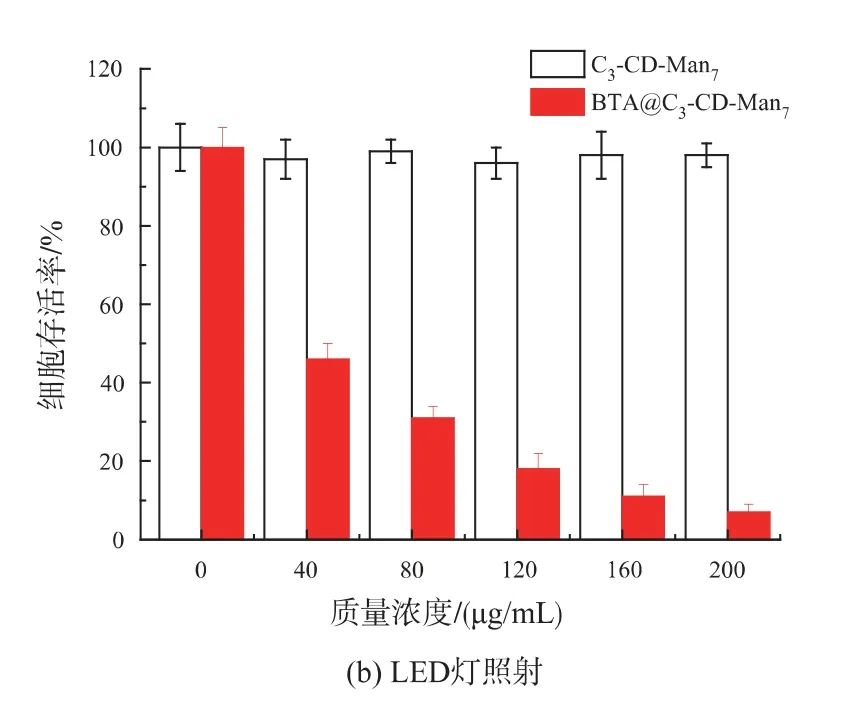
圖7 C3-CD-Man7和BTA@C3-CD-Man7分別與MDAMB-231 癌細胞共培養24 h 后黑暗環境或665 nm LED 燈照射30 min 的細胞存活率(n=6)Fig.7 Viability of MDA-MB-231 cells after 24 h of incubation with C3-CD-Man7or BTA@C3-CDMan7at different doses followed byincubation in the dark or irradiation with LED light for 30 min(n=6)
3 結語
借助具有良好生物相容性的藥物輸送載體,靶向性地將用于光動力治療的光敏劑輸送進入到腫瘤細胞中,減少其在正常組織和細胞中的分布,可以提高光動力治療效率,同時降低毒副作用。本研究利用β-CD 與Ad 之間主客體識別原理制備BTA@C3-CD-Man7,其負載BTA 的量明顯提高,并將BTA@C3-CD-Man7應用于人乳腺癌MDA-MB-231 細胞的光動力治療,考察其用于光動力治療的性能。結果顯示,BTA@C3-CD-Man7能與MDA-MB-231 癌細胞表面的甘露糖受體特異性識別,而被人乳腺癌細胞MDA-MB-231 大量攝入并釋放BTA,在665 nm LED 光照下,表現出對乳腺癌細胞的靶向光動力治療效果。因此,利用甘露糖的靶向作用以及環糊精與金剛烷的特異識別作用,新型高負載BTA 膠束BTA@C3-CD-Man7在乳腺癌的光動力治療中具有極大的應用潛力。

