熒光素鈉引導手術切除腦惡性膠質瘤臨床應用價值分析
神經膠質瘤是常見原發惡性腦瘤,高級別膠質瘤患者1年生存率僅53.7%,2年生存率不到15%[1]。高級別膠質瘤具有死亡率高、復發率高、發病率高、治療難度高、治愈率低等特點,患者預后差。隨著對腦惡性膠質瘤認知的加深,越來越多的研究者發現首次手術中腫瘤切除程度是預后的主要決定因素之一,因此提高腫瘤切除率成為神經外科醫生努力的方向,并創造出術中MRI導航、術中超聲波,皮質點刺激積極熒光引導腫瘤切除等方法[2]。目前熒光引導顯微手術在國內外是較成熟的技術,國外包括術中5-氨基乙酰丙酸(5-ALA)和熒光素鈉(FLS)引導,但國內5-ALA應用極少,且其操作方法較熒光引導繁瑣,儀器昂貴,嚴重限制其推廣。本研究分析了熒光素鈉引導手術切除腦惡性膠質瘤的應用價值,報告如下。
1 資料與方法
1.1 納入標準及排除標準
納入標準[3-4]:家屬及患者均簽署知情同意書;臨床資料齊全;完成隨訪;經CT、MRI等檢查確診的復發腦惡性膠質瘤。排除標準[5]:凝血功能障礙;嚴重肝、腎、心等重要臟器功能異常;有手術禁忌證;臨床資料不全。
1.2 一般資料
選取2014年6月至2016年6月恩施土家族苗族自治州中心醫院住院部腦惡性膠質瘤患者60例,根據術式不同分為2組。觀察組:30例,男性16例,女性14例;年齡(26~73)例,平均(45.87±10.92)歲;病變部位:丘腦1例,島葉4例,頂葉4例,顳葉8例,額葉13例;MRI下16例腫瘤未達腦梗能區,14例侵犯腦功能區;顱內壓升高19例,癲癇1例,一側偏癱6例,不完全失語3例,普遍有不同程度頭痛、頭暈、行走不穩現象。對照組:30例,男性18例,女性12例;年齡(31~70)例,平均(46.01±9.42)歲;病變部位:丘腦1例,島葉3例,頂葉5例,顳葉9例,額葉12例;MRI下17例腫瘤未達腦梗能區,13例侵犯腦功能區;顱內壓升高17例,癲癇2例,一側偏癱4例,不完全失語2例,普遍有不同程度頭痛、頭暈、行走不穩現象。兩組患者上述資料比較,P均>0.05,有可比性。研究經醫院倫理委員會審批通過,患者或家屬均簽署知情同意書。
1.3 方法
觀察組:行全身麻醉,在黃熒光下行顯微外科手術治療,術前30 min行熒光素鈉皮試,稀釋0.5 ml熒光素鈉至5 ml完成靜脈推注,觀察15 min確定皮試陰性為后可行手術,稀釋5 ml熒光素鈉為熒光素鈉液(20%),按5~10 mg/kg行靜脈滴注,常規開顱,暴露腫瘤位置,使用熒光顯微鏡(蔡司Pentero 900型)觀察,剪開硬膜調至熒光模式,波段為560 nm,可見腫瘤實質部位有黃綠熒光腫瘤,周圍為淡黃色,正常腦組織并無熒光黃染,之后切除腫瘤。使用YE560熒光模式監護整個切除過程,若患者出血則調至普通白光模式,止血治療,當YE560熒光模式下術野腫瘤與正常腦組織亮度一致則調至普通光模式。切去熒光染色最外層腫瘤組織及瘤腔無黃染腦組織送至監察室行冰凍切片病理檢查,在保護神經功能前提下爭取顯微鏡下最大限度切除復發腫瘤組織,關閉顱腔行常規治療。觀察染色組織與組織病理學結果是否一致。計算熒光染色特異性、敏感性。對照組:行傳統顯微外科腫瘤切除,具體操作按常規顯微外科手術方法切除腫瘤,術后取腫瘤標本行病理檢查。
1.4 觀察指標
隨訪3~12個月。使用卡氏評分(KPS)評估功能狀態[6]:健康,無體征及癥狀為100分;活動正常有輕微癥狀為90分;活動勉強正常,有部分體征及癥狀為80分;努力自理生活,無法正常工作和生活為70分;能自理大部分生活,偶爾需他人幫忙為60分;大部分生活無法自理,常需他人幫助為50分;生活無法自理,需陪護為40分;生活完全無法自理,危重需住院為30分;危重其必須支持治療為20分;病危,急劇惡化為10分。記錄并發癥、復發率、死亡率。復發診斷標準[7]:出現在原發腫瘤處或其周圍2 cm范圍內,復發時間為首次切除至定期復查發現病灶復發的間隔時間,再次手術術后病理結果確認復發膠質瘤。
1.5 統計學分析
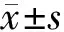
2 結果
2.1 兩組切除情況對比
觀察組整體情況全切率較對照組高,肺功能區及功能區全切率均較對照組高,P<0.05,見表1。

表1 兩組切除情況對比(例,%)
2.2 兩組功能區切除患者術前術后KPS分值對比
兩組功能區切除患者術前術后KPS分值比較均為P>0.05;兩組術后KPS分值均提高,P均<0.05;觀察組術前術后KPS分值之差較對照組大,P<0.05。見表2。

表2 兩組功能區切除患者術前術后KPS分值對比分)
2.3 兩組住院時間、手術時間對比
觀察組住院時間、手術時間均較對照組短,P均<0.05,見表3。
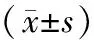
表3 兩組住院時間、手術時間對比
2.4 隨訪結果
隨訪3~12個月,觀察組較嚴重并發癥:肌力下降(4例)經治療后恢復;累及語言區(2例)者術后對癥治療基本恢復至術前水平;并發癥發生率為20.00%。對照組較嚴重并發癥:肌力下降(10例)出院時6例恢復;累及語言區(4例)術后對癥治療基本恢復;術后癲癇(2例)經治療緩解,并發癥發生率為53.00%。觀察組復發5例(16.67%),死亡1例;對照組復發10例(33.33%),死亡2例。兩組并發癥及復發率比較,P均<0.05。
3 討論
熒光素鈉能引導腦惡性膠質瘤切除,是因為腦惡性膠質瘤患者血腦屏障遭到破壞,熒光素鈉經靜脈注射后能順利穿過被破壞的血腦屏障,滲透到血管外,進入白腫瘤侵襲的腦組織以及腫瘤組織內,在腫瘤細胞外間質中聚集,因此術中可見腫瘤組織表面有黃綠熒光色,且正常腦組織并無著色現象[8]。術中結合普通手術用顯微鏡,肉眼下可發現正常腦組織與腫瘤的邊界,故熒光素鈉能能使術者一目了然的觀察切除腫瘤的邊界,減少不必要操作,避免周圍腦組織損傷加重;此外熒光素鈉毒性低,安全性高,可操作性好,避免毒性作用損傷周圍腦組織[9-10]。故觀察組并發癥發生率(20.00%)較對照組(53.00%)低;術后KPS分值明顯提高,且術前術后差值較對照組大,P<0.05。這無疑對患者術后恢復有利,縮短患者住院時間。故觀察組住院時間較對照組短,P<0.05。
治療腦膠質瘤的原則是盡可能用顯微神經外科技術力爭在安全情況下最大范圍切除腫瘤,即部損傷功能區的前提下擴大腫瘤切除范圍[11]。但膠質瘤呈侵襲性生長,故難以確定腫瘤與正常腦實質,難以在短時間內準確定位腫瘤與正常組織邊界,這是腦膠質瘤切除術難點之一[12]。常規顯微鏡神經外科手術以腦回、腦溝為邊界,沿腫瘤邊界白質纖維束做解剖式切除,手術操作主要依靠術者經驗。目前手術方式已經過度到“解剖-功能模式”,但“保護功能并最大范圍切除腫瘤”依然是臨床難點。熒光素鈉引導手術切除提供了更準確、良好的視野,避免術者過于依賴個人經驗,為切除范圍提供有效參考,縮短辨別腫瘤與正常組織的時間,準確定位預備切除區,提高手術效率和全切率[13-14]。故觀察組整體情況全切率較對照組高,肺功能區及功能區全切率均較對照組高;觀察組手術時間較對照組短。P均<0.05。全切率直接關系患者術后預后,故觀察組12年復發率較對照組低,P<0.05。
一些研究者指出熒光素鈉染色較淺的組織及相鄰水腫區在術前MRI增強下并未表現出來,而使用5-ALA引導的腦膠質瘤切除術中也存在染色模糊區在術前MRI并不可見,而切除這些區域將能降低復發和進展風險[15]。而以上切除范圍原則并非適用于處于功能區的腫瘤,若處于肺功能區可以完全切除,若接近功能區或處于功能區則將深色部分切除,染色較淡的部分適當保留,從而保證一定功能。
綜上,熒光素鈉引導手術切除腦惡性膠質瘤能幫助術者確定切除范圍,針對是否處于功能區確定實際切除范圍,提高全切率并保護腦功能,減少并發癥;該方法擴大了非功能區可切除范圍,減少術后復發率;該方法在腦惡性膠質瘤中具有較高臨床應用價值,對于級別較低的腦膠質瘤切除的意義尚需進一步研究。

