手術治療高危型HPV病毒感染致宮頸低級別鱗狀上皮內病變的臨床研究
沈 琳,黃艷艷,張 瀅
(南開大學附屬醫院/天津市第四醫院婦產科 300202)
2008年,Harald zur Hausen教授提出持續性的人乳頭瘤病毒(HPV)感染是宮頸癌發生的必要條件[1],使HPV轉陰是治療或預防宮頸癌及癌前病變的重點。據報道,HPV感染所致低級別宮頸病變會隨病毒的消退而消失,且自然消退率為60%,故一直以來對高危型HPV感染致低級別宮頸病變患者遵循觀察隨訪的治療原則[2]。但年齡、病毒類型及感染數量是否對HPV病毒的消退及病變有影響還未確定。因此筆者對上述因素與高危型HPV病毒及低級別宮頸病變轉陰率的相關性進行研究,現報道如下。
1 資料與方法
1.1一般資料 選取2012年1月至2015年6月經由本院門診檢查初次發現高危型HPV感染,并由陰道鏡下定點活檢確診為低級別宮頸上皮內瘤變的172例患者進行回顧性研究。其中92例為觀察組,80例為手術組。觀察組年齡21~62歲,平均(42.9±10.8)歲。手術組年齡22~61歲,平均(42.5±10.5)歲,兩組患者年齡比較差異無統計學意義(P>0.05),具有可比性。入組標準:(1)兩組患者均為經門診檢查檢驗初次確診為宮頸低級別病變者。(2)手術組患者為心理承受力差,對疾病有恐懼感,要求積極治療者,或自愿接受手術治療研究者,兩組患者均簽署知情同意書。(3)患者依從性好,能配合隨訪。(4)排除妊娠,近期有生育要求,嚴重全身性疾病及惡性疾病者。
1.2方法 觀察組未行手術及任何藥物治療并于第6、12、18個月進行隨訪。手術組行宮頸電熱圈環切術(LEEP)且術后未行藥物治療,于術后3、6、12、18個月隨訪。隨訪內容為HPV病毒檢測及液基細胞學(TCT)液基薄層細胞檢測,以二者均轉陰為標準。病變疑有進展者再次行陰道鏡下宮頸活檢。 為避免重復感染囑患者隨訪期間拒絕頻繁及不潔性生活,工具避孕,適當體育鍛煉,增強自身免疫力。
1.2.1HPV病毒檢測及TCT檢測方法 3 d內禁止陰道沖洗或使用陰道內藥物,24 h內禁止性生活,非月經期做檢查。分泌物過多時先拭干凈再取,有出血時先止血后再取。為防止鱗狀上皮受損影響標本質量,先取TCT標本。用宮頸采樣試子置于宮頸口與黏膜交界處逆時針轉3圈,停留10 s。將試子放于專用試管中保存送檢。再取HPV病毒標本,將宮頸刷毛刷頭完全伸入宮頸內,旋轉5~6圈,停留10 s取出,置于專用試管中送檢。
1.2.2陰道鏡下宮頸活檢 檢查前3 d內禁止性生活、婦科檢查及陰道上藥等可致宮頸上皮損傷的一切操作。宜于月經后3 d至月經前10 d進行。患者取膀胱截石位,陰道窺器暴露宮頸陰道部,生理鹽水棉球擦拭宮頸。3%醋酸溶液浸濕宮頸表面及陰道穹隆20 s,觀察醋白上皮及異型血管等異常變化。3%復方碘溶液浸濕宮頸,30 s后觀察上皮變化。于不著色部位或可疑病變部位取多點活檢送病理(活檢部位按先低后高順序夾取)。
1.2.3LEEP 陰道鏡下確定病變部位,于碘不著色區外0.2 cm處錐形切除。按Ⅰ型轉化區錐高0.7~1.0 cm,Ⅱ型轉化區錐高1.0~1.5 cm ,Ⅲ型轉化區錐高1.5~2.0 cm。切除后電凝止血。陰道放置尾紗壓迫止血,24 h后取出。
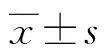
2 結 果
2.1兩組患者轉陰率比較 手術組80例,其中術后病理宮頸上皮內瘤變(CIN)1切緣殘留1例,再次手術后切緣無殘留。病理級別升高為CIN2的4例,切緣無殘留。3個月復查時轉陰60例,6個月后復查有6例HPV病毒再次感染,轉陰54例,18個月復查有3例HPV病毒再次感染,最終轉陰51例(HPV及TCT檢測至少連續2次均轉陰)。觀察組92例,6個月復查時轉陰22例,12個月42例,18個月最終轉陰53例(有13例持續性感染患者,發現病變升級,進一步手術)。兩組轉陰率比較差異無統計學意義(P>0.05),見表1。

表1 兩組患者轉陰率(%)
2.2HPV感染數量對兩組患者轉陰率的影響比較 HPV病毒單一感染患者,手術組59例,最終轉陰36例;觀察組68例,轉陰39例,差異無統計學意義(P>0.05)。多重感染患者,手術組21例,轉陰15例,觀察組24例,轉陰14例,差異無統計學意義(P>0.05),見表2。
表2 單一或多重感染對兩組患者轉陰率的影響
2.3HPV基因型及患者年齡與兩組患者轉陰率的相關性 兩組患者HPV病毒多重感染者,因樣本數量少,完全相同的HPV型別感染者極少,無比較意義。HPV病毒單純感染者中選取所占比例較大的6種病毒作比較,差異均無統計學意義(P>0.05)。按年齡分組,≤44歲年齡段,手術組41例,最終轉陰24例;觀察組48例,轉陰32例,差異無統計學意義(P>0.05)。>44歲患者,手術組39例,轉陰28例,觀察組44例,轉陰23例,差異有統計學意義(P<0.05),見表3。
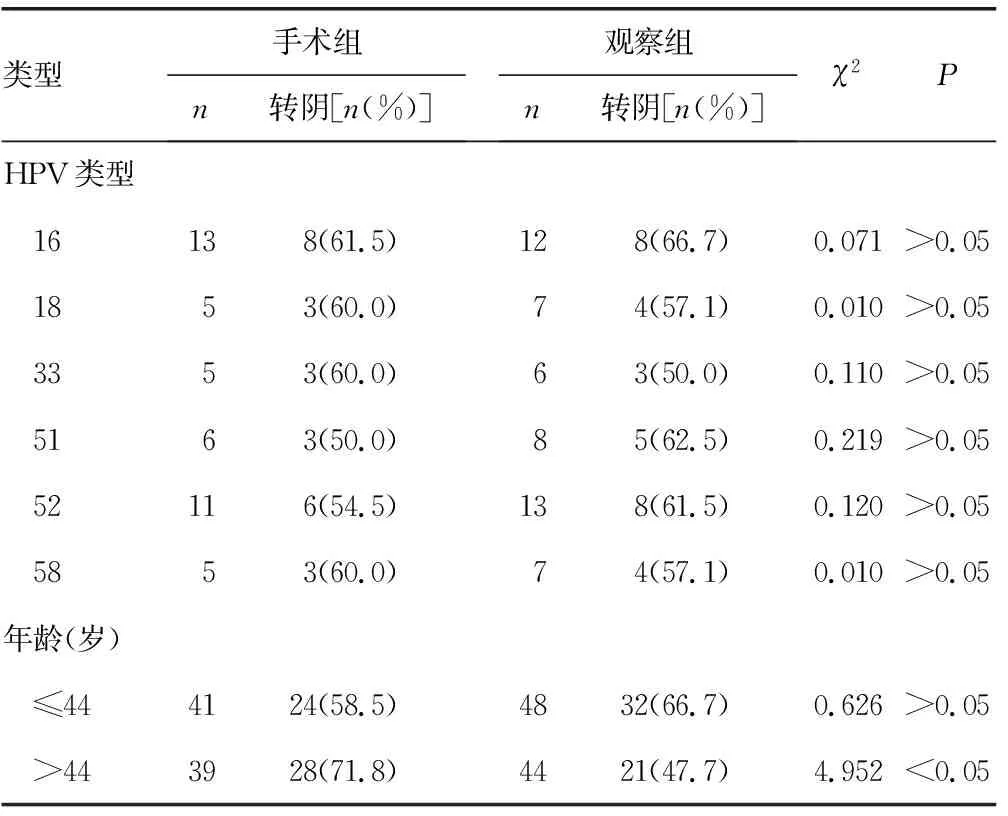
表3 高危型HPV病毒基因分型及患者年齡對兩組患者轉陰率的影響
3 討 論
據2017年美國國立綜合癌癥網絡(NCCN)報道,美國宮頸癌的發生率逐年下降,但在西班牙裔/拉丁美洲人、黑人及亞洲婦女中的發生率仍居高不下。報道稱,85%的宮頸癌患者出現在發展中國家,成為女性癌癥致死的主要原因之一[3]。自2006年以來已有3種HPV疫苗被美國食品與藥品管理局(FDA)認證上市。在歐美等發達國家,因其宮頸癌篩查的普及性及疫苗的廣泛應用,宮頸癌發生率持續下降。而我國CFDA獲批的疫苗剛剛上市,還未普及,且因經濟、保守思想及傳統宮頸防癌刮片篩查的準確度低等原因,我國宮頸病變的發生率仍較高。
目前諸多研究表明持續性高危型HPV病毒感染在宮頸病變及宮頸癌發生、發展中扮演重要角色[4-5]。因此怎樣早期治療HPV病毒及低級別宮頸病變,降低宮頸癌發生率成為醫學研究者共同的目標。許多學者致力于藥物治療HPV病毒感染的研究,均略有成效但仍未達成一致,未被國際認可[6-8]。有研究認為對于高危型HPV病毒感染所致低級別宮頸病變,因其病變進展率低自然轉陰率高,可予以保守治療[9]。本研究發現手術組及觀察組的轉陰率從整體看無明顯差異,且與病毒感染類型及數量無關。但隨年齡增長,HPV的感染率增加,自然轉陰率明顯下降,這與許多研究一致[10],有可能是因為HPV高危型感染與自身免疫力有關[11]。老年婦女因自身免疫力下降,易形成持續性感染,進而發生病變。且老年婦女多為Ⅲ型轉化區,陰道鏡檢查不滿意,單純依據陰道鏡活檢診斷的CIN1不準確[12],易低估病變級別,這也是老年女性自然轉陰率下降的原因之一。而LEEP手術后可切除感染病灶,提高HPV轉陰率,消除病變。且老年女性性生活頻率下降甚至缺失,重復感染機會減少。因此,筆者認為,老年女性低級別宮頸病變的治療應因人而異,建議老年因HPV感染致低級別宮頸病變患者應積極治療,可放寬手術治療指征,增加復查次數,重視隨訪。
綜上所述,我國因努力提高女性的防癌意識,加強宮頸癌篩查治療基本操作的準確性。

