腎血管阻力指數聯合平均動脈壓對重癥腦病患者的預后評估
王婳,劉鵬,許兆軍,王芳,沙宇毅
重癥腦病患者數量逐年升高,外傷導致的重型顱腦損傷,高血壓所致的急性大面積腦梗死及院內院外心肺復蘇后的缺血缺氧性腦病患者,入住重癥監護病房(ICU)的比例越來越高[1]。如何在保證腦灌注壓的同時,避免腎血流的過度灌注,延緩腎功能的進行性惡化,引起了ICU醫師的重視。由于無法直接觀察患者腎血流,床旁腎臟超聲造影的應用受到限制;而具有安全無創、可重復、可動態觀察的床旁重癥多普勒超聲,成為重癥醫師不可替代的“聽診器”。腎血管阻力指數(RRI)最初用于慢性腎病、腎動脈狹窄及腎移植術后血管功能等的評估[2],現逐漸成為預測急性腎損傷(AKI)的指標,其判斷AKI的時機甚至早于“金標準”血肌酐[3]。但由于受年齡、性別、血壓、心率、腹內壓及氧合情況[3]等因素的干擾,RRI的臨床價值一直未能體現。本研究探討RRI聯合平均動脈壓(MAP)對重癥腦病患者預后的評估價值,報道如下。
1 資料與方法
1.1 一般資料 選取 2016年 3月至2017年1月寧波市第二醫院ICU收治的重癥患者56例,根據患者收住時間的長短,進行為期1~7 d的RRI監測。
1.2 診斷標準 血肌酐絕對值升高≥0.3 mg/dl(≥26.4 mmol/L)或者血肌酐較基礎值升高≥50%,則診斷為AKI[4]。
1.3 方法 使用床旁監護儀(Philips,荷蘭)監測患者動脈血壓、MAP、心率及呼吸次數等參數。監測患者入ICU第1周內每天的雙側RRI,記錄當時的生命體征、血乳酸、血管活性藥物及劑量,當天的血肌酐、尿素氮、尿酸(若有多次化驗,則取較高值)及尿量情況。
所有超聲數據均利用彩色多普勒床旁超聲診斷儀(Philips,CX50),腹部超聲探頭型號C5-1,頻率2~5 MHz,測量由同一名熟練掌握超聲技術的醫師操作。患者取側臥位,使用凸陣探頭,從后外側掃查腎臟冠狀切面來獲取腎內血管血流圖,在多普勒模式下測定腎葉間動脈的血流速,取樣容積為2~5 mm。RRI=(收縮期峰流速—舒張期峰流速)/收縮期峰流速[5]。
1.4 統計方法 采用SPSS 17.0統計軟件進行分析,計量資料以均數±標準差表示,兩組比較采用t檢驗;多組間比較采用方差分析,多重比較采用LSD-t檢驗。P<0.05為差異有統計學意義。
2 結果
2.1 重癥腦病患者的臨床特征 以男性患者為主,由于患者多為急性腦卒中和心肺復蘇后患者,機械通氣的比例達到76.79%,由于患者病情危重,自動出院比例高,28 d病死率達到33.93%。急性出血性卒中、缺血性腦卒中和缺血缺氧性腦病患者發生 AKI的比例分別為10.71%、30.77%和66.67%。見表1。
2.2 兩組AKI分組比較 根據是否發生AKI將患者分為AKI組和非AKI組,兩組心率、血乳酸、血肌酐、尿素氮、尿量及生存時間差異均有顯著統計學意義(均P<0.01),去甲腎上腺素劑量、雙側及左側RRI值差異均有統計學意義(均P<0.05),見表2。AKI患者的RRI值的曲線較非 AKI組患者更低。見封二彩圖6。
2.3 不同MAP分組患者比較 根據MAP將患者為<90mmHg(1mmHg≈0.133kPa)組、90~110 mmHg組和>110 mmHg組,3組收縮壓、舒張壓、MAP差異均有顯著統計學意義(均P<0.01),雙側RRI差異有統計學意義(P<0.05),且在90~110mmHg組RRI值最低。見表3。
3 討論
RRI是通過多普勒超聲描記腎血管的血流波形,間接獲得腎血流的動力學特性,它能反應腎血管床的阻力狀態。MAP由收縮壓和脈壓差計算所得,腦灌注壓則取決于MAP與顱內壓(ICP)的差,故在ICP不變的情況下,提高MAP可以改善腦灌注。重癥腦病患者都會直接或間接引起ICP增高,故維持較高的MAP可以改善腦灌注[6]。
本組重癥腦病患者以男性為主,APACHEⅡ評分高,機械通氣和血管活性藥物使用比例高,提示病情危重,發生AKI的比例達到30.36%。近年來隨著AKI意識的普及,對于膠體液如明膠、羥乙基淀粉等的使用大幅減少,以等滲晶體液輸注為主,但文獻報道晶體液亦可引起AKI[7]。研究發現,AKI可導致腎臟的修復不全、慢性炎癥的持續和纖維化的發生,從而進展為慢性腎病[8]。早期識別AKI,早期干預,可以阻止腎功能的惡化。

表1 56例重癥腦病患者的臨床特征
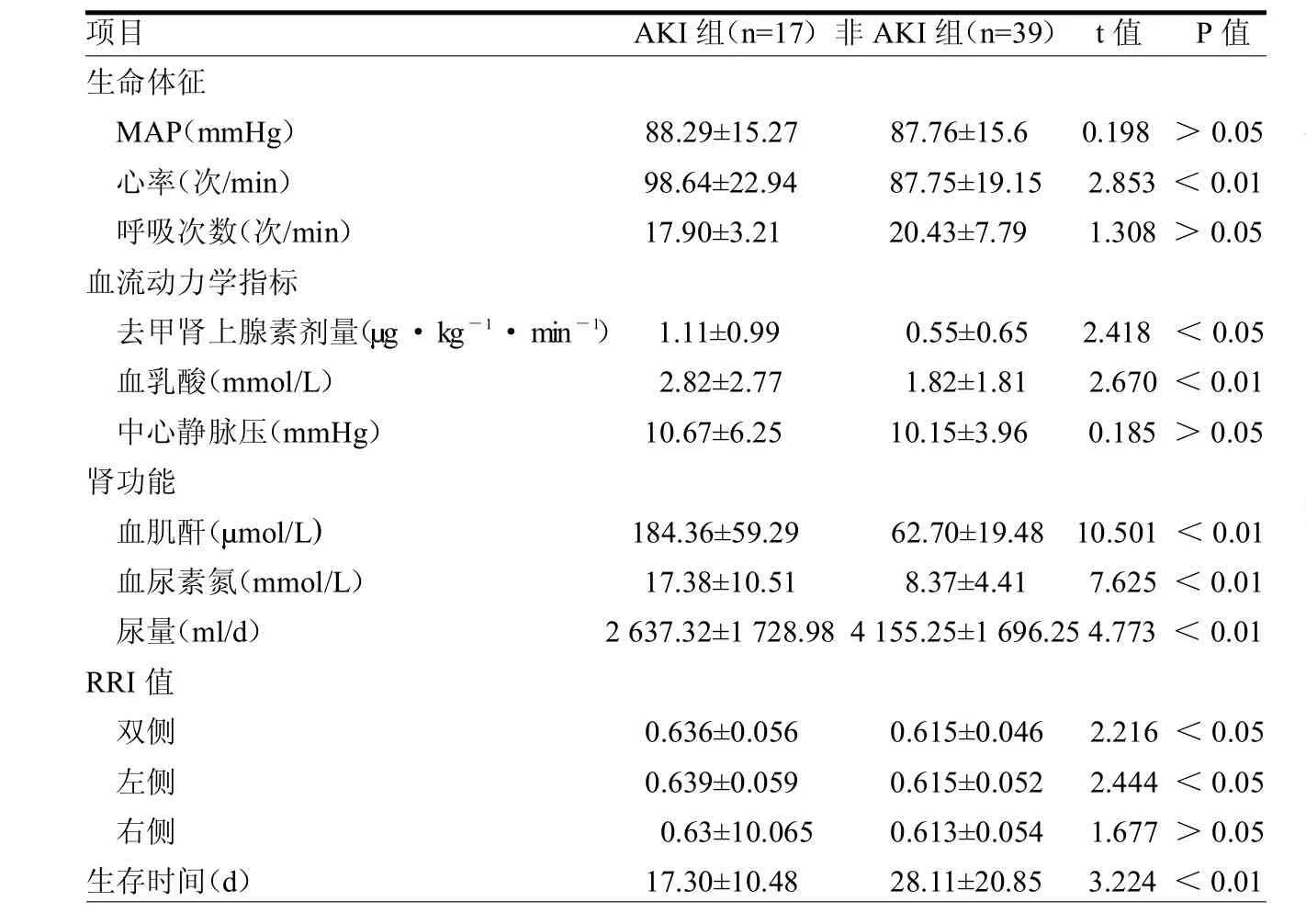
表2 兩組生命體征、血流動力學指標、腎功能指標、RRI值及生存時間比較

表3 不同MAP組臨床資料比較
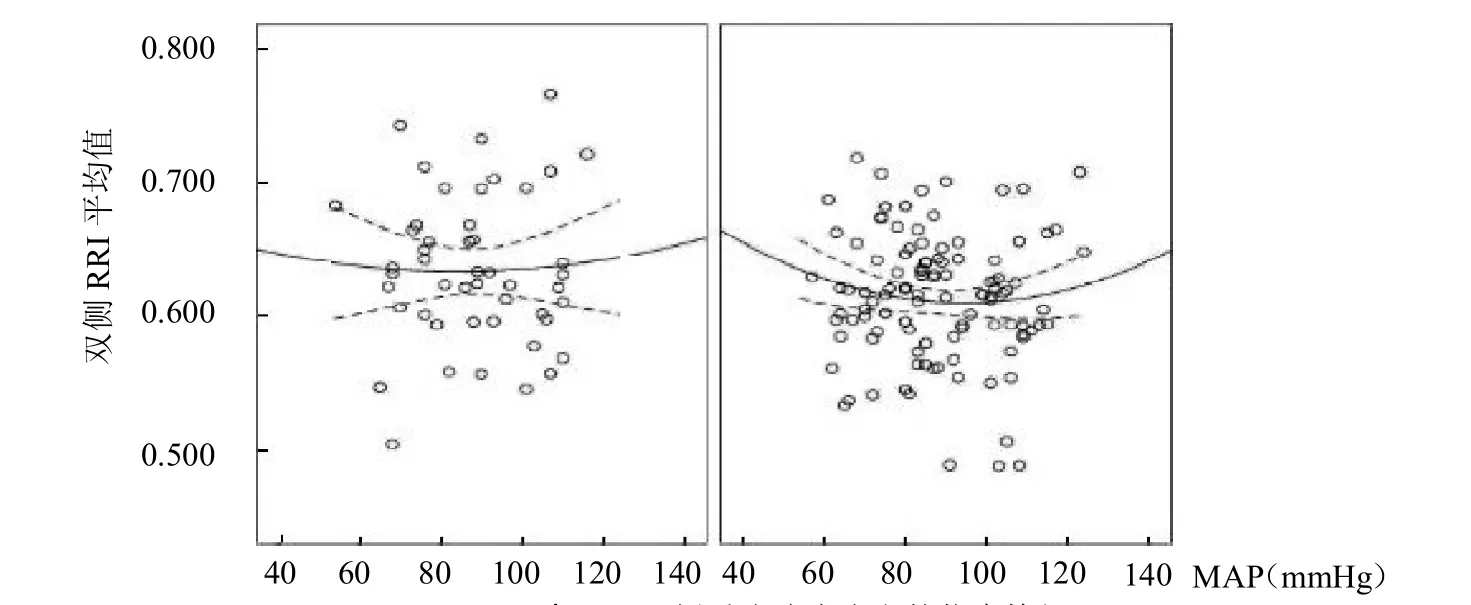
表6 56例重癥腦病患者的臨床特征
本研究顯示,AKI組患者不僅血肌酐、尿素氮更高,尿量更少,而且乳酸高、去甲腎上腺素針劑量更大,生存時間明顯縮短,但兩組患者的中心靜脈壓卻沒有區別。根據不同的MAP進行分組,90~110 mmHg組雙側RRI值最低,MAP低于90 mmHg或高于110 mmHg的患者RRI值均有升高,3組差異有統計學意義(<0.05)。此MAP的目標較臨床休克復蘇時的65 mmHg要高,因為大多數的休克患者不存在嚴重的腦損傷,比單純只有腦損傷的患者要低。劉然等[9]收集342例急性缺血性腦卒中患者,要求MAP> 97mmHg,不存在AKI。MAP過低,全身組織灌注不足,引起無氧代謝增加,有效循環血量不足,引起腎前性的AKI。而MAP過高,對于急性缺血性卒中患者,可能引起患者腦部的出血轉化,ICP急劇升高,加重腦水腫,反而使腦損傷加重[10]。故控制 MAP維持在90~110 mmHg,既能維持腦血流,又不至于造成腎血流的過度灌注,減輕腎損傷。由于本研究的時間短,病例數不多,對于RRI和MAP的關系及其他影響因素未做進一步的對比,得出的結論價值有限,尚需進一步的大型臨床試驗來證明。
參考文獻:
[1]Hoste EA,Bagshaw SM,Bellomo R,et al.Epidemiology of acute renal injury in critically ill patients:the multinational AKI-EPI study[J].Intensive Care Med,2015,41(8):1411-1423.
[2]Granata A,Zanoli L,Clementi S,et al.Resistive intrarenal index:myth or reality[J]?Br J Radiol,2014,87(1038):20140004.
[3]Boddi M,Natucci F,Ciani E.The internist and the renal resistive index:truths and doubts[J].Intern Emerg Med,2015,10(8):893-905.
[4]Schetz M,Schneider A.Focus on acute kidney injury[J].Intensive Care Med,2017,43(9):1421-1423.
[5]周永昌,郭萬學.超聲醫學[M].5版.北京:科學技術文獻出版社,2006:784.
[6]Singh S,Grewal A,Gautam PL,et al.Evaluation of cardiopulmonary resuscitation(CPR)for patient outcomes and their predictors[J].J Clin Diagn Res,2016,10(1):UC01-UC04.
[7]許書添,李世軍.液體復蘇與急性腎損傷[J].腎臟病與透析腎移植,2014,23(5):453-457.
[8]楊莉.急性腎損傷發病與修復的機制[J].中華腎病研究,2013,2(3):120-124.
[9]劉然,王娜,張旭東,等.缺血性卒中急性期平均動脈壓對預后影響研究[J].中國現代神經疾病,2015,15(5):411-414.
[10]Grise EM,Adeoye O,Lindsell C,et al.Emergency department adherence to American Heart Association guidelines for blood pressure management in acute ischemic stroke[J].Stroke,2012,43(5):557-559.

