一種改良的大鼠胃十二指腸動脈逆行給藥方法
管 陽, 劉鳳永, 樊慶勝, 付金鑫, 陳現現, 李 鑫, 袁宏軍, 王茂強
肝癌一直是腫瘤治療中的難點和重點,隨著近年介入放射學技術發展,介入方法在肝臟腫瘤治療中越來越重要。臨床治療有效、安全和經濟要求提高,使得各種新型藥物材料如納米顆粒、載藥微球等不斷開發,而新材料、新藥物應用的臨床前動物實驗是評價安全性、有效性的重要環節。大鼠肝癌模型在臨床前介入治療實驗研究中經常使用,傳統大鼠肝動脈給藥方式為經胃十二指腸動脈逆行插管[1],需游離胃十二指腸動脈及肝總動脈并夾閉肝總動脈。導絲導引經胃十二指腸動脈直接插管至肝固有動脈給藥方法,可避免游離肝總動脈及夾閉肝總動脈,減少肝臟缺血時間,提高給藥效率及成功率。本研究介紹一種改良的大鼠胃十二指腸動脈逆行給藥方法,旨在提供更簡單、安全、高效的肝動脈插管技術。
1 材料與方法
1.1 實驗動物分組與器材
本研究經解放軍總醫院實驗動物福利倫理委員會審查通過。取Sprague-Dawley(SD)雄性大鼠20只(北京維通利華實驗動物公司),體重(301.7±12.4)g,隨機分為A組和B組,各組10只,分籠飼養于無特定病原體(SPF)級環境。實驗器材包括大鼠外科操作臺(解放軍總醫院實驗動物中心)、小動物用剃毛器、2 mL注射器、24 G靜脈留置針(臺灣柏朗公司)、4-0慕斯手術縫線、自制長約20 cm帶導絲扭控器的0.014英寸導絲(圖1)、外科手術刀、動脈夾、玻璃分針、蚊式止血彎鉗、縫合針(角針)、持針鉗、醫用棉簽、1%戊巴比妥、醫用聚維酮碘、0.9%氯化鈉溶液、鹽酸利多卡因、超液化碘油(法國Guerbet制藥公司)、青霉素等。

圖1 24 G靜脈留置針
1.2 經胃十二指腸動脈逆行給藥方法
A組(n=10)實驗大鼠:經腹腔注射1%戊巴比妥(3 mL/kg),完全麻醉后將腹部毛發剔除,仰臥位固定于操作臺,醫用聚維酮碘消毒手術區域,沿腹正中線胸骨柄下作長約5 cm切口,找到胃十二指腸動脈并確定肝固有動脈位置;游離胃十二指腸動脈約2 cm,穿入2根4-0慕斯縫線并分別置于遠端和近端,遠端結扎外科結,近端備用;將蘸有利多卡因醫用棉簽輕柔涂抹游離的胃十二指腸動脈,24 G靜脈留置針自遠端穿刺胃十二指腸動脈,見留置針鞘內回血后向前稍送一小段距離,緩慢抽出部分針芯,同時將近端縫線系一活結固定留置針鞘;完全抽出針芯,將長約20 cm自制帶導絲扭控器的0.014英寸導絲導入留置針鞘內,直視下見導絲導入肝固有動脈,小心解開近端縫線活結,將靜脈留置針鞘沿導絲推入肝固有動脈,再次將近端縫線系一活結固定留置針鞘,取出導絲(圖2①②)。B組(n=10)實驗大鼠:在A組操作基礎上不使用導絲,不將留置針鞘推入肝固有動脈,直接用靜脈留置針穿刺胃十二指腸動脈,同時游離肝總動脈并用動脈夾夾閉(圖2③)。兩組均經留置針鞘注入超液化碘油(0.9%氯化鈉液1∶4稀釋)0.1 mL,為避免藥物反流,推注過程緩慢輕柔,結束后繼續推注0.2 mL 0.9%氯化鈉溶液,給藥完成后靜置片刻,退出留置針鞘,同時將近端縫線結扎外科結;確認無出血跡象后逐層關腹。術后每日肌內注射青霉素鈉80萬U,連續3 d。
以上所有操作均由同一具有相關操作經驗的術者進行。分別記錄整個手術時間(min)、術中術后意外情況(有或無),觀察術后大鼠狀態(活動狀態、飲食飲水正常或異常)。兩組大鼠分別于術前、術后即時、術后1周接受CT平掃檢查。
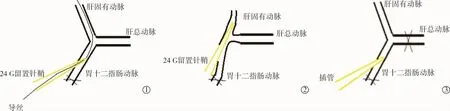
圖2 兩組經胃十二指腸動脈逆行給藥示意圖
1.3 統計學方法
采用SPSS 17.0軟件進行數據處理,以均數±標準差(±s)表示,計量資料比較用獨立樣本t檢驗,雙側檢驗水準α=0.05。
2 結果
A組大鼠經改良胃十二指腸動脈逆行給藥過程均成功(10/10),手術時間為平均(24.7±9.7) min。 B組給藥成功 8例(8/10),手術時間為平均(33.2±5.5)min,給藥失敗2例中1例因穿刺入動脈假腔注射碘油致假腔破裂、碘油進入腹腔,1例因留置針鞘進入胃十二指腸后推送阻力大、進入距離較短,注射碘油時留置針鞘彈出動脈,再次結扎后嘗試再次穿刺失敗。A組與B組手術時間差異有統計學意義(P=0.042)。A組、B組給藥成功大鼠術后活動狀態均正常,飲食飲水均減少,未見明顯差異。A組、B組給藥成功大鼠CT平掃未見明顯差異性,術后即時均可見碘油沉積于肝臟內,胃腸區域未見沉積,術后1周均可見部分碘油清除(圖3)。
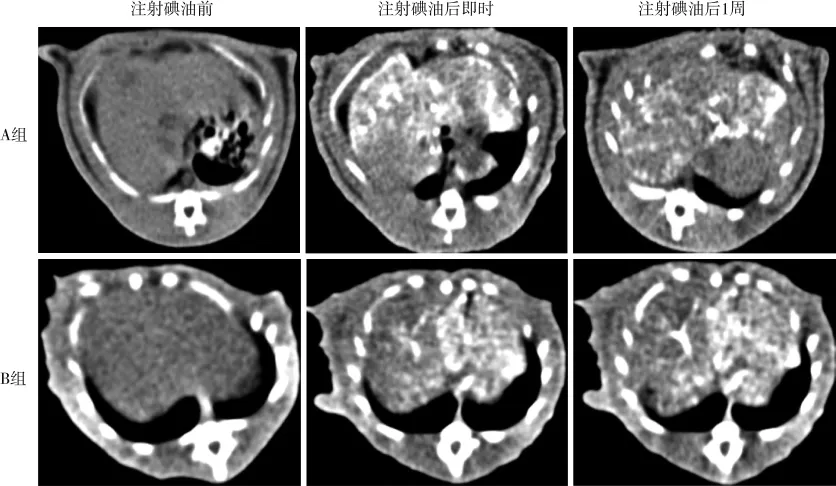
圖3 兩組給藥成功大鼠注射碘油前后CT平掃影像
3 討論
介入治療是中晚期肝癌重要治療方法[2],隨著近年新型載藥材料如納米顆粒、載藥微球等發展[3-4],臨床應用前新型藥物安全性、有效性動物實驗研究有重要價值。大鼠肝癌模型可重復性強、穩定性好,是介入治療研究較常用模型之一[5-8]。大鼠腹腔動脈及胃十二指腸動脈走行較固定,變異較少[9],因此經胃十二指腸動脈逆行肝動脈給藥途徑是介入實驗中較常用給藥方法。但大鼠體型較小,操作有一定難度,需要術者有豐富的手術經驗。
改良胃十二指腸動脈逆行給藥方法的思路,源于臨床介入手術中改良Seldinger穿刺技術[10]。空腔導管無論由何種材料制作,面臨的問題是若所用材料太軟,軸傳導力不好,不能將推送力度傳遞至管腔頭端,致使導管某段無法進入目標位置并出現彎曲;若材料太硬,軸傳導力較好,則勢必增加導管頭端損傷,甚至穿破血管壁的風險。該問題只有在導絲導引下才得到較完美解決,既可增加軸傳導力,又避免損傷或穿破血管壁。將導管推送至目標位置,這是Seldinger技術精髓所在。本研究B組雖有8例插管給藥成功,但術中推送靜脈留置針鞘過程難易不一,在大鼠胃十二指腸動脈未痙攣、走行較直情況下,靜脈留置針鞘沿血管走行方向較易推送入血管腔目標位置,但在大鼠胃十二指腸動脈痙攣或走行迂曲、靜脈留置針鞘方向與血管走行方向偏差較大情況下,推送較困難,阻力較大。本研究顯示導絲不僅導引靜脈留置針鞘順利進入肝固有動脈,還可在穿刺伊始通過導入導絲判斷穿刺針頭是否進入胃十二指腸動脈真腔,若進入動脈外層筋膜層或夾層,導絲導入困難或很易穿出筋膜層外,此時采用導絲導引較無導絲導引可縮短操作時間、降低意外風險、提高成功率。由于導絲能將鞘管導入至肝固有動脈,可在不夾閉肝總動脈、有一定動脈血液流通情況下將藥物注入肝內,較之夾閉肝總動脈給藥方法避免了游離肝總動脈過程,減少了肝臟動脈缺血時間。本研究中兩組給藥成功大鼠術后飲食飲水均減少,可能與注射碘油后肝功能指標升高、食欲下降有關;術后CT平掃碘油沉積于肝臟程度與夾閉肝總動脈方法無明顯區別,說明改良肝內給藥方法可行、安全,能夠縮短操作時間。傳統胃十二指腸動脈逆行肝動脈插管大多需借助顯微外科設備,以顯微剪剪開胃十二指腸動脈一部分,揭起開口后插入細管至(或不至)肝固有動脈,并夾閉肝總動脈[11]。本研究B組插管方法雖不完全相同于傳統胃十二指腸動脈逆行肝動脈插管,但有一致性,且能建立較平衡的實驗因素對照。總體上,改良的大鼠胃十二指腸動脈逆行給藥方法與傳統插管給藥方法相比,有如下優點:①插管過程更容易,幾乎無損傷、穿破血管壁或造成動脈夾層可能;②直接在肝固有動脈給藥,給藥位置更深入和準確,減少了肝臟動脈缺血時間;③可不使用顯微外科設備,降低了操作難度,節省了研究成本。
實驗中應注意的幾個細節:①辨認和游離大鼠胃十二指腸動脈時,動作一定要輕柔、有耐心。大鼠胃十二指腸動脈周圍附有網膜系膜及一些細小血管分支,動作粗魯易造成細小血管分支斷裂出血,繼而引起胃十二指腸動脈痙攣收縮而增加插管難度,涂抹利多卡因對緩解痙攣、擴張胃十二指腸動脈有一定效果。②大鼠胃十二指腸動脈與相應腸系膜靜脈伴行,游離動脈導入慕斯縫線時務必仔細,切勿將腸系膜靜脈一并結扎,導致腸系膜靜脈回流受阻,引起實驗動物出現致命并發癥,甚至死亡,進而影響實驗結果,導致實驗失敗。③大鼠肝乳頭葉遮蓋肝固有動脈及肝總動脈,需分離其系膜和韌帶,將肝乳頭葉移向一側,此過程動作要更輕柔,因為大鼠肝臟較易破損,牽拉系膜和韌帶過猛可導致肝乳頭葉撕裂,進而出血引起實驗意外。由于大鼠樣本數量所限,本研究可能有一定局限性。今后應加大實驗樣本量,進一步完善研究。
[參 考 文 獻]
[1]許衛國,楊建勇,李鶴平,等.建立大鼠肝動脈插管途徑的方法學研究[J].介入放射學雜志, 2007,16:264-265.
[2]Benson AB 3rd, D'Angelica MI, Abbott DE, et al.NCCN Guidelines Insights: hepatobiliary cancers, version 1.2017[J].J Natl Compr Canc Netw,2017,15:563-573.
[3]You Y,Wang Z,Ran H,et al.Nanoparticle-enhanced synergistic HIFU ablation and transarterial chemoembolization for efficient cancer therapy[J].Nanoscale, 2016, 8: 4324-4339.
[4]McDevitt JL,Mouli SK,Tyler PD,et al.MR imaging enables measurement of therapeutic nanoparticle uptake in rat N1-S1 liver tumors after nanoablation[J].J Vasc Interv Radiol, 2014,25:1288-1294.
[5]Li X,Zheng CS,Feng GS,et al.An implantable rat liver tumor model for experimental transarterial chemoembolization therapy and its imaging features[J].World J Gastroenterol, 2002, 8:1035-1039.
[6]Jin Y,Tong DY,Shen JJ,et al.Establishment of experimental implantation tumor models of hepatocellular carcinoma in Wistar rats[J].Tumor Biol, 2014, 35: 9079-9083.
[7]Choi JW,Kim HC,Baek SY,et al.A metastatic hepatoma model of rats using the 13762-MAT-B-Ⅲ cell line: basic characteristics and potential as a tool for interventional oncology experiments[J].Anticancer Res, 2015, 35: 1333-1338.
[8]Cho HR,Choi JW,Kim HC,et al.Sprague-Dawley rats bearing McA-RH7777 cells for study of hepatoma and transarterial chemoembolization[J].Anticancer Res, 2013, 33: 223-230.
[9]向賢宏,李鶴平,陳偉,等.Wistar大鼠腹腔干及其分支動脈的實驗解剖學特征[J].世界華人消化雜志,2008,16:2988-2991.
[10] Verel D.A modified Seldinger needle[J].Clin Radiol, 1973,24:65-66.
[11]王于,李鶴平,連帆,等.胃十二指腸動脈逆行肝動脈插管技術在動物實驗中的應用[J].世界華人消化雜志,2008,16:4088-4092.

