卡左雙多巴控釋片治療帕金森病伴發抑郁癥臨床觀察
楊懷芹 陸 剛 劉阿楠 李華麗
平頂山市第一人民醫院神經內二科,河南 平頂山 467000
帕金森病(Parkinson’s disease,PD)是一種以運動癥狀為核心的運動障礙性疾病,可導致嚴重的神經系統病變,多發于中老年人[1]。非運動癥狀(non-motor symptoms,NMS)對患者生活質量及預后產生重大影響,尤其是神經精神癥狀[2]。抑郁為帕金森病最常見的癥狀,嚴重影響患者的生活質量,如何有效改善其抑郁癥狀被視為帕金森治療目標之一[3-4]。
帕金森伴發抑郁(depression of Parkinson’s disease,dPD)的發生涉及多種神經遞質,臨床治療藥物主要包括多巴胺受體激動劑、5-HT再攝取抑制劑(SSRIs)、三環類抗抑郁藥[5],但尚無統一的用藥標準。左旋多巴(levodopa,L-DOPA)為酪氨酸形成兒茶酚胺的中間產物即多巴胺的前體,可進入中樞神經增加紋狀體中多巴胺遞質濃度,對改善PD患者癥狀療效確切,優越性顯著,是治療帕金森病的金標準[6]。本研究筆者采用卡左雙多巴控釋片治療dPD取得一定療效,為臨床用藥提供新的思路和借鑒。
1 資料和方法
1.1一般資料本次研究經院醫學倫理委員會討論批準,患者及家屬簽署知情同意書。采用前瞻性、隨機、平行對照試驗設計法。入選標準:(1)年齡40~80歲,不限性別;(2)符合中華醫學會神經病學分會帕金森病及運動障礙學組制定修訂《帕金森病抑郁、焦慮及精神病性障礙的診斷標準及治療指南》中帕金森病伴抑郁的診斷標準[7];(3)病程>6個月,且出現抑郁>2周;(4)漢密爾頓抑郁量表(HAMD)評分≥18分;(5)經CT或(和)MRI檢查證實除老年性腦改變外無其他異常;(6)均未接受過抗抑郁治療;(7)依從性良好,遵醫囑用藥并定期隨訪;(8)臨床資料齊全,并自愿參與本次研究。排除標準:(1)不符合入選標準;(2)腦血管病、腦炎、中毒等所致的繼發性帕金森綜合征;(3)既往存在抑郁癥者;(4)合并嚴重肝腎功能不全、惡性腫瘤等器質性疾病者;(5)合并除抑郁外其他精神疾病者;(6)合并構音障礙不能準確表達情感者;(7)老年癡呆患者;(8)MMSE評估確定存在認知障礙者;(9)過敏體質,對本次研究用藥存在嚴重過敏反應者;(10)合并影響療效評價準確性因素者。最終入選90例帕金森病伴抑郁癥患者,利用隨機數字表分為2組。2組性別構成比、年齡、病程、抑郁程度等差異均無統計學意義(P>0.05),具有可比性。見表1。
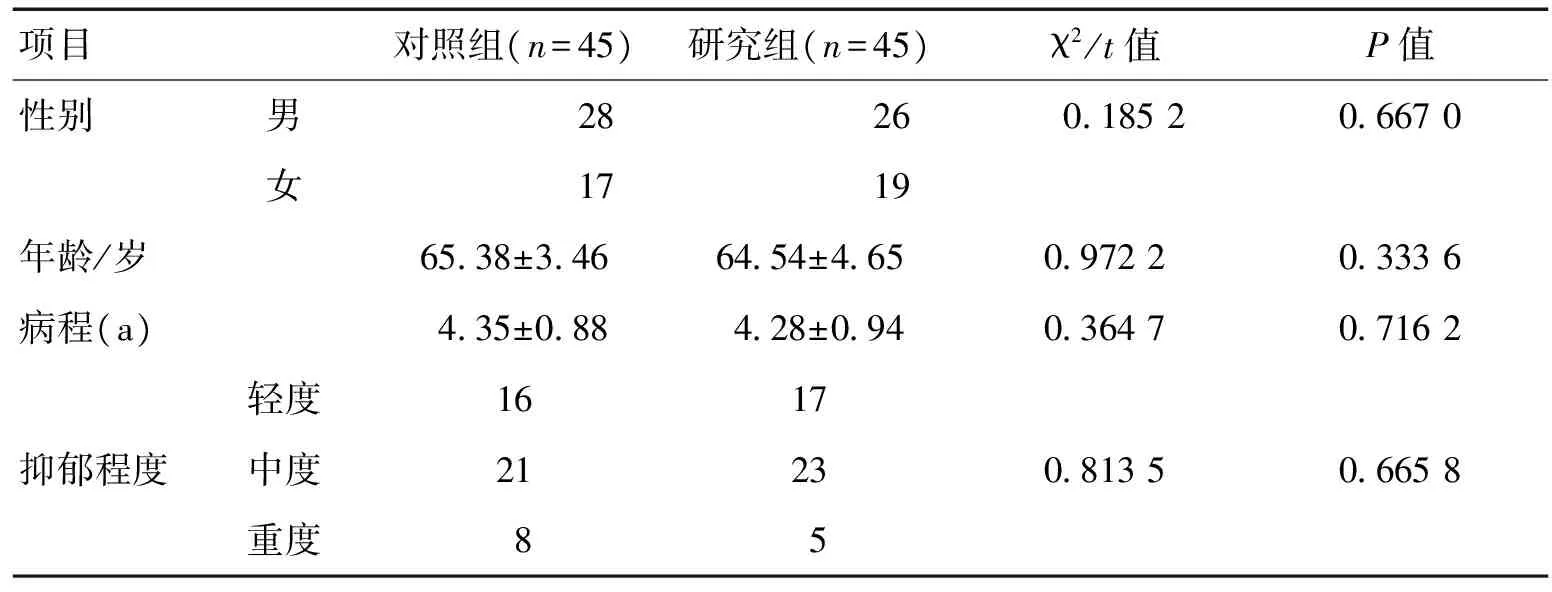
表1 2組一般資料對比
1.2治療方法2組均予以健康教育、康復與運動療法、認知行為療法,對照組予以安慰劑治療,治療組予以卡左雙多巴控釋片[商品名:息寧;生產廠家:MerckSharp & Dohme(Italia)S.P.A;批準文號:進口藥品注冊證號H20100047;規格:卡比多巴50 mg:左旋多巴200 mg],起始劑量0.5片/d,口服,逐漸增加劑量,直至病情有效控制后予以維持最小有效劑量服藥。2組均不合用抗抑郁藥、抗精神病藥物,若出現不良反應則予以對癥處理。
1.3觀察指標和評價標準采用漢密爾頓抑郁量表(HAMD)評估2組治療4周末、8周末抑郁狀態,并計算抑郁狀態療效指數[(治療前HAMD評分-治療后HAMD評分)/治療前HAMD評分×100%]評估抑郁療效[8],抑郁狀態療效指數≥75%判定為治愈,50%~74%判定為顯效,25%~49%判定為有效,<25%判定為無效,總有效=治愈+顯效;同時,觀察2組不良反應發生情況。此外,對2組均進行為期3~12個月隨訪,于治療前、治療后、隨訪末采用帕金森癥生活品質問卷(PDQ-39)從運動、日常生活活動、情感狀態、病恥感、社會支持、認知、交流、身體不適8個維度39個條目評估患者的生活質量,將PDQ-39總評分轉化為0~100分綜合指數,得分越高提示生活質量越低。
2 結果
2.1 2組HAMD評分比較治療后2組HAMD評分較治療前呈下降趨勢(P<0.05),且治療組4周末、8周末HAMD評分均明顯低于對照組(P<0.05)。見表2。
2.2 2組PDQ-39評分比較定期門診隨訪,隨訪截止日期2016-05-01,平均隨訪6.58個月。2組PDQ-39評分均呈下降趨勢,對照組經秩和檢驗P>0.05,治療組經秩和檢驗P<0.05,治療后和隨訪末治療組PDQ-39評分均明顯低于對照組(P<0.05)。見表2。
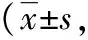
表2 2組不同時點HAMD與PDQ-39評分比較分)
2.3 2組療效比較2組均完成8周治療,用藥4周后治療組總有效率明顯高于對照組(P<0.01),且用藥8周后總有效率亦明顯高于對照組(P<0.01)。見表3。
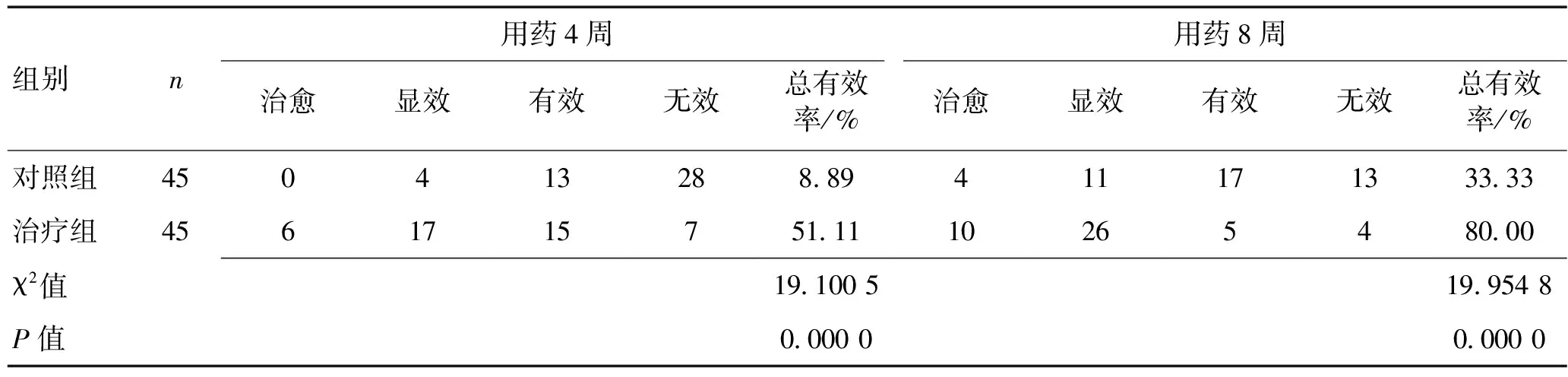
表3 2組治療4周、8周后抑郁療效比較 (n)
2.4不良反應治療組用藥期間出現惡心2例,失眠3例,頭痛2例,口干2例,乏力1例,不良反應發生率22.22%;對照組分別為1例、2例、2例、1例、0,不良反應發生率13.33%,2組比較,經χ2檢驗,差異無統計學意義(χ2=1.216 2,P=0.270 1)。
3 討論
帕金森病是中老年常見的一種慢性退行性中樞神經系統疾病,主要表現為運動障礙癥狀,還可出現抑郁、焦慮等精神癥狀,嚴重影響患者的生存質量[9-11]。帕金森發病與腦內多巴胺合成和代謝相關,中樞多巴胺活動異常和帕金森合并抑郁癥狀密切相關,LAU等[12]報道dPD患者血小板5-HT含量減少,同期和昱辰等[13]亦報道腦內5-HT神經遞質含量顯著降低。5-HT具有阻止紋狀體多巴胺釋放的作用,5-HT減少是紋狀體對多巴胺減少的功能性調節[14],5-HT減少狀態亦是抑郁發生的一項危險因素[15],故帕金森患者抑郁癥發生率高,可先于帕金森癥狀出現,但目前臨床尚無統一的治療標準和原則,多以對癥治療為主。
左旋多巴為多巴胺神經遞質合成的前提,可直接穿過血-腦屏障進入中樞神經系統,并經脫羧酶作用轉化為多巴胺而發揮相應的藥理作用[16],因L-DOPA可轉換為多巴胺和5-HT,故左旋多巴不僅可確切改善PD患者運動癥狀,還可通過減少“關”期減少并減輕抑郁癥狀[17],但大部分左旋多巴在進入中樞系統前已被代謝和消耗,僅約1%左旋多巴進入中樞神經轉化成多巴胺發揮作用,故臨床中極少單獨應用。中國帕金森病治療指南(第3版)指出“盡可能以小劑量達到滿意臨床效果”的用藥原則[18-19],卡比多巴/左旋多巴復方制劑被公認為是治療PD癥狀的金標準[20]。故本次研究選擇卡比多巴/左旋多巴復方制劑——息寧控釋片,發現治療組治療后HAMD評分降低程度較對照組更為顯著(P<0.05),治療4周和8周對抑郁狀態的療效均明顯優于對照組(P<0.05),且未見嚴重的不良反應。另外,對患者進行隨訪,評估其生活質量情況發現對照組PDQ-39評分雖有所下降,但差異無統計學意義(P>0.05),治療組PDQ-39評分下降趨勢較為明顯(P<0.05),且不同時點治療組PDQ-39評分均低于對照組(P<0.05),提示卡比多巴/左旋多巴復方制劑在短期內可明顯改善患者抑郁狀態、療效確切,不良反應少且輕微,還可明顯提高患者的生存質量。STANSLEY等[21]報道,左旋多巴具有一定的神經毒性作用,可導致多巴胺能神經元死亡。LEENTJENS等[22]構建PD抑郁模型發現,左旋多巴的使用為dPD發生的特異性危險因素之一,多項報道證實,長期應用左旋多巴治療帕金森病患者運動障礙癥狀同時損傷腦內5-HT能神經元,可能會誘發或加重抑郁癥狀[23-24],但本次研究尚未監測患者腦內5-HT水平,且未對患者遠期效果及不良反應進行隨訪研究,有待進一步完善。
[1] PRAKASH A,CHOPRA K,MEDHI B.Granulocyte-colony stimulating factor improves Parkinson’s disease associated with co-morbid depression:An experimental exploratory study[J].Indian J Pharmacol,2013,45(6):612-615.
[2] 羅琴.重復經顱磁刺激對帕金森抑郁患者的生活質量及運動癥狀療效的影響[J].國際神經病學神經外科學雜志,2015,42(6):488-491.
[3] 陳伶,符曉蘇,吳婷.帕金森病伴發抑郁研究進展[J].臨床精神醫學雜志,2013,23(6):424-425.
[4] 王雪.鹽酸帕羅西汀對帕金森病伴抑郁及焦慮患者的臨床療效[J].中國實用神經疾病雜志,2016,19(18):35-36.
[5] 姚燕,劉衛國.帕金森病伴發抑郁[J/CD].中華腦科疾病與康復雜志(電子版),2015,5(4):255-259.
[6] 劉慧,陳晨,王曉平.左旋多巴在帕金森病以外的臨床應用[J/CD].中華臨床醫師雜志(電子版),2013,7(22):10 206-10 208.
[7] 中華醫學會神經病學分會神經心理學與行為神經病學組.中華醫學會神經病學分會帕金森病及運動障礙學組.帕金森病抑郁、焦慮及精神病性障礙的診斷標準及治療指南[J].中華神經科雜志,2013,46(1):56-60.
[8] 李兆昌.帕羅西汀治療帕金森病抑郁狀態療效分析[J].現代醫生,2014,14(1):35-37.
[9] 唐曉輝,賀朝暉.帕金森病患者的抑郁癥狀與生活質量[J].中國神經精神疾病雜志,2011,37(10):635-636.
[10] GROVER S,SOMAIYA M,KUMAR S,et al.Psychiatric asp-ects of Parkinson’s disease[J].J Neurosci Rural Pract,2015,6(1):65-67.
[11] MORLEY J F,PAWLOWSKI S M,KESARI A,et al.Motor and non-motor features of Parkinson’s disease that presisitent drug-induced Parkinsonism[J].Parkinsonism Relat Disord,2014,20(7):738-742.
[12] LAU L M,VERBAAN D,MARINUS J,et al.Survival in Parkinson’s disease.Relation with motor and non-motor features[J].Parkinsonism Relat Disord,2014,20(6):613-616.
[13] 和昱辰,張波,瞿瑋,等.血清單胺類神經遞質及其代謝產物在重度抑郁癥共病焦慮障礙診斷中的應用[J].第三軍醫大學學報,2014,36(8):806-810.
[14] 楊秀毅.電針刺激聯合左旋多巴治療帕金森病的療效觀察[J].中國實用神經疾病雜志,2016,19(13):103-105.
[15] SHEN C C,TSAI S J,PERNG C L,et al.Risk of Parkinson disease after depression:a nationwide population-based study[J].J Neurol,2013,81(17):1 538-1 544.
[16] 朱駿,張麗.帕金森病神經精神癥狀的研究進展[J].中風與神經疾病雜志,2015,22(6):390-394.
[17] ESKOW JAUNARAJS K L,ANGOA-PEREZ M,KUHN D M,et al.Potential mechanisms underlying anxiety and depression in Parkinson’s disease:consequences of L-DOPA treatment[J].Neurosci Biobehav Rev,2011,35(3):556-564.
[18] 江名芳,于生元.帕金森抑郁的研究進展[J].中風與神經疾病雜志,2015,32(4):376-377.
[19] 黃瓊,陳燕忠,呂竹芬.復發左旋多巴制劑的研究進展[J].廣東藥學院學報,2013,29(5):561-564.
[20] 中華醫學會神經病學分會帕金森病及運動障礙學組.中國帕金森治療指南(第三版)[J].中華神經科雜志,2014,47(6):159-162.
[21] STANSLEY B J,YAMAMOTO B K.Chronic L-dopa decreases serotonin neurons in a subregion of the dorsal raphe nucleus[J].J Pharmacol Exp Ther,2014,351(2):440-447.
[22] LEENTJENS A F,MOONEN ANJA J H,DUJARDIN K,et al.Modeling depression in Parkinson disease:disease-specific and nonspecific risk factors[J].J Neurol,2013,81(12):1 036-1 043.
[23] 王永春,王釗,王偉.美多芭對帕金森患者血小板中五羥色胺含量的影響與抑郁癥狀[J].腦與神經疾病雜志,2016,24(2):85-87.
[24] 季俊霞,梁桂文,許振華,等.抗抑郁治療對帕金森病伴抑郁患者工作記憶的影響[J].中華行為醫學與腦科學雜志,2017,26(6):513-518.

