AMPK活化對慢性間歇缺氧大鼠胰島素抵抗和炎癥因子的影響*
陳 實(shí),孟慶華,李承紅
(江漢大學(xué)附屬醫(yī)院/武漢市第六醫(yī)院呼吸內(nèi)科,武漢 430000)
AMPK活化對慢性間歇缺氧大鼠胰島素抵抗和炎癥因子的影響*
陳 實(shí),孟慶華,李承紅△
(江漢大學(xué)附屬醫(yī)院/武漢市第六醫(yī)院呼吸內(nèi)科,武漢 430000)
單磷酸腺苷激活蛋白激酶;睡眠呼吸暫停綜合征;胰島素抵抗;炎癥因子;脂聯(lián)素;瘦素
阻塞性睡眠呼吸暫停綜合征(OSAS)是一種發(fā)病率高、危險(xiǎn)性大的疾病[1-2]。其主要病理生理變化是睡眠時(shí)反復(fù)出現(xiàn)的呼吸暫停引起慢性間歇缺氧[3],此過程引起氧化應(yīng)激活化,促發(fā)炎癥因子釋放,影響脂肪代謝和糖代謝,可導(dǎo)致胰島素抵抗(IR)的發(fā)生。上述的發(fā)揮均有賴于單磷酸腺苷激活蛋白激酶(AMPK)的活化。AMPK的活化在機(jī)體炎性反應(yīng)和能量代謝方面具有重要價(jià)值。為此,本文建立慢性間歇缺氧大鼠模型,模擬OSAHS患者存在的缺氧/再復(fù)氧病理生理過程,觀察大鼠脂肪組織中AMPK、炎癥因子的變化和IR情況,探討AMPK活化對炎癥介質(zhì)和胰島素抵抗的影響。
1 材料與方法
1.1材料
1.1.1動(dòng)物及飼料 健康雄性SD大鼠,SPF級(jí),體質(zhì)量(200±10)g,由華中科技大學(xué)同濟(jì)醫(yī)學(xué)院實(shí)驗(yàn)動(dòng)物中心提供。大鼠普通飼料,由北京科奧協(xié)力飼料有限公司提供,合格證號(hào)SCXK(京)-2009-0008。
1.1.2儀器與試劑 數(shù)字測氧儀(上海市嘉定學(xué)聯(lián)儀表廠);全自動(dòng)酶標(biāo)儀(型號(hào)Multiskan-MK3,美國Thermo scientific公司);酶聯(lián)免疫吸附試驗(yàn)(ELISA)試劑盒(伊萊瑞特生物科技有限公司);顯微成像分析系統(tǒng)(日本Olympus公司)、LC-20A高效液相色譜儀(日本島津公司)、AMPK激活劑(AICAR)、兔抗大鼠p-AMPK-α(Thr172)抗體、兔抗大鼠AMPK-α抗體購自美國Cell Signaling公司,AMPK抑制劑(Compound C)購自德國Merck公司,小鼠抗大鼠甘油醛-3-磷酸脫氫酶(GADPH)抗體購自上海康成生物工程有限公司,小鼠抗大鼠α-actinin抗體、羊抗小鼠IgG-辣根過氧化物酶(HRP)及羊抗兔IgG-HRP購自武漢博士德生物工程有限公司,免疫印跡發(fā)光試劑盒購自美國Millipore公司。
1.2模型制備及干預(yù)
1.2.1動(dòng)物分組 用隨機(jī)數(shù)字表法將大鼠分為常氧對照組、間歇缺氧2周組,間歇缺氧8周組,每組12只。
1.2.2慢性間歇缺氧大鼠模型的建立 參考文獻(xiàn)[4]的方法,自制密閉有機(jī)玻璃間歇缺氧箱,選用4 mm厚有機(jī)玻璃制成28 cm×15 cm×15 cm長方體艙,一端留孔加蓋密封用于取放動(dòng)物,側(cè)壁留兩孔用于輸入氮?dú)馀c混合空氣。缺氧過程中動(dòng)物活動(dòng)自由,不進(jìn)飲食。由進(jìn)氣孔向密閉缺氧箱內(nèi)循環(huán)充入氮?dú)夂蛪嚎s空氣,每個(gè)循環(huán)過程為前55 s充入氮?dú)?后55 s充入壓縮空氣,總長110 s,采用數(shù)字測氧儀檢測缺氧箱中氧濃度,調(diào)節(jié)氣體流量,使每個(gè)循環(huán)缺氧箱內(nèi)的最低氧濃度達(dá)到7%~8%,然后逐漸恢復(fù)至21%,每天持續(xù)8 h。
1.2.3干預(yù)處理 對已建立慢性間歇缺氧的大鼠模型使用AICAR(含AICAR 1 mmol/L)和Compound C(含Compound C 1 μmol/L)進(jìn)行相應(yīng)處理。為方便數(shù)據(jù)統(tǒng)計(jì)表達(dá):用N代表常氧對照組和未進(jìn)行干預(yù);H代表間歇缺氧,阿拉伯?dāng)?shù)字代表持續(xù)間歇缺氧時(shí)間;A代表經(jīng)過AMPK特異性激動(dòng)劑處理;C代表經(jīng)過AMPK特異性抑制劑處理。將實(shí)驗(yàn)大鼠分為上述9組,每組4只。干預(yù)6 h后提取大鼠血清樣品和脂肪組織,存放待測。
1.2.4血液樣品的采集和處理 測定各組大鼠體質(zhì)量。血樣采集前,所有大鼠禁食12 h,用3%戊巴比妥鈉進(jìn)行動(dòng)物麻醉,每千克體質(zhì)量給藥15 mg(15 mg/kg)。動(dòng)物麻醉后尾部取血測血糖,沿腹中線切開皮膚,腹主動(dòng)脈取血,置于肝素化的離心管中,3 000 r/min離心20 min,分離出血漿,于-20 ℃存放待測。
1.2.5脂肪組織的采集和處理 將所有處理后的大鼠麻醉后,取各組大鼠腎周脂肪、腸系膜周脂肪,電子天平上準(zhǔn)確稱質(zhì)量后迅速放入-80 ℃低溫冰箱保存待測。
1.3觀察指標(biāo)及方法
1.3.1Western blot法半定量檢測AMPK、GLUT4的表達(dá) 用Western blot分析,加入各種抗體,利用SDS-PAGE電泳,免疫印跡用增強(qiáng)化學(xué)發(fā)光法(ECL)顯影、定洗片。結(jié)果用凝膠成像軟件量掃描條帶灰度,以p-AMPK條帶/β-acdn蛋白條帶值為AMPK活化水平。采用IPP6.0以圖像分析軟件檢測。以GAPDH作為內(nèi)參,以灰度比值表作為內(nèi)參,表示所檢測蛋白質(zhì)的相對含量[5]。
1.3.2血清胰島素和胰島素抵抗測定 采用放射免疫分析法測定空腹胰島素(FINS)水平。采用穩(wěn)態(tài)模型IR指數(shù)(HOMA-IR)作為IR評(píng)價(jià)指標(biāo)[6]:公式為FBG×FINS/22.5,其中空腹血糖單位為mmol/L,FINS單位為μU/mL。
1.3.3血清炎癥因子測定 采用ELISA檢測核因子κB(NF-κB)、缺氧誘導(dǎo)因子(HIF-1)、脂聯(lián)素、瘦素、白細(xì)胞介素-1(IL-1)、白細(xì)胞介素-6(IL-6)、腫瘤壞死因子(TNF-α)、脂聯(lián)素、瘦素。按試劑說明書進(jìn)行。
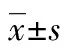
2 結(jié) 果
2.1不同程度慢性間歇缺氧大鼠和常氧對照組大鼠處理前炎癥因子和氧化應(yīng)激因子比較 慢性間歇缺氧大鼠NF-κB、HIF-1、IL-1、IL-6、TNF-α均高于常氧對照組(P<0.05),且缺氧程度越重,炎癥介質(zhì)水平越高,差異有統(tǒng)計(jì)學(xué)意義(P<0.05)。見表1。
2.2不同程度慢性間歇缺氧大鼠經(jīng)AICAR和Compound C處理后炎癥因子和氧化應(yīng)激因子比較 間歇缺氧大鼠經(jīng)AICAR處理后與處理前相比,其炎癥因子(IL-1、IL-6、TNF-α)和氧化應(yīng)激因子(NF-κB、HIF-1)均有所下降,而經(jīng)過Compound C處理后指標(biāo)有所上升(P<0.05)。見表2。
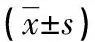
表1 慢性間接缺氧大鼠和常氧對照組大鼠炎癥因子和氧化應(yīng)激因子比較
*:P<0.05,與間歇缺氧2周、8周組比較
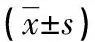
表2 慢性間歇缺氧大鼠經(jīng)AICAR和Compound C處理后炎癥因子和氧化應(yīng)激因子比較
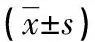
續(xù)表2 慢性間歇缺氧大鼠經(jīng)AICAR和Compound C處理后炎癥因子和氧化應(yīng)激因子比較

圖1 慢性間歇缺氧大鼠經(jīng)AICAR和Compound C處理前后IR指數(shù)比較

N+N:常氧對照組+未干預(yù);N+A:常氧對照組+AICAR組;N+C:常氧對照組+Compound C組;2H+N:間歇缺氧2周組+未干預(yù);2H+A:間歇缺氧2周組+AICAR組;2H+C:間歇缺氧2周組+Compound C組;8H+N:間歇缺氧8周組+未干預(yù);8H+A:間歇缺氧8周組+AICAR組;8H+C:間歇缺氧8周組+Compound C組
圖2慢性間歇缺氧大鼠經(jīng)AICAR和Compound C處理前后AMPK水平比較

N+N:常氧對照組+未干預(yù);N+A:常氧對照組+AICAR組;N+C:常氧對照組+Compound C組;2H+N:間歇缺氧2周組+未干預(yù);2H+A:間歇缺氧2周組+AICAR組;2H+C:間歇缺氧2周組+Compound C組;8H+N:間歇缺氧8周組+未干預(yù);8H+A:間歇缺氧8周組+AICAR組;8H+C:間歇缺氧8周組+Compound C組
圖3慢性間歇缺氧大鼠經(jīng)AICAR和Compound C處理前后GLUT4水平比較
2.3不同程度慢性間歇缺氧大鼠和常氧對照組大鼠經(jīng)AICAR和Compound C處理前后IR指數(shù)比較 8周間歇缺氧組大鼠的IR指數(shù)均高于2周間歇缺氧組大鼠及常氧對照組,差異有統(tǒng)計(jì)學(xué)意義(P<0.05)。見圖1。
2.4Western blot檢測脂肪組織中AMPK水平 Western blot結(jié)果顯示,與慢性間歇缺氧大鼠處理前比較,AICAR組脂肪細(xì)胞AMPK水平增高(P<0.05),Compound C組脂肪細(xì)胞AMPK水平降低(P<0.05),提示AICAR能激活脂肪細(xì)胞AMPK,而Compound C則抑制AMPK激活。見圖2。
2.5Western blot檢測脂肪組織中GLUT4水平 Western blot結(jié)果顯示,與慢性間歇缺氧大鼠處理前比較,AICAR組脂肪細(xì)胞GLUT4水平增高(P<0.05),Compound C組脂肪細(xì)胞GLUT4水平降低(P<0.05),提示AICAR能激活脂肪細(xì)胞GLUT4,而Compound C則抑制GLUT4激活。見圖3。
3 討 論
OSAS是一種發(fā)病率高、危險(xiǎn)性大的疾病。其主要病理生理變化是患者睡眠時(shí)反復(fù)出現(xiàn)的呼吸暫停引起的慢性間歇缺氧,導(dǎo)致低氧血癥及高碳酸血癥,從而導(dǎo)致高血壓、冠心病、腦卒中、代謝綜合征等多種并發(fā)癥[7-10]。本實(shí)驗(yàn)通過建立慢性間歇缺氧大鼠模型,模擬OSAS。
慢性間歇低氧引起的機(jī)體持續(xù)增強(qiáng)的炎性反應(yīng)在其中發(fā)揮重要推動(dòng)作用[11-12]。反復(fù)發(fā)生缺氧/復(fù)氧過程引起氧化應(yīng)激活化NF-κB和HIF-1等信號(hào)途徑,繼而促發(fā)炎癥因子的TNF-α、IL-1和IL-6等的大量釋放,本研究也發(fā)現(xiàn)慢性間歇缺氧大鼠缺氧程度越重,體內(nèi)炎癥介質(zhì)NF-κB、HIF-1、IL-1、IL-6、TNF-α釋放量增加。這些過量釋放的炎癥因子導(dǎo)致各種脂質(zhì)代謝、瘦素、脂聯(lián)素代謝紊亂而最終導(dǎo)致IR的發(fā)生[13]。有研究發(fā)現(xiàn),與健康人群相比,OSAS患者糖代謝異常的發(fā)病率亦明顯增加。Meslier等[14]研究494例男性O(shè)SAS患者,2型糖尿病和糖耐量異常的發(fā)生率分別為30.1%和20.0%,血糖水平與OSAS嚴(yán)重程度呈正相關(guān),并認(rèn)為OSAS是獨(dú)立于年齡、肥胖等因素之外與糖代謝異常相關(guān)的因素。本研究也發(fā)現(xiàn)缺氧程度越重的大鼠體內(nèi)IR的程度越重。
但慢性間歇缺氧介導(dǎo)的OSAS導(dǎo)致的全身炎癥因子的改變和代謝異常是通過什么信號(hào)通路傳導(dǎo),目前尚無相應(yīng)研究。
AMPK是真核細(xì)胞生物中重要的絲氨酸/蘇氨酸蛋白激酶[15]。AMPK可通過影響細(xì)胞物質(zhì)代謝的多個(gè)環(huán)節(jié)維持細(xì)胞能量供求平衡[16]。當(dāng)細(xì)胞內(nèi)三磷腺苷(ATP)減少時(shí),AMPK可通過抑制糖原、脂肪和膽固醇的合成,減少ATP 的利用;另外可通過促進(jìn)脂肪酸氧化、葡萄糖轉(zhuǎn)運(yùn)等,增加ATP 的產(chǎn)生。因此,AMPK 被認(rèn)為是調(diào)節(jié)細(xì)胞能量代謝的開關(guān)。研究表明AMPK在缺乏胰島素情況下AICAR可促進(jìn)葡萄糖的攝取,增加GLUT4從微囊轉(zhuǎn)位到質(zhì)膜上從而促進(jìn)葡萄糖攝取[17]。
AMPK系統(tǒng)是一個(gè)新型的抗炎信號(hào)途徑,AMPK的活化在治療炎癥性疾病中具有重要價(jià)值。AMPK的激活減少cAMP介導(dǎo)的上皮氯化物的分泌,從而減輕炎性反應(yīng)。有研究顯示,AICAR抑制脂多糖誘導(dǎo)的致炎細(xì)胞因子(如TNF-α、IL-1和IL-6)及誘導(dǎo)型一氧化氮合酶的表達(dá)從而調(diào)節(jié)炎性反應(yīng)[18]。
本研究中,通過AICAR和Compound C干預(yù)慢性間歇缺氧大鼠,觀察不同缺氧程度的大鼠脂肪組織炎癥因子水平,AMPK及GLUT4的釋放量,發(fā)現(xiàn)AMPK激活后的大鼠體內(nèi)炎癥因子釋放減少,胰島素抵抗情況較前有改善,GLUT4水平增加。而抑制AMPK活性后大鼠體內(nèi)炎癥因子水平均上升,IR更嚴(yán)重,GLUT4水平也進(jìn)一步下降。以上結(jié)果提示AMPK能夠減少炎癥介質(zhì)的釋放,增加GLUT4水平,改善IR,從而調(diào)節(jié)能量代謝及炎癥介質(zhì)。
綜上所述,本課題研究OSAS大鼠模型缺氧、炎癥、能量代謝與AMPK的關(guān)系,發(fā)現(xiàn)AMPK與OSAS的能量代謝和炎性反應(yīng)有關(guān),其意義在于探討AMPK在OSAS中的發(fā)病機(jī)制,為臨床治療OSAS相關(guān)疾病提供新的思路與靶點(diǎn)。
[1]Fletcher EC.Obstructive sleep apnoea and cardiovascular death:cause-effect[J].Monaldi Arch Chest Dis,1995,50(5):340-341.
[2]Bradley TD.Right and left ventricular functional impairment and sleep apnea[J].Clin Chest Med,1992,13(3):459-479.
[3]Lurie A.Obstructive sleep apnea in adults:epidemiology,clinical presentation,and treatment options[J].Adv Cardiol,2011,46(1):1-42.
[4]Neubaauer JA.Physiological and genomic Consequences of intermittent hypoxia invited review:physiological Consequences of intermittent hypoxia:systemic blood pressure[J].J Appl Physiol,2001,90(4):1593-1599.
[5]Riek U,Scholz R,Konarev P,et al.Structural properties of Amp-Activated protein kinase:dimerization,molecular shape,and changes upon LigandBinding[J].J Biol Chem,2008,283(26):18331.
[6]Matthews DR.Insulin resistance and beta-cell function-a clinical perspective[J].Diabetes Obes Metab,2001,3(Suppl 1):28-33.
[7]Peppard PE,Young T,Palta M,et al.Prospective study of the association between sleep-disordered breathing and hypertension[J].N Engl J Med,2000,342(19):1378-1384.
[8]MesIier N,ouksel H,Racineux JL.Obstructive sleep apnea syndrome and cardiovascular risk[J].Rev Neurol,2001,157(11):S42-S45.
[9]Engleman HM,Kingshott RN,Martin SE,et al.Cognitive function in the sleep apnea/hypopnea syndrome(SAHS)[J].Sleep,2000,23(4):102-108.
[10]Luboshitzky R,Aviv A,Hefetz A,et al.Decreased pituitary-gonadal secretion in men with obstructive sleep apnea[J].J Clin Endocrinol Metab,2002,87(7):3394-3398.
[11]Drager LF,Togeiro SM,Polotsky VY,et al.Obstructive sleep apnea:a cardiometabolic risk in obesity and the metabolic syndrome[J].J Am Coll Cardiol,2013,62(7):569-576.
[12]Surani S,Subramanian S.Effect of continuous positive airway pressure therapy on glucose control[J].World J Diabetes,2012,3(4):65-70.
[13]Ogihara T,Asano T,Katagiri H,et al.Oxidative stress induces insulin resistance by activating the nuclear factor-kappa b pathway and disrupting normal subcellular distribution of phosphatidylinositol 3-kinase[J].Diabetologia,2004,47(5):794-805.
[14]Meslier N,Gagnadoux F,Giraud P,et al.Impaired glucose-insulin metabolism in males with obstructive sleep apnoea syndrome[J].Eur Respir J,2003,22(1):156-160.
[15]Arad M,Seidman CE,Seidman JG.AMP-activated protein kinase in the heart-role during health and disease[J].Circ Res,2007,100(4):474-488.
[16]蔡明春,黃慶愿,高鈺琪.AMPK與能量代謝[J].重慶醫(yī)學(xué),2005,34(1):120-122.
[17]Koistinen HA,Galuska D,Chibalin A.5-Amino-Imidazole Carboxamide Riboside increases glucose transport and cell-surface GLUT4 content in skeletal muscle from subjects with type 2 diabetes[J].Diabetes,2003,52(5):1066-1072.
[18]Jung CH,Lee MJ,Kang YM,et al.Vaspin inhibits cytokine-induced nuclear factor-kappa B activation and adhesion molecule expression via AMP-activated protein kinase activation in vascular endothelial cells[J].Cardiovasc Diabetol,2014,13(1):41.
EffectsofAMPKactivationoninsulinresistanceandinflammatoryfactorsinratswithchronicintermittenthypoxia*
ChenShi,MengQinghua,LiChenghong△
(DepartmentofRespiration,AffiliatedHospitalofJianghanUniversity/WuhanMunicipalSixthHospital,Wuhan,Hubei430000,China)
AMP activated protein kinase;sleep apnea hypopnea syndrome;insulin resistance;inflammatory factor;adiponectin;leptin
目的探討單磷酸腺苷激活蛋白激酶(AMPK)活化對慢性間歇缺氧大鼠胰島素抵抗和炎癥因子的作用及其機(jī)制。方法建立慢性間歇缺氧大鼠模型模擬阻塞性睡眠呼吸暫停綜合征(OSAS),將36只雄性SD大鼠分為常氧對照組、2周間歇缺氧組、8周間歇缺氧組。觀察AMPK激動(dòng)劑和AMPK抑制劑作用不同缺氧程度的大鼠體內(nèi)炎癥介質(zhì)、血脂、脂聯(lián)素、瘦素及胰島素抵抗水平,監(jiān)測大鼠脂肪組織AMPK、葡萄糖轉(zhuǎn)運(yùn)蛋白(GLUT4)水平,并進(jìn)行統(tǒng)計(jì)學(xué)分析。結(jié)果間歇缺氧大鼠總膽固醇、三酰甘油、腫瘤壞死因子-α(TNF-α)、白細(xì)胞介素(IL)-6、IL-2、核因子κB(NF-κB)、缺氧誘導(dǎo)因子(HIF-1)顯著高于對照組(P<0.05);脂聯(lián)素、瘦素及胰島素抵抗指數(shù)顯著低于對照組(P<0.05)。使用AMPK激活劑后的大鼠體內(nèi)炎癥因子釋放減少,脂聯(lián)素、瘦素含量增加,血脂、胰島素抵抗情況較前有改善,GLUT4水平增加。而使用AMPK抑制劑處理后大鼠體內(nèi)炎癥因子、脂聯(lián)素、瘦素水平均上升,胰島素抵抗更嚴(yán)重,GLUT4水平也進(jìn)一步下降。結(jié)論AMPK能夠減少炎癥介質(zhì)的釋放,促進(jìn)脂聯(lián)素、瘦素的釋放,增加GLUT4水平,改善胰島素抵抗,從而調(diào)節(jié)能量代謝及炎癥介質(zhì),為臨床治療OSAS相關(guān)疾病提供新的思路與靶點(diǎn)。
R446.62
A
1671-8348(2017)31-4332-04
10.3969/j.issn.1671-8348.2017.31.004
湖北省自然科學(xué)基金面上項(xiàng)目(ZRY2014000966)。
陳實(shí)(1983-),碩士,主治醫(yī)師,主要從事睡眠呼吸暫停疾病的研究。△
,E-mail:15827636399@163.com。
ObjectiveTo investigate the effect and mechanism of adenosine monophosphate activated protein kinase(AMPK) activation on insulin resistance and inflammatory factors in rats with chronic intermittent hypoxia.MethodsThe chronic intermittent hypoxia rat model was established to simulate the obstructive sleep apnea syndrome (OSAS),and the 36 male SD rats were divided into the normal oxygen control group,2-week intermittent hypoxia group and 8-week intermittent hypoxia group.The levels of rat inflammatory medium,serum lipid,adiponectin,leptin and insulin resistance in different hypoxia degrees of rats by the action of AMPK agonist and AMPK inhibitor were observed,and the levels of AMPK and GLUT4 in rat adipose tissue were monitored and statistically analyzed.ResultsThe levels of total cholesterol,triglyceride,TNF-α,IL-6,IL-2,NF-κB and HIF-1 in the intermittent hypoxia rats were significantly higher than those in the control group(P<0.05);while the levels of adiponectin,leptin and insulin resistance index were significantly lower than those in the control group(P<0.05).The release of inflammatory factors in rats after using AMPK activator was decreased,the contents of adiponectin and leptin were increased,blood lipid and insulin resistance were improved compared with before,and the expression level of GLUT4 was increased.But after treatment by using AMPK inhibitor,the levels of inflammatory factors,adiponectin and leptin were increased,insulin resistance was more severe,and the expression level of GLUT4 protein was also further decreased.ConclusionAMPK can reduce the release of inflammatory mediators,promotes the release of adiponectin and leptin,increases the level of GLUT4,improves insulin resistance,thus regulates the energy metabolism and inflammatory mediators,which provides a new idea and target for clinical treatment of OSAS related diseases.
2017-03-22
2017-06-10)

