風心病合并房顫患者心肌microRNA表達譜分析與靶基因預測
韓莉莉+沈曉麗+賴力+林賽梅+劉小晴+翁國星+陳同+丁杭+胡潔+浦曉東

[摘要] 目的 研究風心病合并房顫患者心肌microRNAs的表達差異,預測其靶基因并分析其可能的生物學功能。方法經知情同意,整群采集2013年1—12月收治的14例住院風心病房顫患者和8例風心病無房顫患者右心耳組織;提取總RNA進行miRNAs芯片雜交檢測,應用RMA和FC法篩選差異表達的miRNAs,并用RT-PCR進行驗證;運用生物信息學軟件預測靶基因并分析其生物學功能。結果 與風心病無房顫組相比,風心病合并房顫組有22個miRNAs表達有差異,其中6個miRNAs表達上調,16個miRNAs表達下調;驗證結果表明與風心病無房顫組比較,miR-661、miR-520d-5p和miR-145-5p表達顯著下調(P<0.01);經GO和KEGG數據分析,差異miRNA 靶基因的一部分亦與心肌纖維化相關。結論 該研究獲得與房顫相關的差異miRNAs,可能是房顫新的生物標志物和潛在治療靶點。
[關鍵詞] 房顫;微小RNA;表達譜;生物信息學
[中圖分類號] R4 [文獻標識碼] A [文章編號] 1674-0742(2017)02(c)-0007-04
Analysis of Myocardium MicroRNA Expression Profile and Prediction of Target Gene of Patients with Rheumatic and Atrial Fibrillation
HAN Li-li1, SHEN Xiao-li1, LAI Li1, LIN Sai-mei1, LIU Xiao-qing1, WENG Guo-xing2, CHEN Tong2, DING Hang1, HU Jie1, PU Xiao-dong1
1.Clinical Medical College of Medical University of Fujian, Fujian Key Laboratory of Cardiovascular Disease, Judicial Appraisal Institute of Fujian Province-owned Hospital, Fuzhou, Fujian Province, 350001 China;2.Department of Cardiac surgery, Fujian Provincial Hospital, Fuzhou, Fujian Province, 350001 China
[Abstract] Objective To research the expression difference of myocardium microRNA of patients with rheumatic and atrial fibrillation and predict the target gene and analyze the potential biology function. Methods Auricula dextra tissues of 14 cases of inpatients with rheumatic and atrial fibrillation and 8 cases of patients were group selected with rheumatic but without atrial fibrillation from January to December 2013 were collected, and the total RNA was extracted for miRNAs hybridization test, and the miRNAs was screened by RMA and FC, and then RT-PCR was used for verification, and the target gene was predicted by the biology information software and the biology function was analyzed. Results The expression of 22 miRNAs had differences in the combined group, including 6 whose expression increased and 16 whose expression decreased, and the expressions of miR-661, miR-520d-5p and miR-145-5p obviously decreased compared with the other group, all P<0.01, the GO and KEGG data analysis showed that the some of differential miRNA target genes was correlated with the myocardial fibrosis. Conclusion The differential miRNA related to atrial fibrillation may the new biomarkers of atrial fibrillation and potential treatment target point.
[Key words] Atrial fibrillation; mini RNA; Expression profile; Information biology
風濕性心臟病是因風濕活動引起的心臟病變,常導致房顫發生。房顫(Atrial Fibrillation ,AF),是多因素導致的心律失常[1]。微小RNA(miRNA)是長約22個核苷酸的非編碼單鏈RNA,可使靶mRNA降解或者抑制其翻譯而在轉錄后和翻譯水平發揮調控作用,繼而影響細胞增殖分化和凋亡等[2]。既往研究miR-30、miR-21、miR-150和miR-146[3-4]等可能參與AF, 而miRNA在AF心肌纖維化的作用尚缺少研究。通過分析2013年1—12月收治的22例風心病瓣膜置換者miRNAs表達,該研究擬尋找新的調控AF心肌纖維化的miRNAs并預測其靶基因,為進一步揭示miRNAs在AF的作用機制及尋求安全、有效診治AF的靶點提供理論依據,現報道如下。
1 資料與方法
1.1 一般資料
整群選擇該院心外科接受風心病瓣膜置換的患者,知情同意后入選。分兩組:風心病合并房顫組14例,風心病無房顫組8例。采集患者右心耳心肌組織放入液氮凍存備用。
1.2 RNA抽提
Trizol法提取總RNA并檢測其質量和含量,用瓊脂糖電泳檢測其完整性,質控標準:1.7
1.3 miRNA芯片雜交
先分析總RNA,然后選用FlashTag Biotin HSR 標記試劑對樣品進行標記后雜交,繼而用 GeneChip雜交洗染試劑來洗染芯片,最后掃描得到圖片和原始數據。
1.4 芯片結果的RT-PCR驗證
1.4.1 引物設計 擴大樣本量,挑取6個差異miRNAs進行組織驗證,用Primer 5.0設計引物,U6 為內參照,見表1。
1.4.2 RT-PCR 擴增 反應體系為20 μL,10μL SYBR premix ex taq,0. 5 μL 上、下游引物(2.5 μM) ,8 μL H2O,加入1 μL cDNA 后混勻。循環條件為: DNA變性1 個循環:95℃ 30 s,目標DNA擴增45個循環:95℃ 5 s、60 ℃,30s,反應結束后制作熔解曲線。
1.5 靶基因預測和功能分析
采用targetscan、miRDB與mimada 3種軟件對差異表達miRNA靶基因進行預測。基于Gene Ontology數據庫,通過GO分析對靶基因進行GO分類,再通過KEGG數據庫分析靶基因的信號通路及功能分布,初步了解差異miRNAs對AF發生、發展的調控情況。
1.6 統計方法
采用RMA方法和倍數變化法(FC)篩選差異miRNAs,判斷標準為|FC|>2或|FC|<0.5。熒光定量PCR 數據采用2 - ΔΔCt法分析,采用SPSS 13.0統計學軟件對計量資料進行t檢驗,P<0.05為差異有統計學意義。
2 結果
2.1 miRNA表達譜芯片數據分析結果
miRNA表達譜芯片檢測顯示,該研究中與風心病無房顫組相比,風心病合并房顫組患者有16個miRNAs(miR-520d-5p、miR-661、miR-4490、miR-4474-3p、miR-4518、miR-379*、miR-3939、miR-1243、miR-4793-3p、miR-548c-3p、miR-4711-5p、miR-4754、miR-4677-5p、miR-4423-3p、miR-145*、miR-1252)相對表達下調,6個miRNAs相對表達上調(miR-4800-3p、miR-3174、miR-4723-5p、miR-218-2*、miR-920、miR-4470)(P<0.05)。
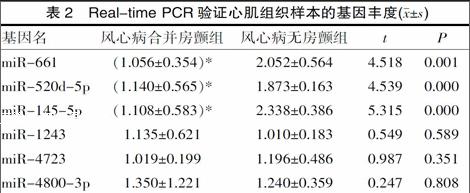
2.2 Real-time PCR驗證結果
選擇6條miRNAs做組織驗證,結果與風心病無房顫組相比,風心病有房顫組中miR-661、miR-520d-5p和miR-145-5p表達顯著下調(P<0.01),與芯片結果一致;而miR-4800-3p、miR-1243和miR-4723在兩組表達差異無統計學意義,與芯片結果不一致,不適于進一步功能研究,見表2。
注:與風心病無房顫組比較,*P<0.01。
2.3 miRNA靶基因的預測和功能分析
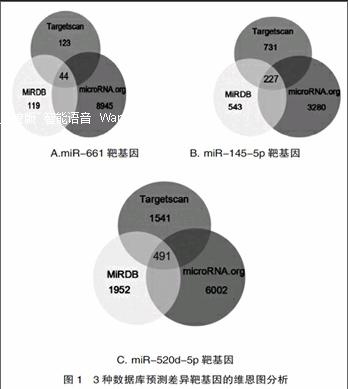
通過分析差異miRNA的靶基因,選擇3個數據庫共同預測得出有交集的靶基因, miR-661、miR-145-5p和hsa-520d-5p靶基因分別有44、227個和491個,具體分布及重疊情況見圖1。
A.miR-661靶基因 B. miR-145-5p靶基因
C. miR-520d-5p靶基因
通過在Pubmed檢索并對照《人類基因功能手冊》,確定上述差異miRNA最有可能的靶基因,見表4。
基于 Gene Oncology和KEGG數據庫,進行GO和Pathway分析,結果除涉及核酸、蛋白代謝外,這些靶基因生物學途徑還涉及信號轉導(Wnt通路為主)及胞外基質合成,此外也參與了心臟組織發育、細胞增殖,調節粘附、轉錄因子活性及炎癥等。
3 討論
miRNA是近年來生命科學研究的熱點,既往對其研究主要集中在生物發生等方面,在心血管疾病中的研究起步較晚。雖然已發現多種在心血管發育及疾病病理發生過程中發揮非常重要作用的miRNAs,但有關房顫和心肌細胞外基質纖維化研究較少,而且絕大多數是動物實驗的結果。因此,該研究選擇風心病接受瓣膜置換患者右心耳組織作為實驗材料,探討了miRNAs在房顫發生發展的機制,實驗結果更具真實性。
寡核苷酸芯片具有特異性和敏感性高、重復性好、假陽性率低等優點,在心肌組織miRNA分析中得到廣泛應用。RT-PCR驗證結果發現風心病房顫組較風心病無房顫組miR-520d-5p、 miR-661和miR-145-5p表達顯著下調(P<0.01),與芯片結果一致;而另3種miRNA在兩組表達差異無統計學意義,與芯片結果不一致,可能原因有:①基因芯片具有高通量優勢也存在假陽性的不足之處,②FC法篩選差異miRNAs具有簡便、節約成本等優點,也存在結論過于簡單、閾值劃分主觀性較強等缺點,易產生假性結果[5],適用于預實驗和實驗初篩。
既往有關miRNAs與AF的研究中,Liu Z等[6]報道miR-188-5p、miR-1181等8條表達上調,miR-497、miR-145等20條下調。另有報道miR-17、miR-10b、等5條miRNA表達上調;miR-30c、miR-100等5條miRNA表達下調[7]。該研究首次發現miR-661和miR-520d-5p與AF有關,且與風心病無房顫患者相比,風心病合并房顫患者上述miRNA表達水平降低。由于AF機制的復雜性,該研究推測AF形成可能是諸多miRNA調控下游靶基因的結果。
為進一步探討差異miRNA調控預測靶基因的功能,該研究應用PubMed檢索顯示多數預測的靶基因尚未見與AF相關的報道,提示這些miRNA可能通過信號通路級聯效應對AF進行調控。GO分析結果顯示除涉及核酸、蛋白代謝外,miR-661靶基因生物學功能主要集中在細胞外基質的合成與代謝上,而胞外基質在調節心肌細胞收縮和胞間信息中起重要作用[8],表明差異miRNA與AF發生有關。AF涉及電重構、結構重構等過程,其都涉及信號通路的調控。KEGG分析顯示這些miRNA影響的靶基因主要在Wnt、細胞骨架、粘附連接和MAPK等信號通路上,尤以Wnt通路富集指數最高,Wnt通路可能是這些miRNA調控的核心通路。
綜上所述,該研究為了解AF發生機制提供了新視野,miR-661、miR-520d-5p和miR-145-5p可作為檢測AF的新的標志物,后續研究中也將進一步通過功能實驗等探索其與靶基因的關系,以期為AF機制的研究及尋找安全、有效治療AF的藥物提供新的思路。
[參考文獻]
[1] Lip GY, Tse HF, Lane DA. Atrial fibrillation[J].Lancet, 2012,379(9816):648-661.
[2] Shi KH, Tao H, Yang JJ, et al. Role of microRNAs in atrial fibrillation: new insights and perspectives[J].Cell Signal, 2013,25(11):2079-2084.
[3] Li H, Li S, Yu B,et al. Expression of miR-133 and miR-30 in chronic atrial fibrillation in canines[J].Mol Med Rep, 2012,5(6):1457-1460.
[4] Goren Y, Meiri E, Hogan C,et al.Relation of reduced expression of MiR-150 in platelets to atrial fibrillation in patients with chronic systolic heart failure[J]. Am J Cardiol, 2014, 113(6):976-981.
[5] 高利宏, 曹佳. 基因芯片可靠性分析及數據處理[J]. 第三軍醫大學學報, 2006,28(1):80-82.
[6] Liu Z, Zhou C, Liu Y,et al.The expression levels of plasma micoRNAs in atrial fibrillation patients[J]. PLoS One, 2012,7(9):e44906.
[7] Cooley N, Cowley MJ, Lin RC,et al.Influence of atrial fibrillation on microRNA expression profiles in left and right atria from patients with valvular heart disease[J].Physiol Genomics, 2012,44(3):211-219.
[8] Shi KH, Tao H, Yang JJ,et al.Role of microRNAs in atrial fibrillation: new insights and perspectives[J]. Cell Signal, 2013,25(11):2079-2084.
(收稿日期:2016-11-28)

