GeneXpert MTB/RIF在脊柱結核診斷中的應用
周正,王曉蕾,陳海燕,馬源慧,周西清,景輝,趙躍然
(1濟南大學·山東省醫學科學院醫學與生命科學學院,濟南250013;2山東省胸科醫院;3山東省醫學科學院)
GeneXpert MTB/RIF在脊柱結核診斷中的應用
周正1,2,王曉蕾2,陳海燕2,馬源慧2,周西清2,景輝2,趙躍然3
(1濟南大學·山東省醫學科學院醫學與生命科學學院,濟南250013;2山東省胸科醫院;3山東省醫學科學院)
目的 探討GeneXpert MTB/RIF在脊柱結核診斷中的應用價值。方法 采用GeneXpert MTB/RIF對臨床及病理檢查確診的72例脊柱結核患者和20例非脊柱結核患者的脊柱組織標本進行檢測,計算其診斷脊柱結核的敏感性、特異性、陰性預測值、陽性預測值,并與MGIT960液體培養、抗酸涂片染色法進行比較;評價GeneXpert MTB/RIF檢出利福平(RIF)耐藥性的效能。結果 GeneXpert MTB/RIF檢測診斷脊柱結核的敏感性為76.38%(55/72)、特異性為95.00%(19/20),MGIT 960液體培養診斷診斷脊柱結核的敏感性為54.60%(39/72)、特異性為90.00 %(18/20),抗酸涂片染色法診斷診斷脊柱結核的敏感性為27.77 %(20/72)、特異性為100%(20/20)。GeneXpert MTB/RIF檢測診斷脊柱結核的敏感性高于MGIT 960液體培養和抗酸涂片染色法(P均<0.05)。結論 GeneXpert MTB/RIF可輔助診斷脊柱結核能顯著提高脊柱結核的檢出率。
脊柱結核;脊柱組織標本評價系統;結核分枝桿菌;利福平;MTB/RIF檢測系統
中國是全球結核病高發病率國家之一,結核病患者數量僅次于印度[1]。脊柱結核是結核病的重要類型之一,占結核病患者的1%~5%[2]。其中,脊柱結核占骨結核的50%[3]。結核分枝桿菌(MTB)培養和抗酸桿菌染色法是傳統結核病實驗室診斷的金標準。然而,傳統試驗存在諸多弊端,如抗酸染色法陽性率偏低,結核培養周期較長,需3~8周,且對活菌的要求高。GeneXpert MTB/RIF作為一種快速、有效的分子診斷手段,可在2 h內直接從痰液標本中檢測MTB和利福平(RIF)耐藥性,其敏感性為67%~98%,特異性為98%[4,5]。本研究采用術后脊柱病灶組織標本,評價GeneXpert MTB/RIF在脊柱結核中的診斷價值。
1 資料與方法
1.1 臨床資料 收集2016年1~12月山東省胸科醫院收治的經臨床診斷和病理檢查確診的脊柱結核患者72例,經影像學檢查明確診斷,排除既往有結核感染的患者。其中男42例、女30例,年齡11~77歲、平均39.76歲,頸椎結核2例、胸椎結核22例、腰椎結核45例、骶椎結核3例,癥狀為咳嗽33例、咳痰23例、發熱15例、咯血8例、胸痛11例、血液傳播2例、繼發性肺結核19例,經液體藥敏法檢測RIF耐藥38例。選擇同期經臨床診斷和病理檢查確診的非結核患者20例,男11例、女9例,年齡22~45歲、平均37.89歲,椎間盤突出癥11例、其他非結核疾病9例。兩組均經手術治療,術中獲取脊椎病灶組織。
1.2 檢測方法 根據患者病灶不同部位選取疑似結核病灶組織(膿液、干酪樣組織、肉芽組織等),將所獲取的脊椎病灶組織進行充分粉碎研磨,加入氫氧化鈉、磷酸鹽緩沖液震蕩離心,離心后的沉淀物分成3份待用,分別采用GeneXpert MTB/RIF、MGIT 960液體培養和藥物敏感試驗、抗酸涂片染色法進行檢測。GeneXpert MTB/RIF檢測:取沉淀物樣本1 mL加入GeneXpert MTB/RIF樣本前處理液2 mL,置于渦旋振蕩器上混勻孵育15 min,取處理液加入反應盒后置于GeneXpert檢測模塊中,2 h后判讀結果。結果判讀:根據GeneXpert MTB/RIF探針的循環閾值(Ct值),當內對照探針Ct值≤38為陽性。MGIT960液體培養和藥物敏感試驗:取沉淀物0.5 mL置于添加營養劑和雜菌抑制劑的MGIT960液體培養管中,放于MGIT 960培養儀中,監測管中氧氣濃度,當氧氣被消耗時,管底部的熒光顯示劑在特定光源下激發出熒光,儀器通過數據處理得出陽性結果。對陽性樣本進行RIF(1 μg/mL)藥敏試驗。抗酸涂片染色法:按照《結核病診斷實驗室檢驗規程》中的要求進行標準化操作,當涂片結果≥1+(3~9條抗酸桿菌/100個視野)時,該涂片結果為陽性。
1.3 統計學方法 采用SPSS16.0統計軟件。以臨床診斷及病理學檢查為金標準計算各類檢查方法診斷脊柱結核的敏感性、特異性、陰性預測值、陽性預測值及其95%置信區間。以液體藥敏結果為金標準,評價GeneXpert MTB/RIF檢出MTB及RIF耐藥性的準確性。計數資料比較采用χ2檢驗。P<0.05為差異有統計學意義。
2 結果
2.1 GeneXpert MTB/RIF對脊柱結核的診斷效能 脊柱結核患者72例,GeneXpert MTB/RIF 檢測MTB陽性55例、陰性17例,MGIT 960液體培養MTB陽性39例、陰性33例,抗酸涂片染色法MTB陽性20例、陰性52例。非結核患者20例,GeneXpert MTB/RIF 檢測MTB陽性1例、陰性19例, MGIT 960液體培養MTB陽性2例、陰性18例,抗酸涂片染色法MTB陽性0例、陰性20例。三種檢測方法對脊柱結核的診斷效能見表1。
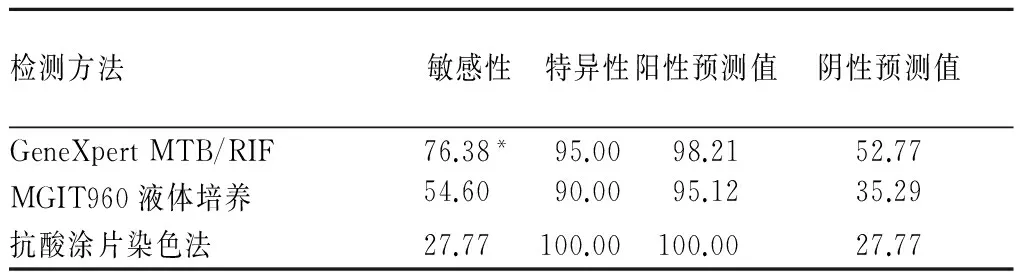
表1 三種檢測方法診斷脊柱結核的效能比較(%)
注:與MGIT960液體培養、抗酸涂片染色法比較,*P<0.05。
2.2 GeneXpert MTB/RIF對RIF耐藥性的診斷價值 GeneXpert MTB/RIF對38例RIF耐藥患者進行檢測,檢出RIF耐藥23例。GeneXpert MTB/RIF對RIF耐藥的敏感性為81.81%(18/22),特異性為68.75%(11/16)。
3 討論
近年來,我國脊柱結核患者日趨增多,并且耐多藥的患者比例較高,約占22%[6]。傳統的結核培養和抗酸染色涂片方法敏感性較低,常誤診[7]。WHO對結核病控制的重點是快速準確的診斷結核病尤其是提高耐多藥結核的診斷能力。在結核病的分子診斷技術中,檢測MTB的DNA可提高試驗的有效性和準確性[8]。GeneXpert MTB/RIF以半巢式實時定量PCR為基礎,檢測MTB中rpoB基因,檢測周期為2 h左右,并且可以檢測RIF的耐藥性。其在痰標本中檢測結核病以及RIF耐藥性的敏感性和特異性較高,成為WHO推薦的檢測結核病的方法[9]。本研究以臨床診斷和病理檢查為金標準,使用的標本類型為脊柱結核病灶組織,比較GeneXpert MTB/RIF、MGIT960液體培養、抗酸涂片染色法三種方法對檢測脊柱結核的效能。結果顯示,GeneXpert MTB/RIF的敏感性遠優于MGIT960液體培養、抗酸涂片染色法。Sun等[10]報道, GeneXpert MTB/RIF結果敏感性為80%,與本研究的76.38%相符,遠高于結核桿菌固體和液體培養。本研究利用GeneXpert MTB/RIF分別與MGIT960液體培養、抗酸涂片染色法合并診斷脊柱結核,取得較好研究結果。其中,單獨使用抗酸涂片診斷結核病的敏感性僅為27.77%,但與GeneXpert MTB/RIF合并后診斷的敏感性提升至51.85%,使用GeneXpert MTB/RIF聯合抗酸涂片診斷能顯著的降低了抗酸涂片的假陰性率。使用GeneXpert MTB/RIF聯合抗酸涂片染色法可以在2 h內檢測出MTB和RIF耐藥性的結果,大大縮短診斷結核病的TAT時間[11,12]。本研究中在確診脊柱結核患者中仍有17例標本的GeneXpert MTB/RIF結果顯示陰性,此假陰性出現的原因可能為脊柱結核患者在術前已經使用大量的抗結核藥物,并且手術后取得的標本被其他菌污染,干擾儀器的檢測。
李力韜等[13]用GeneXpert MTB/RIF試驗檢測脊柱結核患者的敏感性和特異性均達到98%以上,明顯高于本實驗,與以下原因有關:①李力韜等研究中使用結核培養陽性的標本進行GeneXpert MTB/RIF試驗,而本實驗直接使用臨床標本,未使用結核培養陽性標本菌株。②本實驗樣本量較少,并且病例中有兒童病例,有國外文獻報道,GeneXpert MTB/RIF 試驗檢測兒童結核患者時,其敏感性和特異性明顯低于成人[14]。③Arman等[15]試驗結果為重復試驗兩次以上后記錄的最后檢測結果,而本實驗僅檢測一次。因此,GeneXpert MTB/RIF 檢測次數的增加會在一定程度上可以加大其檢測MTB的敏感性和特異性。
本研究以液體藥敏結果為金標準,GeneXpert MTB/RIF檢測RIF的敏感性為81.81%,此結果與國外結果基本一致。然而特異性為68.75%,有5例標本未能檢測出耐藥基因的突變,原因可能為標本類型為術后組織標本,標本類型差異較大,組織標本含菌量較低,粉碎組織不徹底,并且其他組織雜質較多,標本的采集及運輸中存在污染,從而影響GeneXpert MTB/RIF儀器中DNA的擴增。
本研究顯示,GeneXpert MTB/RIF是一種快速、準確診斷脊柱結核及RIF耐藥性的方法。由于樣本量較少,本文僅就GeneXpert MTB/RIF對脊柱結核的診斷價值進行了總體研究,未對頸椎、胸椎、腰椎、骶椎結核的診斷進一步分析。因此,驗證GeneXpert MTB/RIF對脊柱不同部位結核的早期診斷意義將是未來的研究方向。
[1] Pawar UM, Kundnani V, Agashe V, et al. Multidrug-resistant tuberculosis of the spine--is it the beginning of the end? A study of twenty-five culture proven multidrug-resistant tuberculosis spine patients[J]. Spine, 2009,34(22):E806-810.
[2] Trecarichi EM, Di ME, Mazzotta V, et al. Tuberculous spondylodiscitis: epidemiology, clinical features, treatment, and outcome[J]. Eur Rev Med Pharmacol Sci, 2012,16(Suppl 2):58-72.
[3] Massi MN, Biatko KT, Handayani I, et al. Evaluation of rapid GeneXpert MTB/RIF method using DNA tissue specimens of vertebral bones in patients with suspected spondylitis TB[J]. J Orthop, 2017,14(1):189-191.
[4] 郭明日,張麗霞,周洪經,等.Xpert MTB/RIF、T-SPOT·TB及BACTEC MGIT960在結核病診斷中的應用[J].山東醫藥,2016,56(37):93-95.
[5] Boehme CC, Nabeta P, Hillemann D, et al. Rapid molecular detection of tuberculosis and rifampin resistance[J]. N Engl J Med, 2010,363(11):1005-1015.
[6] Hillemann D, Rüsch-Gerdes S, Boehme C, et al. Richtee E. Rapid molecular detection of extrapulmonary tuberculosis by the automated GeneXpert MTB/RIF system[J]. J Clin Microbiol, 2011,49(4):1202-1205.
[7] 董偉杰,秦世炳,趙立平,等.骨關節結核各類標本進行結核分枝桿菌培養與PCR檢測的陽性率結果分析[J].結核病與胸部腫瘤,2014 (2): 97-100.
[8] 牛家峰,尚永明,張寧,等.復治肺結核患者痰液耐藥結核分枝桿菌鑒定中熒光定量PCR與反向點雜交技術的聯合應用[J].山東醫藥,2016,56(31):69-71.
[9] Rachow A, Zumla A, Heinrich N, et al. Rapid and accurate detection of Mycobacterium tuberculosis in sputum samples by Cepheid Xpert MTB/RIF assay-a clinical validation study[J]. PloS One, 2011,6(6):e20458.
[10] Sun J,Teng J, Yang H,et al. Endobronchial ultrasound-guided transbronchial needle aspiration in diagnosing intrathoracic tuberculosis[J]. Ann Thorac Surg, 2013,96(6):2021-2027
[11] Lawn SD, Nicol MP. Xpert ? MTB/RIF assay: development,evaluation and implementation of a new rapid molecular diagnostic for tuberculosis and rifampicin resistance[J]. Future Microbiol, 2011,6(9):1067-1082.
[12] Friedrich SO, Von GF, Diacon AH. Xpert MTB/RIF assay for diagnosis of pleural tuberculosis[J]. J Clin Microbiol, 2011,49(12):4341-4342.
[13] 李力韜,李洪敏,馬遠征,等.應用Xpert MTB/RIF對脊柱結核臨床標本行結核分枝桿菌與RIF耐藥性檢測的驗證性研究[J].中華骨科雜志,2014, 34(2):211-215.
[14] Nicol MP, Workman L, Isaacs W, et al. Accuracy of the Xpert MTB/RIF test for the diagnosis of pulmonary tuberculosis in children admitted to hospital in Cape Town,South Africa:a descriptive study[J]. Lancet Infect Dis, 2011,11(11):819-824.
[15] Armand S, Vanhuls P, Delcroix G, et al. Comparison of the Xpert MTB/RIF test with an IS6110-TaqMan real-time PCR assay for direct detection of Mycobacterium tuberculosis in respiratory and nonrespiratory specimens[J]. J Clin Microbiol, 2011,49(5):1772-1776.
趙躍然(E-mail:yrzhao@sdu.edu.cn)
10.3969/j.issn.1002-266X.2017.17.032
R529.2
B
1002-266X(2017)17-0090-03
2017-02-24)

