血管支架對顱內動脈瘤血液動力學的數值模擬*
胡成龍,木合塔爾·克力木,張光武,劉鵬,劉小月,王麗君
(新疆大學 機械工程學院,烏魯木齊830047)
1 引 言
動脈瘤一旦破裂,會導致蛛網膜下腔出血,致死率和致殘率非常高[1]。目前治療顱內動脈瘤的方法主要是顱內動脈瘤夾閉術和彈簧圈栓塞術。隨著高分辨率的二維、三維血管影像的出現,神經外科顯微技術和血管內介入技術的完善和普及,以及應用材料的不斷改進,血管內介入治療方法已廣泛應用于顱內動脈瘤的治療中,成為顱內動脈瘤治療的重要方法[2]。但是由于彈簧圈跑圈及移位等現象,使得常規的彈簧圈栓塞介入治療方法對于某些特殊形狀的動脈瘤如梭形動脈瘤、寬頸以及巨大動脈瘤的治療有很大困難。如果采用常規的彈簧圈栓塞介入治療方法進行治療,需要對動脈瘤進行致密填塞,需要的彈簧圈數量大,費用高,易形成移位效應,且動脈瘤易復發,風險高。而支架的使用明顯提高了治療效果[3]。Mase等[4]首次將支架應用于治療顱內寬頸動脈瘤中,血管支架成為治療顱內動脈瘤的新方法,且使用越來越普遍。Metcalfe等[5]研究發現,載瘤動脈置入支架后,瘤內的血流速度及壁面剪切力明顯減少,渦流運動減弱甚至消失,并隨著支架網眼密度的增加而更加減弱,而對血管中的流場影響不大。Ohta等[6]的數值模擬結果發現,置入支架后,動脈瘤內尤其是瘤頸處血液動態黏度明顯增加,易于形成血栓。但我們也應該看到,血管支架技術仍然是一個正在發展中的技術,還存在諸多待解決的問題,例如:支架植入后的血栓堵塞問題依然是影響后期通暢率的關鍵。植入支架后的患者需要在很長一段時間內服用抗血栓藥物,以抑制支架與血液成分的不良反應[7]。因此,支架的設計與選材就顯得尤為重要。
2 支架結構的設計
2.1 矩形截面網格狀支架的設計
自主設計的網格支架每一排梯形環狀支撐體為一個單元組,網格支架單元組之間由S型連接體連接,連接體沿支架周向均勻分布,使支架在不損失徑向支撐力情況下,能夠提供優良的軸向順應性;支架尺寸:網格狀矩形截面支架長0.12 mm,寬 0.09 mm,通透率 77%[8],見圖 1。
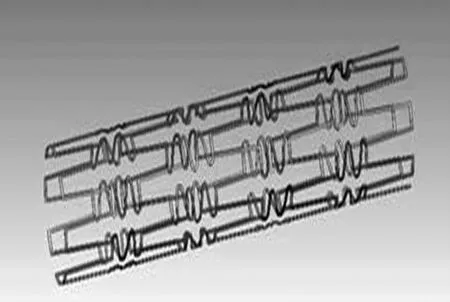
圖1 矩形截面網格狀支架Fig 1 Rectangular grid shaped stent
2.2 網絲編織成的圓形截面螺旋形支架的設計
圓形截面螺旋形支架也是在UG8.5中進行繪制的,是由4根金屬絲順時針旋繞,另4根金屬絲逆時針旋繞,8根金屬絲相互交織形成。螺旋狀圓形截面支架直徑 d取值為0.12 mm[9],通透率取為78%左右。繪制出圓形截面螺旋形支架見圖2。該支架在前期臨床上已經使用,術后血管易再狹窄。

圖2 圓形截面螺旋形支架Fig 2 Spiral shaped stent with circular
3 結構靜力學分析比較兩種支架的彎曲變形能力與扭轉變形能力
3.1 血管支架的彎曲變形能力
3.1.1 支架材料屬性的選取 支架材料大多使用不銹鋼或者鈦合金等,其中鈦合金的密度一般在4 500 kg/m3,僅為不銹鋼的60%左右,而且純金屬鈦的密度已經與普通不銹鋼的密度差不多,一些高強度的鈦合金甚至超過了許多不銹鋼的強度極限。因此,鈦合金的強度遠大于了其他金屬材料的強度,而且鈦合金的生物相容性比較好,可用于制造強度高、剛性良好、質量輕柔的部件。這些均符合血管支架的設計理念,所以,我們在本研究中采用鈦合金作為血管支架的材料,其楊氏模量取為110 GPa,泊松比為 0.45[10],密度取 4 500 kg/m3。
3.1.2 結構靜力學分析 將設計好的圓形橫截面積螺旋狀血管支架模型和矩形截面網格狀支架分別導入ANSYS結構靜力學模塊的Geometry中,在Engineering Data中設定支架的參數,采用自由劃分網格進行網格劃分。然后在Setup模塊中施加標準地球力,施加一端固定約束,再施加力載荷設為0.1N,最后受力分析求解。在Result中觀察支架彎曲總變形云圖,見圖3。
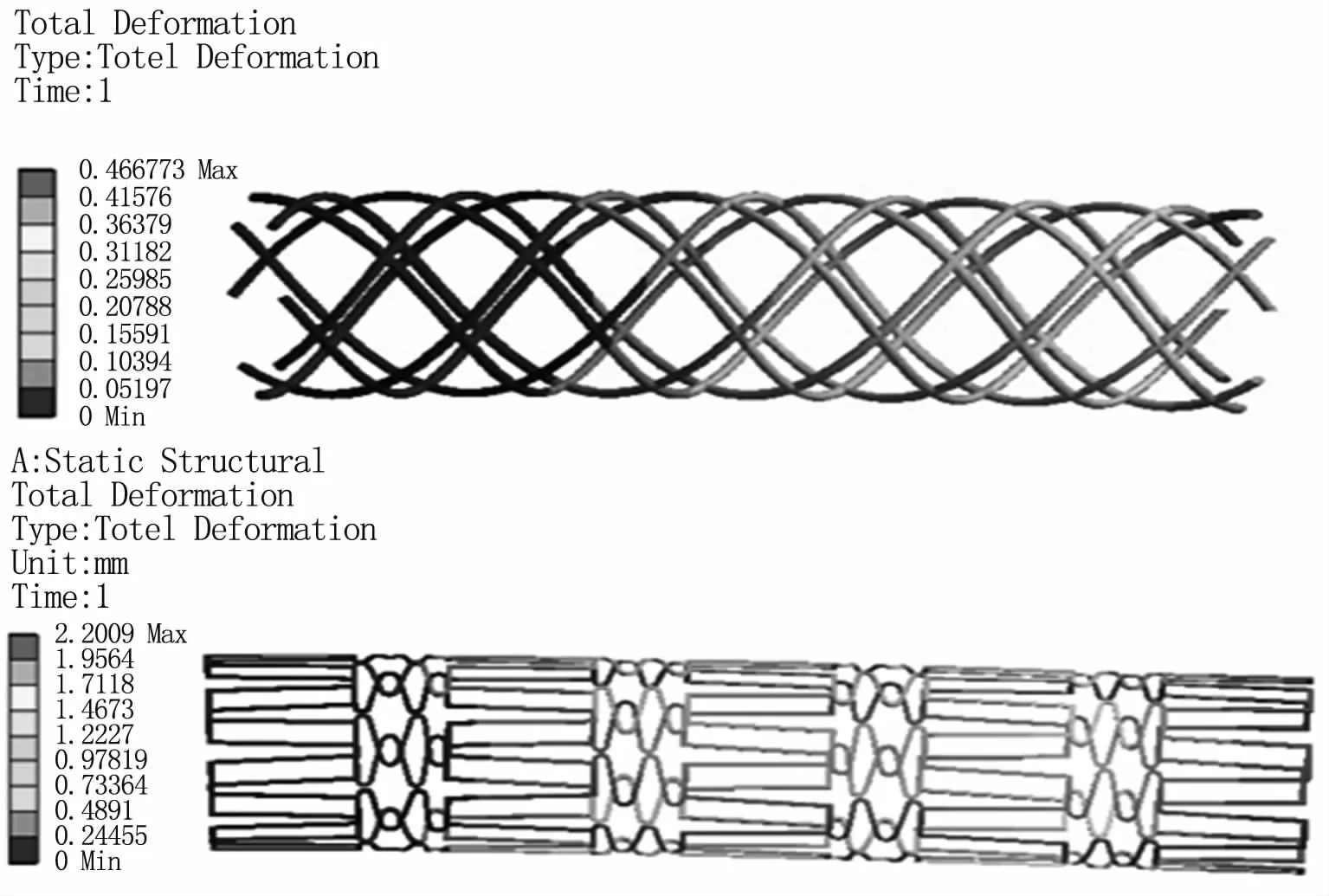
圖3 支架彎曲總變形云圖Fig 3 Total deformation of stent bending
根據以上兩個支架總變形云圖可以很直觀的發現這兩種支架彎曲變形能力有較大的差異,且網格狀支架的彎曲變形能力遠遠大于螺旋形支架。
3.2 血管支架的扭轉變形能力
因為我們研究的是扭轉變形能力,所以,此處采用懸臂梁一端固定后,另一端施加一個固定力偶矩的方法對血管支架扭轉能力進行分析研究。支架的材料屬性與上部分分析彎曲變形時采用相同的材料屬性。
3.2.1 結構靜力學分析 將設計好的螺旋狀血管支架模型和網格狀支架模型導入結構靜力學模塊的Geometry中,在Engineering Data中設定支架的各項參數,采用自由劃分網格進行網格劃分。然后在Setup模塊中施加標準地球力,施加一端固定約束,再施加力偶矩設為0.00004 N.m,最后受力分析求解。在結果中觀察兩種支架扭轉總變形云圖,見圖4。
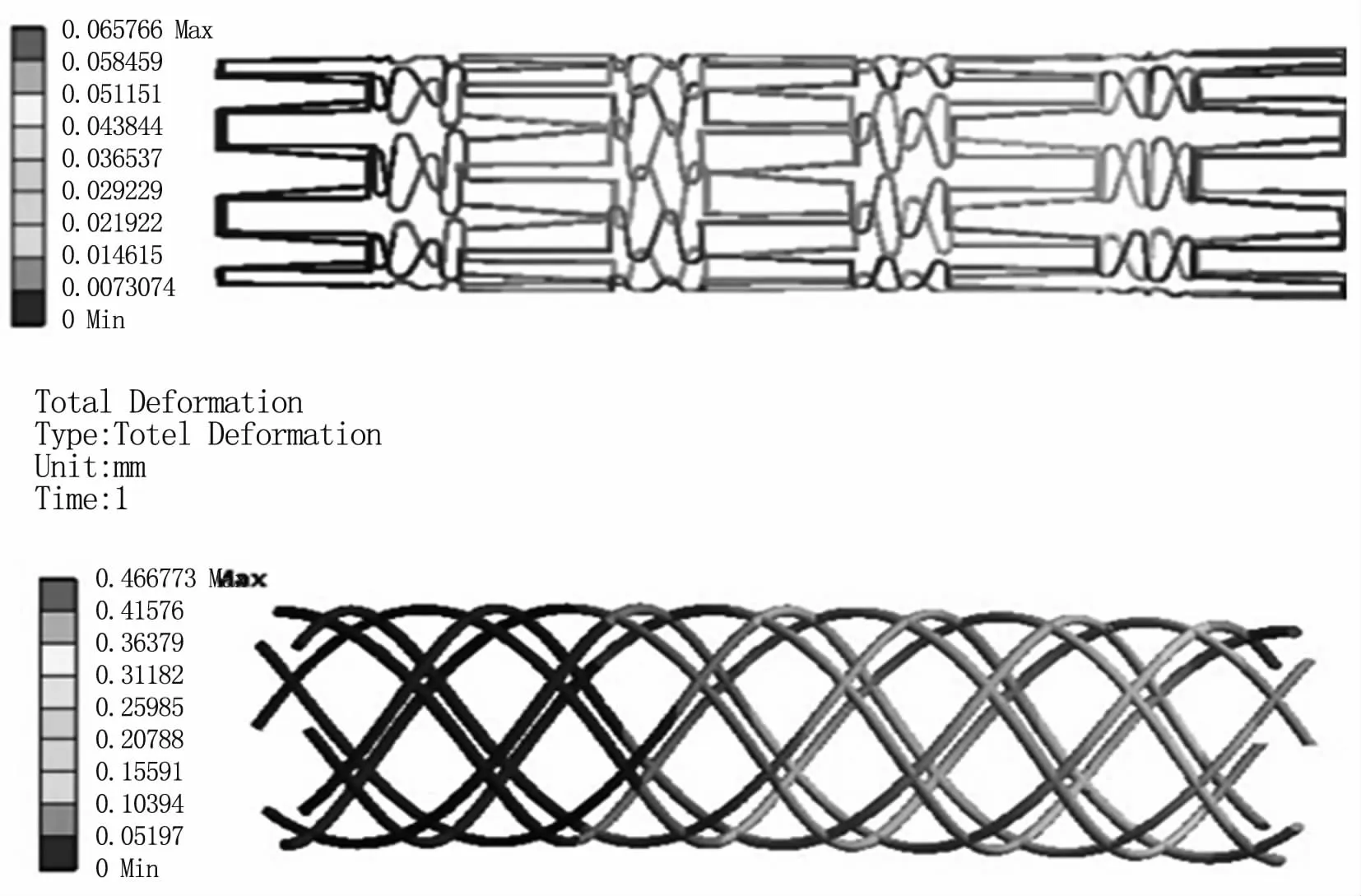
圖4 支架扭轉總變形云圖Fig 4 Total deformation of stent reverse
根據以上兩種支架的扭轉變形的比較,與彎曲變形相類似,很容易看出網格狀支架的扭轉變形能力也遠高于螺旋形支架,故網格支架有更強的順應變形能力。以下研究中選取網格支架植入真實腦動脈瘤分析其對動脈瘤血液動力學影響。
4 支架植入后對動脈瘤血液動力學影響分析
4.1 動脈瘤三維重建
依托于新疆醫科大學附屬醫院,針對此醫院收治的50例年齡在35~65歲之間的腦動脈瘤患者,進行腦部CT影像資料的采集。綜合50例動脈瘤的病發形態及位置因素,從中選取了一例形狀較為理想且有代表性的49歲女性患者的動脈瘤模型進行提取。對動脈瘤CT影像進行 calculate 3D frommask操作,生成三維圖并進行修建及光滑處理。使用Geomagic Studio 11.0逆向工程軟件對動脈瘤流場表面網格和動脈瘤壁表面網格進行優化處理,然后將STL與NURBS格式進行轉換,另存為STP格式輸出,分析結果對此類動脈瘤模型均實用,具有普遍實用性,見圖5。
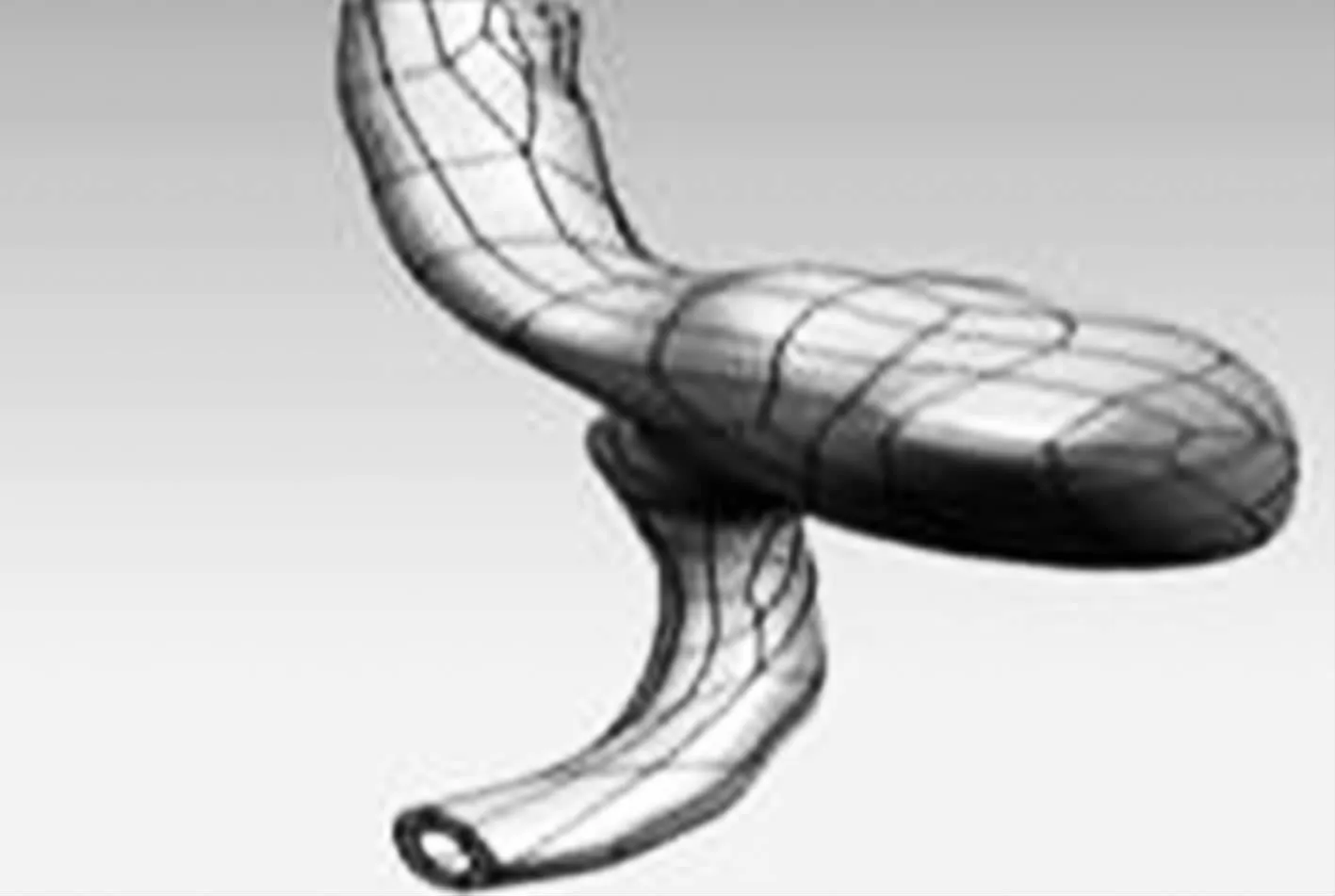
圖5 動脈瘤模型Fig 5 The model of aneurysm
4.2 腦動脈瘤流固耦合邊界條件設定
研究中將血液看作是不可壓縮的牛頓流體[11],密度為1 050 kg/m3,血液粘度設置為0.004 Pa.s。據相關文獻可以設定入口邊界為速度入口邊界,出口邊界為壓力出口邊界,其余為流-固耦合邊界。根據文獻[12]假設血流速度按正弦規律變化,其最大值取人體管徑動脈血流速度的平均值v=0.8 m/s-1。出口壓力設定為恒壓 0 pa[13]。為了簡化計算,可以假設動脈壁與瘤壁為線性、各向同性的彈性材料,計算時,設置血管壁的楊氏模量為1×108Pa[14],泊松比為 0.45[15],血管壁面設置無滑移條件(即壁面速度為0 m/s-1)。
4.3 仿真結果分析
如圖6所示,置入后對顱內動脈瘤血液流速并無太大的影響,因為置入前動脈瘤頂部的血液流動非常緩慢,而在支架置入后,該地方的血流速度幾乎完全停滯,所以無需另行計算血管支架置入后瘤頂部的速度值,但是瘤體內部還有漩渦出現,只是較置入血管支架前略大。

圖6 為支架置入前、后速度矢量圖Fig 6 Velocity vector before and after stenting
如圖7所示,未置入血管支架時腦動脈瘤瘤頸部位的壁面剪切力偏高,且最大壁面剪切力發生在動脈瘤頸口附近血液流入一側;置入血管支架后瘤頸遠側壁高剪切力區域(血流直接沖擊的部位)范圍明顯減小,動脈瘤頂部血液流動速度非常緩慢,壁面剪切力也隨之降低接近于零,且下降幅度極大。

圖7 支架置入前、后壁面剪切力Fig 7 The wall shear stress before and after stenting

圖8 支架置入前、后壁面壓力分布圖Fig 8 Pressure distribution before and after Stenting
圖8為血管支架置入前,由于載瘤動脈受到血液流動沖擊,所以入口處壁面壓力較大,瘤體表面壓力也隨之增大,血液流經瘤體后壁面壓力開始逐漸減小;置入血管支架后瘤體壁面壓力也無明顯變化,但是收縮峰期出現于瘤頸遠側壁的壓力梯度在血管支架植入后基本上消失。
5 結論
本研究對支架進行了結構靜力學分析,結果發現網格狀支架的變形能力(彎曲變形和扭轉變形)均高于螺旋狀支架,說明網格狀支架具有更好的順應性。如果置入復雜的動脈瘤中的話,網格狀支架要更具臨床意義。支架植入前由于二次流的存在,在血液直接沖擊到的瘤體下游附近彎曲部位或者形狀不規則的部位,壁面壓力和剪切力比其他部位要大一些,支架植入后瘤內血液流動速度、壁面剪切力及壁面壓力均相應減小,促進動脈瘤內部血栓的形成,降低動脈瘤破裂和血管再狹窄的風險。為臨床治療動脈瘤提供可靠的理論依據。

