3,5-二甲基苯酚的合成與應用
方東兵,馮柏成
(青島科技大學 化工學院,山東 青島 266042)
3,5-二甲基苯酚又名5-羥基間二甲苯,是一種重要的精細化工原料及有機合成中間體,其主要合成方法:①苯酚烷基化法[1],使用苯酚與甲醇為原料,通過高溫烷基化反應得到目的產物。該方法操作簡單,僅需一步反應即可完成,但是反應選擇性低,只有30%左右,且反應生成的副產物難以分離,因此該方法不能滿足實際生產應用的需要;②間二甲苯磺化堿熔法[2-3],這是3,5-二甲基苯酚的傳統生產方法。以間二甲苯為原料,經過磺化、堿熔以及酸化,得到最終產品。該方法用于生產3,5-二甲基苯酚收率可達到60%左右并且產品純度較高,但是工藝過程復雜,并且最大的問題在于反應過程的進行主要依賴強酸強堿的作用,對設備的腐蝕和環境的污染都十分嚴重,并不符合當前綠色化學的要求;③是異佛爾酮芳構化法[4],以異佛爾酮為原料,在高溫(350 ~400 ℃)下反應生成3,5-二甲基苯酚。該方法具有操作簡單的優點,但是由于異佛爾酮在高溫下會發生酚酮的重排[5],產物中除了3,5-二甲基苯酚和甲烷,還會有異佛爾酮的分解產物,比如均三甲苯、間甲酚、雙丙酮醇等。
3,5-二甲基苯酚作為重要的精細化工原料及有機合成中間體,主要有以下幾種重要的應用。①制備酚醛樹脂粘合劑和酚·脲·醛樹脂粘合劑[6-8],這種樹脂是不僅對木材同時也對玻璃、陶瓷、紙類、皮革和金屬等許多材料都有很好的粘合作用,是一種應用非常廣泛的樹脂粘合劑。②用于生產殺菌劑,消毒劑等產品[9],其中4-氯-3,5-二甲基苯酚就是較為重要的一種產品。這是一種具有獨特的殺菌性和防腐性,并能使兩種性能達到良好結合的消毒殺菌劑,被認為是高效、安全、廣譜的殺菌劑。③用于合成殺蟲劑[10],例如3,5-二甲基苯酚和氨基甲酸反應可以制得滅除威。滅除威是一種高效低毒的殺蟲劑,對高等動物毒性中等,對魚類毒性小,具有觸殺作用強,速效性強,殘效期短(只需要2 ~3 d)和藥效不易受溫度變化影響等優點,是當今應用相當廣泛的殺蟲劑之一。④用于合成維生素E[11]。3,5-二甲基苯酚作為合成保健品維生素E 的原料,近些年已經引起了人們越來越多的關注。用它合成的維生素E,就廣泛用于保健品、藥品、食品添加劑、化妝品及營養劑中。
本研究采用異丙基間二甲苯氧化分解法合成3,5-二甲基苯酚。該方法以工業上成熟的異丙苯法生產苯酚丙酮工藝為原型,首先通過反應原料間二甲苯與異丙醇的烷基化反應,得到5-異丙基間二甲苯,然后通過氧化酸解工藝得到3,5-二甲基苯酚和丙酮。
1 實驗部分
1.1 試劑與儀器
間二甲苯、異丙醇、三氯化鋁、偶氮二異丁腈(AIBN)、N-羥基鄰苯二甲亞酰胺(NHPI)、乙腈、濃硫酸、丙酮均為分析純。
精密增力電動攪拌器;恒溫油浴;高效液相色譜儀;DAD230 紫外檢測器;Varian 3800 氣相色譜儀;Bruker500M 型核磁共振儀。
1.2 實驗方法
1.2.1 烷基化 向帶有溫度計、回流冷凝管、滴液漏斗和攪拌裝置的250 mL 四口燒瓶中加入74.88 g間二甲苯,攪拌下加入13.34 g 三氯化鋁,用冰水降至10 ℃以下,慢慢滴加含異丙醇6.01 g 與間二甲苯10 g 的混合液,不斷攪拌,滴完繼續反應30 min,然后用恒溫油浴升溫至70 ℃反應7 h。反應結束后,水解,分液,取油相。將油相減壓精餾,得到產品9.83 g,收率為75%。其結構通過NMR 確認,純度通過氣相色譜分析,確定產品純度為90%。
1.2.2 氧化反應 向帶有溫度計、回流冷凝管和磁力攪拌裝置的250 mL 四口燒瓶中加入蒸餾得到的5-異丙基間二甲苯純凈物30 g,乙腈200 mL,攪拌下加入NHPI 3.26 g,AIBN 1 g,使其全部溶解。然后升溫至50 ℃,通入空氣,空氣流速為600 mL/min,不斷攪拌。反應過程中使用液相檢測,控制氧化反應深度為15%,反應16 h 后停止。將反應液減壓蒸餾,過濾,得反應液23 g。
1.2.3 酸解反應 向帶有溫度計、回流冷凝管和攪拌裝置的250 mL 四口燒瓶中加入氧化反應液20 g,攪拌下加入濃硫酸0.5 g、丙酮49.5 g 的混合溶液。然后將反應液升溫至50 ℃,不斷攪拌反應2 h。反應產物進行液相色譜分析并與標準品對照確定結構。
2 結果與討論
2.1 烷基化反應
間二甲苯與異丙醇的反應屬于傅-克烷基化反應,間二甲苯芳環上的氫原子被異丙基取代,而在逆向傅-克反應或者稱之為傅-克去烷基化反應過程中異丙基同樣可以在路易斯酸的存在下去除。本反應中,間二甲苯上甲基的存在提高了苯環的活性,使異丙基的烷基化更容易進行,同時由于甲基的定位效應,異丙基優先進入苯環上的鄰位或對位,生成4-異丙基間二甲苯。但是由于異丙基的空間位阻較大,間位產物比起鄰對位產物具有較小的空間位阻,因此熱力學控制該反應產生熱力學上更穩定的間位產物,最終在一系列烷基化與去烷基化共同作用的結果下,反應形成穩定產物5-異丙基間二甲苯。
2.1.1 催化劑對烷基化反應的影響 本實驗中分別實驗了三氯化鋁、三氯化鐵、濃硫酸、磷酸的催化效果。實驗結果見表1。

表1 催化劑對反應轉化率和選擇性的影響Table 1 The influence of catalyst on the reaction conversion and selectivity
由表1 可知,三氯化鐵以及濃磷酸對反應沒有明顯的催化效果。三氯化鋁以及濃硫酸的催化效果較好,原料的轉化率較高。但是濃硫酸作為催化劑,反應的選擇性較差,副產物較多,主產物的選擇性只有75%左右。而三氯化鋁選擇性可以達到90%,轉化率可達到75%以上。因此,選擇三氯化鋁作為該反應的催化劑是較為合適的。
2.1.2 反應溫度對烷基化反應的影響 反應溫度對烷基化反應有明顯影響。當溫度過高時,反應會生成包括4-異丙基間二甲苯在內的多種副產物。而當反應溫度過低時,反應速率較慢,反應所需時間大大延長。本實驗在40 ~100 ℃的范圍內分別選擇40,50,60,70,80 ℃進行考察,結果見圖1。

圖1 反應溫度與收率的關系Fig.1 The relation of reaction temperature and yield
由圖1 可知,在相同的反應時間內,40 ℃時產物的收率只有43%,隨著溫度的提高,產品的收率也在提高。在70 ℃時達到75%以上。繼續升高溫度,產品收率開始下降。這是由于過高的溫度導致了副反應的發生,雖然原料轉化率在提高,但是反應的選擇性在下降,最終導致了反應收率的下滑。結果表明,70 ℃是較好的反應溫度,此時反應的轉化率較高、選擇性較好。
2.1.3 反應時間對烷基化反應的影響 依前述所選出的最佳條件,在70 ℃下反應8 h,反應4 h 后每隔1 h 取樣進行分析,結果見圖2。
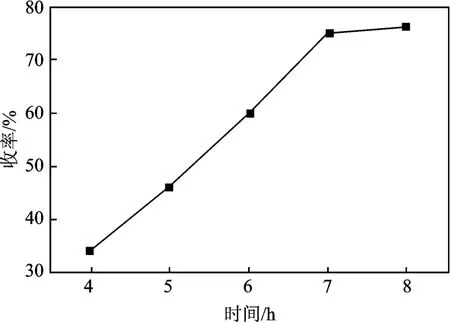
圖2 反應時間與收率的關系Fig.2 The relation of reaction time and yield
由圖2 可知,隨著反應時間的延長,產品收率逐漸提高,5 ~7 h 內收率提高較快,表明此時反應速度較快。反應至7 h 時收率達到75%。隨后反應速度開始減慢,收率變化較小。因此從反應效率的角度考慮,7 h 的反應時間是比較合適的。
2.2 氧化反應
5-異丙基間二甲苯的氧化反應是自由基引發的鏈式反應,其主要根據是該反應存在誘導期,若是存在能夠解離成自由基的物質,則氧化反應的反應速度會加快,反應時間會大大縮短;若是存在酚類等雜質,氧化反應的反應速度會減慢,甚至可能停止。此外,對于該氧化反應,當反應溫度較高或者反應時間較長時,會有醇類或酮類副產物的出現[12]。因此在反應過程中要嚴格控制反應時間和反應溫度,以此來達到控制氧化反應深度的目的,最終得到選擇性較好的目的產物。
2.2.1 引發劑的影響 自由基鏈式反應大致可分為三步:鏈的引發、鏈的增長以及鏈的終止[13]。其中鏈引發是控制反應時間的關鍵,選擇合適的引發劑可以大大的縮短鏈引發的時間,從而減少反應所需的時間。
根據文獻報道,選擇偶氮二異丁腈(AIBN)作為該反應的引發劑。考察了在50 ℃,空氣流量為600 mL/min的反應條件下,引發劑對反應的影響,結果見圖3。

圖3 引發劑對氧化反應收率的影響Fig.3 The influence of the initiator on the oxidation reaction yield
由圖3 可知,當沒有引發劑加入時,反應進行20 h 仍無過氧化物產生;而加入引發劑,4 h 后氧化反應就開始發生,過氧化物含量迅速增加,反應時間為12 h 時,反應轉化率達到10%。可以看出,引發劑的加入對加快反應速度有重要作用。因為自由基鏈式反應,其反應速度主要受鏈引發反應速率的影響,而引發反應的活化能很高,引發劑或催化劑的存在可以降低活化能,加快引發速度。偶氮類引發劑反應穩定,是一級反應[13],容易控制,對加快氧化反應有很好的作用。因此,選擇偶氮二異丁腈作為該反應的引發劑。
2.2.2 反應時間的影響 氣液兩相反應需要經過擴散和反應兩個階段來完成[14],所以需要一定的反應時間,如果反應時間不足,則氣液兩相沒有完全反應,反應物轉化率較低,如果反應時間過長,則會促進副反應的發生,雖然反應轉化率較高,但選擇性較差。

圖4 反應時間對氧化反應轉化率的影響Fig.4 The influence of reaction time on the oxidation reaction conversion
由圖4 可知,5-異丙基間二甲苯的轉化率是隨著反應時間的增加而增加的,從反應開始至20 h,反應速度較快,在反應時間超過20 h 之后反應速度有所下降,此時原料轉化率達20%以上,反應24 h,5-異丙基間二甲苯的轉化率達到25%以上;反應時間較短時,5-過氧化氫異丙基間二甲苯的選擇性較好,約為90%。隨著反應的進一步進行,選擇性逐漸下降,副反應增多。因此,為了得到較好的反應選擇性,就需要控制反應時間來控制反應的轉化率。研究發現,16 h 是原料轉化率和產物選擇性的較好契合點,是適當的反應時間,此時5-異丙基間二甲苯轉化率為15%左右,選擇性可以達到85%以上。
2.2.3 反應溫度的影響 反應溫度是影響氧化反應方向和氧化深度的重要因素。本研究中考察了40,50,60,70 ℃下反應的不同變化,見圖5。
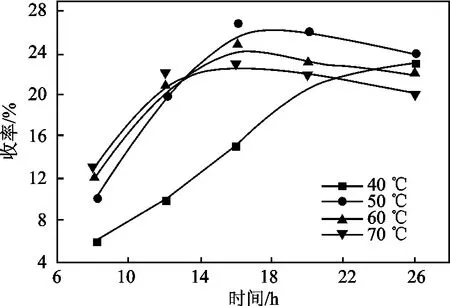
圖5 反應溫度與氧化反應收率的關系Fig.5 The relation of reaction temperature and yield
由圖5 可知,反應時間在12 h 以內,產品的收率隨著反應溫度的升高而增加,因為反應溫度越高,氧化反應越劇烈,氧化速度越快。但是當反應時間達到12 h 時,氧化反應情況出現分化,60,70 ℃下,產品收率開始下降,因為此時發生了氧化產物的熱分解反應,生成相應的芐醇和間二甲基苯乙酮等副產物,引起了產品收率的下降。40 ℃和50 ℃下,反應進行至16 h 時,產品收率也出現收率下降的情況。這說明,副反應開始的時間與反應溫度有關,溫度越高,副反應開始的也越早。另外,在反應過程中,當反應溫度較高時,溶劑乙腈會大量揮發,不利于反應溶劑的回收利用。當溫度較低時,氧化反應的速度較慢,在較長的反應時間內也無法達到理想狀態。因此總體來說,50 ℃是較為理想的反應溫度,在此溫度下,反應轉化率平穩上升,反應選擇性可以保持在85%以上。
2.3 酸解反應
過氧化氫物在酸催化條件下生成3,5-二甲基苯酚和丙酮,根據反應條件的變化,也有可能生成醇、烯等副產物。本實驗從反應溫度,催化劑用量,反應時間三個方面考察了各因素對酸解反應的影響之后得出:當溫度為50 ℃,催化劑濃硫酸用量為2.5%,硫酸丙酮溶液濃度為1%,反應時間2 h 時,3,5-二甲基苯酚的收率可達到80%。
3 結論
本論文通過異丙基間二甲苯氧化酸解法,使用間二甲苯與異丙醇為原料,實現3,5-二甲基苯酚的新法合成。其優化的合成工藝條件如下:①烷基化工藝條件:原料摩爾比n(間二甲苯)∶n(異丙醇)∶n(三氯化鋁)=8∶1∶1,反應溫度為70 ℃,反應時間為7 h,在此工藝下產品收率為75%,純度為90%;②氧化工藝條件:5-異丙基間二甲苯30 g,NHPI 3.26 g,AIBN 1.0 g,乙腈200 mL,空氣流速為600 mL/min,反應溫度50℃,反應時間16 h;③酸解工藝條件:氧化反應液20 g,濃硫酸與丙酮混合液50 g(濃硫酸質量分數為5%),反應溫度為50 ℃,反應時間為2 h。
3,5-二甲基苯酚作為重要的精細化工原料和有機合成中間體,其用途十分廣泛,市場需求量很大。而異丙基間二甲苯氧化分解法生產3,5-二甲基苯酚,是一種綠色安全的新型合成方法,其原料利用率高,對環境污染小,符合當前綠色化學的要求,是對已有合成工藝的有效補充。
[1] 于金剛.異佛爾酮催化芳構化法制備3,5-二甲基苯酚[D].天津:天津大學,2006.
[2] 章思規,章偉.精細化學品及中間體手冊(下卷)[M].北京:化學工業出版社,2000:1831.
[3] 徐克勛.精細有機化工原料及中間體手冊[M].2 版.北京:化學工業出版社,1999.
[4] Paul H,Berkeley,Seaver A.Production of phenolic compounds:US,2369196[P].1942-07-13.
[5] 金姬.間二異丙苯氧化合成間苯二酚[D].大連:大連理工大學,2010.
[6] Yomoto Masatoshi.Antimicrobial phenolic resin molding materical:JP,11189503[P].1999-07-13.
[7] Miyagl Sachiko,Maeda Toyohiko,Masuda Toru.New trisphenol compound:JP,10218815[P].1998-08-18.
[8] Mcallister L,Dietrich H.Fire retardant polymer resin:US,4471089[P].1984-09-11.
[9] 湯鳳,黃洪.3,5-二甲基苯酚的合成與分離[D].廣州:華南理工大學,2005:1-75.
[10]姜紅宇,張敏,湛雪輝.3,5-二甲基苯酚的新法合成[J].湖南科技學院學報,2009,29(12):42-44.
[11]洪記.維生素E 開發應用現狀及發展趨勢[J].江蘇化工,2000,28(6):7-10.
[12]劉佳.間二異丙苯氧化制備間苯二酚[D].北京:北京化工大學,2009.
[13] Eiichi Yonemitsu,Takeo Igarashi.Process for preparing hydroperoxide:US,4013725[P].1977-03-22.
[14]史福濤,陳標華.仲丁基苯氧化分解生產苯酚丁酮的研究[D].北京:北京化工大學,2011.

