人工胃腸液模型在藥物穩定性研究中的應用現狀
黃財順,李寶才,向 誠,2*
1昆明理工大學生命科學與技術學院,昆明 650500;2 北京大學天然藥物及仿生藥物國家重點實驗室,北京 100191
口服藥物吸收的主要場所是胃腸道,胃腸液的消化作用可能使藥物降解失活,所以進行胃腸道的穩定性研究具有一定的價值。人工胃腸液模型主要包括人工胃液和人工腸液孵育,制作簡單,操作簡便,有助于了解藥物在體內的穩定性情況,探討影響藥物穩定性的因素,有助于指導藥物結構優化和制劑的開發,已經被廣泛應用[1-7]。然而各家的實驗設計、考慮因素差異較大,例如人工胃液的作用時間少則5 min,多則可達24 h[10];人工腸液的作用時間少則10 min,多則可達24 h;是否需要邊孵化邊攪拌以模擬腸胃蠕動,也沒有統一;其他因素的設定也沒有統一規范,故本文對影響藥物在人工胃腸液中穩定性的主要因素、因素范圍及其分析方法進行了綜述,并提出包括時間、pH 值、酶濃度和攪拌速度在內的四因素析因設計的實驗方法,為更好地采用該模型進行研究提供參考依據。
1 人工胃腸液模型用于藥物穩定性研究的基本操作
《中國藥典》(2010 版)記載的人工胃腸液的配制方法為:稀鹽酸16.4 mL,加水約800 mL 與胃蛋白酶10 g,搖勻后,加水稀釋成1000 mL;人工腸液的配制方法為:取磷酸二氫鉀6.8 g,加水500 mL 使溶解,用0.1 mol/L 氫氧化鈉溶液調節pH 值至6.8,取胰酶10 g,加水量使溶解,將兩液混合后,加水稀釋至1000 mL 即得。
利用人工胃、腸液模型研究藥物的消化穩定性主要包括以下步驟:1、配制人工胃液和腸液;2、將待測藥物稀釋成一定濃度加入到配好的人工胃液和腸液中,并設計孵化溫度和時間,定時取出孵化液樣品;3、樣品經過處理后進行含量檢測,綜合分析后可知該藥物在胃腸道中的穩定性情況。
2 人工胃腸液模型的主要考察因素和實驗方法
影響藥物在人工胃、腸液中的穩定性的因素除了藥物本身性質以外主要還有五個,分別是1.胃、腸液的pH;2.胃、腸蛋白酶;3.胃腸道作用時間;4.胃腸道溫度;5.胃腸蠕動速度。
若想詳細認識藥物在胃、腸液中的穩定性情況,有必要規范操作對各因素做系統的分析。目前,大部分學者采用以下四種實驗設計的方法:簡單分析、單因子分析、雙因子分析、胃液-腸液整體分析的方法。
2.1 簡單分析
簡單分析是指直接用《中國藥典》規定的人工胃、腸液處理藥物,時間等因素不做考慮。例如尚曉婭等[6]用此類方法對抗性淀粉進行了體外穩定性研究;伍妍俊等[8]對甲基化EGCG 的合成及其在人工模擬胃、腸液中的穩定做了研究。以上研究均直觀地表明了藥物穩定性是否受人工胃、腸液的影響。該分析方法較簡單,以含量的變化為指標就能判斷藥物在消化模型中是否穩定,但不能分析原因。
2.2 單因子分析
單因子分析方法是目前采用較多的方法,多以胃腸道作用時間作為單因子,以一定的時間間隔點抽取反應產物進行分析。例如金暉等[9]探討南瓜多糖在人工胃液中的穩定性情況,經30、90、150、720 min 作用后,還原糖及分子量的變化表明南瓜多糖在人工胃液中隨時間的延長降解程度越大。周園等[10]對煙酰水楊酸在人工胃、腸液中10 min、30 min、1、2、3、4、5、6、10、18、24 h 分別取樣,結果顯示煙酰水楊酸在人工腸液中的降解程度較人工胃液的大,且隨作用時間延長降解率更高。冼小敏等[11]制備燕窩水提物,分別與等體積的人工胃、腸液混合,37 ℃消化,按時間梯度0、1、5、10、15、30、60 min 準確計時并終止反應,SDS-PAGE 凝膠電泳方法檢測燕窩蛋白質的降解情況,結果發現燕窩蛋白降解物沒有隨著反應時間的延長而增多。這類實驗設計可以得到消化時間對藥物穩定性的影響。
2.3 雙因子分析
雙因子分析方法是另外一種應用較廣泛的實驗設計方法:即以胃腸道消化酶和pH 作為雙因子,考察pH、消化酶和作用時間對藥物穩定性的影響。主要出現以下四種情況,統計結果見表1。
情況一:藥物在人工胃、腸液(酸堿環境+消化酶)和不含消化酶的人工胃、腸液NE(僅含酸堿環境)中均穩定,即可推斷該藥物可能耐受胃、腸液的酸堿環境和消化酶。陳國慶等[12]以此方法對四乙酰葛根素的穩定性進行研究,發現四乙酰葛根素在人工腸液和不含胰蛋白酶的人工腸液NE 中穩定性均很好,推斷四乙酰葛根素在人工腸液中穩定性較好,可開發腸溶制劑。
情況二:藥物在人工胃、腸液中不穩定,但在人工胃、腸液NE 中穩定性良好,即可推斷影響穩定性的最主要因素是胃、腸蛋白酶。榮娜娜等[13]以人工胃、腸液和不含蛋白酶的人工胃、腸液NE 處理燈盞花乙素,并間隔0.5 h 取樣,發現燈盞花乙素在人工胃液中不穩定,從0.5 h 到2.5 h 之間出現降解產物,在空白人工胃液NE 中沒有任何變化。據此推斷,胃蛋白酶是影響燈盞花乙素穩定性的主要因素。
情況三:藥物在人工胃、腸液和人工胃、腸液NE中均不穩定,且二者對藥物穩定性的影響基本相同,即可推斷影響穩定性的最主要因素是胃液pH。馬劍敏等[14]以此方法處理過辣根氧化物酶,并于不同時間點取樣,結果標準人工胃液與人工胃液NE 對HRP 穩定性的影響基本相同,反映出胃液pH 是影響HRP 穩定性的主要因素;汪景長等[15]研究超氧化物歧化酶在模擬胃腸道中穩定性時以同樣的方法反映出天然超氧化物歧化酶對胃蛋白酶具有較強的耐受力,對其穩定性最直接的影響可能是由胃酸造成的。
情況四:人工胃、腸液對藥物穩定性的影響比人工胃、腸液NE 的大,即可推斷胃、腸pH 及消化酶均對藥物穩定性有影響。葉盛英等[16]以此方法研究重組人表皮生長因子在人工胃液和腸液中的穩定性,發現人工胃、腸液和人工胃、腸液NE 對重組人表皮生長因子的穩定性均有影響,且酶存在時重組人表皮生長因子的降解更明顯,反映了胃、腸液pH和蛋白酶對重組人表皮生長因子的穩定性均有影響。米坤等[17]對芽孢桿菌纖溶酶進行穩定性的研究,發現芽孢桿菌纖溶酶在人工胃液和人工胃液NE中活性均下降,且在人工胃液中失活率更高,所以人工胃液的強酸性及胃蛋白酶的存在對芽孢桿菌纖溶酶的穩定性均有影響。
2.4 胃液-腸液整體分析
若需要更詳細了解藥物在整個胃腸道消化吸收中的穩定性,可使用人工胃液和人工腸液串聯式的研究方法,即將人工胃液處理后的產物轉移至人工腸液中繼續反應。例如王玉蓉等[18]在腸安康膠囊的體外釋藥考察研究中,將人工胃液處理后的腸安康膠囊轉移至人工腸液中,更準確得知藥物在人工胃液中1 h 后約釋放藥物17%左右,在人工腸液中5 h 后基本釋藥完全;Lee BJ 等[19]以同樣的方法,發現藥物在二者中的釋藥情況完全不一樣,藥物在胃液中釋放平穩,卻在腸液中線形釋放。McDougal GJ[20]、Kerstin F[21]等也有類似研究,較為完整系統地評價了藥物在消化過程中的穩定性,更有效地指導藥物制劑開發。
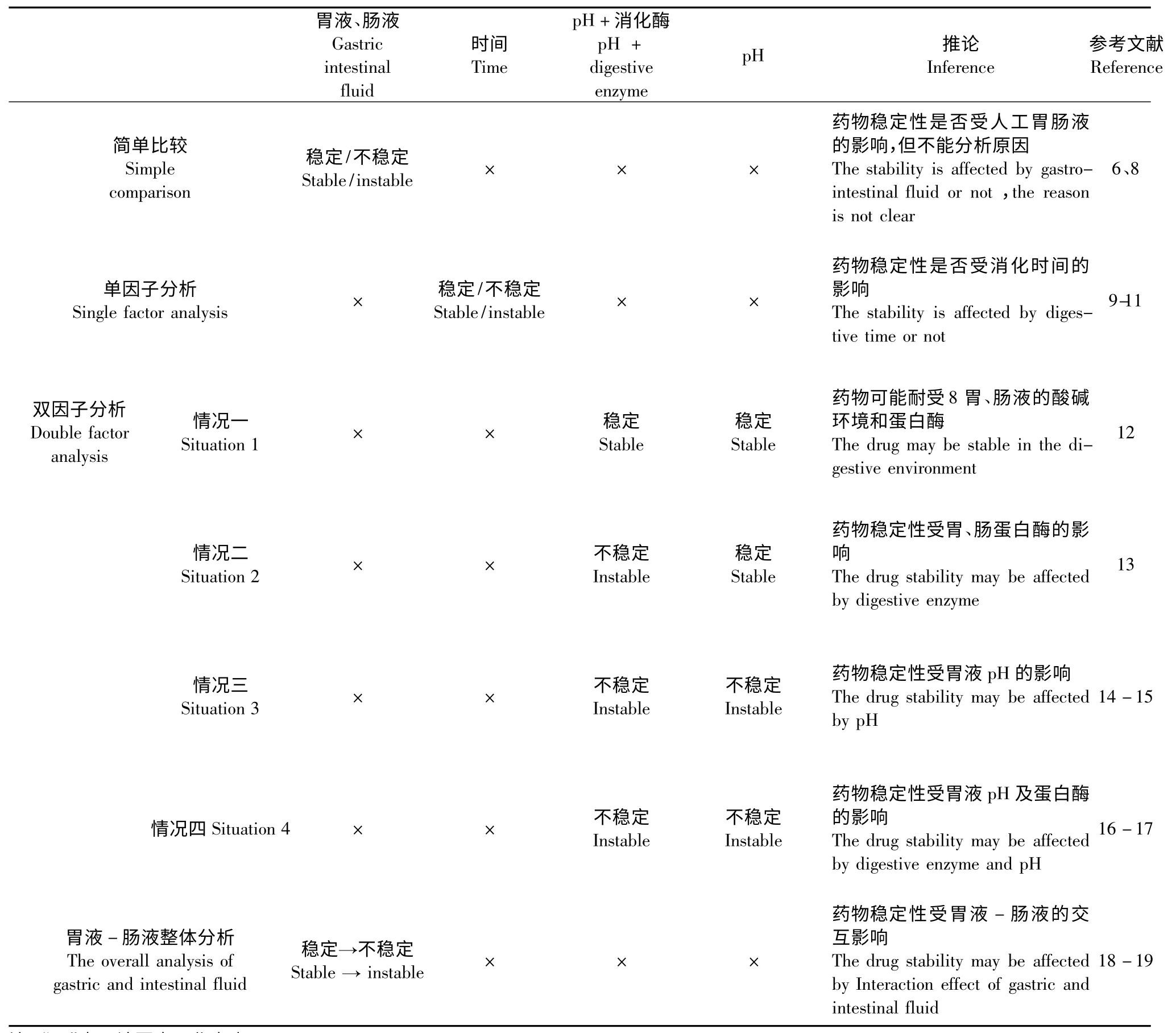
表1 常用的實驗設計方法Table 1 Commonly used experimental designs
3 人工胃腸液模型的應用
口服藥物在胃腸道中的穩定性將直接影響藥物的吸收。人工胃腸液模型在新藥開發中可針對上述影響因素,指導新藥或新劑型的開發,以提高藥物的穩定性,方法主要包括制備該藥物的前藥和改良劑型。除此以外,還可以對胃腸道內產生的代謝產物做簡單分析。
3.1 指導前藥的制備
通過藥物的穩定性研究,可以指導前藥的設計。胃液的強酸性環境是引起抗生素類藥物失效的主要因素,把它們制備成前藥是增強其穩定性的主要方法。例如紅霉素在酸性溶液中也容易分解失效,因此將紅霉素制成難溶性的酯[22]。除抗生素類藥物外,某些藥物也可以進行衍生化而提高其穩定性。伍妍俊等[8]研究甲基化的EGCG 在人工胃腸液中的穩定性,結果EGCG4dMe 由于甲基化,穩定性提高。
3.2 指導劑型的改良
通過藥物的穩定性研究,可針對性地對現有劑型進行改良,提高藥物的吸收率。若腸道環境是影響其穩定性的主要因素,那么可將其設計成胃滯留片,例如Wei ZP 等[23]設計了一種胃滯留片以提高藥物的穩定性。若胃腸道的作用時間是影響其穩定性的主要因素,那么可根據其起效的時間規律進行設計,例如茶堿在胃液中隨作用時間延長降解率升高,但茶堿需在夜間有一定的吸收才能有效治療疾病,因此Danckwerts MP 等[24]設計了一種三階段釋藥的緩釋片劑,該片劑能在腸液中穩定存在并持續釋放茶堿。若胃腸液pH 和消化酶是影響穩定性的主因,那么可將其進行包衣以抵御酸堿環境和消化酶,例如蛋白質類藥物易受胃腸道pH 和消化酶的影響,為解決這一問題,Nadia Rasool 等[25]用胰島素作為模式藥物,成功制備了能有效抵御胃液和消化酶的水凝膠包衣材料;Anal AK 等[26]以殼聚糖和藻酸鹽作為包衣材料,設計了一種能有效抵御胃酸和胃腸道消化酶的丸劑。
類似的針對影響因素,提高藥物的胃腸道穩定性的新劑型主要有環糊精包合物[27]、微球[28]、微乳[29]、腸溶劑[30]等。
3.3 代謝產物的檢測
胃腸道是藥物代謝轉化的重要場所,人工胃腸液作為模擬體內的體外模型,雖不能完全代表體內消化情況,卻也可能發生代謝反應,尤其是人工腸液。例如迷迭香酸在人工腸液中反應生成兩個代謝產物,應用液相LC-MS 技術鑒定為丹參素和咖啡酸[31]。但也有體內在腸道發生代謝反應,而在人工腸液中不發生代謝的情況[32],因為大部分藥物的代謝是由于腸內菌引起的[33,34],因此可考慮在人工腸液中加入腸內菌以更真實地模擬腸內代謝反應。
4 現行方法存在的不足
仔細分析藥物的胃腸道情況,方能正確指導制劑的開發,提高藥物的穩定性,但目前藥物在胃、腸液中穩定性因素的分析方法普遍存在以下四方面的不足:1.采用的單因子和雙因子分析方法不夠全面,沒有考慮因子間可能產生的先后交互作用,各因素可能以先后順序對藥物穩定性產生影響。例如汪景長等[35]發現天然結構的超氧化物歧化酶先經過胃液的酸化才能被消化酶降解,而傳統的分析方法只能得出影響因素是pH 和消化酶;2.胃腸道作用時間設計較隨意,沒有根據胃、腸的生理情況進行設計。綜述的文獻顯示:人工胃液的作用時間少則5 min,多則可達24 h;人工腸液的作用時間少則10 min,多則也可達24 h,而且部分時間的設計跨度較大,取樣點多,大大增加了工作量而無實際意義;3.大部分實驗沒有對胃、腸液pH 進行設計。正常情況下,人體胃液的pH 值范圍是1~4,空腹時胃液pH 值可為0.9~1.5,飲水或進食后可上升到3.0~5.0,這些范圍內的pH 值對某些藥物的穩定性產生的影響是不一樣的。例如張明等[36]用不同pH 的人工胃液處理非厭氧下HJ9211 凍干雙歧桿菌,結果表明雙歧桿菌在pH 為2~3 時失活率較接近,pH為1 時失活很明顯。4.傳統的分析方法沒能考慮胃腸道蠕動的情況。腸胃蠕動有助于磨碎食物并將其逐步向后推移,體外試驗雖難以實現,但簡單的震蕩攪拌也有很好的模擬效果,不同的攪拌速度可模擬腸胃的蠕動情況。因此,胃腸道蠕動也應作為考察因素,目前已有少數實驗將人工胃腸液結合攪拌更真實地模擬體內消化[37-39],只是設計有待改善。
5 展望
綜述各文獻后,本文認為可以采用析因設計[40]的實驗方法對影響藥物穩定性的四個主要因素進行分析。其優點是效率更高、可評估因子間的交互作用。除此以外,根據胃腸道的生理條件,小腸對藥物的吸收程度遠遠大于大腸,因此主要以小腸的生理條件為依據對消化液pH 值和消化時間[41,42]進行設計,調整攪拌器速度以模擬腸胃蠕動[37],方案見表2、3。若最后發現所研究藥物在腸液中不穩定,需要在胃液中提高吸收,可對人工胃液的作用時間進行調整,根據的是胃滯留片[43]的一般作用時間,可設為8、12、16、20、24 h。
本試驗涉及四個試驗因素:消化酶、時間、pH 和攪拌速度,觀察指標為降解率,可采用SPSS 軟件進行多因素方差分析,將四個因素對降解率影響的主次關系進行分析,可得到多個因素單獨作用和交互作用的信息。

表2 人工胃液中影響藥物降解的因素分析Table 2 The influence factors of gastric fluid in the drug degradation
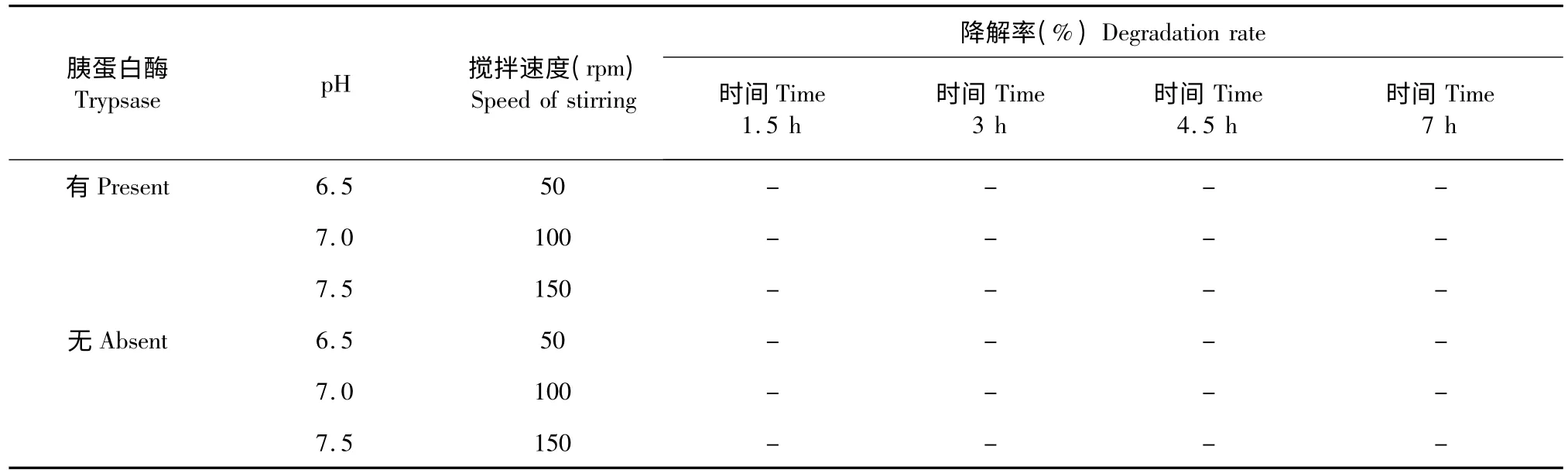
表3 人工腸液中影響藥物降解的因素分析Table 3 The influence factors of intestinal fluid in the drug degradation
長期以來,人工胃腸液模型主要用于藥物的穩定性研究,但本文認為其也可應用于中藥和天然產物活性成分的篩選。中藥和天然藥物多口服且成分復雜,一般而言,其在胃腸道穩定存在的成分才可能吸收入血、發揮藥效。篩選中藥和天然藥物中消化穩定的成分,將縮小研究范圍,再進行針對性分離、鑒定和活性篩選,將提高篩選的成功率。
1 Qiu S,et al.Effect of 1-MCP on quality and antioxidant capacity ofin vitrodigests from Sunrise'apples stored at different temperatures.Food Res Int,2009,42:337-342.
2 Biehler E,Bohn T.Methods for assessing aspects of carotenoid bioavailability.Curr Nutri Food Sci,2010,6:44-69.
3 Gil-Izquierdo A,et al.Influence of industrial processing on orange juice flavanone solubility and transformation to chalcones under gastrointestinal conditions.J Agric Food Chem,2003,51:3024-3028.
4 Bermúdez-Soto MJ,et al.Stability of polyphenols in chokeberry (Aronia melanocarpa)subjected to in vitro gastric and pancreatic digestion.Food Chem,2007,102:865-874.
5 Rufián-Henares JA,Morales FJ.Effect ofin vitroenzymatic digestion on antioxidant activity of coffee melanoidins and fractions.J Agric Food Chem,2007,55:10016-10021.
6 Shang XY(尚曉婭),et al.The digestion research of starchin vitro.Sci Technol Food Ind(食品工業科技),2007,5:218-220.
7 Hu SW,et al.Integrity and stability of oral liposomes containing bile salts studied in simulated and ex vivo gastrointestinal media.Int J Pharm,2013,441:693-700.
8 Wu YJ(伍妍俊),et al.Synthesis of methylated EGCG and its stability in artificial simulation gastric juice and artificial simulation intestinal juice.J Anhui Agric Univ(安徽農業大學學報),2010,37:688-691.
9 Jin H(金暉),et al.Pumpkin polysaccharidein vitrosimulator under artificial gastric juice.Food Sci Technol(食品科技),2012,37:178-181.
10 Zhou Y(周園),et al.Studies on the stability of nicotinyl salicylic acid in gastric juice,intestinal juice and plasmainvitro.J Shihezi Univ(石河子大學學報,自科版),2005,23:299-301.
11 Xian XM(冼小敏),et al.Study on degradation of protein of the edible birds nest (Aerodramus)in vitro.Chin Med Mat(中藥材),2010,33:1760-1763.
12 Chen GQ(陳國慶),et al.Stability research of tetraacetylpuerarin in artificial gastric juice and intestinal juice.Lishizhen Med Mater Med Res(時珍國醫國藥),2010,21:1709-1710.
13 Rong NN(榮娜娜),et al.Study the stability of Scutellarin on simulated gastric fluid and simulated intestinal fluid.J Yunnan Univ TCM(云南中醫學報),2011,34(5):30-33.
14 Ma JM(馬劍敏),et al.The stability of HRP in simulated conditions of human stomach and intestine.J Henan Norm Univ(河南師范大學學報,自然科學版),2002,12(5):28-29.
15 Wang JC(汪景長),et al.A study on stability of superoxide dismutasein simulated conditions of human stomach and intestines.J Shanghai Jiaotong Univ(上海交通大學學報),1995,29:153-157.
16 Ye SY(葉盛英),et al.Stability of recombinant human epidermal growth factor in artificial intestinal juice and gastric juice.Acade J Second Mil Med Univ(第二軍醫大學學報),2003,24:810-811.
17 Mi K(米坤),et al.Study on the stability of fibrinolytic enzyme from Bacillus.J Sichuan Univ,Nat Sci Ed(四川大學學報,自科版),2004,41:852-855.
18 Wang YR(王玉蓉),et al.Investigation of the drug release of pH-dependent Changankang capsulesin vitro.J Beijing Univ TCM(北京中醫藥大學學報),2004,27:36-38.
19 Lee BJ,et al.Biphasic release characteristics of dual drugloaded alginate beads.Arch Pharm Res,1998,21:645-650.
20 McDougall GJ,et al.Anthocyanins from red wine -Their stability under simulated gastrointestinal digestion.Phytochemistry,2005,2540-2548.
21 Kerstin F,et al.Stability of anthocyanin-rich W/O/W-emulsions designed for intestinal release in gastrointestinal environment.J Food Sci,2012,77:50-57.
22 Liu JP(劉建平).Biopharmaceutics and Pharmacokinetics(生物藥劑學與藥物動力學).Beijing:People’s Medical Publishing House,2011:39.
23 Wei ZP,et al.Design and evaluation of a two-layer floating tablet for gastric retention using cisapride as a model drug.Drug Dev Ind Pharm,2001,27:469-474.
24 Danckwerts MP.Optimization and development of a core-in-cup tablet for modulated release of theophylline in simulated gastrointestinal fluids.Drug Dev Ind Pharm,2000,26:767-772.
25 Rasool N,et al.Synthesis and characterization of novel pH-,ionic Strength and temperature-sensitive hydrogel for insulin delivery.Polymer,2010,51:1687-1693.
26 Anal AK,et al.Chitosan-alginate multilayer beads for gastric passage and controlled intestinal release of protein.Drug Dev Ind Pharm,2003,29:713-724.
27 He FC(何鳳慈),et al.Preparation of slowly released microspheres of dextro-ketoprofen-B-cyclodextrin inclusion.Acta Acade Med Milit Tertiae(第三軍醫大學學報),2004,26:1655-1657.
28 Zhang YH(張艷華),et al.Preparation andin vitroevaluation of chitosan microspheres containing matrine.Chin Hosp Pharm J(中國醫院藥學雜志),2006,26:307-310.
29 Attama AA,Nkemnele MO.In vitroevaluation of drug release from self micro-emulsifying drug delivery systems using a biodegradable homolipid fromCapra hircus.Int J Pharm,2005,304(1-2):4-10.
30 Qi XL(祁小樂),et al.Preparation of tablets containing enteric-coated diclofenac sodium pellets.Acta Pharm Sin(藥學學報),2008,43:97-101.
31 Sun SF(孫士豐).The metabolism research of the rosemary acid inSalvia miltiorrhiza.J Heilongjiang Univ TCM(黑龍江中醫藥大學),PhD.2008.
32 Li WL(李文蘭),et al.Metabolism of butylbenzyl phthalate in creatural organs.J Harbin Inst Technol(哈爾濱工業大學學報),2005,37:1674-1677.
33 Tang R(譚銳),et al.A comparative study of ephedra soup metabolism in the body.Chin Med Pharmacol Clinic(中藥藥理與臨床),2002,18(2):1-4.
34 Chen XM(陳新梅).Experimental study on metabolism and bio-transformation of ginsenoside Rgl by intestinal enzyme and microflora in rats.Chin J Exp Tradit Med Form(中國實驗方劑學雜志),2011,17:210-212.
35 Wang JC(汪景長),et al.A study on stability of superoxide dismutasein simulated conditions of human stomach and intestines.J Shanghai Jiaotong Univ(上海交通大學學報),1995,29:153-157.
36 Zhang M(張明),et al.Survival property of freeze-dried bifidobacterium HJ9211 in non-anaerobic condition.J East China Univ Sci Technol(華東理工大學學報),1999,25:36-38.
37 Song L(宋力),Ping QN(平其能).Study on the stability of 5-aminosalicylyl-glycine in the gastrointestinal tract.Chin J Biochem Pharm(中國生化藥物雜志),2003,24:294-296.
38 Peng Y,et al.A protease-resistant exo-polygalacturonase fromKlebsiellasp.Y1 with good activity and stability over a wide pH range in the digestive tract.Biores Technol,2012,123:171-176.
39 Bumsang K,Peppas NA.In vitrorelease behavior and stability of insulin in complexation hydrogels as oral drug delivery carriers.Int J Pharm,2003,266:29-37.
40 Berecz B,et al.Stability of sunflower 2S albumins and LTP to physiologically relevantin vitrogastrointestinal digestion.Food Chem,2013,138:2374-2381.
41 Fu YS(傅鈺生),et al.Design and analysis of experiments(實驗設計與分析).Beijing:Posts & Telecom Press,2008:152.
42 Graff J,et al.Grastrointestinal mean transit times in young and middle-aged healthy subjects.Clin Physiol,2001,21:253-259.
43 Shi XJ(施祥杰),Zhou JP(周建平).Current advances in gastro-retentive drug delivery system.Progr Pharm Sci(藥學進展),2010,34(2):55-60.

