甲型流感病毒M2e通用疫苗的研究進展
譚偉,謝芝勛
廣西壯族自治區獸醫研究所,廣西畜禽疫苗新技術重點實驗室,廣西 南寧 530001
流感病毒屬于正粘病毒科,根據其基質蛋白(matrix protein,M)和核蛋白(nucleoprotein,NP)的不同,流感病毒分為甲、乙、丙共3 型[1-2]。季節性流感主要由甲型流感病毒H1、H3 亞型及乙型流感病毒所引起,不同年齡段的人群都可感染,特別是老人、嬰幼兒、免疫功能有缺陷的病人及慢性病患者更易感且發病癥狀較重,全世界每年有25~50 萬人死于季節性流感[3-4]。人甲型流感病毒于1933 年首次分離成功[1],1945 年第一個商品化人用流感滅活疫苗在美國投放市場[5],不久又研制出流感病毒減毒活疫苗[1]。流感滅活疫苗通過肌肉內接種,主要誘導產生體液免疫;而流感病毒減毒活疫苗則經鼻腔內噴霧接種,同時誘導產生體液免疫和細胞免疫。
目前市場上的季節性流感疫苗包括人甲型流感病毒H1N1 亞型和H3N2 亞型的血凝素(haemagglutinin,HA)及乙型流感病毒的HA 三價苗[6],在北美地區和我國主要采用三價疫苗,但也有一些國家和地區使用單價苗。季節性流感疫苗具有高度特異性,即對相同亞型的流感毒株預防效果良好,而對不同亞型流感毒株的預防效果則不理想。由于流感病毒的HA 蛋白易于發生抗原變異[7],常會導致流感疫苗生產株與流行株的抗原性不一致,使疫苗起不到保護作用。生產季節性流感疫苗需要每年春季根據各地流感病毒流行株的監測數據和分析結果,預測在當年冬季可能出現的流感病毒流行株,并篩選出相應的流感毒株來制備疫苗。傳統的流感疫苗生產周期長、工藝復雜,且生產能力受不含特定病原體(specific-pathogen free,SPF)雞胚供應量的限制。此外,易感人群每年都要接種新的疫苗來預防季節性流感,且老年人的疫苗接種效果常欠佳[6]。流感滅活疫苗的免疫保護期短、不易刺激產生細胞免疫,無法預防流感病毒變異株引發的全球性流感。因此,人們期望能研發出一種流感通用疫苗來預防所有亞型流感病毒的感染,并解決上述一系列難題。我們將介紹基于M2e短肽的甲型流感病毒通用疫苗的研究進展。
1 甲型流感病毒通用疫苗的概念
目前廣泛使用的季節性流感疫苗主要預防H1、H3亞型的甲型流感病毒和乙型流感病毒的感染,而不能預防其他亞型的甲型流感病毒(如H5、H7和H9等亞型)的感染,因此,流感通用疫苗的理念應運而生[8-9]。甲型流感病毒通用疫苗利用不同亞型流感病毒含有的共同抗原表位誘導產生交叉免疫保護反應,來預防所有亞型流感病毒的感染。流感通用疫苗還可以避免每年篩選流感疫苗生產株的麻煩,降低疫苗的生產成本。
理想的甲型流感病毒通用疫苗應能誘導產生針對所有亞型流感病毒的保護性免疫,包括體液免疫和細胞免疫。因此,用于流感病毒通用疫苗的免疫原應含有能引起交叉保護反應的B 細胞和T 細胞抗原表位。目前用于甲型流感病毒通用疫苗研發的免疫原主要包括流感病毒的M2 離子通道蛋白、M2 蛋白的外膜區(M2e)、HA蛋白的莖部區、NP蛋白、酸性聚合酶(PA)和基質蛋白(M1)等[3],這些病毒蛋白含有相對保守的氨基酸序列,可以誘導產生交叉免疫保護反應。
1.1 M2e短肽流感通用疫苗的研究
M2e 短肽是流感病毒M2 蛋白暴露于外膜的部分。M2 蛋白最早是由Lamb 等于1981 年發現[10],它鑲嵌于流感病毒囊膜中,形成受pH 調控的質子通道,并參與病毒脫殼及新生病毒子粒的裝配和釋放過程[11-12]。起初研究者利用M2蛋白作為通用疫苗的免疫原[13],但M2是膜蛋白,由97個氨基酸殘基組成,相對分子質量較大,不易分離純化;而M2e短肽只有24 個氨基酸殘基,分子較小,溶于水并易于純化,因此M2e短肽更適合作為流感通用疫苗的免疫原。
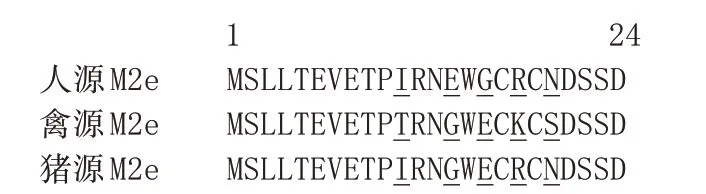
圖1 來源于人、禽和豬流感病毒的M2e短肽序列
M2蛋白的N端含有24個氨基酸殘基,暴露于病毒囊膜表面或感染細胞的表面,與新生病毒顆粒的裝配有關,被稱作M2e(圖1)[14];而M2 蛋白C 端的54個氨基酸殘基能與M1基質蛋白相互作用,影響病毒顆粒的裝配和釋放[14]。M2e 的氨基酸序列在人、禽和豬等甲型流感病毒中都很保守[1,15]。Liu 等分析比較了人、禽和豬流感病毒M2e短肽的氨基酸序列,發現人源與禽源流感病毒M2e 短肽有5 個氨基酸殘基不同,而人源與豬源流感病毒M2e 短肽僅有2 個殘基不同(圖1)[16-17]。M2e 短肽N 端的8 個氨基酸殘基(殘基2~9:SLLTEVET)在不同亞型的甲型流感病毒中的同源性超過99%,而在人甲型流感病毒中的保守性可達100%[15],因此針對人M2e 短肽的免疫血清能夠識別禽M2e的序列[18]。
M2e 短肽可誘導產生針對多種亞型流感病毒的抗體,因此M2e 是研發流感通用疫苗的首選免疫原之一。M2e短肽與適當的載體分子結合或與流感滅活疫苗同時使用,可以減輕流感癥狀,提高免疫動物抵抗流感病毒攻擊的能力,產生較好的交叉免疫保護[19]。動物試驗和人體臨床試驗的初步結果都顯示,M2e 流感通用疫苗安全、免疫原性好,且無明顯的副作用[2,20]。
1.2 M2e通用疫苗的免疫保護機制
目前關于流感病毒HA 蛋白中和抗體的免疫保護機制已研究得比較清楚,針對HA 蛋白的血凝抑制抗體可以有效地中和游離的流感病毒及與細胞結合的病毒,有效預防流感發生。針對神經氨酸酶(neuraminidase,NA)的抗體雖不具有直接中和流感病毒的作用,但它能夠抑制NA 蛋白的活性,使得新生病毒粒子在細胞表面聚集,降低感染細胞的排毒量[21]。針對流感病毒NP和M蛋白的T細胞免疫能幫助清除流感病毒感染的細胞[22]。
M2e 誘導產生的確切保護機制仍不明了[23]。雖然針對M2e 短肽的抗體不能中和流感病毒,但它可提供交叉保護免疫并減輕流感癥狀[23-24]。M2e 短肽和載體分子結合或與佐劑聯合使用,可以明顯抑制不同亞型流感病毒在細胞內的復制,降低流感病毒在肺組織中的滴度和感染動物的排毒量,提高免疫動物的存活率,而且這種保護作用還可以通過其免疫血清被動轉移給未經免疫的動物[8,25]。
目前普遍認為Fc 受體介導的巨噬細胞的吞噬作用、NK 細胞的直接殺傷作用、抗體依賴性細胞毒性、補體介導的細胞溶解等多種機制均可能與M2e通用疫苗的保護作用有關[1,18,26-28]。因此,進一步研究M2e 通用疫苗誘導免疫保護的機制,對弄清M2e 通用疫苗產生保護的途徑,建立評估M2e 通用疫苗效力的檢測方法,具有十分重要的意義。
2 M2e通用疫苗的特點及提高M2e通用疫苗免疫效果的方法
2.1 M2e通用疫苗的特點
盡管目前M2e 產生的免疫保護機制尚不清楚,但M2e 依然是一個頗具潛力的流感通用疫苗免疫原,理由主要如下:①M2e疫苗在動物實驗中具有良好的保護效果;②M2e 的氨基酸序列在絕大多數甲型流感病毒株中高度保守,自1933 年分離出流感病毒以來M2e 的序列幾乎未變,用其作為疫苗可避免常規流感疫苗只具有“毒株特異性免疫”的不足[15];③M2e 疫苗可誘導產生交叉保護免疫反應,減少疫苗生產對流感病毒流行株預測結果的依賴,提前生產儲備性疫苗預防突發性流感大流行;④M2e 大量存在于感染細胞的表面,容易被抗體識別[29];⑤M2e的分子小,易于體外大量表達、純化、制備;⑥M2e與適當的載體分子結合后,可大幅度提高其免疫原性及增強M2e疫苗的穩定性。
2.2 提高M2e通用疫苗免疫效果的方法
M2e 短肽的免疫原性不夠強[30],常需要加強免疫。為了克服這些不足,研究人員將不同的載體分子與M2e 短肽結合以增強M2e 短肽的免疫原性,提高M2e通用疫苗的免疫效果。目前常用的載體分子有乙型肝炎病毒核心蛋白(HBc)、人乳頭狀瘤病毒結構蛋白L1、鑰孔血藍素、腦膜炎奈瑟菌外膜復合體、脂質體及鞭毛蛋白等[2,4]。
2.2.1 M2e 四聚體通用疫苗 在流感病毒感染的細胞表面,M2 蛋白是以四聚體形式存在的,De Filette等發現針對M2 蛋白四聚體的抗體的保護效果明顯優于針對其單體的抗體[31]。將酵母轉錄激活蛋白GCN4(general control nondepressible 4)四聚體與M2e 融合可形成M2e-GCN4 四聚融合體,明顯提高M2e 短肽的免疫原性[31]。小鼠接種這種M2e-GCN4融合蛋白后,產生針對M2e的特異性抗體,即使小鼠在致死攻毒劑量情況下,100%被攻毒的小鼠均得到免疫保護而存活[31]。
2.2.2 M2e-病毒樣顆粒疫苗 病毒樣顆粒(viruslike particle,VLP)是指由病毒的結構蛋白自行裝配而成的、不具感染性、不能復制的病毒蛋白顆粒。通過VLP 表達的蛋白能保持蛋白的天然構象及活性,并具有多價、免疫原性強等特點[17]。VLP 能使大量相同的外源免疫原(例如M2e)在VLP 表面有序排列,從而大幅提高外源蛋白的免疫原性和穩定性,因此通過表達M2e-VLP 可提高M2e 的免疫原性。由于沒有流感病毒HA及NA這2種主要表面蛋白的遮蔽,并且M2e 短肽能以天然膜蛋白的形式充分暴露于VLP 表面,使M2e 便于被抗體識別。M2e-VLP 與流感滅活疫苗合用可提高M2e 誘導的交叉保護效果,抵抗不同亞型的甲型流感病毒(H1N1、H3N2 及H5N1)的攻擊,而且這種交叉保護作用可以經抗血清轉移給未被免疫的動物[19,32]。通過將M2e 與HBc的N 端融合,可產生M2e-HBc 融合蛋白。這種疫苗的免疫原性強,可大大降低流感病毒感染后的發病率,并提高小鼠攻毒后的存活率[8]。
2.2.3 M2e 多表位通用疫苗與佐劑聯合使用 含有多個M2e短肽的通用疫苗能誘導產生針對M2e的抗體[25],若將人源、禽源及豬源的M2e 短肽通過VLP 的形式同時表達,誘導產生的交叉保護反應更強,免疫保護持續的時間也更長[33-34]。將M2e 與HA2、NP 或M1 蛋白中保守的抗原表位共同表達,亦可提高M2e通用疫苗交叉保護的效果[35-36]。M2e 多表位疫苗與佐劑聯合也可提高M2e 通用疫苗的保護效果。將M2e-HBc 與黏膜佐劑CTA1-DD 聯合使用,通過鼻腔內接種,可誘導更強的免疫應答,使免疫動物獲得完全的保護[15,37]。目前用于流感通用疫苗研發的佐劑還包括革蘭陰性菌外膜鞭毛蛋白、MF59、CpG 寡核苷酸及免疫刺激復合物(immune stimulating complex,ISCOM)[35]。ISCOM 的特點是可以誘導產生體液和細胞免疫反應,降低疫苗使用量,且免疫力持續時間長。
3 M2e通用疫苗的試驗動物模型
M2e通用疫苗在小鼠、雪貂、豬和恒河猴中表現出了不同程度的保護效果[2,38]。小鼠不是流感病毒的天然宿主,本身對流感病毒不易感,若以小鼠為流感病毒的實驗動物模型,則需要產生能適應于小鼠組織的流感病毒株[39]。豬是甲型流感病毒的天然中間宿主,可被多種亞型的人或禽流感病毒感染,以豬作為流感病毒感染的動物模型可能要優于小鼠模型。雪貂對人流感病毒株易感,產生的流感癥狀與人流感相似,是流感病毒感染常用的動物模型[40]。恒河猴與人在免疫系統方面更相近,采用恒河猴作為流感病毒的感染模型所得到的結果可能與人體實驗結果更接近[20]。大動物模型是否比小動物模型能更客觀地反映M2e 通用疫苗的實際保護效果,值得進一步深入研究。
4 結語
動物實驗和人體臨床試驗都表明,M2e 流感通用疫苗安全,具有較好的免疫原性和交叉免疫保護效果,無明顯的副作用,顯示出其良好的發展前景。理想的M2e流感通用疫苗應能有效刺激產生體液和細胞免疫反應,抵御不同亞型流感病毒的感染[41],并具有保護效果好、免疫力持久、適用于不同年齡段的易感人群等特點。
深入探索M2e 的免疫保護機制,找出能反映M2e 通用疫苗免疫保護作用的免疫學及生物學指標,有助于建立有效評估M2e 疫苗免疫效果的方法。M2e 流感通用疫苗的近期發展目標,應以能降低流感病人死亡率、減輕流感的臨床癥狀、減少患者排毒量及控制病毒傳播為主;同時應探索M2e 通用疫苗和佐劑配合使用及疫苗接種的最佳途徑,進一步提高M2e疫苗的交叉免疫保護效果及免疫持續時間。而制備安全、高效和成本低的M2e通用疫苗,則是流感通用疫苗研發的最終目標之一。
[1]Kang S M,Song J M,Compans R W.Novel vaccines against influenza viruses[J].Virus Res,2011,162(1-2):31-38.
[2]Ebrahimi S M,Tebianian M.Influenza A viruses:why focusing on M2e-based universal vaccines[J].Virus Genes,2011,42(1):1-8.
[3]Subbarao K,Matsuoka Y.The prospects and challenges of universal vaccines for influenza[J].Trends Microbiol,2013,21(7):350-358.
[4]Lee Y T,Kim K H,Ko E J,et al.New vaccines against influenza virus[J].Clin Exp Vaccine Res,2014,3(1):12-28.
[5]Salk J E,Pearson H E,Brown P N,et al.Protective effect of vaccination against induced influenza B[J].J Clin Invest,1945,24(4):547-553.
[6]Krammer F,Palese P. Universal influenza virus vaccines:need for clinical trials[J].Nat Immunol,2014,15(1):3-5.
[7]譚偉,徐倩,謝芝勛.禽流感病毒研究概述[J].基因組學與應用生物學,2014,33(1):194-199.
[8]Neirynck S,Deroo T,Saelens X,et al.A universal influenza A vaccine based on the extracellular domain of the M2 protein[J].Nat Med,1999,5(10):1157-1163.
[9]Schotsaert M,De Filette M,Fiers W,et al.Universal M2 ectodomain-based influenza A vaccines:preclinical and clinical developments[J].Expert Rev Vaccines,2009,8(4):499-508.
[10]Lamb R A,Lai C J,Choppin P W.Sequences of mRNAs derived from genome RNA segment 7 of influenza virus:colinear and interrupted mRNAs code for overlapping proteins[J].Proc Natl Acad Sci USA,1981,78(7):4170-4174.
[11]Schnell J R,Chou J J.Structure and mechanism of the M2 proton channel of influenza A virus[J].Nature,2008,451(7178):591-595.
[12]Stouffer A L,Acharya R,Salom D,et al.Structural basis for the function and inhibition of an influenza virus proton channel[J].Nature,2008,451(7178):596-599.
[13]Slepushkin V A,Katz J M,Black R A,et al.Protection of mice against influenza A virus challenge by vaccination with baculovirus-expressed M2 protein[J].Vaccine,1995,13(15):1399-1402.
[14]Chen B J,Leser G P,Jackson D,et al.The influenza virus M2 protein cytoplasmic tail interacts with the M1 protein and influences virus assembly at the site of virus budding[J].J Virol,2008,82(20):10059-10070.
[15]Fiers W,De Filette M,Birkett A,et al.A "universal" human influenza A vaccine[J].Virus Res,2004,103(1-2):173-176.
[16]Liu W,Zou P,Ding J,et al.Sequence comparison between the extracellular domain of M2 protein human and avian influenza A virus provides new information for bivalent influenza vaccine design[J].Microbes Infect,2005,7(2):171-177.
[17]Kang S M,Kim M C,Compans R W.Virus-like particles as universal influenza vaccines[J].Expert Rev Vaccines,2012,11(8):995-1007.
[18]Fiers W,De Filette M,El Bakkouri K,et al.M2e-based universal influenza A vaccine[J].Vaccine,2009,27(45):6280-6283.
[19]Song J M,Van Rooijen N,Bozja J,et al.Vaccination inducing broad and improved cross protection against multiple subtypes of influenza A virus[J].Proc Natl Acad Sci USA,2011,108(2):757-761.
[20]Gilbert S C.Advances in the development of universal influenza vaccines[J].Influenza Other Respir Viruses,2013,7(5):750-758.
[21]Rebmann T,Zelicoff A.Vaccination against influenza:role and limitations in pandemic intervention plans[J].Expert Rev Vaccines,2012,11(8):1009-1019.
[22]Epstein S L,Kong W P,Misplon J A,et al.Protection against multiple influenza A subtypes by vaccination with highly conserved nucleoprotein[J].Vaccine,2005,23(46-47):5404-5410.
[23]Epstein S L,Price G E.Cross-protective immunity to influenza A viruses[J].Expert Rev Vaccines,2010,9(11):1325-1341.
[24]Zebedee S L,Lamb R A.Influenza A virus M2 protein:monoclonal antibody restriction of virus growth and detection of M2 in virions[J].J Virol,1988,62(8):2762-2772.
[25]De Filette M,Min Jou W,Birkett A,et al.Universal influenza A vaccine:optimization of M2-based constructs[J].Virology,2005,337(1):149-161.
[26]Jegerlehner A,Schmitz N,Storni T,et al.Influenza A vaccine based on the extracellular domain of M2:weak protection mediated via antibody-dependent NK cell activity[J].J Immunol,2004,172(9):5598-5605.
[27]El Bakkouri K,Descamps F,De Filette M,et al.Universal vaccine based on ectodomain of matrix protein 2 of influenza A:Fc receptors and alveolar macrophages mediate protection[J].J Immunol,2011,186(2):1022-1031.
[28]Huber V C,Lynch J M,Bucher D J,et al.Fc receptor-mediated phagocytosis makes a significant contribution to clearance of influenza virus infections[J].J Immunol,2001,166(12):7381-7388.
[29]Lamb R A,Zebedee S L,Richardson C D.Influenza virus M2 protein is an integral membrane protein expressed on the infected-cell surface[J].Cell,1985,40(3):627-633.
[30]Feng J,Zhang M,Mozdzanowska K,et al.Influenza A virus infection engenders a poor antibody response against the ectodomain of matrix protein 2[J].Virol J,2006,3:102.
[31]De Filette M,Martens W,Roose K,et al.An influenza A vaccine based on tetrameric ectodomain of matrix protein 2[J].J Biol Chem,2008,283(17):11382-11387.
[32]Wang B Z,Gill H S,Kang S M,et al.Enhanced influenza virus-like particle vaccines containing the extracellular domain of matrix protein 2 and a Toll-like receptor ligand[J].Clin Vaccine Immunol,2012,19(8):1119-1125.
[33]Kim M C,Song J M,O E,et al.Virus-like particles containing multiple M2 extracellular domains confer improved crossprotection against various subtypes of influenza virus[J].Mol Ther,2013,21(2):485-492.
[34]Kim M C,Lee J S,Kwon Y M,et al.Multiple heterologous M2 extracellular domains presented on virus-like particles confer broader and stronger M2 immunity than live influenza A virus infection[J].Antiviral Res,2013,99(3):328-335.
[35]張立霞,周劍芳,舒躍龍,等.通用型流感疫苗的研究進展[J].病毒學報,2014,30(1):73-78.
[36]Rudolph W,Ben-Yedidia T.A universal influenza vaccine:where are we in the pursuit of this "Holy Grail"[J]? Hum Vaccin,2011,7(1):10-11.
[37]De Filette M,Ramne A,Birkett A,et al.The universal influenza vaccine M2e-HBc administered intranasally in combina-tion with the adjuvant CTA1-DD provides complete protection[J].Vaccine,2006,24(5):544-551.
[38]Fan J,Liang X,Horton M S,et al.Preclinical study of influenza virus A M2 peptide conjugate vaccines in mice,ferrets,and rhesus monkeys[J].Vaccine,2004,22(23-24):2993-3003.
[39]Bodewes R,Rimmelzwaan G F,Osterhaus A D.Animal models for the preclinical evaluation of candidate influenza vaccines[J].Expert Rev Vaccines,2010,9(1):59-72.
[40]Smith H,Sweet C.Lessons for human influenza from pathogenicity studies with ferrets[J].Rev Infect Dis,1998,10(1):56-75.
[41]Ben-Yedidia T,Arnon R.Epitope-based vaccine against influenza[J].Expert Rev Vaccines,2007,6(6):939-948.

