新診2型糖尿病患者血清缺血修飾蛋白與糖化血紅蛋白相關性分析
王邦瓊,張先祥,羅 涌
(重慶三峽中心醫院內分泌科,重慶萬州404000)
慢性高血糖的毒性作用可通過晚期糖化終產物的蓄積,毛細血管基底膜成分的改變,氧化應激反應,炎性反應等導致糖尿病性微血管病變、大血管病變的發生[1]。糖化血紅蛋白(glycosylated hemoglobin,HbA1c)是國際公認的衡量血糖控制水平的重要指標,且是控制及預防糖尿病并發癥的評價指標[2]。缺血修飾蛋白(ischemia modified albumin,IMA)是近年來發現的早期診斷急性心肌缺血的指標之一[3]。研究發現與健康人相比,2型糖尿病(T2DM)患者IMA水平顯著升高,且與血糖控制水平顯著相關[4]。本文就新診T2DM人群HbA1c與IMA的相關性及其影響因素進行研究,現報道如下。
1 資料與方法
1.1 一般資料 收集本院新診T2DM患者124例,其中男80例,女44例,年齡44~74歲,平均(60.3±11.3)歲。T2DM診斷采用1999年WHO推薦的標準。排除標準:目前處于治療期的急慢性感染、手術、嚴重全身性疾病、外傷、孕婦和哺乳期婦女、3個月內使用過激素等影響糖脂代謝的藥物,伴隨糖尿病嚴重并發癥等。研究對象IMA水平為(11.65~94.5)u/mL,HbA1c為(6.7~14.7)%。以體質量指數(BMI)為25kg/m2為界點,BMI<25kg/m2為非肥胖組,BMI≥25kg/m2為肥胖組。兩組間年齡、性別比率、HbA1c、空腹血糖(FBG)、空腹胰島素(Fins)、總膽固醇(TC)、低密度脂蛋白膽固醇(LDLC)、高密度脂蛋白膽固醇(HDL-C)差異無統計學意義(P>0.05)。所有研究對象均簽署知情同意書,經醫院倫理委員會通過批準。
1.2 方法
1.2.1 資料收集 所有受試者由專業人員進行問卷調查及體檢。收集研究對象現病史、既往史、個人史、家族史,飲食習慣及生活方式等,包括吸煙,飲酒及運動。空腹狀態下測身高(m)、體質量(kg)、腰圍(WC,cm)及血壓(mm Hg)。以實測體質量(kg)/身高2(m2)計算BMI。
1.2.2 生化指標測定 所有受試者均清晨空腹采集靜脈血樣。應用葡萄糖氧化酶法測FBG;高效液相色譜法測定HbA1c;酶學法測定血清TC、三酰甘油(TG)、HDL-C及LDLC;化學發光法測定Fins;比色法測定IMA。上述檢測均有本院生化科及核醫學科完成。
1.3 統計學處理 采用SPSS13.0統計軟件進行分析。計量資料以表示,計數資料以率表示。偏態變量(TG、Fins、FBG)均作自然對數轉換后分析。兩組間均數比較采用兩獨立樣本t檢驗,兩樣本率間的比較用χ2檢驗。Pearson相關及Partial相關分析IMA與HbA1c的簡單相關性。多元回歸分析HbA1c對IMA水平的影響程度。以P<0.05為差異有統計學意義。
2 結 果
2.1 IMA與各代謝指標簡單相關性分析 IMA與BMI、WC、HbA1c、FBG 正相關(r=0.62、0.55、0.72、0.53,P<0.01)。校正性別、年齡和BMI后,Partial相關分析示IMA仍然與 HbA1c顯著正相關(r=0.64,P<0.01),見表1。
2.2 多元線性回歸分析IMA與HbA1c的相關性 以IMA為應變量,以年齡、性別、BMI、HbA1c、FBG、血脂為自變量,采用逐步回歸分析各指標對IMA的影響,分析發現僅HbA1c進入回歸方程(P<0.01),Y=-47.5+1.81a,其中 Y代表IMA,a代表 HbA1c(%)。
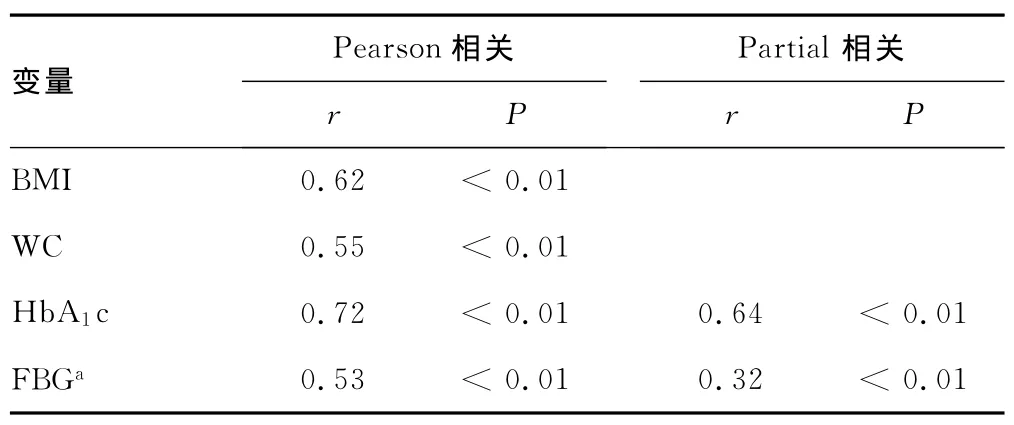
表1 IMA與各代謝簡單相關性
3 討 論
本研究發現,在新診T2DM人群中,肥胖組血清IMA水平明顯高于非肥胖組。IMA與BMI、FBG及HbA1c均正相關,但多元逐步回歸分析中,僅HbA1c進入線性方程,提示在T2DM人群中,IMA水平主要受慢性高血糖狀態影響。
IMA也稱鈷結合清蛋白,其形成機制尚無定論,可能為缺血時局部細胞因血流灌注不足而發生低氧、酸中毒、自由基損傷、細胞膜鈉鈣泵破壞致使游離鈷離子從循環蛋白的金屬結合位點釋放,鈷離子增加,與經修飾的清蛋白結合形成IMA[5]。IMA是急性心肌缺血的早期診斷指標,具有較高的靈敏度[6]。但進一步研究發現,IMA在心肌缺血方面并無高度的組織及臨床特異性,在非心源性缺血時IMA水平也會升高[7]。Pi-wowar等[4]研究發現,與健康人相比糖尿病患者呈現出較高的IMA水平,同時也報道了IMA和調節血糖水平之間有顯著相關性。但也有學者報道,T2DM患者在發生血管并發癥前IMA水平不受影響,與HbA1c之間無顯著相關性[8]。本研究以新診T2DM患者為研究對象,同樣發現IMA水平與慢性高血糖或血糖控制水平顯著正相關,IMA水平主要受HbA1c影響。
IMA作為氧化應激產物,與慢性炎性反應密切相關[9]。本研究發現,IMA與肥胖相關指標如BMI、WC顯著正相關。肥胖可引起慢性輕度炎癥[10],伴隨多種炎癥因子如C反應蛋白,IL-6、TNF-α及各種脂肪因子的升高。同時肥胖人群局部脂肪組織處于缺氧狀態[10]。炎性狀態和缺氧均可誘發氧化應激而致IMA升高[9]。T2DM患者多伴有肥胖或內臟脂肪增多,這可能與其IMA升高相關。但本文同樣發現,BMI并不為IMA的獨立影響因素。因此筆者提出,肥胖為T2DM患者IMA升高的協同因素。
本研究發現,FPG雖與IMA正相關,但卻不是其獨立影響因素。代表血糖控制水平或慢性高血糖狀態的指標HbA1c為IMA的主要影響因素。糖尿病以慢性高血糖為特征,而高血糖被認為是引起糖尿病并發癥的主要病理因素。高血糖可通過多種途徑引起組織的氧化應激升高,其中一個重要途徑是血糖生物氧化時經線粒體電子傳遞鏈過度產生超氧根陰離子[11-12]。因此,糖尿病患者往往伴有廣泛的自由基升高和抗氧化防御機制受損。并有學者發現,糖尿病患者存在血清Cu2+增高[13]。上述自由基及鈷離子的增高,可使人血清蛋白發生化學修飾作用,導致lMA水平升高。慢性高血糖還可通過誘發氧化應激、炎性反應、內皮細胞損害等誘發大血管病變和微血管病變。有研究發現存在糖尿病視網膜病變或糖尿病腎病患者其血清IMA水平較對照組升高,支持上述結果。但是本文僅以初發T2DM患者為研究對象,存在一定局限性。
綜上所述,T2DM患者HbA1c為血清IMA水平的主要影響因素。IMA在一定程度上可反應血糖控制水平,或許可作為T2DM患者慢性高血糖氧化應激產物,可代表廣泛內皮功能障礙、低度炎癥及未來可能發生血管病變的標志物,但上述推測還有待于進一步研究。
[1]李幼陽,李江源.慢性高血糖的毒性作用[J].中國醫刊,2004,39(9):9-12.
[2]潘長玉.2型糖尿病血糖控制的意義及實踐[J].國外醫學內分泌分冊,2003,23(4):228-229.
[3]Bar-Or D,Lau E,Rao N,et al.Reduction in cobalt binding capacity of human albumin With myocardial ischemica[J].Ann Emerg Med,1999,34(4Suppl):s56.
[4]Piwowar A,Knapik-kordecka M,Warwas M.Ischemiamodified albumin level in type 2diabetes mellitus-Preliminary report[J].Dismarkers,2008,24(6):311-317.
[5]Gutierrez-Correa J,Stopoani AO.Inactivation of yeast glutathione reductase hy Fenton systems:effect of metal chelators,catecholamines and thiol compounds[J].Free Radic Res,1997,27(6):543-555.
[6]Collinson PO,Gaze DC.Biomarkers of Cardiovascular Damage[J].Med Princ Pract,2007,16(4):247-261.
[7]Borderie D,Allanore Y,Meune C,et al.High ischemiamodified albumin concentration reflects oxidative stress but not myocardial involvement in systemic sclerosis[J].Clin Chem,2004,50(11):2190-2193.
[8]Dahiya K,Aggarwal K,Seth S,et al.Type 2diabetes mellitus without vascular complications and ischemia modified albumin[J].Clin Lab,2010,56(5/6):197-190.
[9]Ukinc K,Eminagaoglu S,Ersoz HO,et al.A novel indicator of widespread endothelial damage and ischemia in diabetic patients:ischemia-modified albumin [J].Endocrine,2009,36(3):425-432.
[10]龐璨,賈偉平.肥胖與慢性炎癥的研究[J].中國細胞生物學學報,2011,33(3):297-305.
[11]Rolo AP,Palmeira CM.Diabetes and mitochondrial function:role of hyperglycemia and oxidative stress[J].Toxicol Appl Pharmacol,2006,212(20):167-178.
[12]Aronson D.Hyperglycemia and the pathobiology of diabetic complication [J].Adv Cardiol,2008,45:1-16.
[13]張濤,劉義.糖尿病微血管病變與微量元素鋅銅的相關性[J].微量元素與健康研究,2005,22(2):50-52.

