蒙特卡洛模擬優化鮑曼不動桿菌感染的治療方案
劉佳,許建國,陸強 (江蘇省蘇北人民醫院藥劑科,江蘇 揚州 225001)
鮑曼不動桿菌是不發酵糖的革蘭陰性桿菌,具有強大的獲得耐藥性和克隆傳播的能力,多重耐藥(multi-drug resistance,MDR)、廣泛耐藥(Extensively-drug resistence,XDR)、全耐藥鮑曼不動桿菌(Pan-drug resisitence,PDR)呈世界性流行[1],已成為我國院內感染最重要的病原菌之一。2010年中國CHINET監測數據顯示不動桿菌對頭孢哌酮/舒巴坦耐藥率為30.7%、米諾環素為31.2%,其他大多數抗菌藥物的耐藥率均在50%以上。2011年“中國鮑曼不動桿菌感染診治和防控專家共識”提出了國內針對鮑曼不動桿菌感染的治療首選頭孢哌酮舒巴坦,并根據藥動/藥效學(pharmacokinetics/pharmacodynamics,PK/PD)理論制定合理給藥方案。單純的耐藥監測無法了解藥物的劑量時間效應關系,所以優化抗生素治療的策略,對改善致病的微生物學結局和防止細菌耐藥非常關鍵[2]。
藥物臨床研究的計算機模擬,是近年來興起的一門交叉學科,運用計算機模擬技術,可以揭示設計中變量和假設對結果的影響,預測和評價不同研究方案可能產生的結果,為制訂研究方案提供客觀令人信服的證據。美國FDA提倡用電腦模擬方法來制定臨床的給藥方案,蒙特卡洛模擬法(Monte Carleo simulation,MCS)在化學及多種自然科學中應用廣泛[3-4],在抗菌藥物的臨床研究中,可用其模擬PK/PD模型優化給藥方案[5-8]。以下以此評價頭孢哌酮/舒巴坦對鮑曼不動桿菌感染的給藥方案,為臨床用藥提供科學的客觀依據。
1 材料與方法
1.1 細菌耐藥監測 頭孢哌酮舒巴坦(2∶1)對于鮑曼不動桿菌的最低抑菌濃度(MIC)和耐藥率、敏感率分布數據引自2005年中國十五家教學醫院的耐藥性分析[9]和2010年CHINET中國鮑曼不動桿菌耐藥性監測[10]。頭孢哌酮舒巴坦對鮑曼不動桿菌的 MIC和耐藥率數據:MIC5016μg·mL-1,MIC9064 μg·mL-1,R為30.7%。
1.2 給藥方案 2011年中國鮑曼不動桿菌專家共識中提出,對于一般感染,舒巴坦的常用劑量不超過4.0g·d-1,對 MDRAB、XDRAB、PDRAB感染國外推薦可增加至6.0g·d-1,甚至8.0g·d-1,分3~4次給藥[2]。由以上的給藥方案,對于頭孢哌酮舒巴坦(2∶1)給出4種給藥方案,3 g/q6 h ivd;3 g/q8 h ivd;6 g/q6 h ivd;6 g/q8 h ivd。
1.3 藥動/藥效學模型 抗菌藥物可分成時間依賴性和濃度依賴性兩類。前者的殺菌速率與游離藥物濃度超過MIC的時間密切相關,其PK/PD指數是血藥濃度大于MIC的時間間期與給藥間期之比(f%T> MIC,即藥物濃度超過MIC的時間占給藥間隔的百分率;后者的PK/PD指標是峰濃度Cmax或藥時曲線下的面積與MIC的比值,即Cmax/MIC和AUC/MIC。頭孢菌素類抗生素為時間依賴性,體外實驗和動物實驗表明頭孢菌素/單環類抗菌藥物的f%T>MIC大于40%,就可以達到較好的殺菌作用[8]。因為MIC是體外條件下測定游離藥物的濃度,而藥動學往往是測定總血漿的藥物濃度,只有未與蛋白結合的游離藥物才具有抗菌活性。因此用血漿蛋白結合率(protein bounding,PBs)將總血藥濃度轉化成游離濃度,以前綴f(fraction of drug,游離分數f=l-PBs)來表示。按一室模型處理時[11]:
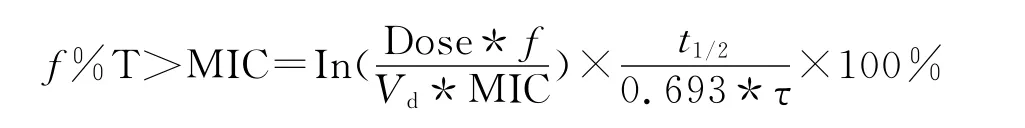
Dose為給藥劑量;f為游離藥物分數;Vd為表觀分布容積;t1/2為生物半衰期;τ為給藥間隔。各藥物的藥動學參數t1/2和Vd,引自頭孢哌酮舒巴坦(2∶1)的國外藥動學研究數據[13],PBs數據引自《新藥臨床藥理與應用手冊》[12],頭孢哌酮舒巴坦的健康人體藥動學參數[13]:t1/2為 (1.6±0.3)h,Vd為 (10.2±1.0)L,PBs為0.7~0.9。
1.4 蒙特卡洛模擬 模擬采用Crystal Ball軟件(美國Decisioneering公司),采用隨機化統計模型和蒙特卡洛模擬為手段,假定藥動學參數服從對數正態分布,游離藥物分數f服從均勻分布,MIC服從離散分布,使用5 000例次模擬,用模擬出來的中靶概率(probability of target attainment,PTA ),作為評價指標越高越好。PTA>90% 可選為給藥方案。
2 結果
2.1 MCS結果 根據藥效學指標的殺菌靶值,模擬獲得頭孢哌酮舒巴坦各治療方案的中靶概率和PK/PD指數模擬預測的統計值。3 g/q6 h,3 g/q8 h,6 g/q6 h和6g/q8 h這4種給藥方案:達到最佳治療效果f%T>MIC大于40%的中靶概率分別如下表所示:92.04%、77.90%、99.63%、97.04%,不同給藥方案對鮑曼不動桿菌的(MIC50=16μg·mL-1)的中靶概率如圖1~4所示。
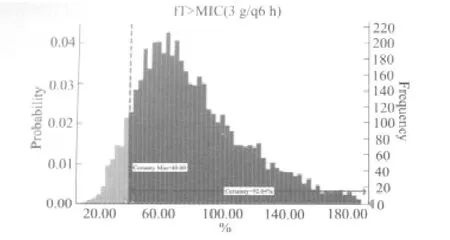
圖1 頭孢哌酮舒巴坦3 g/q6 h給藥時對鮑曼不動桿菌的中靶概率Fig 1 The probability of target attainment(PTA)against Acinetobacter baumanni in the regimen of cefoperazone sulbactam under 3 g/q6 h
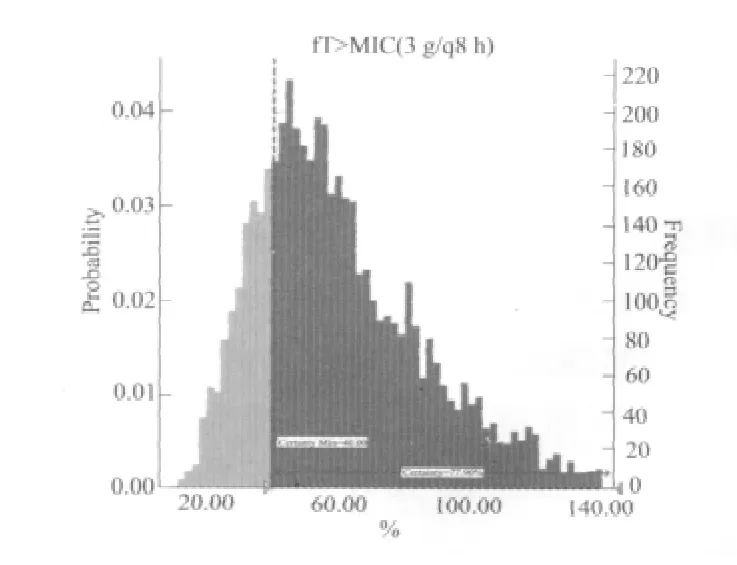
圖2 頭孢哌酮舒巴坦3 g/q8 h給藥時對鮑曼不動桿菌的中靶概率Fig 2 The probability of target attainment(PTA)against Acinetobacter baumanni in the regimen of cefoperazone sulbactam under 3 g/q8 h
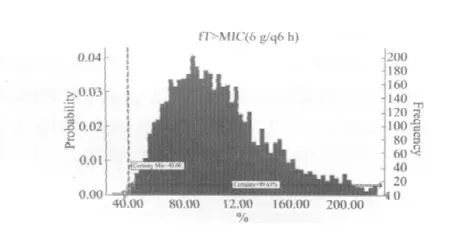
圖3 頭孢哌酮/舒巴坦6 g/q6 h給藥時對鮑曼不動桿菌的中靶概率Fig 3 The probability of target attainment(PTA)against Acinetobacter baumanni in the regimen of cefoperazone sulbactam under 6 g/q6 h
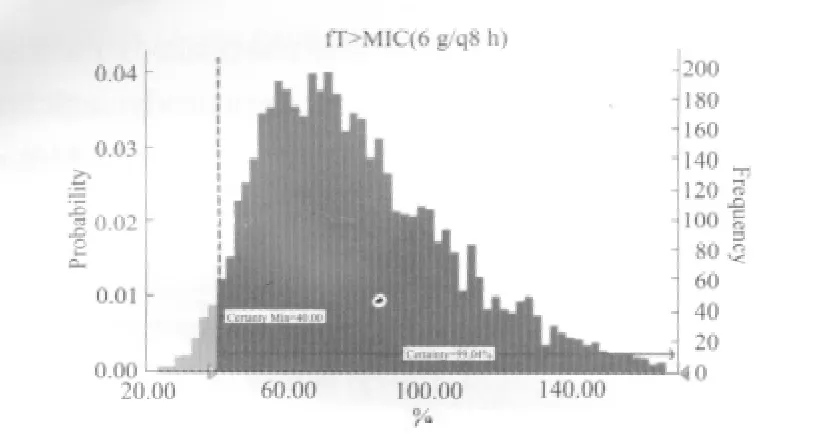
圖4 頭孢哌酮/舒巴坦6 g/q8 h給藥時對鮑曼不動桿菌的中靶概率Fig 4 The probability of target attainment(PTA)against Acinetobacter baumanni in the regimen of cefoperazone sulbactam under 6 g/q8 h
2.2 敏感性分析結果 對影響以上給藥方案治療效果的因素進行敏感性分析見表1,從表1可見對頭孢哌酮舒巴坦的f%T>MIC中靶概率影響較明顯的參數敏感度。結果表明,t1/2和f對中靶概率影響是正相關,即t1/2越長,f越大,中靶概率越高;而MIC和給藥間隔對中靶概率影響負相關,即MIC越低,給藥間隔越短,中靶概率越高。t1/2,f和MIC等是藥物特有的PK/PD參數無法調整,因此只有縮短給藥間隔來提高中靶概率和療效。敏感性分析結果表明不同給藥方案的給藥間隔影響也存在差異,6 g劑量給藥時給藥間隔的影響相當(-7.8%和-7.5%);而3 g劑量給藥時,q6 h和q8 h的差異明顯分別為-5.9%和-13.8%。說明同樣較低劑量給藥時,給藥間隔縮短更能增加療效。
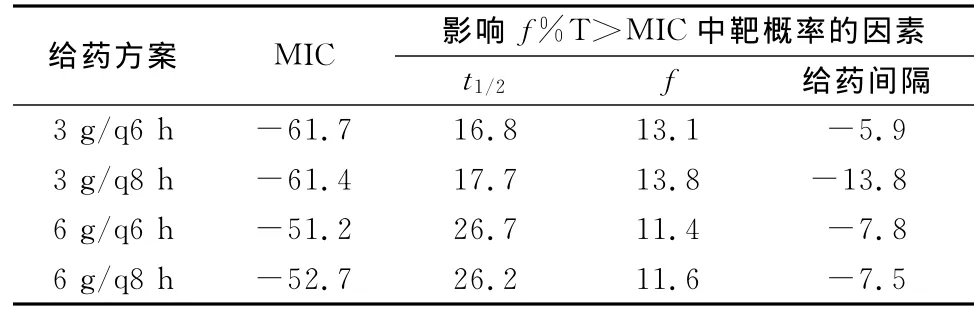
表1 敏感性分析結果(%)Tab 1 Results of sensitivity analysis(%)
3 討論
蒙特卡洛模擬結果顯示:頭孢哌酮舒巴坦治療鮑曼不動桿菌在靜脈滴注給藥途徑下按照3 g/q6 h,6 g/q6 h 和 6 g/q8 h方案給藥時中靶概率高(PTA>90%),模擬表明增加給藥次數和給藥劑量可以提高藥物對鮑曼不動桿菌的殺菌效果,這與2011年中國鮑曼不動桿菌專家共識中的抗菌藥物治療原則相符合。各參數對于模擬結果的敏感性分析表明:MIC及其分布對PTA的影響最大,達到50%以上;藥動學參數t1/2的影響約為15%以上;此外頭孢哌酮舒巴坦的血漿蛋白結合率較高,敏感性分析結果表明該因素也影響中靶效率。排除藥物的PK/PD因素外,影響治療結果的顯著因素是給藥間隔,給藥劑量對于PTA的影響可以忽略,分析原因可能為頭孢哌酮舒巴坦是時間依賴型且較短PAE的抗菌藥物,該類藥物的抗菌作用受峰濃度影響較小,主要評價參數是T>MIC。結果表明頭孢哌酮舒巴坦治療鮑曼不動桿菌時應該縮短給藥間期以提高療效。按照3 g/q6 h,6 g/q6 h和6 g/q8 h方案給藥時均能達到較好的治療效果(PTA>90%),推薦臨床以3 g/q6 h的方案靜滴給藥兼顧了提高抗菌療效和降低治療成本問題。
為提高臨床療效,減少耐藥菌的產生,可運用蒙特卡洛模擬優化給藥方案的設計。該法根據藥動學和藥效學模型,通過預測并比較不同給藥方案的中靶概率或累積反應分數,為用藥再評價和進一步調整提供更為科學和客觀的依據,給臨床優化抗菌藥物的治療方案提供新的研究方法。
[1]Peleg AY,Seifert H,Paterson DL.Acinetobacter baumannii:emergence of a successful pathogen[J].Clin Microbiol Rev,2008,21:538-582.
[2]陳佰義 何禮賢 胡必杰,等.中國鮑曼不動桿菌感染診治與防控專家共識[J].中華醫學雜志,2012.92(2):76-85.
[3]吳洪特,廖森,吳文偉.蒙特卡羅法用于多指標試驗設計的優化計算[J].計算機與應用化學,2007,24(7):929-931.
[4]張波,朱珠.蒙特卡羅模擬在抗生素藥動學和藥效學中的應用[J].中國藥學雜志,2008,43(4):341-344.
[5]史軍.藥物動力學和藥效動力學在抗菌藥物新藥開發和臨床治療上的應用[J].中國臨床藥理學與治療學,2007,12(2):121-133.
[6]Wang H,Zhang B,Ni Y,et al.Pharmacodynamic targetattainment of seven antimicrobials against Gram-negative bacteriacollected from China in 2003 and 2004[J].Int J Antimicrob Agents,2007,30(5):452-457.
[7]于廣華,高璀鄉,李芳,等.亞胺培南和左氧氟沙星給藥方案蒙特卡洛模擬的比較[J].計算機與應用化學,2009,26(11):1467-1470.
[8]Kuti JL,Nightingatle CH,Nicolau DP.Optimizing pharmacodynamic target attainment using the MYSTIC antibiogram:data collected in North America in 2002[J].Antimicrob A-gents Chemother,2004,48(7):2464-2470.
[9]楊啟文,徐英春.2005年中國十五家教學醫院院內獲得革蘭陰性病原菌耐藥性分析[J].中華醫學雜志,2007,87(39):2753-2758.
[10]習慧明,徐英春.2010年中國CHINET鮑曼不動桿菌耐藥性監測。中國感染與化療雜志,2012,12(2):98-104.
[11] Mouton JW,Dudley MN,Cars O,et al.Standardization of pharmacokinetic/pharmacodynamic(PK/PD)terminology for anti infective drugs:an update[J].J Antimicrob Chemother 2005,55(3):601-607.
[12]張石革,孫定人.新藥臨床藥理與應用手冊[M].2版.北京:化學工業出版社,2007:607-609.
[13]Reitberg DP,Marble DA,Schultz RW,et al.Pharmacokinetics of cefoperazone(2.0g)and sulbactam (1.0g)coadministered to subjects with normal renal function,patients with decreased renal function,and patients with end-stage renal disease on hemodialysis[J].Antimicrobial agents Chemothe,1988,32(4):503-509.

