影響HBeAg 陽性慢性乙肝拉米夫定抗病毒療效的預測因素探討
周穩蘭,陸春芬,盧應梅,朱蔚崗
核苷(酸)類似物是臨床治療慢性乙型肝炎患者的重要藥物,療效已經得到肯定,但因對HBV-cccDNA無直接作用,需長期使用,故如何取得更好療效及何時停藥是患者最關心的問題。本研究對近年來HBeAg陽性慢乙肝(HBV DNA>105copies/ml)接受拉米夫定抗病毒治療者進行回顧性分析,探討基線ALT、HBV-DNA水平與24周時HBV-DNA檢測不到率以及與遠期療效的關系;并探討發生HBeAg/抗HBe血清轉換后鞏固治療時間的長短與停藥復發的關系,現報告如下。
1 資料與方法
1.1 一般資料 病例來源于我院2000年10月~2006年10月住院或門診可隨訪的慢性乙肝患者共124例,其中男82例,女42例,平均年齡為(43.7±14.3)歲。均為 HBeAg(+)、HBV-DNA>105copies/ml者,診斷符合2000年(西安)中華醫學會傳染病與寄生蟲病學分會、肝病學分會聯合修訂的診斷標準。124例患者中單用拉米夫定組(A組)78例,拉米夫定加胸腺肽α1治療組(B組)46例,這些患者在接受抗病毒前6個月內均未行抗病毒或免疫調節劑治療。所有病例按基線ALT水平分為:組1:ALT≥5ULN;組2:5ULN>ALT>2ULN;組3:2ULN≥ALT>1ULN;按基線HBV-DNA水平分為:組4:HBV-DNA≥5.0 ×107copy/ml,組 5:HBV DNA <5.0 ×107copy/ml。
1.2 治療方法 A、B 2組均采用拉米夫定(葛蘭素威康公司生產)100 mg口服每日1次,而B組于治療后3個月開始加用胸腺肽α1(海南雙成藥業有限公司生產)1.6 mg皮下注射,每周2次×6個月,各組患者均同時應用一般護肝藥物治療。治療過程中發生HBV-YMDD變異,加用阿德福韋酯(葛蘭素威康公司生產)10 mg口服,每日1次。
1.3 觀察指標 全部病例于治療前、治療期間(前12月內每月、以后每3月)觀察臨床和生化指標,于治療前、治療后每3個月檢測血清 HBVM(ELISA法)、HBV DNA(PCR法,HBV DNA<1×103copy/ml為陰性),HBV YMDD變異檢測送江蘇省人民醫院。
1.4 統計學方法 組間率的比較用χ2檢驗,P<0.05為差異有顯著性意義。
2 結果
2.1 基線ALT水平與治療24周時HBV-DNA檢測不到率的關系 見表1。
2.2 基線HBV DNA水平與24周時HBV DNA檢測不到率的關系 見表2。
2.3 基線ALT水平與治療12月時HBeAg/抗HBe血清轉換率的比較 見表3。

表1 基線ALT水平與治療24周時HBV DNA檢測不到率的關系(n,%)
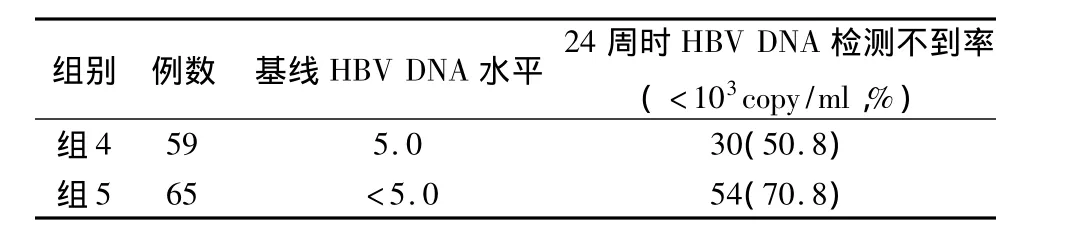
表2 基線HBV DNA水平與24周時HBV DNA檢測不到率的關系(n,%)

表3 基線ALT水平與治療12月HBeAg/抗HBe血清轉換率的比較(n,%)
2.4 A、B2組治療后12、24、36月的療效比較 26例血清轉換者繼續鞏固治療1年,停藥觀察1年,復發率23.1%(6/26)。20例血清轉換者繼續鞏固治療6月,停藥觀察1年,復發率50%(10/20);二者相比差異有顯著性(χ2=3.612,P <0.05),見表4、表5。CCCDNA[1]。由于其作用機理是抑制而不是殺滅HBV,肝細胞內的HBV能否被清除,取決于機體的免疫清除能力[2],患者在治療未達到HBeAg/抗HBe血清轉換前停藥,病毒可再度活躍復制,導致疾病復發,因此,長期服用可使病毒受到持續抑制,在機體免疫應答的協助下,有望取得持續緩解[1]。ALT>2ULN的患者往往是處于免疫清除階段,因而血清轉換較高。胸腺肽α1是一種免疫增強劑,可以調節機體的細胞免疫,促進淋巴細胞的成熟,增強輔助性T淋巴細胞、NK細胞的活性,誘導毒性T淋巴細胞的活化,并通過調節活性的淋巴細胞,釋放各種淋巴因子攻擊受病毒感染的肝細胞,直接導致cccDNA的減少,從而使病毒蛋白的表達減少[2]。
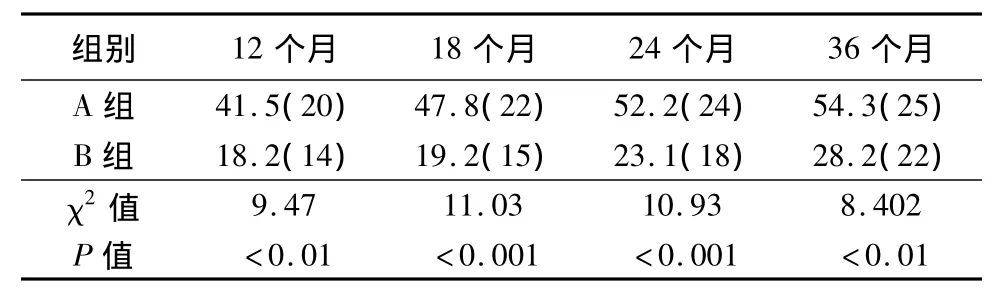
表4 2組治療后HBeAg/抗HBe轉換率(%)比較
本組資料顯示:基線ALT≥5ULN,24周時HBV DNA檢測不到率、治療1年HBeAg/抗 HBe血清轉換率均顯著高于5ULN>ALT>2ULN、2ULN≥ALT>1ULN(統計學有顯著性差異);基線HBV DNA<5.0×107copy/ml,24周時HBV DNA檢測不到率顯著高于 HBV DNA≥5.0×107copy/ml(P<0.001);A、B2組于治療3個月時HBV-DNA陰轉率為60%左右,此時A組在病毒復制受到明顯抑制時加用胸腺肽α1,結果顯示:HBV DNA陰轉率逐漸上升,于治療12月時達84.8%,而B組雖然也有上升,但顯著低于A組(P<0.05),經檢測已有7例發生了YMDD變異。而HBeAg/抗HBe的轉換率比較,在9個月、12個月時A組均顯著高于B組(P<0.05或0.01)。延長療程至24月、36月顯示:HBV DNA的陰轉率、HBeAg/抗HBe的轉換率均顯著高于B組(P<0.01或0.001);而24周時HBV DNA檢測不到者,36月時HBV DNA檢測不到率66.7%、HBeAg/抗HBe血清轉換率達51.2%;A組在治療24月時、36月時HBV-YMDD變異累計發生率分別為:10.9%、23.9%,顯著低于B組(P<0.05或0.01),且A組患者發生HBV-YMDD變異在治療后18個月,而B組在治療后9個月即有患者出現HBV-YMDD變異。124例患者中26例血清轉換者繼續鞏固治療1年,停藥觀察1年,復發率23.1%(6/26);20例血清轉換者繼續鞏固治療6月,停藥觀察1年,復發率50%(10/20),二者比較,差異有顯著性(χ2=3.612,P <0.05)。
本研究結果顯示:基線ALT高、HBV-DNA低(<107copy/ml),24周時HBV-DNA檢測不到率高,遠期(三年)療效持久。患者發生HBeAg/抗HBe血清轉換后鞏固治療時間越長停藥后復發率越低。慢性乙肝患者在拉米夫定治療后病毒復制大幅度降低時加用免疫增強劑胸腺肽α1,可以進一步降低HBV DNA水平,減少并延遲HBV YMDD變異株的發生,提高了HBeAg/抗HBe的轉換率,減少了停藥后復發,遠期療效肯定,是一種治療慢性乙型肝炎的安全有效方法。
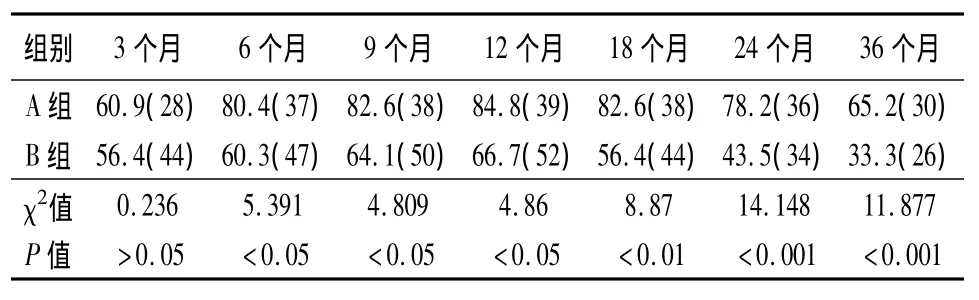
表5 A、B2組治療后HBV-DNA的陰轉率(%)比較
2.5 24周時HBV檢測不到者與36月時的療效關系 24周時HBV DNA檢測不到者,36月時 HBV DNA檢測不到率66.7%、HBeAg/抗HBe血清轉換率達51.2%。
2.6 AB2組治療24月、36月的累計變異率的比較 A、B2組治療24月時HBV-YMDD變異累計發生率分別為:10.9%(5例)、37.2%(29 例),A 組顯著低于 B 組(χ2=10.06,P <0.01);36月時HBV-YMDD變異累計發生率分別為23.9%(11例)、47.4%(37例),A 組仍顯著低于 B 組(χ2=4.85,P<0.05)。
3 討論
拉米夫定是一種安全有效的藥物,能較好地抑制HBV復制。但尚無證據顯示拉米夫定可清除肝細胞內的
[1]姚光弼,崔振宇,姚集魯,等.國產拉米夫定治療2200例慢性乙型肝炎的期臨床試驗[J].中華肝臟病雜志,2003,11(2):102-108.
[2]周穩蘭,陸春芬,朱蔚崗,等.拉米夫定聯合胸腺肽α1治療慢性乙型肝炎的遠期療效觀察[J].淮海醫藥,2009,27(2):159-160.

