氯胺/亞氯酸鹽對模擬給水管網硝化作用的控制*
周玲玲,張永吉,葉河秀,宋正國,張一清
(1.同濟大學城市污染控制國家工程研究中心,上海 200092; 2.同濟大學蘇州研究院,江蘇蘇州 215000;3.同濟大學長江水環境教育部重點實驗室,上海 200092)
隨著氯胺作為初級消毒劑和二級消毒劑的廣泛應用,人們發現在使用氯胺消毒的管網中會發生硝化作用,出現管網中消毒劑減少,出水異養菌、亞硝酸鹽和硝酸鹽超標等水質問題.據調查,美國應用氯胺消毒63%的水廠發生硝化作用;我國由于水源水質污染嚴重,水中氨氮含量較高,目前我國部分使用氯胺消毒的城市給水管網中也發現存在硝化作用[1-3].
硝化作用主要是由管網中的氨氧化菌(AOB)氧化水中的氨氮引起的,如何有效地滅活水中和管壁中的AOB成為控制管網硝化作用的關鍵[4].氨氧化菌可在4~6.5mg/L的氯胺濃度下存活,美國95%以上管網系統中存在一定濃度的消毒劑,但多數管網內仍發生了硝化反應.因此當硝化作用發生時,單純提高氯胺投量或改投氯并不能有效控制硝化作用[5].
經過對現有技術文獻檢索發現,亞氯酸鹽對AOB具有良好的滅活效果.本研究采用生物膜培養反應器(RAB)模擬實際管網,分別比較了氯胺、亞氯酸鹽及氯胺與亞氯酸鹽聯用的方法對氨氧化細菌和異養菌的滅活效果,為更好地控制給水管網硝化作用提供科學依據.
1 試驗材料與方法
1.1 試驗方法
1.1.1 氯胺的配制
在pH為8.0的磷酸鹽緩沖溶液中先加入25g/L的NH4Cl溶液,再緩慢加入400mg/L的NaClO溶液,同時不斷地搖勻混合溶液,然后將混合物置于20℃左右的避光處反應30min后檢測生成的一氯胺溶液濃度.氯胺濃度的測定方法見1.2.1.
1.1.2 試驗裝置及試驗過程
試驗裝置采用生物膜培養反應器(RAB),如圖1所示,其有效容積為800mL,水力停留時間為53~160min,每個RAB掛有20個掛片,掛片的掛膜面積為18.2cm2,安裝于反應器的轉子上,轉子轉速為50~150r/min.轉子在直流電機的驅動下轉動.
由于AOB的世代時間約為數小時至數天,一定濃度的AOB附著在管壁生長也需較長的時間.因此,為加速反應器內生物膜(硝化細菌和異養細菌構成)的形成,使用MPN培養基與自來水(水溫25℃)按照1∶5的配比作為生物膜培養反應器的進水,在反應器運行的20d內連續檢測反應器出水中亞硝酸氮濃度、pH和生物膜中AOB密度的變化.20d后R1,R2和R3反應器掛片上的AOB分別增至3 800MPN/cm2,2 400MPN/cm2和2 300 MPN/cm2,說明一定密度的AOB已經附著在生物膜中.接著以自來水作為反應器R1,R2和R3進水,3臺反應器連續進出水,R1反應器連續5d投加0.6mg/L亞氯酸鹽(亞氯酸鈉0.80mg/L),R2反應器中投加0.6mg/L亞氯酸鹽1d,接著投加(1.5±0.15)mg/L氯胺4d,R3反應器連續投加(1.5±0.25)mg/L氯胺.
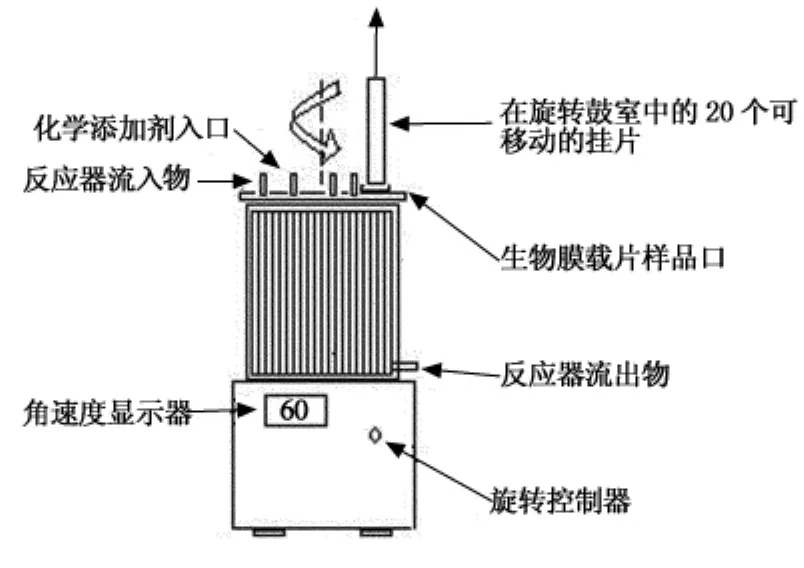
圖1 RAB裝置示意圖Fig.1 RAB experimental apparatus
1.2 檢測方法
1.2.1 余氯
采用DPD法測定[6].
1.2.2 異養菌(HPC)計數
水中懸浮菌的測定采用R2A培養基.R2A培養基組成如下:酵母浸膏0.5g,蛋白胨0.5g,酸水解干酪素0.5g,葡萄糖0.5g,可溶性淀粉0.5g,丙酮酸鈉0.3g,磷酸氫二鉀0.3g,七水合硫酸鎂0.05 g,瓊脂15g,pH=7.0~7.2,1L蒸餾水.取懸浮菌液1mL,使用10%的生理鹽水依次10倍稀釋菌液,得到一系列稀釋度的菌液,取100μL菌液平板涂布,23℃黑暗培養7d計數,以單位體積的細菌數表示(CFU/mL).
1.2.3 生物膜上異養菌的測定
用2~3根滅菌的棉簽從上到下擦拭掛片掛膜面5~6次,將擦拭完的棉簽放入盛有10mL滅菌緩沖液的試管中,將試管置于超聲波清洗器(功率250W)作用25min,再按照水中懸浮菌的測定方法測定生物膜中HPC數量,以單位面積的細菌數表示(CFU/cm2).
1.2.4 氨氧化菌MPN計數法
氨氧化菌(AOB)的培養采用Soriano and Walker培養基,培養基的組成成分見表1.采用4管MPN稀釋培養計數方法測定[7].在12個試管中分別加入5mL培養基,分為3列,每列4個平行樣.在每列中分別接種1,0.1和0.01mL樣品,接種后將試管置于28℃恒溫培養箱中黑暗培養21d.若需要稀釋,則使用緩沖溶液稀釋(SM9050C)[8].將300 μL等體積的0.6%二甲基α萘胺和0.8%磺胺酸混合溶液加入到試管中,若在5min內呈深紅色,則表明有亞硝酸氮生成,說明該樣品中存在AOB[1].
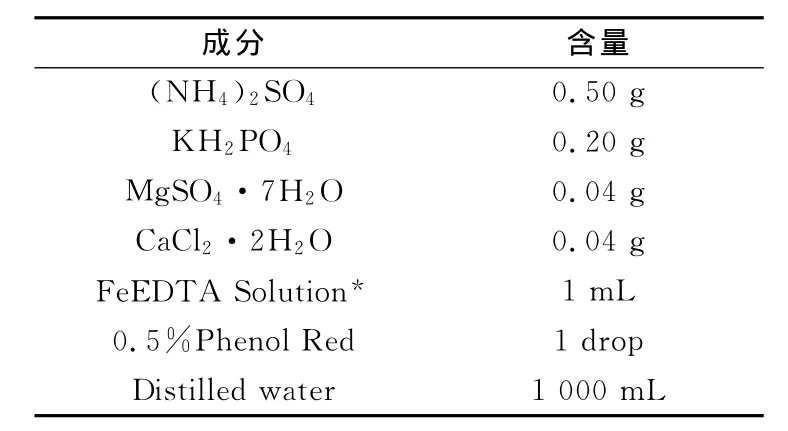
表1 MPN計數培養基組成成分Tab.1 Composition of the MPN enumeration
2 試驗結果與討論
2.1 氯胺對附著態和懸浮態AOB的滅活效果
圖2是氯胺在5d內對生物膜和水中AOB的滅活情況.氯胺在前3d對AOB的滅活效率較高,特別是前24h的滅活效果明顯,3d后滅活速率較為平緩.在前24h,氯胺對生物膜和水中的AOB的滅活速率分別是4.8×10-2log/h,5.7×10-2log/h.附著態的AOB在生物膜中的胞外聚合物(EPS)的保護下,對消毒劑具有一定的抗性,因此滅活速率較低[9].本試驗中,1.5mg/L氯胺滅活水中99%的AOB需要48h,CT99值是4 320mgCl2·min/L,而Cunliffe應用氯胺滅活水中99%的AOB所需CT99值是760mgCl2·min/L[5].本研究結果較Cunliffe試驗需要更長的時間,可能是由于AOB在管網系統中比在培養基生長的AOB對消毒劑具有更強的抗性,或者由于硝化細菌種類不同導致的差異.另外,實驗中的水質條件存在一定差別,如水溫和pH值等,可能也是導致不同CT99值的原因.
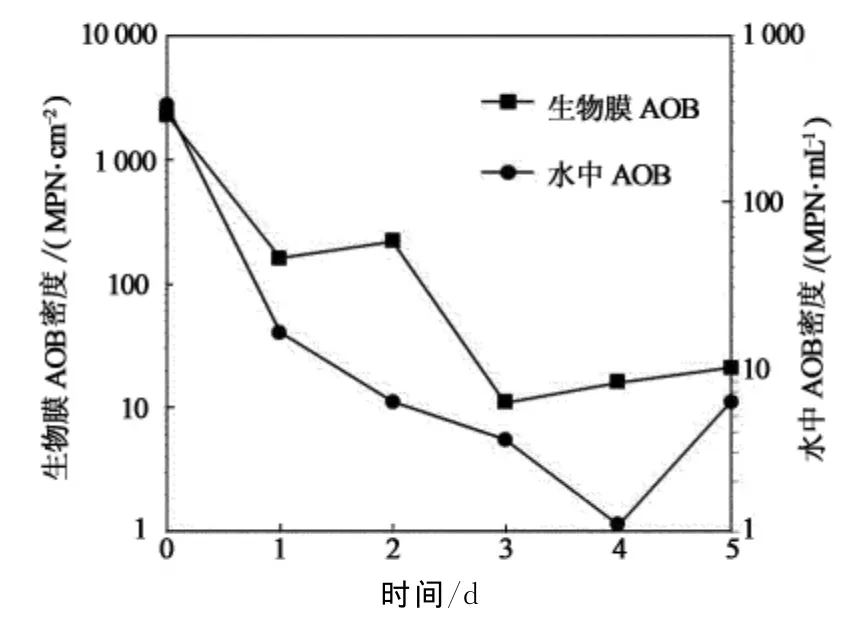
圖2 氯胺對生物膜和水中AOB的滅活Fig.2 Biofilm AOB inactivation for chloramine
2.2 亞氯酸鹽與氯胺聯用對AOB的滅活效果
圖3是單獨亞氯酸鹽及亞氯酸鹽與氯胺聯用對AOB的滅活情況.反應器R1投加0.6mg/L的亞氯酸鹽5d,反應器R2中投加0.6mg/L亞氯酸鹽1d,接著投加1.5mg/L的氯胺4d.24h之內2個反應器生物膜中AOB滅活速率在6.4×10-2~6.6×10-2log/h之間.而24h之后的滅活速率下降為0.6×10-2~0.7×10-2log/h,可以看出AOB的滅活主要發生在前24h.未投加消毒劑前,生物膜中AOB濃度約為3.6log MPN/cm2,而5d后降低至1.3log MPN/cm2,單獨亞氯酸鹽對懸浮態AOB的滅活速率與亞氯酸鹽和氯胺聯用時效果相當.比較R1和R2反應器中消毒劑對生物膜中的AOB的滅活效果,發現3d與5d的滅活效果相當,約滅活2.2log的AOB,說明3d的接觸時間足以阻止AOB的生長.對于水中懸浮態的AOB也發現相同的規律,3d約滅活2.0log的AOB[10].

圖3 亞氯酸鹽和亞氯酸鹽、氯胺聯用對生物膜和水中AOB的滅活Fig.3 Biofilm and bulk AOB inactivation for chlorite and chlorite switched to chloramine
表2比較了亞氯酸鹽和氯胺對生物膜和水中AOB的2h內的滅活速率,可以看出,亞氯酸鹽對生物膜和水中AOB的滅活速率要高于氯胺消毒.如當亞氯酸鹽質量濃度為0.6mg/L時,對生物膜和水中AOB的滅活速率分別為6.4×10-2log/h和7.2×10-2log/h,而1.5mg/L二氧化氯對生物膜和水中AOB的滅活速率分別為4.8×10-2log/h和5.7×10-2log/h.Mcguire等對亞氯酸鹽滅活AOB的機制進行了研究,認為當AOB氧化氨氮時會釋放出氫離子,此時細胞內部膜結構中會呈現暫時的酸性pH條件,亞氯酸鹽離子進入細菌內部形成二氧化氯(ClO2)[如式(1)所示],較低濃度的二氧化氯就可以通過改變細胞膜的滲透性、損害合成細胞酶和蛋白質的功能,最終破壞核酸而實現對AOB的滅活[11].
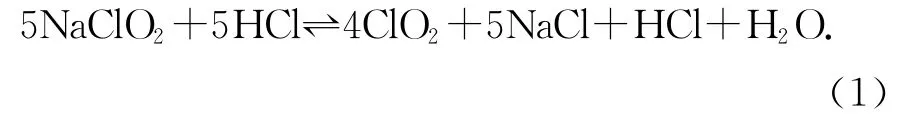

表2 氯胺和亞氯酸鹽滅活AOB效果比較(24h)Tab.2 Inactivation rates for chloramine and chlorite based on 24hdosage
2.3 氯胺、亞氯酸鹽對HPC的滅活效果比較
圖4考察了氯胺對生物膜及水中懸浮異養菌的滅活效果.由圖4可知,氯胺對水中異養菌的滅活速率要高于對生物膜中的異養菌的滅活速率,分別為8.3×10-2log/h和5.5×10-2log/h.
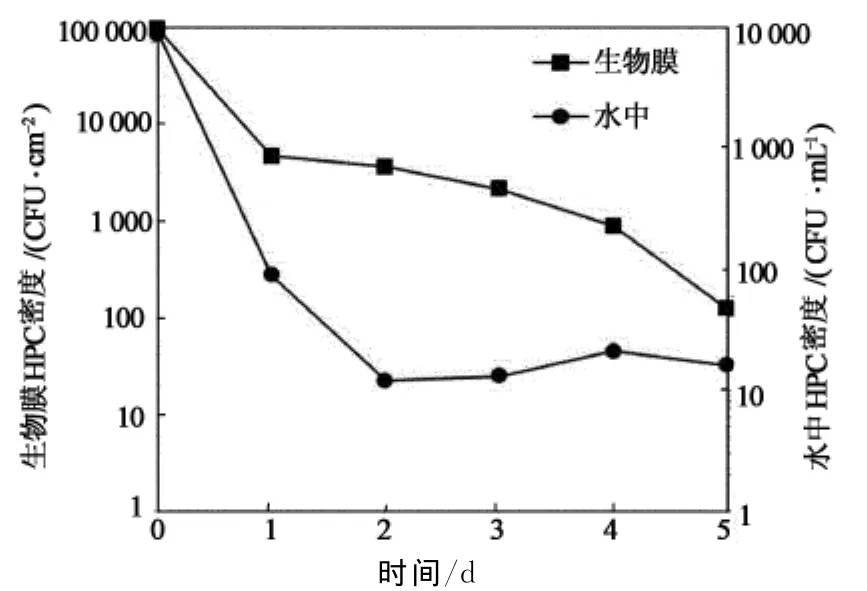
圖4 氯胺對生物膜和水中HPC的滅活Fig.4 Biofilm and bulk HPC inactivation
圖5是亞氯酸鹽對異養菌的滅活效果.從圖中可以看出,亞氯酸鹽對生物膜和水中懸浮態HPC均沒有滅活作用,HPC密度反而增加.連續投加0.6 mg/L亞氯酸鹽,生物膜中的HPC由3.2×105CFU/cm2增加至1.9×106CFU/cm2,水中的HPC由最初的103CFU/mL增至105CFU/mL.Mcguire采用不同濃度的亞氯酸鹽和接觸時間對水中懸浮態HPC的滅活試驗,證實亞氯酸鹽對生物膜中的HPC沒有滅活作用,與本文的研究結果是一致的,同時也說明亞氯酸鹽對異養菌和AOB的作用機理不同[12].在反應器中投加0.6mg/L的亞氯酸鹽1d后轉而投加1.5mg/L的氯胺,4d后生物膜中HPC減少了1.6logCFU/cm2,對比圖2可知,亞氯酸鹽與氯胺聯用時,亞氯酸鹽主要對AOB起到滅活作用,而氯胺除了對AOB有一定滅活效果外,對異養菌具有較好的滅活作用.亞氯酸根本身對氨氧化細菌和異養細菌均沒有滅活作用,在2.2節中提到亞氯酸鹽對AOB有滅活作用,而對異養細菌沒有滅活作用的原因是異養細菌在利用底物的過程中內部不能形成酸性pH條件,因此不能形成二氧化氯.
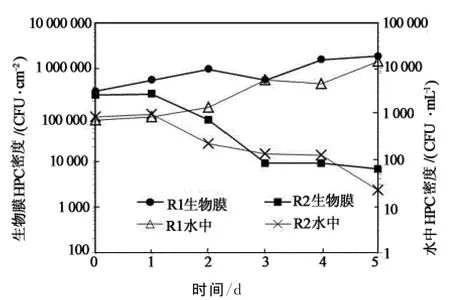
圖5 亞氯酸鹽和氯胺對生物膜和水中異養菌的滅活Fig.5 Biofilm and bulk HPC inactivation for chlorite and chlorite switched to chloloramine
2.4 討 論
研究顯示,一旦給水管網中發生了硝化作用,通過提高氯胺濃度并不能對硝化作用起到理想的控制效果;另一方面,由于硝化作用管網中會生成大量的亞硝酸氮,亞硝酸氮與氯胺發生反應導致氯胺迅速衰減,因此難以保持足夠的余氯濃度控制管網中的微生物生長.亞氯酸鹽對AOB具有良好的滅活效果,通過投加亞氯酸鹽,可以達到對硝化作用的有效控制.Michael進行的連續6個月中試試驗結果證實,0.1mg/L的亞氯酸鹽能夠阻止已經發生的硝化作用,0.2mg/L亞氯酸鹽可以抑制硝化作用數個星期,并且越高濃度的亞氯酸鹽抑制硝化再次發生的時間越長[13].McGuire的中試試驗結果也證實連續投加0.2mg/L的亞氯酸鹽可以有效控制硝化作用[13].將氯胺與亞氯酸鹽結合,充分利用氯胺對異養菌滅活效率高而亞氯酸鹽對AOB滅活效率高的特點,可實現對管網中AOB和異養菌的滅活、硝化作用的控制.
然而,亞氯酸鹽是一種對人體有害的物質,如何有效地控制其濃度在不影響人體健康的范圍,還需進一步通過試驗確定.
3 結 論
1)氯胺對水中和生物膜中的AOB均有一定的滅活效果,亞氯酸鹽對水中和生物膜中AOB的滅活效果高于氯胺.
2)亞氯酸鹽對異養菌沒有滅活效果.
3)采用氯胺和亞氯酸鹽聯用可有效滅活AOB和異養菌,實現對管網硝化作用的控制.
[1] WOLFE R L,LIEU N I,IZAGUIRRE G,et al.Ammonia-oxidizing bacteria in a chloraminated distribution system:seasonal occurrence,distribution and disinfection resistance[J].Appl Environ Microbiol,1990,56(2):451-462.
[2] WILCZAK A,JOSEPH G,JACANGELO J P,et al.Occurence of nitrification in chloraminated distribution systems[J].Ammerican Water Works Association Journal,1996,88(7):74-85.
[3] 張永吉,周玲玲,李偉英.氯胺消毒管網中的硝化作用及其研究進展[J].中國給水排水,2008,24(2):1-4.ZHANG Yong-ji,ZHOU Ling-ling,LI Wei-ying.Nitrification in chloraminated drinking water distribution system and its control[J].China Water &Wastewater,2008,24(2):1-4.(In Chinese)
[4] HARRINGTON G W,NOGUERA D R,BONE C C,et al.Ammonia from chloramine decay:effects on distribution system nitrification[M].Denver,Colo:American Water Works Association,2003.
[5] CUNLIFFE D A.Bacterial nitrification in chloraminated water supplies[J].Applied and Environmental Microbiology,1991,57(11):3399-3402.
[6] 國家環保局.水和廢水監測分析方法[M].4版.北京:中國環境科學出版社,2002:170-177.Environmental Protection Administration of China.Water &wastewater monitor and analysis methods[M].4th ed.Beijing:China Environmental Science Press,2002:170-177.(In Chinese)
[7] SORIANO S,WALKER N.Isolation of Ammonia-oxidizing autotrophic bacteria[J].Jour Appl Bact,1968,31(4):493-497.
[8] APHA.Standard methods for the examination of water and wastewater[M].20th ed.Washington,DC:American Public Health Association,1998.
[9] LECHEVALLIER M W,CAWTHON C D,LEE R G.Inactivation of biofilm bacteria[J].Appl Environ Microbiol,1988,54(10):2492-2499.
[10]CHICK H.An investigation of the laws of disinfection[J].Journal of Hygiene,1908,8:92-158.
[11]STEWARD M H,OLSON B H.Bacterial resistance to potable water disinfectants[M]//Hurst C J,ed.Modeling Disease Transmission and its Prevention by Disinfection.Cambridge,England:Cambridge University Press,1996:140-192.
[12]MICHAEL J M,NANCY I L,MARIE S P.Using the chlorite ion tocontrol nitrification[J].American Water Works Association Journal,1999,91(10):52-61.
[13]MCGUIRE M J,PEARTHREE M S,BLUTE N K,et al.Nitrification control by chlorite ion at pilot scale[J].American Water Works Association Journal,2006,98(1):95-105.

