Akt在非小細胞肺癌中作用的研究現狀
陳勃江 綜述 李為民 審校
肺癌是目前對人類健康威脅最大的惡性腫瘤之一,全球每年約有135萬人被確診為肺癌,120萬人死于肺癌[1]。雖然醫學技術有了長足發展,但肺癌患者的5年生存率并未得到明顯改善,僅為15%左右[1]。其根本原因在于肺癌的發病機制尚不清楚、臨床缺乏有效的早期診斷和治療手段。病理學上,肺癌分為小細胞肺癌(small cell lung cancer, SCLC)和非小細胞肺癌(non-small cell lung cancer, NSCLC),后者約占80%-85%。20世紀90年代以來,信號傳導通路逐漸成為腫瘤學研究領域的熱點。絲氨酸/蘇氨酸蛋白激酶B(protein kinase B, PKB/Akt)因其處于多條信號通路的交叉點而受到廣泛關注。
1 Akt 的研究現狀
Akt是存在于人類染色體基因組中鼠類胸腺淋巴瘤病毒(T-8 strain from AKR/J mouse, AKT8)致癌基因(v-Akt)的同源物,其編碼的蛋白質Akt是一種絲氨酸/蘇氨酸蛋白激酶,因與蛋白激酶A、C高度同源,又名蛋白激酶B(protein kinase B, PKB)[2]。Akt經磷脂酰肌醇3-激酶(phosphatidylinositol 3-kinase, PI3K) 活化后,磷酸化其下游多種底物,參與細胞生物學功能的調節,影響細胞生物學行為,主要表現為促進細胞增殖、抑制細胞凋亡、提高細胞的乏氧耐受性、促進腫瘤細胞侵襲轉移和組織血管生成等,從而參與多種腫瘤的發生[3]。隨著研究的深入,現已基本繪制了以Akt為中心的信號通路圖(圖1)。
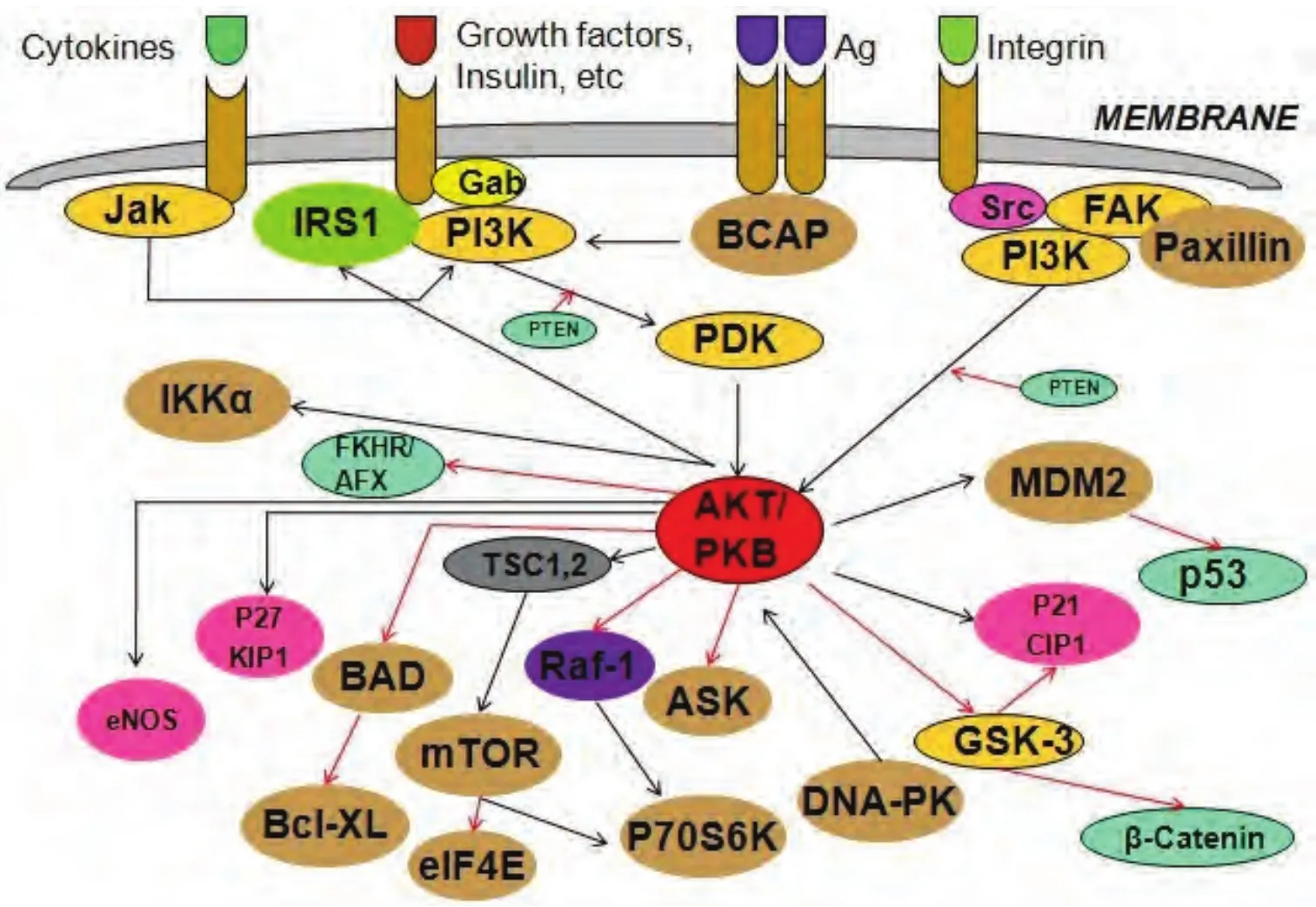
圖1 Akt信號通路圖Fig 1 Signaling pathway of Akt
Akt家族包括Akt1、Akt2、Akt3三種亞型,其中Akt2是最重要的一種,不僅具有Akt的普遍特征,還有其獨特的生物學功能,主要介導腫瘤細胞的粘附、運動、侵襲和轉移[4-6]。有學者研究發現,約10%-20%的原代胰腺癌細胞和胰腺癌細胞株存在Akt2的擴增或過表達。當用Akt2反義核苷酸轉染胰腺癌細胞后,腫瘤生長明顯受抑,且僅局限于管腔內;而導入正義核苷酸的對照組腫瘤細胞,其生長則無明顯變化,并侵入管壁。此現象表明Akt2的過度表達促進了胰腺癌細胞的生長和侵襲[7-10]。Rychahou等[11]用qRT-PCR的方法檢測了86例結腸癌患者腫瘤組織和正常結腸組織中Akt2 mRNA的水平,發現腫瘤組織中的Akt2 mRNA是正常組織的8倍-10倍;隨后對36例有肝轉移的結腸癌患者的正常組織、結腸癌原發灶及肝轉移灶進行免疫組織化學染色,結果顯示:超過80%的病例的原發灶和轉移灶存在Akt2的高表達。為了進一步驗證Akt2對細胞侵襲及轉移能力的影響,他們用特異性的Akt2 siRNA載體感染已被熒光素標記的腫瘤細胞,并以空轉腫瘤細胞為對照,將細胞注入裸鼠脾臟。4周后,實驗組裸鼠均未出現肝臟轉移,而對照組則出現明顯的多發肝臟轉移灶。該研究從不同的水平說明了Akt2在促進結腸癌形成和轉移中的重要作用,與其在前列腺癌及腦膠質細胞瘤中的結果基本一致[12,13]。
關于Akt在NSCLC中的研究,有學者發現NSCLC組織中,Akt2基因的重要功能位點(激酶區)低突變,而Akt1與Akt3則未見突變,提示Akt2基因突變可能是促進肺癌發生的重要原因[14]。Nishioka等[15]用煙草的主要致癌物質之一亞硝胺吡啶基丁酮(NNK)處理小鼠支氣管上皮細胞,1小時后即檢測到細胞中的Akt被激活,形成磷酸化Akt(phosphorylated Akt, p-Akt)。Binaifer等[16]利用免疫組織化學染色技術檢測p-Akt在支氣管上皮細胞中的表達,發現16例發育不良或化生的支氣管上皮組織中p-Akt為陽性,9例增生組織呈弱陽性,而所有的正常組織則均為陰性。進一步對110例NSCLC組織進行分析,結果顯示NSCLC中p-Akt的陽性率為51%(56/110),明顯高于正常組織,且免疫組織化學染色提示56例腫瘤組織均表達p-Akt2。以上研究提示:Akt尤其是Akt2的活化可能是導致支氣管上皮細胞惡變的重要早期事件。
Park等[17]將細胞間粘附分子-3(intercellular adhesion molecule-3, ICAM-3)基因過表達載體導入NSCLC NCI-H1299細胞株,發現細胞中的Akt被激活,繼而細胞的遷移和侵襲能力明顯增加。我國學者[18]也證實肺腺癌細胞的Akt的活化與細胞的侵襲能力呈正相關。另有動物試驗[16]顯示,p-Akt不僅能在體外促進細胞的遷移,而且還能在體內增強氣道上皮細胞對粘膜的侵蝕,促進氣道腫瘤的生長。
關于Akt與NSCLC患者預后的關系,目前的研究結果尚不完全一致。Shah等[19]分析了82例NSCLC患者病灶組織中p-Akt的表達與患者術后生存時間的關系,結果顯示:p-Akt高表達組較低表達組生存時間更長,差異有統計學意義(P=0.007);而另一項納入335例NSCLC患者的研究[20]結果則與之相反,單因素和多因素分析均提示:高水平的p-Akt是患者預后不良的獨立危險因素。然而,Binaifer[16]的研究發現,在110例NSCLC患者中,p-Akt陽性組與陰性組的中位生存時間差異無統計學意義(23個月 vs 26個月,P=0.796 4)。
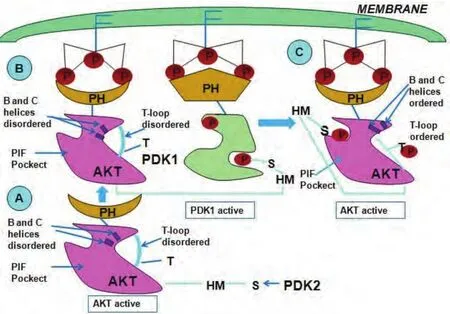
圖2 PDK1的作用機制Fig 2 Mechanism of the action of PDK1
2 Akt上游信號通路蛋白分子——PDK1的研究現狀
業已證明,Akt屬酯類激酶家族,其活化依賴于上游信號分子的作用。當細胞受到胰島素樣生長因子、血小板源性生長因子等胞外信號刺激時,PI3K的P110催化亞基被激活,磷酸化二磷酸酯酰肌醇[phosphtidylinositol (4,5)-bisphosphate, PIP2]生成三磷酸酯酰肌醇[phos-phatidylinositol (3,4,5)- triphosphate, PIP3],誘導無活性的Akt和PDK1從細胞質易位至細胞膜,同時使Akt的構象發生改變,暴露出Thr308和Ser473磷酸化位點。位于細胞膜的Akt與PDK1相互靠近,PDK1催化Akt磷酸化,使其活化[21],見圖2。由此可見,PDK1是Akt的重要上游調節分子。
Liu等[22]觀察到EGF誘導細胞中PDK1和Akt共易位。當用PDK1 siRNA干擾乳腺癌細胞PDK1的表達時,Akt的磷酸化水平明顯降低,且細胞的轉移和趨化能力明顯受損。在裸鼠體內,PDK1 siRNA干擾的乳腺癌細胞成瘤速度緩慢,且不能形成肺部轉移病灶。Lee等[23]用PDK1抑制劑OSU-03012處理惡性神經鞘瘤細胞,亦發現細胞的增殖減慢,凋亡增加,體內成瘤能力下降。
然而,目前鮮有關于PDK1在NSCLC中的作用及其對Akt的調節機制的報道。筆者所在課題組在前期研究中發現PDK1和Akt在NSCLC組織中的表達均增高,推測PDK1可能參與Akt的活化,進而影響NSCLC的發生。
3 Akt下游信號通路蛋白分子——Raf-1和p70S6K的研究現狀
現已證實,Raf是一種原癌基因,其編碼產物為絲氨酸/蘇氨酸蛋白激酶,主要參與Ras/Raf/MEK/ERK信號通路的傳導。Raf有3種同型異構體,分別為A-Raf、B-Raf和C-Raf(Raf-1)。B-Raf的作用機制目前已較清楚,而Raf-1的功能則了解較少,一般認為與細胞的抗凋亡作用有關[24]。近年來,有學者研究發現,Raf-1除了通過Ras/Raf/MEK/ERK通路發揮作用外,還存在非MEK/ERK依賴機制。Raf-1被Akt磷酸化后,在調節細胞增殖、分化和凋亡等方面發揮重要作用[25]。p70S6K是Raf-1的作用底物之一,它是核糖體40s小亞基S6蛋白激酶,被Raf-1活化后,促進含5’-末端寡聚嘧啶(5’-terminal oligopolypyrimidine,5’-TOP)mRNA的翻譯,刺激細胞生長、增殖等[26]。
Jilavean等[27]檢測了263例痣和523例惡性黑色素瘤組織中Raf-1的表達,發現腫瘤組織Raf-1的水平較痣明顯增高(P<0.000 1),且轉移灶較原發灶更高(P=0.022 5)。用Raf-1 siRNA干擾惡性黑色素瘤細胞株Raf-1的表達,細胞凋亡增加。Lyustikman等[28]的研究結果也顯示:神經膠質瘤組織中Raf-1的表達增高;將Raf-1重組逆轉錄病毒導入小鼠神經膠質細胞,細胞惡變形成神經膠質瘤。目前尚未在NSCLC組織中檢測到Raf-1的基因突變;Raf-1轉基因小鼠的肺內腺瘤形成的發生率也較低,存在時間亦較短[29]。然而,Cekanov等[30]利用煙草致癌原NNK誘導倉鼠發生肺腺癌,并用NNK處理人氣道上皮細胞。5周、10周和20周后,倉鼠肺微腺瘤及人氣道上皮細胞均被檢出有Raf-1的高表達,且呈時間依賴性增加。該實驗提示Raf-1可能與肺腺癌的形成有關,是肺腺癌發生的早期標志物之一。實際上,早在20世紀90年代,就有學者利用反義寡核苷酸技術來特異性阻斷NSCLC組織中Raf-1的表達,結果發現大部分細胞出現包括染色質濃縮、DNA斷裂、annexin V結合等在內的凋亡現象,最終細胞死亡[31]。Kerkhoff等[29]的分析進一步顯示:肺癌細胞株中Raf-1蛋白激酶表達水平的升高可能導致細胞惡性轉化。因此臨床上出現了利用Raf激酶抑制劑BAY 43-9006治療NSCLC的方法。2005年在美國臨床腫瘤學會(American Society of Clinical Oncology, ASCO)會議上,Adjei等[32]首次報道了12例NSCLC患者的BAY43-9006 I期臨床試驗結果:1例患者達部分緩解;8例(67%)患者處于疾病穩定期,其中2例長達24周。
p70S6K在乳腺癌及消化道腫瘤中的作用研究較多,而其與NSCLC的關系則報道相對較少。多項研究[33-35]表明,p70S6K在乳腺癌、肝癌、食道癌、膽囊癌等腫瘤組織中高表達,且磷酸化水平與腫瘤轉移、術后復發或死亡等明顯正相關。p70S6K對NSCLC意義的研究中,Shen等[36]用高通量免疫印跡、Western blot和免疫組織化學染色等方法檢測肺腺癌和正常支氣管上皮組織中p70S6K的表達水平,發現p70S6K在肺腺癌組織中增高,故其在肺腺癌的鑒別診斷中有一定價值。本課題組在前期研究中探討了Raf-1和p70S6K在不同病理類型NSCLC中的表達,結果顯示Raf-1在肺腺癌和鱗癌組織中均呈高表達;而p70S6K則在肺腺癌組織中表達增高,在鱗癌組織中陰性表達。因此,Akt/Raf-1在肺腺癌和鱗癌組織中是否均通過作用于底物p70S6K而發揮作用尚需進一步的研究和分析。
4 小結
綜上所述,現有的研究已經提示PDK1、Akt、Raf-1和p70S6K四種蛋白質參與了包括NSCLC在內的多種腫瘤的發生。然而,以Akt為中心的PDK1/Akt/p70S6K信號通路在NSCLC中的作用機制尚有待于系統的深入研究,以期進一步明確NSCLC的發生機制,探尋NSCLC早期診斷的分子標志物和靶向治療新靶點。

