基礎有機化學電子效應教學實踐





摘 要:電子效應是“基礎有機化學”課程教學的主線之一,采用集中學習與分散學習相結合的教學方法,有利于學生深入全面地理解有機物的性質。緒論部分集中學習電子效應的分類和概念、電子效應對酸堿性、穩定性、親核性、反應活性、反應方向和反應機理的影響,培養學生自覺運用電子效應分析相關問題的思維習慣。在各類官能團化合物的教學中分散學習電子效應,幫助學生深刻理解和熟練運用電子效應。實踐證明,將電子效應貫穿于“基礎有機化學”教學的始終能顯著提高學生的學習效率,提升教師的教學效果。
關鍵詞:電子效應;誘導效應;共軛效應;超共軛效應
中圖分類號:G642 " " " " " " " " " " " " " " " " " " " " " " " " " " "文獻標識碼:A " " 文章編號:1009-3583(2024)-0118-04
Teaching Practice of Electronic Effects of Basic
Organic Chemistry
CHEN Xin1,2, CHEN Li-juan1,2, WANG Yu-juan1,2, ZHONG Yu1,2*
(1.School of Materials and Chemical Engineering, West Anhui University, Lu’an 237012, China; 2. Anhui Provincial Key
Laboratory of Bio-mimetic and Sensors, Lu’an 237012, China)
Abstract: Electronic effects is one of principle lines of “Basic Organic Chemistry” teaching, combination of centralized learning and distributed learning is helpful for students to understand the properties of organic compounds. The introduction section focuses on studying the classification and concepts of electronic effects, the impact of electronic effects on acidity, stability, nucleophilicity, reactivity, reaction direction, and reaction mechanism, and cultivating students’ conscious thinking habits of using electronic effects to analyze related issues. Disperse the learning of electronic effects in the teaching of various functional compounds, helping students to deeply understand and proficiently apply electronic effects. Practice has proven that incorporating electronic effects throughout the teaching of “Basic Organic Chemistry” can significantly improve students’ learning efficiency and enhance teachers’ teaching effectiveness.
Keywords: electronic effects; induction effects; conjugation effects; hyper-conjugation effects
“基礎有機化學”是化學化工、材料、制藥、環境、食品等專業的必修課,該課程內容龐雜。“基礎有機化學”的教學需抓住電子效應、反應機理和官能團基本性質三條主線,其中電子效應是基礎,是深入理解官能團性質和反應機理的前提,也是將有機化學內容系統化的一個關鍵點,電子效應貫穿于基礎有機化學教學的始終。但是,現有國內的基礎有機化學教材對電子效應并沒有做到集中、系統、詳盡地闡述,而是分散于多個章節中,不利于學生全面系統地掌握電子效應的原理和應用。黃池寶等[1]通過系統闡述苯及其衍生物、吡啶及呋喃、噻吩、吡咯的大 -電子云分析法,揭示了大 -電子云分析法不僅是把握化合物性質與反應特性的便捷辦法,而且是解答有機化學問題的一把鑰匙。用大 -電子云分析法來理解與掌握有機化學理論體系可以收到高屋建瓴、事半功倍的效果,是一種優良的教學方法,值得大力推廣應用。朱萬強等[2]采用密度泛函方法研究了取代基的電子效應對噁二唑化合物光電性質的影響,揭示了含氟基團通過吸電子效應對模型分子的紅外振動、電子吸收光譜和前線軌道能量以及分子能量有規律的影響,進而影響模型分子光電性質變化的規律性。
鑒于電子效應在基礎有機化學教與學方面的重要性,同時,為了加強后續章節知識體系教學的連貫性和邏輯性,作者多年來一直推行電子效應集中學習與分散學習相結合的教學方法,取得了較好的教學效果。電子效應的集中學習安排在緒論部分,該部分介紹電子效應的預備知識、電子效應的分類和概念以及電子效應對有機物酸堿性、穩定性、親核性、反應活性、有機反應方向和反應機理的影響;電子效應的分散學習安排在各類官能團化合物的教學部分。
1" 預備知識的教學
在緒論的教學中,除了介紹有機物概念、特點,有機化合物的分類、有機化學酸堿理論、共價鍵斷裂方式、有機反應的類型外,還介紹了共價鍵的主要參數、有機物結構表示方法(重點講解路易斯電子式)、碳原子的雜化狀態、有機化學中常見的富電子和缺電子體系、親核反應與親電反應的概念、共振論等。
2" 電子效應的分類和概念
該部分的教學內容[3-5]如表1所示,列舉典型例子將該部分內容講解透徹。用2~3學時講清楚“電子效應的分類與概念”“電子效應的應用”,培養學生自覺運用電子效應知識分析有機化學中各種問題的良好思維習慣,為后續有機物性質的學習奠定堅實的基礎。
上述三種電子效應講授完畢后,與同學一起探討下列問題:(1)三種電子效應的相對強弱如何?(2)PhNH2和PhOH中苯環電子云密度的相對大小如何?(3)離開具體體系,孤立地說某個原子或基團(如-OH、-NH2等)是吸電子或供電子基團有沒有意義?
3" 電子效應的應用
多篇文獻[3-7]介紹了電子效應在有機物結構分析、偶極矩比較、酸堿性強弱比較、有機反應方向和有機反應機理和波譜分析等方面的應用,但是這些文獻對電子效應在有機化學中的應用介紹還不夠深入。本文選取典型例子,從七個方面闡述電子效應的應用。
3.1 "穩定性比較
例1:比較(CH3)3C+、(CH3)2CH+、CH3CH2+、ClCH2CH2+、PhCH2+和O2NCH2CH2+的穩定性;
例2:比較PhO -及其對位硝基、氯、甲基和氨基取代物的穩定性;
例3:比較PhCH2+及其對位硝基、氯、甲基和氨基取代物的穩定性;
例4:比較CH3CH2、H2C=CHCH2、(CH3)3C和H2C=CHCHCH=CH2的穩定性;
例5:比較(CH3)3C-、(CH3)2CH-、CH3CH2-、ClCH2CH2-、PhCH2-和O2NCH2CH2-的穩定性。
要求學生掌握穩定性的判定依據:共軛作用越強越穩定,參與超共軛的碳氫鍵數目越多越穩定,帶電體系電荷越分散越穩定。
3.2" 酸性強弱比較
例1:比較乙酸、苯酚、水、甲醇、乙醇、異丙醇、叔丁醇氣相條件的酸性強弱;
例2:比較苯酚及其對位硝基、氯、甲基和氨基取代物的酸性強弱;
例3:比較4-溴丁酸、4-氟丁酸、3-氟丁酸、2-氟丁酸、2,2-二氟丁酸的酸性強弱;
例4:比較、、的酸性強弱;
例5:比較正丙苯 、 和 -H的酸性強弱;
例6:比較(CH3CO)2CH-H、CH3COCH2-H和CH3CH2CH2-H的酸性強弱;
例7:比較乙烷、乙烯和乙炔的酸性強弱;
例8:比較苯酚、鄰甲基苯酚和2,6-二甲基苯酚的酸性強弱;
酸性強弱判定依據:對于同一化學鍵,電子云密度越小越容易斷裂;共軛堿越穩定越容易生成,離解出氫離子越容易,酸性越強;碳原子雜化狀態中s成分越高吸電子能力越強。
3.3" 堿性強弱比較
例1:比較CH3CH2O-、CH3O-、HO-、PhO-的堿性;
例2:比較三甲胺、二甲胺、甲胺、氨、苯胺、二苯胺的堿性;
例3:比較吡咯、二氫吡咯和四氫吡咯的堿性;
例4:比較CH3CH2-、CH2=CH-、CH≡C-的堿性;
例5:比較苯胺及其對位硝基、氯、甲基和氨基取代物的堿性;
例6:比較、NH3、和苯胺的堿性;
例7:比較CH3CH2O-、ClCH2CH2O-、BrCH2CH2O-、ICH2CH2O-、O2NCH2CH2O-的堿性。
堿性強弱判定依據:對于帶負電荷和孤對電子的體系,負電荷越集中或孤對電子電子云密度越大,結合氫離子越容易,堿性越強。共軛酸酸性越弱,共軛堿的堿性越強。
3.4親核性強弱比較
例1:比較C2H5O-、OH-、PhO-、CH3COO-、"" C2H5OH、H2O、PhOH、CH3COOH的親核性;
例2:比較NH2-、OH-、F-的親核性,NH3和H2O的親核性;
例3:比較I-、Br-、Cl-、F-的親核性,H2S和H2O的親核性。
親核試劑親核性強弱比較依據:先比較親核試劑的堿性,再看親核試劑的進攻原子。如進攻原子相同或同周期,親核性強弱順序同堿性強弱順序一致,如進攻原子同主族,親核性強弱順序同堿性強弱順序相反。
3.5" 反應活性大小比較
例1:比較CH2=CH2、CH3CH=CH2、CH3CH=CHCH3和(CH3)2C=CHCH3與H+的反應活性;
例2:比較苯甲醚、甲苯、苯、苯胺、硝基苯和苯乙酮與Br+的反應活性;
例3:比較1,3-丁二烯與氨基乙烯、丙烯、乙烯、氯乙烯和硝基乙烯反應的反應活性;
例4:比較乙烯與1,3-丁二烯及其2-位氨基、甲基、氯和硝基取代物的反應活性;
例5:PhCH2+、(CH3)2CH+、CH3CH2+、O2NCH2CH2+、ClCH2CH2+與Br-的反應活性;
例6:比較乙酰氯、乙酸酐、乙酸乙酯和乙酰胺在堿性條件下水解的反應活性(先告知學生羧酸衍生物在堿性條件下的水解機理)。
反應活性大小比較依據:不考慮空間位阻的情況下,富電子體系與缺電子體系反應,富電子體系電子越富,缺電子體系電子越缺,反應越容易。反應中間體或產物越穩定,反應越容易。由于學生有機化學知識欠缺,該部分內容教學時需要給學生提供一些背景知識,教會學生利用電子效應分析反應活性的方法,為后續官能團性質的教學奠定基礎。
3.6 對反應方向的影響(反應選擇性)
該部分教學內容旨在培養學生根據中間體和產物穩定性判斷反應主產物的思維方法。
3.7" 對反應機理的影響
例1:
例2:
通過上述機理分析,富電子的C=C和苯環可以發生親電加成或親電取代反應,當連有強吸電子基團時,富電子的C=C和苯環可以轉變為缺電子性質,從而發生親核反應。
4"" 電子效應在有機物性質教學中的應用
現行大學基礎有機化學教材[8-10]大多按照官能團安排章節,對有機物化學性質和反應機理的教學需要靈活嵌入電子效應的教學,學生才能擺脫死記硬背的學習方法。官能團性質教學中涉及的電子效應內容見表2。
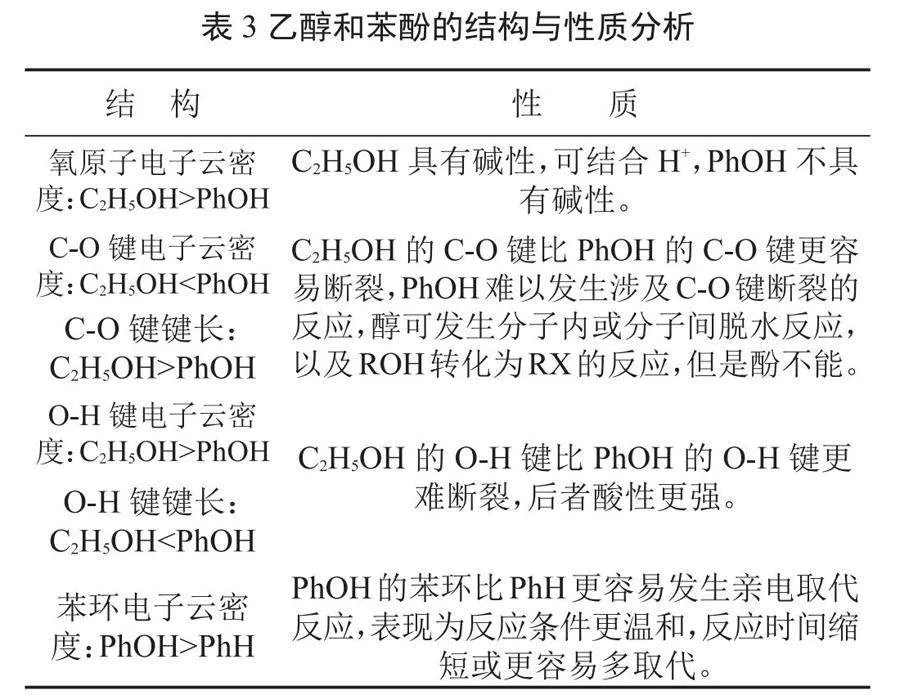
在學習官能團化學性質之前,根據電子效應分析官能團的結構特點,啟發學生根據“結構決定性質”分析官能團的化學性質。比如醇酚章節的教學,首先和學生共同分析在C2H5OH分子中-OH對乙基只存在-I效應,在PhOH中-OH對苯環同時存在-I和+C效應,且后者更強,導致C2H5OH中-OH對乙基吸電子,而PhOH中-OH對苯環供電子。再啟發學生根據上述結果,從-OH氧原子電子云密度、C-O鍵O-H鍵的電子云密度和鍵長以及苯環電子云密度的變化幾個方面分析乙醇和苯酚的結構特點,進而分析兩者的化學性質(如表3所示)。
5" 結論
電子效應的教學應當著眼于啟發學生抓住有機化學的學習規律,幫助學生徹底擺脫死記硬背的學習方法。實踐證明:電子效應采用集中教學和分散教學相結合的方法,有利于學生吃透電子效應,激發學生學習有機化學的興趣,培養學生自覺運用電子效應分析有機化學問題的良好習慣,從而使基礎有機化學的學習達到事半功倍的效果。
參考文獻:
[1]黃池寶,胡明華,曾啟華,等.有機化學中的大-電子云分析法[J].遵義師范學院學報,2015(1):93-98.
[2]朱萬強,楊媛.2,3,5,6-四氟苯基與三氟甲基苯基對噁二唑化合物光電性質影響的理論研究[J].遵義師范學院學報,2014,16(2):62-67.
[3]劉洋,林友文.有機化學中電子效應應用的教學思考[J].化工高等教育,2012(1):105-108.
[4]陳益,孫夕禮.從電子效應談把握《有機化學基礎》的學科內涵[J].化學教學,2016(5):3-7.
[5]丁萍,繆建.淺談電子效應在有機化學中的應用[J].化學教學,2011(5):52-55.
[6]黃宜祥,許招會.電子效應與波譜解析教學探討[J].光譜實驗室,2011,28(3):1249-1252.
[7]王迎進,孫金魚,趙明根.共軛效應的本質及其應用[J].化學通報,2019,82(4):368-372.
[8]趙溫濤,鄭艷,王光偉,等.有機化學(第六版)[M].北京:高等教 育出版社,2019.
[9]刑其毅,裴偉偉,徐瑞秋,等.有機化學(第四版,上下冊)[M].北京:北京大學出版社,2017.
[10]伍越寰,李偉昶,沈曉明.有機化學(第二版)[M].合肥:中國科 學技術大學出版社,2007.
(責任編輯:朱 彬)

