影響慢加急性肝衰竭短期預后的危險因素分析
巴志偉,詹步同,劉傳苗
(蚌埠醫科大學第一附屬醫院 感染性疾病科,安徽 蚌埠 233004)
肝衰竭是一組臨床常見的嚴重癥候群,可由多種因素造成,在中國慢加急性肝衰竭(acute on chronic liver failure,ACLF)是肝衰竭中最常見的類型,該病進展快,無特效治療,晚期ACLF病人病死率可達76%[1-2],預后極差。盡早準確地評估病人病情,及時有效地調整治療方案對改善預后極其重要,故本研究通過對95例不同預后ACLF病人的臨床數據進行回顧性分析,評估各個指標在ACLF病人短期預后中的價值。
1 資料與方法
1.1 一般資料
收集2018年7月至2020年12月于我院就診入院的95例ACLF病人的臨床資料,依據確診后30 d預后隨訪情況將病人分為死亡組(38例)和生存組(57例),納入病人參照《肝衰竭診治指南(2018年版)》有關ACLF診斷標準[1]。其中乙型肝炎相關64例,酒精相關19例,藥物相關4例,免疫相關3例。急性腎損傷(acute kidney injury,AKI)的診斷參照相關共識建議標準進行[3]。所有病人入院后均予以內科規范化支持治療,包括保肝降酶、利尿退黃、白蛋白及冰凍血漿輸注、核苷(酸)類似物抗病毒、必要時應用人工肝等治療。
1.2 方法
收集病人一般臨床資料,包括年齡、性別、AKI并發情況等,并記錄病人入院24 h內外周血檢驗結果,包括白細胞計數(WBC)、中性粒細胞計數(NEU)、血小板計數(PLT)、丙氨酸氨基轉移酶(ALT)、總膽紅素(TBil)、膽堿酯酶(CHE)、白蛋白(Alb)、血肌酐(SCr)、血清鈉(Na+)、三酰甘油(TG)、載脂蛋白A(ApoA)、載脂蛋白B(ApoB)、胱抑素C(Cystatin C,CysC)、凝血酶原時間(PT)、國際標準化比值(INR)、凝血酶原活動度(PTA)和D-二聚體(D-Dimer)。并計算每位病人的終末期肝病模型(model for end-stage liver disease,MELD)評分,其公式為R=3.8ln[TBil(mg/dL)]+11.2ln(INR)+9.6ln[SCr(mg/dL)]+6.4(病因:膽汁性或酒精性0,其他1)。
1.3 統計學方法
采用t檢驗、曼-惠特尼U檢驗、χ2檢驗和多因素logistic回歸分析。
2 結果
2.1 2組一般資料比較
本研究共納入95例病人,其中男81例,女14例,平均(48.57±13.68)歲。隨訪30 d期間38例死亡(死亡組),57例生存(生存組)。2組病人年齡、性別方面差異均無統計學意義(P>0.05),2組病人在并發AKI和MELD評分方面差異均有統計學意義(P<0.05)(見表1)。

表1 2組病人一般資料的比較
2.2 2組實驗室指標比較
死亡組WBC、NEU、CysC、PT、INR水平均高于生存組,TG、ApoB、PTA水平均低于生存組(P<0.05~P<0.01),PLT、ALT、TBil 、CHE、Alb、SCr、Na+、ApoA、D-Dimer在2組間差異均無統計學意義(P>0.05)(見表2)。
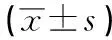
表2 實驗室指標比較
2.3 多因素logistic分析
以ACLF病人30 d隨訪結果是否死亡為因變量,將2組間單因素分析差異有統計學意義的WBC、NEU、TG、ApoB、CysC、PT、INR、PTA、并發AKI、MELD評分等指標作為自變量納入多因素logistic回歸方程,結果顯示CysC是ACLF病人短期(30 d)死亡的獨立危險因素(P<0.05)(見表3)。

表3 多因素logistic分析結果
3 討論
ACLF是一種主要發生在具有慢性肝病或肝硬化基礎病人中的急性肝損傷,以黃疸迅速加深及凝血功能障礙為主要特征,短期死亡率高[4],是威脅人類健康的重要疾病之一[5]。目前ACLF尚無特效治療,經內科積極治療等處理難以好轉者肝移植是其最佳選擇[1],但不少病人在等待移植期間因病情加重死去,未能行肝移植[6]。故早期預測病人臨床結局,制定診治方案,對降低病人病死率,改善病人預后十分關鍵。
單因素分析發現死亡組WBC、NEU、CysC、PT、INR、并發AKI情況以及MELD評分等水平顯著高于生存組,而TG、ApoB、PTA低于生存組,提示上述指標可能與ACLF病人短期預后有關。將上述單因素分析中有差異的指標納入多因素分析,結果示CysC是影響ACLF病人短期預后的獨立危險因素。
CysC作為半胱氨酸蛋白酶抑制劑,參與調控細胞內外蛋白的水解,避免細胞受到內、外源性不適當的蛋白酶水解,對細胞有一定保護作用。朱婭鴿等[7]研究發現CysC與肝纖維化密切相關,并且隨著肝炎病人肝纖維化向明顯肝纖維化、肝硬化的進展,CysC水平也逐漸升高,肝硬度值也與CysC水平成正相關。而ACLF作為一種發生在慢性肝炎、肝纖維化以及肝硬化基礎上新的肝損傷綜合征,與CysC相關的研究卻鮮見。
本文中95例ACLF病人CysC水平均高于正常水平,且死亡組與生存組間水平差異有統計學意義。CysC參與炎癥反應、抗原加工等過程,CysC水平更是與炎癥反應指標如IL-6、TNF-α以及CRP等正相關,并推進炎癥反應的發展[8]。相較于非ACLF病人,ACLF病人IL-6、TNF-α、CRP等指標水平也明顯升高,ACLF顯著特點便是具有強烈的全身炎癥反應,其反應強度更與ACLF嚴重程度平行[9]。可推測ACLF病人肝臟處于新發損傷壞死狀態下,隨著肝臟的損傷,CysC合成與表達增加并被釋放進血,導致血液CysC水平升高,肝臟損傷壞死越重,CysC水平越高。
本研究顯示死亡組發生AKI比例明顯高于生存組(P<0.05),AKI是ACLF常見并發癥,研究[10-11]指出AKI在ACLF病人發生器官衰竭中有重要影響,與病人病死率高和預后不佳密切相關,故及早診斷和干預AKI,對降低病死率和改善ACLF病人預后尤為重要。本研究發現2組病人入院時SCr值均在正常范圍,但CysC明顯異常,并在2組間差異明顯(P<0.01)。SCr作為評估腎功能最常用指標,受諸多因素影響,敏感度不高,當病人腎功能損傷約50%時SCr水平才開始變化,對AKI的診斷存在延誤[12]。而CysC是一種小分子量堿性蛋白,相對分子質量較小,生產速率穩定,廣泛存在于人體組織與體液中,其血清水平不受性別、年齡、體質量及種族等因素干擾,僅從腎小球濾過而最終清除,可通過CysC水平判斷腎小球濾過率高低[13-14],此外CysC分布容積明顯小于SCr,任何輕微的腎功能喪失,CysC都將較SCr更快上升[15],這說明CysC對AKI的預警能力優于SCr。另有研究[16]顯示CysC是發生AKI的獨立危險因素,CysC水平隨肝衰竭病情進展而升高,與本文結果一致。
綜上所述,本研究通過分析ACLF病人30 d預后指標,發現CysC較SCr更早預警ACLF病人合并腎臟損傷,且其是影響ACLF病人短期預后的獨立危險因素。

