乳酸清除率聯合磁共振彌散加權成像ADC值對一氧化碳中毒遲發性腦病的預測價值
徐一文
湖北江漢油田總醫院放射影像科,湖北省潛江市 433124
急性一氧化碳中毒(ACOP)是生產或生活中較為常見的中毒性疾病,一氧化碳(CO)與血紅蛋白結合后會導致其喪失攜氧能力,引起機體缺氧而損害各組織器官。由于中樞神經系統對缺氧最為敏感,患者在2~60d的假愈期內可能出現癡呆、反應遲鈍、譫妄等腦功能障礙,臨床稱之為一氧化碳中毒遲發性腦病(DEACMP)。DEACMP發病率為10%~40%,一旦發生則預后極差,將嚴重影響患者及其家庭的生活質量[1]。因此,盡早準確預測ACOP患者的DEACMP發生風險對指導臨床診療、改善患者預后具有重要價值。DEACMP的病機尚不完全明晰,通常認為與缺氧導致的腦組織損害有關。乳酸清除率(LCR)可反映機體的氧代謝狀態,在多種危重病預后評估中均有重要價值[2]。核磁共振彌散加權成像(MRI-DWI)檢查可通過顯示水分子的運動明確組織內結構,是臨床評價腦損傷程度的重要方法,表觀擴散系數(ADC)即是反映水分子擴散運動速度、范圍的參數[3]。基于此,本文旨在探究LCR聯合ADC值對DEACMP的預測價值,為臨床研究提供一定參考。
1 對象與方法
1.1 觀察對象 本研究為回顧性研究。選取2020年1月—2022年12月本院收治的177例ACOP患者為觀察對象。納入標準:(1)符合ACOP診斷標準;(2)ACOP病情分級為中、重度;(3)年齡18~65歲;(4)ACOP時間<7d;(5)完成LCR、MRI-DWI等檢查,且各項臨床資料清晰完整。排除標準:(1)有癲癇、腦炎、腦血管疾病、代謝性腦病、腦外傷、腦腫瘤、精神疾病既往史者;(2)因吸入其他氣體或藥物中毒者;(3)失訪或死亡者。以患者出院后60d為觀察終點,按患者是否發生DEACMP將其分為DEACMP組(n=21)和預后良好組(n=156)。
1.2 診斷標準 ACOP診斷標準:有較高濃度一氧化碳吸入史,有急性發生的中樞神經損害體征和癥狀,碳氧血紅蛋白定性試驗(HBCO)結果為陽性,在排除其他病因后,即可診斷為ACOP。DEACMP診斷標準:有明確ACOP病史;2~60d假愈期內,出現癡呆、譫妄、震顫麻痹、小便失禁、偏癱、去皮層狀態、病理反射陽性、失明、失語、繼發性癲癇、帕金森綜合征、精神癥狀等任意1項臨床表現;腦電圖檢查有中、高度異常;頭部CT檢查有病理性密度減低區[4]。
1.3 觀察指標 (1)一般資料:包括性別、年齡、體重指數(BMI)、ACOP病情分級、格拉斯哥昏迷量表(GCS)評分、昏迷時間。(2)LCR:采集入組患者治療前及治療24h后(吸氧者停止吸氧30min后)的動脈血1ml,使用全自動血氣分析儀(GEM Premier 3000,美國Instrument laboratory)檢測乳酸(Lac)水平,計算LCR。LCR=(Lac初始值-Lac復查值)/Lac初始值×100%。(3)ADC值:于患者入院后7d內,使用核磁共振掃描儀(GE Signa Twinspeed HDxt 1.5T)行顱腦檢查,掃描序列包括橫斷面和矢狀面液體衰減反轉恢復(FLAIR)序列T1WI、橫斷面和冠狀面快速恢復快速自旋回波序列(FRFSE)序列T2WI及橫斷面彌散加權成像(DWI),設置常規參數:間隔=1.5mm,層厚=5.0mm。橫斷面和矢狀面FLAIR T1WI:TR=2 078.0ms、2 257.0ms,TE=9.3ms、9.3ms;橫斷面和冠狀面FLAIR T2WI:TR=4 900.0ms、8 502.0ms,TE=99.3ms、126.0ms。DWI參數:間隔=1.5mm,層厚=5.0mm,矩陣為128×128,FOV為24cm×18cm,TR=600ms,TE=78ms,梯度場強=40mT/m,擴散梯度向正交方向X、Y、Z軸方向施加,b值=0、1 200s/mm2。利用Functool軟件對掃描圖像進行處理,對稱性測量側腦室周圍白質(頂葉、額葉、枕葉、半卵圓中心)、大腦皮層(頂葉、額葉)ADC值,ROI提取面積均為30mm2,每部位測量3個點的ADC值,計算平均ADC值(ADCav)。

2 結果
2.1 兩組一般資料比較 DEACMP組重度中毒占比明顯高于預后良好組(P<0.05),兩組性別、年齡、BMI、GCS評分及昏迷時間比較差異均無統計學意義(P>0.05)。見表1。
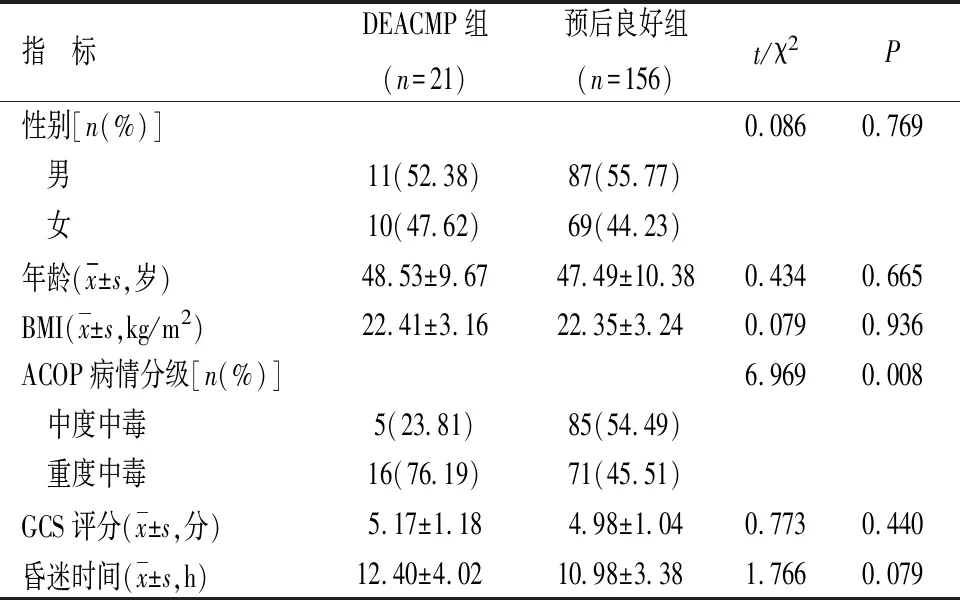
表1 兩組一般資料比較
2.2 兩組LCR及ADC值比較 DEACMP組的LCR及側腦室周圍白質ADCav值均明顯低于預后良好組(P<0.05),而兩組皮層ADCav值比較差異無統計學意義(P>0.05)。見表2。

表2 兩組LCR及ADC值比較
2.3 相關性分析 Pearson相關性分析顯示,ACOP患者的LCR與側腦室周圍白質ADCav值之間呈正相關關系(r=0.395,P<0.05);LCR與皮層ADCav值相關性不顯著(r=0.104,P>0.05)。
2.4 LCR、ADC值及其聯合預測DEACMP的ROC曲線 ROC曲線分析顯示,LCR、側腦室周圍白質ADCav值預測DEACMP的曲線下面積(AUC)分別為0.716、0.898;且以二者聯合的AUC最大,為0.979,敏感度、特異度分別為90.48%、99.00%。見表3、圖1。
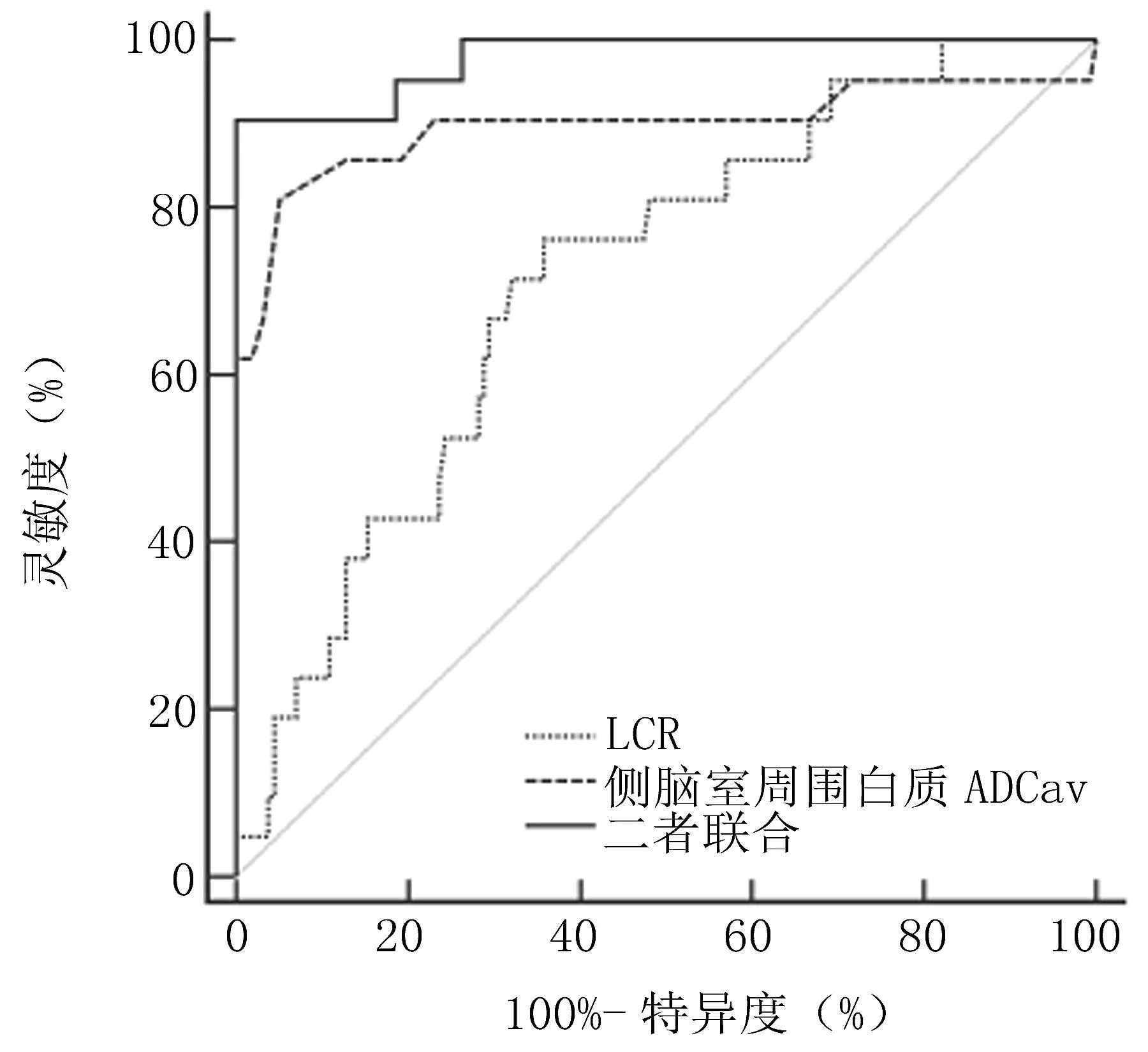
圖1 LCR、ADC值及其聯合預測DEACMP的ROC曲線

表3 LCR、ADC值及其聯合對DEACMP的預測效能
3 討論
DEACMP是ACOP的嚴重并發癥之一,以反應遲鈍、智力低下、四肢張力增高、昏迷等神經癥狀為主要臨床表現,致殘率較高,嚴重影響患者生活質量。因此,對ACOP患者是否發生DEACMP予以早期、準確的預測,科學指導臨床診療,對防治DEACMP顯得尤為重要。本文中,DEACMP的發生率為11.86%,處于既往研究報道的DEACMP發生率范圍內[1]。
腦組織對缺氧的耐受力極差,ACOP引起的缺氧是造成腦組織病變的重要原因。提高機體氧含量、清除有害氣體是臨床ACOP治療的重要環節。Lac作為無氧糖酵解的終末產物,其濃度升高是機體組織缺氧及灌注不足的敏感指標。Lac水平增高常提示機體出現缺氧、氧代謝障礙等問題。因而連續監測Lac水平可反映機體缺氧等問題改善情況。因此,檢測患者LCR可以更準確地評價治療反應,LCR越高提示Lac清除得越快,患者恢復越好,可用作預后評估指標[5]。本文結果顯示,DEACMP組的LCR明顯低于預后良好組,提示LCR越低,ACOP患者越有可能發生DEACMP,這可能與LCR越高的患者機體氧合、組織灌注等功能恢復的越高,腦組織受損程度越輕有關,與既往研究[6]結果基本一致。
MRI-DWI是臨床評估腦組織損傷程度的重要檢查手段,可通過水分子的運動明確組織內結構,通過DWI信號強度計算ADC,反映組織結構在不同狀態下的差異,為疾病早期診斷提供細致、多樣的信息。腦缺氧發生后,腦組織無氧代謝比重增加,Lac等酸性代謝產物大量堆積,將破壞血—腦脊液屏障,增加血管通透性,引起細胞毒性水腫,限制腦組織內水分子的擴散能力,因而在DWI上表現為高信號、ADC值降低[7]。本文結果顯示,DEACMP組的側腦室周圍白質ADCav值均明顯低于預后良好組,這可能與ACOP可引起大腦白質出現廣泛性變質、脫髓鞘斑塊等有關,導致ADC值降低。基礎研究證實,腦組織損害嚴重的模型兔存在腦部局灶出血、嗜神經、脫髓鞘等病理改變[8]。腦白質聚集了大量神經纖維,是重要的中樞神經系統組成部分,腦白質受損可引起認知障礙、運動障礙等一系列神經癥狀,因而腦白質受損越嚴重,患者發生DEACMP的風險也就越大。但本文中,兩組大腦皮層ADCav值比較無明顯差異,這可能與DEACMP主要累及大腦白質區有關。
本研究進一步將LCR、側腦室周圍白質ADCav值用于DEACMP的早期預測,ROC曲線分析顯示,LCR、側腦室周圍白質ADCav值預測DEACMP的AUC分別為0.716、0.898;且以二者聯合的AUC最大,達到0.979,敏感度、特異度分別為90.48%、99.00%,明顯高于單項指標應用,表明LCR、側腦室周圍白質ADCav值聯合應用對DEACMP的發生具有較高預測效能。
綜上所述,LCR、側腦室周圍白質ADCav及其二者聯合均對DEACMP具有一定預測價值,以二者聯合應用價值最高,臨床應重點關注LCR、側腦室周圍白質ADCav值較低的ACOP患者,積極采取防治措施以期改善預后。

