智能運動康復訓練儀對急性心肌梗死經皮冠狀動脈介入術后患者心肺功能和心室重構的影響
汪微微,王晶晶,米亞非
浙江省臺州醫院 (浙江臨海 317000)
急性心肌梗死(acute myocardial infarction,AMI)是心內科常見的急重癥,主要表現為持久的胸骨后疼痛。如不及時治療,患者可出現心力衰竭、惡性心律失常、休克或猝死等并發癥[1]。經皮冠狀動脈介入(percutaneous coronary intervention,PCI)是治療AMI 患者的首選手段,能在較短時間內恢復AMI 患者的心肌血供,降低其病死率,但術后患者易出現心室重構,影響心肺功能[2]。近年來,循證醫學證據表明,運動訓練可顯著改善缺血性心臟病患者的預后[3]。智能運動康復訓練儀是一種智能化的下肢康復訓練系統,具有類似腳踏車運動的連續旋轉運動訓練模式,逐漸被應用于AMI 介入術后患者中,并取得了較好的效果[4]。基于此,本研究旨在探討智能運動康復訓練儀對AMI 介入術后患者心肺功能和心室重構的影響,現報道如下。
1 資料與方法
1.1 一般資料
選取2018 年9 月至2021 年2 月于浙江省臺州醫院住院治療的78 例AMI 介入術后患者為研究對象,采用隨機雙盲法分為對照組與試驗組,各39 例。對照組男24 例,女15 例;年齡41~85 歲,平均(64.91±5.78)歲;病程3~11 h,平均(5.51±0.69)h;其中,冠脈病單支病變24 例,多支病變15 例。試驗組男22 例,女17 例;年齡42~86 歲,平均(65.16±5.23)歲;病程4~12 h,平均(5.46±0.74)h;其中,冠脈病單支病變21 例,多支病變18 例。兩組一般資料比較,差異無統計學意義(P>0.05),具有可比性。
納入標準:符合《急性心肌梗死診斷和治療指南》中AMI 診斷標準[5];經冠狀動脈造影證實;患者有行急診PCI 治療的指征;術后生命體征平穩。排除標準:以往有明顯的心肺疾病;有溶栓、PCI治療、冠脈搭橋史;PCI 治療后生命體征不穩定。
1.2 方法
對照組術后予日常活動干預:術后第2 天,囑患者臥床休息,指導患者進行肢體關節被動運動,包括肩、肘、腕、踝、膝及手指等部位,10~20 min/次,3 次/d;術后第3 天,囑患者下床活動,進行床邊站立、攙扶行走等訓練;術后第3~4 天,囑患者開展室內步行鍛煉,3~5 min/次;術后第5~7 天,囑患者進行上、下樓梯訓練。
試驗組術后在對照組基礎上應用智能運動康復訓練儀(南京康龍威科技實業有限公司,型號:KLW-SKF4)干預。應用扎帶固定患者雙下肢,用小腿支架支撐下肢,選擇心肺模式。設定參數:頻率為50 Hz,轉速20 r/min,阻力等級5 級,并在干預過程中逐漸提高轉速及阻力等級。30 min/次,2~3 次/周。
兩組均連續干預8 周。
1.3 評價指標
(1)心肺功能:干預前后,采用心肺功能測定儀(瑞士席勒公司,型號:CS-200)進行評估,包括最大攝氧量(maximal oxygen consumption,VO2max)、最大每搏攝氧量(maximal oxygen consumption/heart rate,VO2max/HR)和最大代謝當量(maximum metabolic equivalent,METmax)。(2)心室重構指標:干預前后,采用心臟彩超(德國西門子公司,型號:SC2000)進行測量,包括左心室射血分數(left ventri cular ejection fraction,LVEF)、 左 心室收縮末期容積(left ventricle end systolic volume,LESV)、左心室舒張末期容積(left ventricular end diastolic volume,LEDV)和左心室短軸縮短率(shortening rate of short axis of left ventricle,FS)。
1.4 統計學處理
采用SPSS 18.0 統計軟件進行數據處理,計量資料以±s表示,采用t檢驗。計數資料以率表示,采用χ2檢驗。P<0.05 為差異有統計學意義。
2 結果
2.1 心肺功能
干預前,兩組VO2max、VO2max/HR 和METmax比較,差異無統計學意義(P>0.05);干預后,兩組VO2max、VO2max/HR 和METmax均高于干預前,且試驗組高于對照組(P<0.05),見表1。
表1 兩組干預前后VO2max、VO2max/HR和METmax 比較(±s)
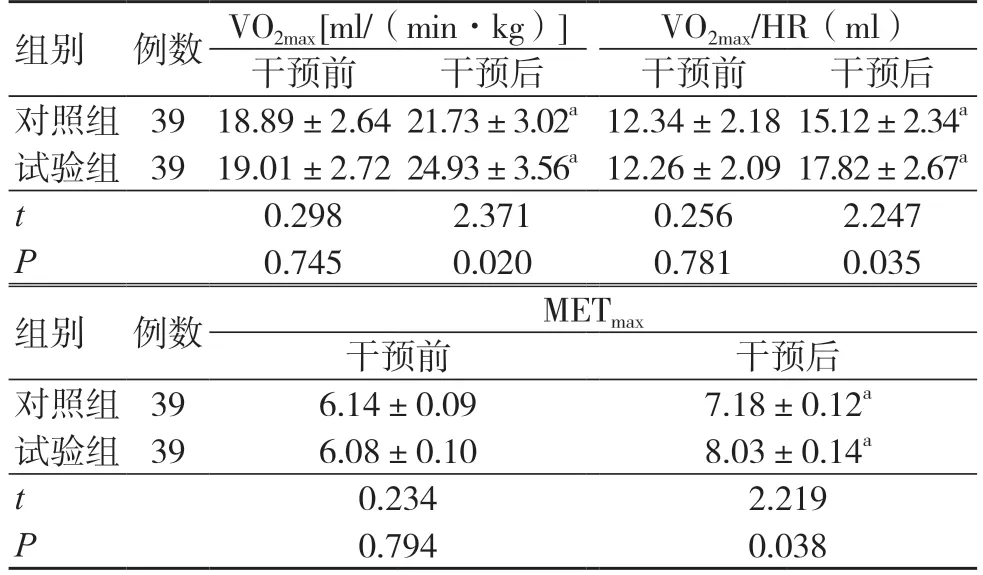
表1 兩組干預前后VO2max、VO2max/HR和METmax 比較(±s)
注:與同組治療前比較,aP<0.05;VO2max 為最大攝氧量;VO2max/HR 為最大每搏攝氧量;METmax 為最大代謝當量
組別 例數 VO2max [ml/(min·kg)] VO2max/HR(ml)干預前 干預后 干預前 干預后對照組 39 18.89±2.64 21.73±3.02a 12.34±2.18 15.12±2.34a試驗組 39 19.01±2.72 24.93±3.56a 12.26±2.09 17.82±2.67a t 0.298 2.371 0.256 2.247 P 0.745 0.020 0.781 0.035組別 例數 METmax干預前 干預后對照組 39 6.14±0.09 7.18±0.12a試驗組 39 6.08±0.10 8.03±0.14a t 0.234 2.219 P 0.794 0.038
2.2 心室重構指標
干預前,兩組LVEF、LESV、LEDV 和FS 比較,差異無統計學意義(P>0.05);干預后,兩組LVEF 和FS 均高于干預前,LESV 和LEDV 均低于干預前,且試驗組LVEF 和FS 均高于對照組,LESV 和LEDV 均低于對照組(P<0.05),見表2。
表2 兩組干預前后LVEF、LESV、LEDV和FS 比較(±s)

表2 兩組干預前后LVEF、LESV、LEDV和FS 比較(±s)
注:與同組治療前比較,aP <0.05;LVEF 為左心室射血分數;LESV 為左心室收縮末期容積;LEDV 為左心室舒張末期容積;FS 為左心室短軸縮短率
組別 例數 LVEF(%) LESV(ml)干預前 干預后 干預前 干預后對照組 39 51.45±9.04 55.45±9.12a 132.45±20.26 106.35±17.12a試驗組 39 50.93±8.07 59.03±9.72a 134.10±19.27 94.08±17.20a t 0.356 2.397 0.297 2.416 P 0.724 0.019 0.730 0.018組別 例數 LEDV(ml) FS(%)干預前 干預后 干預前 干預后對照組 39 168.24±24.16 147.24±20.45a 19.12±2.89 24.27±3.04a試驗組 39 167.79±23.07 133.46±19.13a 19.27±2.95 28.10±3.35a t 0.312 2.376 0.278 2.341 P 0.739 0.020 0.757 0.022
3 討論
隨著心血管介入醫學的不斷發展,PCI 術已成為AMI 的主要治療方法,但術后易發生心臟收縮舒張功能異常,進而誘發心力衰竭、惡性心律失常或心源性猝死等心血管不良事件[6]。由于PCI 術中僅將狹窄的罪犯血管進行疏通恢復血流,并不能根除AMI 患者冠狀動脈斑塊的病理基礎,難以從而根本上逆轉動脈斑塊發生、發展的進程;同時,由于PCI 術無法修復已發生壞死的心肌組織,且易出現心肌再灌注損傷,術后患者可因非梗死區及梗死區纖維組織增生,進一步引起心肌纖維化和心室重構,影響患者心肺功能的恢復,甚至可引發血栓、冠脈再狹窄等并發癥[7]。
近年來,運動鍛煉對心肌梗死后心臟的保護效應及相關機制是心臟運動康復的研究熱點[8-9]。研究表明,運動訓練可減輕左心室重塑作用,提高心肌細胞線粒體能量供應,加快心臟血管的舒張,有利于微血管的再生,從而實現對梗死心臟的保護作用,并可在降低心血管病病死率及改善患者生命質量等方面獲得確切受益[10-11]。智能運動康復訓練儀是一種智能化的模擬康復運動儀器,主要通過完全的模擬人體運動增加全身肌力,不僅可提高機體的基礎代謝率,達到增加運動耐力及提高生命質量目的,同時可提高心臟前后壓力負荷,促進人體的血液循環供應,從而維持心肌氧供需的平衡,改善患者的心血管機能[4,12]。本研究結果顯示,干預后,試驗組VO2max、VO2max/HR 和METmax均高于對照組(P<0.05);干預后,試驗組LVEF 和FS 均高于對照組,LESV 和LEDV 均低于對照組(P<0.05)。表明智能運動康復訓練儀不僅可提高AMI 介入術后患者的心肺功能,且可改善其心室重構。分析其原因可能為,智能運動康復訓練儀通過提升患者心臟壓力負荷,可促進血液循環,增加心肌供氧量,改善術后心肌能量代謝,提高線粒體功能,從而可在一定程度上改善或逆轉心室重構過程,提高患者心肺功能[13-14]。
綜上所述,智能運動康復訓練儀不僅可提高AMI介入術后患者的心肺功能,而且可改善其心室重構。

