曲妥珠單抗聯合SOX方案治療進展期胃癌的效果及對患者血清腫瘤標志物水平的影響
戶軍燕 邱作棟 周 寧 于 婷
作者單位:450000 鄭州大學第五附屬醫院
胃癌(gastric cancer,GC)是指在各種致癌因子和高危因素作用下胃黏膜上皮細胞發生異常增生的消化道惡性腫瘤疾病[1],早期無明顯癥狀,大多數患者確診時已處于進展期,錯過了手術治療的最佳時間,即使行手術治療仍存在50%~70%的復發率和30%的5年生存率,整體預后較差[2-3]。故如何提高進展期胃癌(advanced GC,AGC)患者的手術效果,延長生存期成為當前研究的重點。目前多推薦替吉奧聯合奧沙利鉑的SOX方案作為新輔助化療的手段,其對殺傷腫瘤細胞,延緩病情進展的作用顯著,但也存在惡心嘔吐、腹瀉等不良反應[4-5],因此臨床上多采用SOX方案聯合放療、靶向治療、免疫治療等來減少不良反應的發生,提高治療效果。有研究表明[6],存在25%~30%的AGC患者表現人表皮生長因子受體-2(human epidermal growth factor receptor-2,HER-2)陽性表達,其與腫瘤細胞的增殖、分化、浸潤、遷移等密切相關,故其治療方案的選擇以作用于HER-2靶向的抗癌藥物聯合SOX方案較為適宜。基于此,本研究選用曲妥珠單抗聯合SOX方案來探究其對AGC患者的療效,以期為臨床實踐提供新的參考。
1 資料與方法
1.1 一般資料
將2021年1月至2023年2月期間本院收治的68例AGC患者納入研究,并按隨機數字表法將符合下列標準的患者分成對照組(34例)和研究組(34例),2組一般資料無明顯差異(P>0.05)。見表1。
表1 2組一般資料的對比
納入標準:①符合2020版《胃癌診治難點中國專家共識》[7]中AGC的標準并經病理活檢確診;②參照《胃癌HER-2檢測指南》[8]中染色評分標準確診為HER-2陽性AGC;③年齡20~75歲,首次接受新輔助化療;④過去3個月未接受其他抗腫瘤治療;⑤預計生存時長>3個月;⑥患者對本研究知情同意。
排除標準:①存在免疫疾病、凝血功能異常、心腎功能不全、惡性腫瘤等疾病;②存在精神障礙或溝通困難;③不耐受本研究所選治療藥物;④存在化療禁忌證;⑤存在胃部手術史或消化道大出血、消化道穿孔等并發癥;⑥中途退出或依從性較差者。倫理委員會已批準本研究。
1.2 治療方法
對照組應用SOX方案治療。每個療程第1天給予靜脈滴注奧沙利鉑130 mg/m2+5% 500 ml葡萄糖溶液,3 h內輸注完成;第1~14天給予口服替吉奧,劑量據體表面積調整:S體表<1.25 m2,每次40 mg;1.25 m2≤S體表<50 m2,每次50 mg;S體表≥1.50 m2,每次60 mg,每日2次(早、晚飯后口服)。21 d為1個療程,連續治療4個療程。研究組應用曲妥珠單抗聯合SOX方案治療,SOX方案的治療方法同對照組,在此基礎上給予靜脈滴注曲妥珠單抗+0.9% 250 ml氯化鈉溶液,首次劑量為8 mg/kg,時長為90 min,而后以6 mg/kg的劑量維持治療,每周1次,連續服用12 w。
1.3 觀察指標
1.3.1 短期療效 參照RECIST1.1進行療效評價[9]。①完全緩解(CR):癥狀、體征和腫瘤病灶基本消失,維持時間>4周;②部分緩解(PR):癥狀、體征有所緩解,病灶直徑減小≥30%;③病情穩定(SD):癥狀、體征無明顯改善,病灶直徑減小<30%或增加≤20%;④疾病進展(PD):癥狀、體征無明顯改善甚至加重,病灶直徑增加>20%或產生新病灶;⑤總有效率(ORR)=(CR例數+PR例數)/總例數×100%。
1.3.2 血清腫瘤標志物 分別于治療前后空腹采集靜脈血3 ml,置于抗凝管后行3000 r/min離心處理10 min,取上層血清于-75 ℃下冷藏保存。應用電化學發光法檢測糖類抗原724(Carbohydrate antigen 724,CA724)、癌胚抗原(Carcinoembryonic antigen,CEA)、糖類抗原199(Carbohydrate antigen 199,CA199)水平。1.3.3 免疫功能 分別于治療前后采集靜脈血,離心處理后應用酶聯免疫吸附法檢測免疫球蛋白A(Immune globulin A,IgA)、免疫球蛋白G(IgG)、免疫球蛋白M(IgM)水平。
1.3.4 藥物毒副作用發生情況 參考CTCAE v4.0藥物不良事件評價標準[10],記錄2組惡心嘔吐、胃腸道反應、骨髓抑制、肝功能異常、外周神經毒性、貧血、心臟毒性、白細胞減少等藥物毒副作用的發生率。
1.4 統計學方法
2 結果
2.1 2組短期療效的對比
研究組的ORR率為67.65%,高于對照組的41.18%(χ2=4.802,P=0.028)。見表2。

表2 2組短期療效的對比(例,%)
2.2 2組血清腫瘤標志物水平的對比
治療后,2組的血清CA724、CEA、CA199水平均低于同組治療前,且研究組低于對照組(P<0.05)。見表3。
表3 2組血清腫瘤標志物水平的對比
2.3 2組免疫功能的對比
治療后,2組的IgA、IgG、IgM水平均低于同組治療前,但研究組高于對照組(P<0.05)。見表4。
表4 2組免疫功能的對比
2.4 2組藥物毒副作用發生率的對比
2組各項藥物毒副作用的發生率無明顯差異(P>0.05)。見表5。
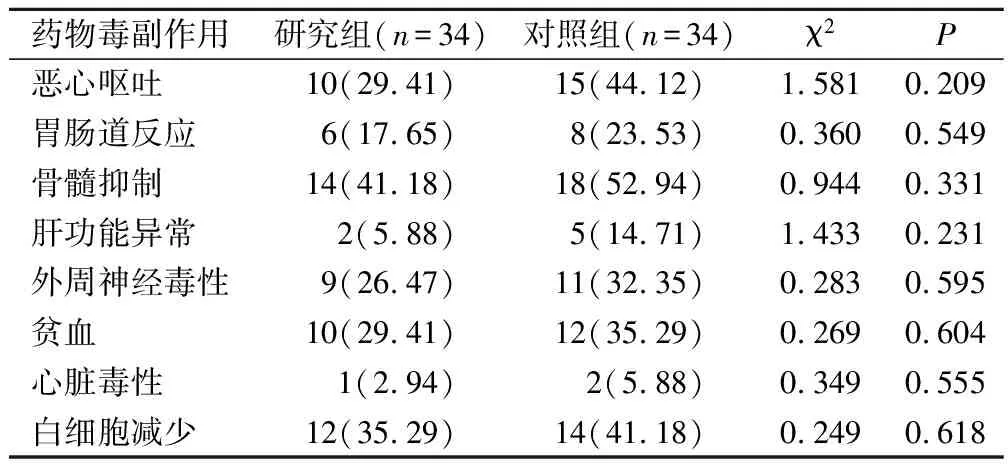
表5 2組藥物毒副作用發生率的對比(例,%)
3 討論
近年隨著社會經濟發展、生活方式改變和飲食結構調整,消化系統疾病發生的危險因素普遍暴露,GC的發生率也呈現逐年上升的趨勢,其中以病情較為嚴重的AGC最為多見,對患者的生命健康造成嚴重威脅[11]。AGC患者已失去手術根治的最佳時機,較多研究指出[12],新輔助化療在縮小病變范圍,降低腫瘤分期,提高手術切除率,延長患者生存時間方面發揮重要作用。奧沙利鉑聯合替吉奧的SOX方案是最常用的新輔助化療方案,二者聯合更能顯著抑制DNA的復制和轉錄,提高抑癌效果,但也會增加藥物毒副作用,降低治療依從性[4,12]。而有研究指出[13],靶向治療輔助SOX方案能顯著提高治療效果,加之HER-2靶點在AGC中具有較高的特異性和敏感性,故選用靶向HER-2的分子靶向藥物即曲妥珠單抗較為適宜。為了探究曲妥珠單抗聯合SOX治療AGC的效果,本文開展此次研究。
本研究結果顯示,治療后研究組總有效率和疾病控制率均高于對照組,結果表明曲妥珠單抗聯合SOX方案相比于單用SOX方案治療AGC的療效更加顯著。其原因在于SOX方案聯合兩種化療藥物,抗癌作用顯著;HER-2屬原癌基因,與配體結合后可激活酪氨酸激酶活性,介導多種通路參與調節細胞的增殖、分化、遷移過程,而曲妥珠單抗為人源化單克隆抗HER-2抗體,能特異性抑制HER-2基因表達,阻斷其介導的信號轉導和轉錄過程來發揮抑制癌細胞增殖的作用[14]。兩種方案的聯合更能發揮協同效應,進一步提高抗腫瘤效果。
治療后2組的血清CA724、CEA、CA199水平均低于同組治療前,且研究組低于對照組。CA724屬高分子糖蛋白,其在消化系統腫瘤中呈異常高表達;CEA多分布于內胚葉起源的消化系統癌,其表達水平與GC的發生呈顯著正相關;CA199屬低聚糖腫瘤相關抗原,分布于消化系統的上皮組織,在GC患者中呈高表達[15]。本研究結果提示曲妥珠單抗聯合SOX方案更能顯著降低AGC患者的血清中腫瘤標志物水平,提高抗癌效應。
治療后2組的IgA、IgG、IgM水平均低于同組治療前,而研究組的水平高于對照組。蔣世海等[16]研究指出,腫瘤細胞和化療藥物副作用均會對機體的免疫功能造成損傷,上述指標水平與免疫功能呈正相關。治療后2組指標均下降表明SOX化療方案會損傷患者的免疫功能,而研究組高于對照組則提示聯合曲妥珠單抗能降低化療所致的免疫抑制效應,維護機體安全。除此之外,2組藥物毒副作用發生率無明顯差異。提示曲妥珠單抗聯合SOX方案不會顯著增加不良反應的發生,應用較安全,也從側面證明了曲妥珠單抗的免疫保護作用,與楊喬等[17]研究結果相一致,進一步證實了本研究方案的安全性。
綜上所述,曲妥珠單抗聯合SOX方案治療AGC的效果顯著,對于降低患者血清腫瘤標志物水平,減弱化療對機體的免疫抑制作用,減少藥物毒副作用的發生均具有重要作用,值得在臨床上廣泛應用。

