MnSOD基因Val16Ala多態性與前列腺癌骨轉移患者易感性的關系
孫俊紅 張方方 張麗媛 李雷花
作者單位:457000 河南省濮陽市人民醫院
前列腺癌疾病屬于臨床上常見的上皮性惡性腫瘤,主要發生于男性生殖系統。近幾年,隨著人們生活方式及飲食習慣的變化,前列腺癌疾病的發生率逐漸增加[1]。晚期前列腺癌患者發生骨轉移的幾率比較大,前列腺癌骨轉移患者并發骨痛,嚴重情況下,可能引起病理性骨折,影響其生活質量[2]。前列腺癌骨轉移疾病的發病原因備受關注。目前,大多數研究學者表示前列腺癌骨轉移疾病的發生主要與遺傳及環境因素有關[3]。相同環境下,不同個體前列腺癌骨轉移的發病風險也存在差異性,進一步表明遺傳因素屬于前列腺癌骨轉移易感性關鍵原因[4]。目前關于基因多態性與前列腺癌易感性相關的研究較多[5-6],但是其潛在發病機制尚且不清楚。機體正常情況下,錳超氧化物歧化酶(MnSOD)主要通過清除機體內多于的氧物質,目的為維持氧化-還原系統,但是若此系統被破壞,ROS過剩,引起氧化應激反應,最終促進腫瘤疾病發展[7]。研究證實,MnSOD基因Ala多態性與多種腫瘤發病風險有關,如食管癌[8]、乳腺癌[9]、前列腺癌[10]等,尤其前列腺癌。但關于MnSOD基因Ala多態性與前列腺癌骨轉移發病關系值得探討。
1 材料與方法
1.1 研究對象
選擇本院腫瘤科2019年3月至2021年3月前列腺癌患者94例為研究對象。納入標準:①本研究納入的研究對象均中華醫學會泌尿外科分會符合《2019版EAU前列腺癌指南更新摘要》中關于前列腺癌疾病的診斷標準[11];②均為首次確診的患者;③以往均未采用去勢或者藥物治療;③年齡均在50-80歲;④前列腺癌分期均≥M1b期;⑤均無心、肝、腎等疾病重要臟器障礙的患者;⑥臨床資料完整。排除標準:①既往存在精神異常的患者;②合并嚴重骨折疾病史者;③合并血液系統類、代謝性類疾病史者;④其他部位合并惡性腫瘤的患者;⑤既往具有腫瘤手術史的患者。本研究納入對象均簽署對研究的知情同意書且研究設計符合《赫爾辛基宣言》。根據患者是否發生骨轉移進行分組,將發生骨轉移的前列腺癌患者作為骨轉移組,將未發生骨轉移的前列腺癌患者作為前列腺癌組。收集入組研究對象年齡、病程、TNM分期、體質量指數等臨床資料。
前列腺癌骨轉移的診斷標準[12]:根據《2011版中國泌尿外科疾病診斷治療指南》,即①患者存在明顯的臨床癥狀,如排尿困難、血尿以及骨轉移造成的臨床癥狀;②經腫瘤標記物證實;③均經過直腸指診、B超、CT以及MRI等檢查存在腫塊;④經穿刺活檢病理證實,且骨掃描顯示具有至少1處的骨轉移病灶。
1.2 研究方法
1.2.1 主要儀器與試劑 主要儀器:-80 ℃冰箱(澳柯瑪生物醫療,DW-86L290);PCR儀(美國/Thermo Scientific,PikoReal);DNA提取試劑盒(美國/MP Biomedicals,50 preps);MnSOD基因引物設計及合成(美國BLP,Dr.Oligo);主要試劑:溴化乙錠(鈺博生物,1.5 mL);3%瓊脂糖(雅吉,1 g)。
1.2.2 MnSOD基因多態性檢測 入院當天抽取肘部靜脈血溶液2~5 ml,置于-80 ℃冰箱,酚-氯仿抽取基因DNA,聚合酶鏈式反應-限制性片段長度多態法(PCR-RFLP)檢測基因型。Primer Premier 5.0設計引物,上游引物:5'-CAGATGTAGTGGTTAGCGCC-3';下游引物:5'-CATGGATTGCGCTTAAGGGC-3';PCR反應條件:94 ℃預變性3 min,94 ℃變性30 s,58.5 ℃退火45 s,72 ℃延伸7 min。采用3%瓊脂糖凝膠電泳檢測酶切產物,溴化乙錠染色,數碼凝膠成像系統確定MnSOD基因Val16Ala基因型。
1.3 統計學分析
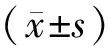
2 結果
2.1 兩組臨床資料比較
前列腺癌患者發生骨轉移40例,即骨轉移組40例,未發生骨轉移患者為前列腺癌組54例。兩組年齡、病程、TNM分期、體質量指數等臨床資料比較,差異無統計學意義(P>0.05),見表1。
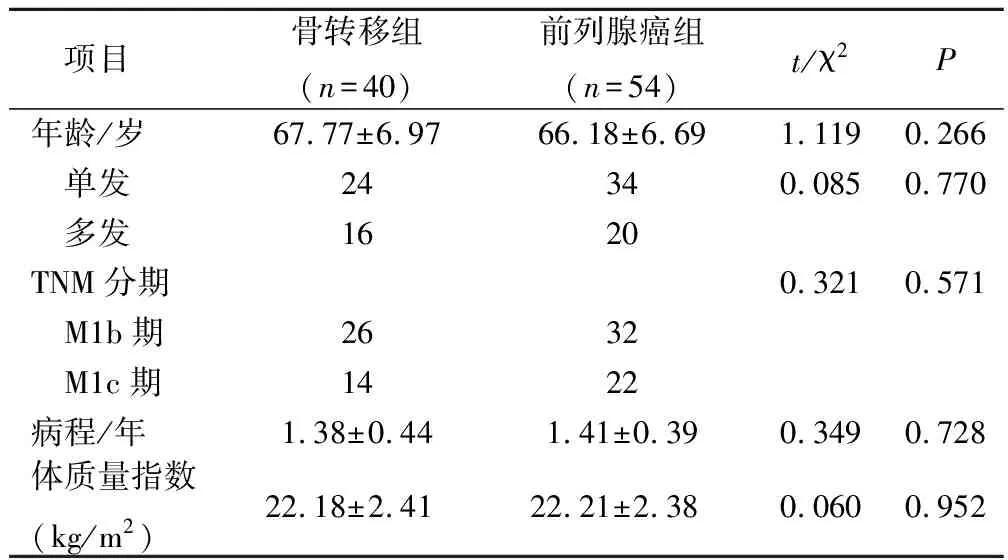
表1 兩組臨床資料比較
2.2 兩組MnSOD基因Val16Ala遺傳平衡檢驗
骨轉移組和前列腺癌組MnSOD基因Val/Val、Val/Ala和Ala/Ala基因型實際頻數和理論頻數分布比較,差異無統計學意義(P>0.05),見表2。
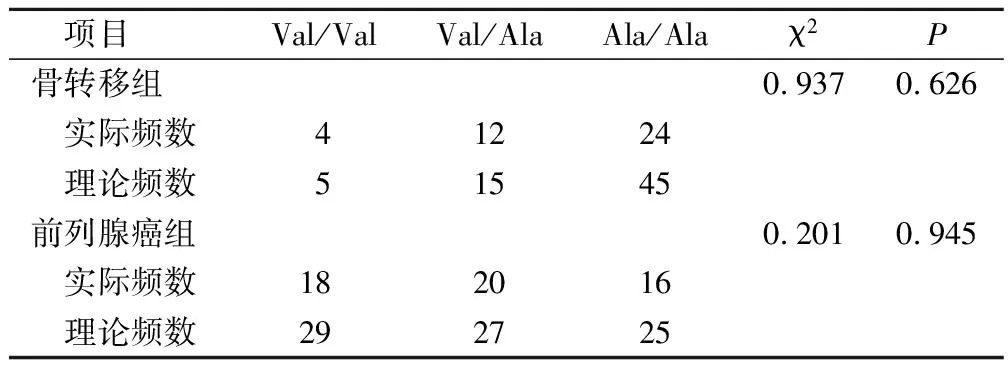
表2 兩組MnSOD基因Val16Ala遺傳平衡檢驗
2.3 兩組MnSOD基因Val16Ala多態性分布比較
骨轉移組MnSOD基因Ala/Ala基因型、Ala等位基因頻率高于前列腺癌組,Val/Val基因型頻率、Val等位基因頻率低于前列腺癌組,差異具有統計學意義(P<0.05),見表3。
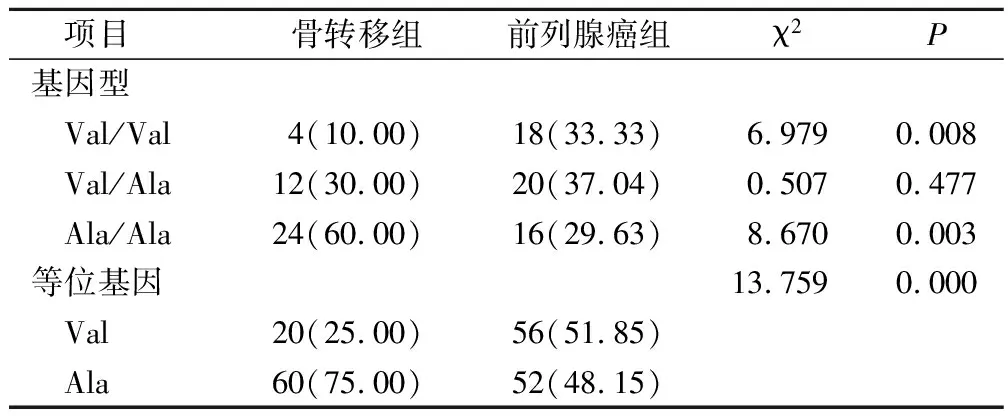
表3 兩組MnSOD基因Val16Ala多態性分布比較(例,%)
2.4 攜帶不同基因型前列腺癌骨轉移患者臨床特征比較
MnSOD基因Val16Ala基因型與前列腺癌骨轉移患者PSA、年齡以及Gleason評分無關(P>0.05);TNM分期為Ⅲ~Ⅳ期患者Ala/Ala比例[75.00%(18/24)]顯著高于Ⅰ~Ⅱ期患者[37.5%(6/16)](P<0.05)。見表4。
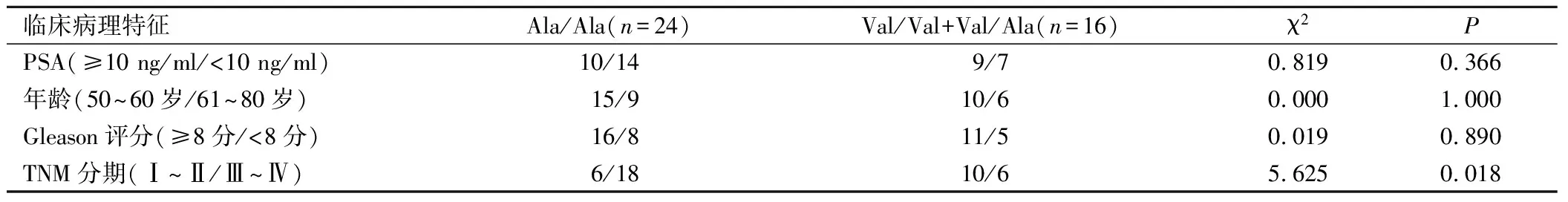
表4 攜帶不同基因型前列腺癌骨轉移患者臨床特征比較/例
3 討論
關于腫瘤遺傳易感性屬于目前研究熱點。尤其關于MnSOD基因多態性與腫瘤疾病之間的關系受到越來越多研究學者的關注,發現MnSOD基因多態性可以參與多種腫瘤疾病進展,如前列腺癌[13]、肝癌[14]以及肺癌[15]等。MnSOD主要來源于線粒體,屬于一類較為關鍵的抗氧化酶,主要將O2-轉化氧化為H2O2,再經過氧化酶等物質的轉化,最終分解為水及氧氣,使細胞表現為無毒化[16]。MnSOD基因表達水平下降后,ROS濃度上升,引起細胞內DNA、脂質等水平異常增加,進一步導致正常細胞出現異常分化,同時促進腫瘤疾病的發生和發展。MnSOD基因啟動子區域處16號位點,T轉為C,可引起Val轉為Ala,無法有效清除線粒體內ROS物質,從而促進腫瘤進展。
前列腺癌屬于男性好發疾病,目前,已有多項研究證實了MnSOD基因Val16Ala多態性與前列腺癌易感性存在關系,但是也有研究表明兩者無關系,同時MnSOD基因Val16Ala多態性與前列腺癌骨轉移之間的關系研究報道不多。由此,本次研究分析了MnSOD基因Val16Ala多態性與前列腺癌骨轉移患者的關系。結果顯示,骨轉移組MnSOD基因Ala/Ala基因型、Ala等位基因頻率高于前列腺癌組,Val/Val基因型頻率、Val等位基因頻率低于前列腺癌組,差異具有統計學意義(P<0.05),提示MnSOD基因Ala等位基因突變可能促進前列腺癌骨轉移疾病的發病風險,此基因rs16位點單核苷酸多態性與疾病進展有關,也可能是前列腺癌骨轉移疾病發生和發展的遺傳因素之一,MnSOD是SOD調節的關鍵酶,Ala等位基因可能通過干擾MnSOD酶的活性進而影響前列腺癌骨轉移疾病的發生和發展。張超賢等人的研究中[17],研究顯示MnSOD基因攜帶Ala基因的頻率在Ⅲ~Ⅳ期患者明顯高于Ⅰ~Ⅱ期,其研究結果與本次研究結果具有一致性。另外在WIKLUND的研究中[18],研究顯示MnSOD基因多態性與前列腺癌發病風險無關,與本次研究存在一定差異性,分析其原因可能與種族、樣本量不同存在關系。
綜上所述,MnSOD基因Val16Ala多態性與前列腺癌骨轉移患者易感性存在關系,可能存在促進前列腺癌發生骨轉移的作用。但是本研究也存在不足,關于遺傳因素與前列腺癌骨轉移之間的關系還需要大樣本、多中心的隨機對照研究,以進一步提高研究結果的準確性,同時為預防以及控制前列腺癌骨轉移提供理論依據。

