減肥藥物及相關(guān)靶點(diǎn)研究進(jìn)展
陳弋,王鵬源,劉霞,孫旸
(海軍軍醫(yī)大學(xué)/第二軍醫(yī)大學(xué),上海 200433)
肥胖是體內(nèi)局部或總體脂肪過(guò)度堆積或異常堆積的一種慢性代謝性疾病。近期,一項(xiàng)10萬(wàn)多人隊(duì)列分析顯示:肥胖與21種疾病密切相關(guān),廣泛涉及心血管、消化、呼吸、神經(jīng)、肌肉、骨骼等系統(tǒng)乃至傳染病[1]。據(jù)報(bào)道,肥胖人群患有≥4種肥胖相關(guān)疾病(復(fù)雜共病)的風(fēng)險(xiǎn)約為體重正常人群的12.39倍,且患病年齡大大提前[1],并且肥胖可引起3~8年的壽命縮短[2]。另有研究表明,亞洲人在同等體重指數(shù)(body mass index,BMI)下更易患2型糖尿病和心血管疾病[3]。因此中國(guó)對(duì)于肥胖的判斷更為嚴(yán)格,BMI>24即為超重,BMI>28屬于肥胖,而歐美國(guó)家則將BMI>25定為超重,BMI>30為肥胖。在2022年世界肥胖日,世界衛(wèi)生組織(World Health Organization,WHO)公布顯示:目前全球已有超過(guò)10億人肥胖。而根據(jù)《2020年我國(guó)居民營(yíng)養(yǎng)與慢性病狀況報(bào)告》顯示,我國(guó)城鄉(xiāng)各年齡組居民超重肥胖率繼續(xù)上升,有超過(guò)一半的成年居民超重或肥胖,6~17歲、6歲以下兒童青少年超重肥胖率分別達(dá)到19%和10.4%。肥胖患者逐年增多,給社會(huì)的經(jīng)濟(jì)和醫(yī)療都造成了嚴(yán)重的負(fù)擔(dān)。
1 肥胖的發(fā)生機(jī)制
在正常條件下,機(jī)體的能量攝入和能量消耗處于一種動(dòng)態(tài)平衡的狀態(tài)(見(jiàn)圖1)。當(dāng)能量攝入大于能量消耗,即能量失調(diào)時(shí),多余能量在體內(nèi)蓄積,引起脂肪細(xì)胞內(nèi)以甘油三酯為主的脂質(zhì)積累,過(guò)多的脂肪還會(huì)被分配到機(jī)體各個(gè)部位造成局部體態(tài)的變化,并伴有肝臟、肌肉等組織器官體積增加,最終導(dǎo)致肥胖的發(fā)生。
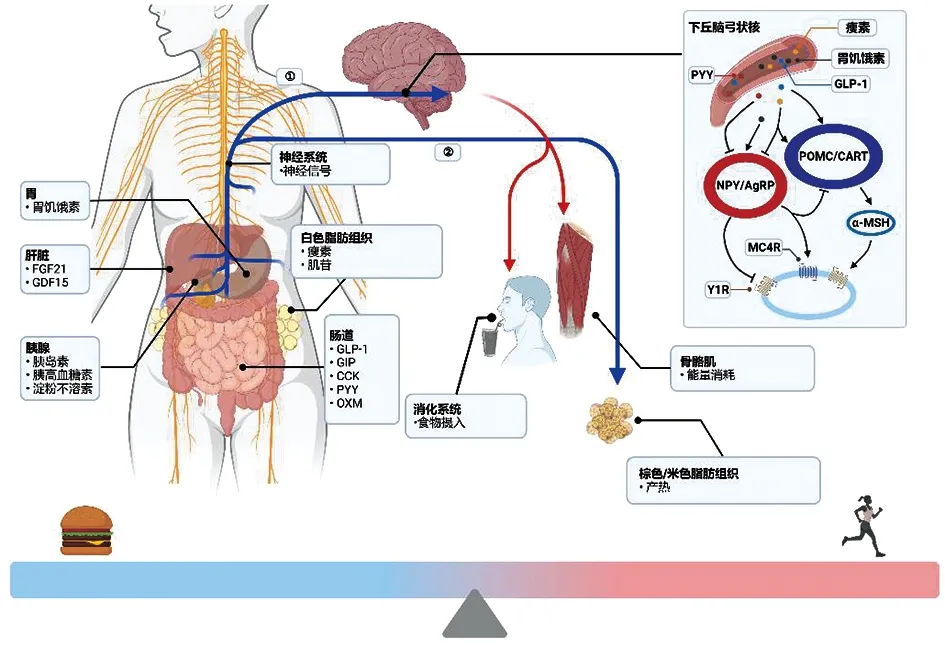
圖1 肥胖產(chǎn)生的機(jī)制示意圖 注:外周組織器官分泌多種調(diào)控因子,分別作用于:①中樞神經(jīng)系統(tǒng)攝食中心調(diào)節(jié)促進(jìn)攝食相關(guān)神經(jīng)元與抑制攝食神經(jīng)元活動(dòng)影響攝食行為;②外周能量消耗器官調(diào)節(jié)能量消耗及產(chǎn)熱。當(dāng)能量攝入與能量消耗之間的平衡被破壞時(shí)可引起能量過(guò)度繼續(xù)導(dǎo)致肥胖。FGF21:成纖維細(xì)胞生長(zhǎng)因子21;GDF15:生長(zhǎng)分化因子15;GLP-1:胰高血糖素樣肽;GIP:葡萄糖依賴的胰島素多肽;CCK:縮膽囊素;PYY:肽酪氨酸酪氨酸;OXM:胃泌酸調(diào)節(jié)素;Y1R:神經(jīng)肽Y受體1型。
2 肥胖的治療
目前,國(guó)際上主流指南推薦的肥胖治療主要包括生活方式干預(yù)、藥物治療、外科手術(shù)等方法。其中,生活方式的干預(yù)作為一種非侵入性的治療方法,作為肥胖治療后及后期體重維持的一線治療方案被廣泛推薦。但大量研究表明,僅采取生活方式干預(yù)時(shí),肥胖患者體重通常可以減輕5%,但往往難以維持[4]。其原因在于肥胖患者體內(nèi),抑制食欲的神經(jīng)內(nèi)分泌機(jī)制往往已經(jīng)出現(xiàn)失調(diào),僅依靠個(gè)人意志力的生活方式干預(yù)手段治療肥胖可能會(huì)反復(fù)失敗。外科手術(shù)主要是通過(guò)胃部手術(shù)達(dá)到限制食物攝入和吸收的目的。減肥手術(shù)雖能有效減輕體重,并帶來(lái)改善血糖、血脂收益,但因外科侵入性治療具有較為嚴(yán)重的圍手術(shù)期風(fēng)險(xiǎn)及術(shù)后并發(fā)癥,極大限制了其應(yīng)用,一般僅推薦用于BMI大于35或合并并發(fā)癥的重度肥胖患者。
因此,藥物治療依然是肥胖的重要治療手段,被推薦用于中重度肥胖患者以及有并發(fā)癥的輕度肥胖患者[5-6]。多年來(lái),減肥藥物研發(fā)及上市雖然一直在前進(jìn),但藥物審批一直保持謹(jǐn)慎態(tài)度,很多上市的藥物由于嚴(yán)重不良反應(yīng)而被及時(shí)撤市。目前FDA批準(zhǔn)在市用于減肥治理的藥物僅6種(脂肪酶抑制劑奧利司他、腎上腺素受體激動(dòng)劑/AMPA受體拮抗劑的復(fù)方芬特明/托吡酯、腎上腺素吸收抑制劑/多巴胺攝取抑制劑的復(fù)方納曲酮/安非他酮、腎上腺素受體激動(dòng)劑芐非他明、胰高血糖素樣肽-1(glucagon-like peptide-1, GLP-1)受體激動(dòng)劑利拉魯肽和司美格魯肽)。此外,日本還上市了脂肪酶抑制劑賽利司他,韓國(guó)還批準(zhǔn)了AMPK激動(dòng)劑二甲雙胍用于肥胖治療。而在國(guó)內(nèi),奧利司他自2007年獲批以來(lái)獨(dú)占減肥藥市場(chǎng)多年,這一情況即將被打破,利拉魯肽注射液用于肥胖或超重適應(yīng)證的上市許可申請(qǐng)于2022年1月獲得受理。這些在市肥胖治療的藥物不僅種類少,還有不同程度的不良反應(yīng)。因此改良、研發(fā)副反應(yīng)小且有效的肥胖治療藥物是當(dāng)前所面臨的最主要挑戰(zhàn)。
3 減肥相關(guān)靶點(diǎn)及藥物
近年來(lái),能量代謝領(lǐng)域的研究取得了很多新進(jìn)展,為治療肥胖提供許多治療新靶點(diǎn),同時(shí)也為新的減肥治療藥物研發(fā)奠定了理論基礎(chǔ)。目前發(fā)現(xiàn)的具有減肥前景的靶點(diǎn)及藥物眾多,根據(jù)其機(jī)制,可以大體分為:作用于中樞神經(jīng)系統(tǒng)控制攝食的相關(guān)靶點(diǎn)及藥物、作用于外周組織減少能量攝取的相關(guān)靶點(diǎn)及藥物、作用于外周組織促進(jìn)能量消耗的相關(guān)靶點(diǎn)及藥物、同時(shí)作用于中樞和外周的相關(guān)靶點(diǎn)及藥物(見(jiàn)表1)。
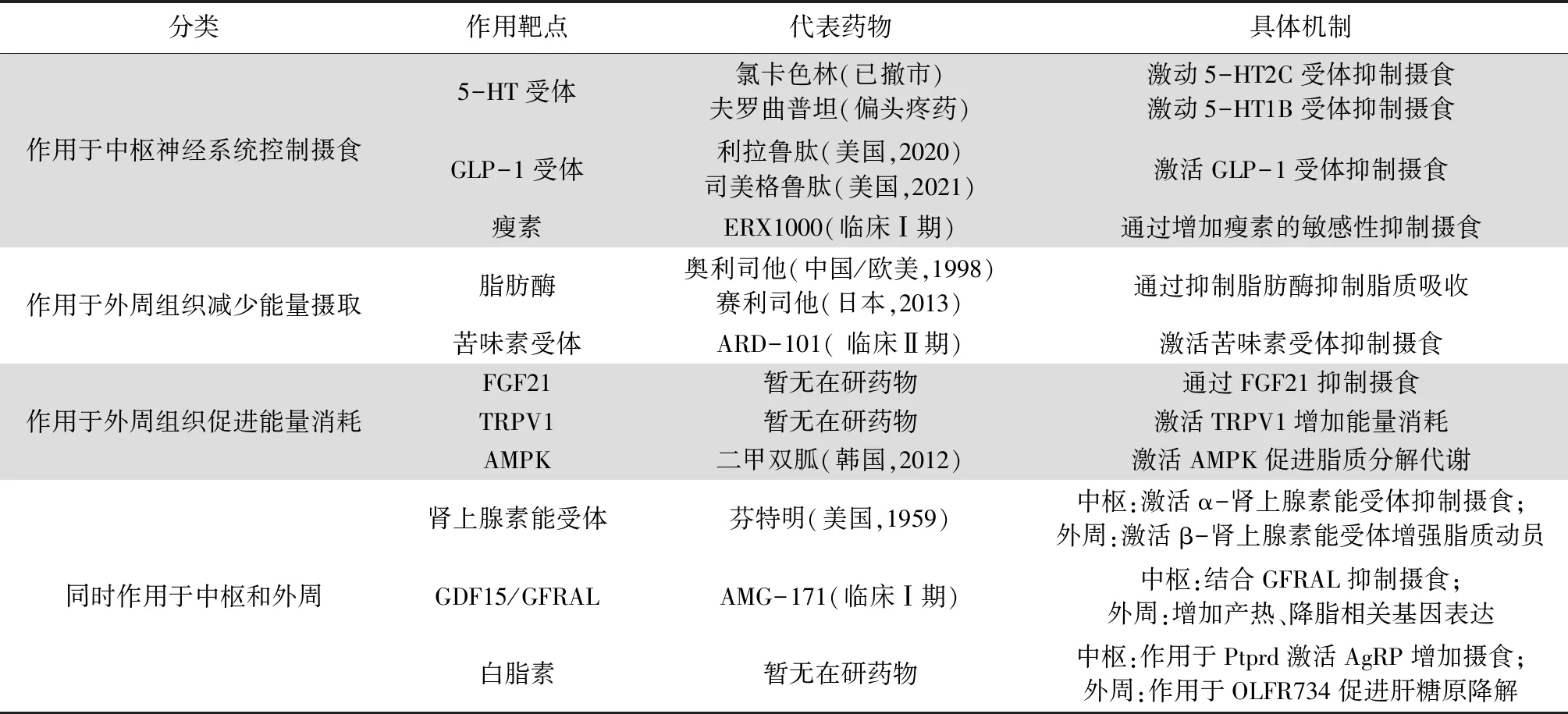
表1 減肥相關(guān)靶點(diǎn)及代表藥物作用機(jī)制
3.1 作用于中樞神經(jīng)系統(tǒng)控制攝食的相關(guān)靶點(diǎn)及藥物
3.1.1 5-羥色胺受體激動(dòng)劑20世紀(jì)70年代,研究發(fā)現(xiàn)大腦血清素水平增加會(huì)導(dǎo)致飽腹感,并且小鼠體內(nèi)血清素轉(zhuǎn)運(yùn)體的表達(dá)量對(duì)其體重的影響較大[7]。血清素即5-羥色胺(5-hydroxytryptamine,5-HT),其受體5-HT受體目前已經(jīng)被發(fā)現(xiàn)的有14種亞型,其中證實(shí)可以起到調(diào)節(jié)食欲作用的主要有4種亞型,分別是5-HT1A、5-HT1B、5-HT2C和5-HT6受體。5-HT1B、5-HT6受體敲除可引起實(shí)驗(yàn)動(dòng)物攝食量和體重的顯著增加[8-9]。動(dòng)物的攝食量也可因選擇性5HT1B受體激動(dòng)劑的作用而增加,且該現(xiàn)象會(huì)在5-HT1B受體拮抗劑的作用下被弱化[10]。5-HT2C和5-HT1B受體主要在弓狀核內(nèi)表達(dá),激活后作用于黑素細(xì)胞皮質(zhì)素原(pro-opiomelanocortin,POMC)神經(jīng)元,刺激α黑素細(xì)胞刺激素(alpha-melanocyte-stimulating hormone,α-MSH)合成,并減少刺鼠相關(guān)肽(agouti-related peptide,AgRP)合成,最終抑制攝食。5-HT6受體激活也可增加α-MSH的表達(dá),還可與γ-氨基丁酸(γ-aminobutyric acid,GABA)能神經(jīng)元的相互作用,引起體內(nèi)GABA水平的降低,而GABA也是弓狀核中激活POMC神經(jīng)元的主要神經(jīng)介質(zhì)。5-HT1A受體是一類主要用于精神疾病治療的藥物作用靶點(diǎn),但也有研究表明其被抑制后可通過(guò)減少攝食達(dá)到減肥的效果[11]。
5-HT受體激動(dòng)藥曾是減肥藥研發(fā)的熱點(diǎn)。1996年FDA批準(zhǔn)的第一個(gè)用于長(zhǎng)期治療肥胖的減肥藥右芬氟拉明,具有良好的減肥功效,但由于其對(duì)5-HT2B和5-HT2C受體沒(méi)有選擇性,導(dǎo)致了心臟瓣膜嚴(yán)重病變,已于1997年撤市。為避免因激動(dòng)5-HT2B而引起的心臟瓣膜不良反應(yīng),結(jié)構(gòu)改造后的5-HT2C受體激動(dòng)藥氯卡色林于2012年獲FDA批準(zhǔn)上市用于肥胖的長(zhǎng)期治療。但在2020年,氯卡色林因有致癌風(fēng)險(xiǎn)撤市,給以5-HT受體為靶點(diǎn)的減肥藥研發(fā)帶來(lái)了重創(chuàng)。但在2022年7月,一類常用的偏頭痛藥物——曲譜坦類及其他5-HT1B受體激活劑被報(bào)道具有抑制食欲的功效,并且表現(xiàn)出比氯卡色林更強(qiáng)的減肥效果[12]。此類藥物作為已上市藥物,未來(lái)有望拓展減肥適應(yīng)證。
3.1.2 GLP-1GLP-1是一種由腸道L細(xì)胞以及腦干尾側(cè)孤束核(nucleus of the solitary tract,NTS)神經(jīng)元分泌的多肽激素。GLP-1表現(xiàn)出與進(jìn)食相關(guān)的分泌特性:在空腹或餐間狀態(tài)下,GLP-1以較低的基礎(chǔ)水平持續(xù)分泌,但在食物攝入幾分鐘內(nèi)迅速上升。研究發(fā)現(xiàn)在正常或患有糖尿病的動(dòng)物和人類中,GLP-1能增強(qiáng)葡萄糖依賴的胰島素分泌[13],提高胰島素mRNA轉(zhuǎn)錄水平[14]。GLP-1還可抑制高血糖狀態(tài)下的胰高血糖素分泌[15],但在血糖正常時(shí)這種抑制效果不顯著。因其顯著的血糖調(diào)節(jié)作用,GLP-1受體激動(dòng)劑作為降糖藥被廣泛開(kāi)發(fā)用于治療2型糖尿病,并在使用中發(fā)現(xiàn)其減輕糖尿病患者的體重的現(xiàn)象[13]。
GLP-1減肥作用主要是通過(guò)作用于下丘腦POMC/可卡因和苯丙胺調(diào)節(jié)轉(zhuǎn)錄物(cocaine and amphetamine-regulated transcript,CART)神經(jīng)元上的GLP-1受體,產(chǎn)生抑制攝食的效應(yīng)。深入研究其機(jī)制發(fā)現(xiàn),GLP-1受體的活化可導(dǎo)致PKA的激活,從而引起AMPK[16]和AKT[17]活性的快速抑制,同時(shí)激活MAPK(即ERK1/2)信號(hào)通路[16]。雖然這些PKA、AKT、MAPK和AMPK信號(hào)對(duì)GLP-1R激活后抑制攝食是必不可少的,但尚不清楚這些GLP-1R介導(dǎo)的細(xì)胞內(nèi)信號(hào)如何影響神經(jīng)元的興奮性。
2014年,GLP-1受體激動(dòng)藥利拉魯肽(Liraglutide)被FDA批準(zhǔn)上市用于治療糖尿病,并于2020年拓展適應(yīng)證用于肥胖治療。同類藥物司美格魯肽(Semaglutide)亦于2021年在美國(guó)獲批上市用作肥胖的治療藥物。針對(duì)司美格魯肽的一項(xiàng)試驗(yàn)表明,一周一次的司美格魯肽注射治療可使肥胖患者體重下降14.9%[18]。盡管減肥效果顯著以及不良反應(yīng)整體輕微,但注射給藥方式還是影響了患者長(zhǎng)期用藥的依從性。值得一提的是,司美格魯肽已有口服劑型應(yīng)用于糖尿病治療,已完成臨床Ⅲ期試驗(yàn),試驗(yàn)中發(fā)現(xiàn)其在治療2型糖尿病的同時(shí)觀察到其能帶來(lái)減輕糖尿病患者體重的收益[19],在未來(lái)有望獲批用于肥胖癥的治療。
3.1.3 瘦素增敏劑瘦素是一種由脂肪細(xì)胞產(chǎn)生,負(fù)反饋?zhàn)饔糜谥袠猩窠?jīng)系統(tǒng)抑制攝食行為的激素。瘦素作用于下丘腦的瘦素受體,使得下丘腦中STATTyr705磷酸化水平增高,發(fā)揮抑制食物攝入的作用,可使肥胖小鼠體重下降45%。然而,由于瘦素抵抗的存在,瘦素作為減肥藥的研發(fā)一直沒(méi)能獲得成功。因此研發(fā)重點(diǎn)也從瘦素本身轉(zhuǎn)向了瘦素增敏。
雷公藤紅素是從雷公藤(雷神藤)根中提取的五環(huán)三萜類化合物,是一種新發(fā)現(xiàn)的瘦素增敏劑。除了增強(qiáng)瘦素本身的作用外,研究還發(fā)現(xiàn)了白細(xì)胞介素1受體 1 (interleukin-1 receptor,IL1R1) 是雷公藤紅素發(fā)揮生物學(xué)效應(yīng)的關(guān)鍵介質(zhì)。IL1R1在雷公藤紅素促進(jìn)瘦素致敏、減少食物攝入、減輕體重、恢復(fù)葡萄糖耐量、增加胰島素敏感性、緩解肝臟脂肪變性以及改善肝功能等方面發(fā)揮重要作用[20]。目前ERX1000(雷公藤紅素衍生物)作為減肥的治療藥物已進(jìn)入臨床Ⅰ期研究階段。
3.2 作用于外周組織減少能量攝取的相關(guān)靶點(diǎn)及藥物
3.2.1 脂肪酶抑制劑食物攝入的脂肪主要成分為混合甘油三酯,經(jīng)消化道中胃脂肪酶、胰脂肪酶水解成游離脂肪酸后被腸上皮細(xì)胞吸收。抑制脂肪酶的活性可以影響對(duì)脂質(zhì)的消化吸收,進(jìn)而達(dá)到不影響攝食量而減少能量攝取的效果。奧利司他是一類脂肪酶抑制劑,可特異性抑制胰脂肪酶使近三分之一的膳食脂肪吸收被抑制。因此作為減肥藥于1999年在美國(guó)獲批上市,并于2001年在我國(guó)批準(zhǔn)上市。2013年日本還上市了同類藥物賽利司他(Cetilistat)。此類藥物僅作用在胃腸道上,因此可引起部分患者不能耐受的主要原因也主要集中在胃腸道方面,包括油性大便、腹痛、腹瀉、脂肪痢等[21],導(dǎo)致部分患者不能耐受。
3.2.2 苦味受體(bitter taste receptor/bitter taste-sensing type 2 receptors,TAS2R)及其激動(dòng)劑味覺(jué)是生物體可獲得的基本感官之一,其中苦味作為五種基本味覺(jué)之一,其感知主要通過(guò)外來(lái)物質(zhì)與苦味受體(TAS2R)結(jié)合后,激活磷脂酶C(PC)、環(huán)磷酸腺苷(cAMP)和三磷酸肌醇(IP3)等第二信使,導(dǎo)致細(xì)胞內(nèi)Ca2+的釋放及細(xì)胞去極化,再通過(guò)鼓索和舌咽神經(jīng)將神經(jīng)沖動(dòng)傳遞到大腦,產(chǎn)生相應(yīng)的味覺(jué)。TAS2R為一類G蛋白偶聯(lián)受體,不僅存在于口腔和喉嚨中,還分布于腦、膀胱、呼吸道、胰腺和消化道等組織器官。最新研究發(fā)現(xiàn),TAS2R和肥胖之間的聯(lián)系密切。奎寧(苦味劑)可降低空腹?fàn)顟B(tài)下的血漿中發(fā)揮促食欲作用的胃饑餓素水平[22-23];除此之外TAS2R還被發(fā)現(xiàn)可以誘導(dǎo)釋放CCK[24]、GLP-1[24]等胃腸激素,在上述腸道激素的共同作用下通過(guò)抑制攝食發(fā)揮減肥作用。TAS2R減肥效應(yīng)的發(fā)現(xiàn),將飲食偏好與減肥相聯(lián)系,拓寬了肥胖治療的方法。通過(guò)提升日常飲食中苦瓜、蓮子心、苦蕎麥等苦味食物的比例,達(dá)到“吃苦”減肥的目的。另外,針對(duì)激動(dòng)TAS2R的原創(chuàng)藥物ARD-101已進(jìn)入臨床Ⅱ期試驗(yàn)階段,ARD-101作用于腸道細(xì)胞表面TAS2R,通過(guò)增加GLP-1等腸激素的表達(dá),對(duì)全身代謝起調(diào)節(jié)作用。
3.3 作用于外周組織促進(jìn)能量消耗的相關(guān)靶點(diǎn)及藥物
3.3.1 成纖維細(xì)胞生長(zhǎng)因子21(fibroblast growth factor 21,FGF21)FGF家族在機(jī)體內(nèi)作用廣泛,參與包括細(xì)胞生長(zhǎng),細(xì)胞分化和胚胎發(fā)育等在內(nèi)的多種生理活動(dòng)。大多數(shù)FGF分子量很小,約為17至34 kDa,主要通過(guò)與質(zhì)膜上表達(dá)的成纖維細(xì)胞生長(zhǎng)因子受體 (fibroblast growth factor receptors,FGFR)結(jié)合后,產(chǎn)生生物學(xué)效應(yīng),激活的下游信號(hào)主要有:Ras/MAPK、磷脂酰肌醇3-激酶 (PI3K)/AKT和蛋白激酶C (PKC)。
FGF21于2005年首次被發(fā)現(xiàn)具有調(diào)節(jié)代謝的作用,可通過(guò)調(diào)節(jié)脂肪細(xì)胞中GLUT1的表達(dá)來(lái)調(diào)控葡萄糖攝取,后續(xù)研究發(fā)現(xiàn)其在增加胰島素敏感性、增加能量消耗、降低甘油三酯等方面發(fā)揮重要作用[25]。其減輕體重的具體機(jī)制為FGF21通過(guò)調(diào)控UCP1[26]和誘導(dǎo)白色脂肪棕色化促進(jìn)產(chǎn)熱[27],增加能量消耗。相對(duì)于其他減肥藥物,FGF21優(yōu)勢(shì)在于其可直接作為小分子藥物直接給藥。研究表明,過(guò)表達(dá)或注射人源性FGF21均能使動(dòng)物體重明顯降低,并能抵抗高脂飲食所致的肥胖[28],這為FGF21可直接改造成為減肥藥物提供了理論基礎(chǔ)。此外,FGF21受到其上游過(guò)氧化物酶體增殖劑激活受體α(peroxisome proliferator-activated receptor alpha,PPARα)的調(diào)節(jié),PPARα激動(dòng)劑可顯著增加肝臟 FGF21 表達(dá)[29]。因此PPARα激動(dòng)劑也是一類潛在的減肥藥物。
3.3.2 瞬時(shí)感受器電位香草酸受體1(transient receptor potential vanilloid receptor 1,TRPV1)及其激動(dòng)劑TRPV1是瞬時(shí)受體電位(transient receptor potential,TRP) 通道家族成員,主要在感覺(jué)神經(jīng)元上表達(dá),受到熱、化學(xué)刺激后可使陽(yáng)離子通道開(kāi)放并引起Ca2+、Na+內(nèi)流。研究表明,TRPV1參與調(diào)節(jié)多種肥胖相關(guān)蛋白的表達(dá),包括促進(jìn)GLP-1的產(chǎn)生,刺激胰島素分泌增加,促進(jìn)脂聯(lián)素(adiponectin)以及瘦素分泌,最終達(dá)到控制食欲和調(diào)節(jié)體重的作用。除此之外,TRPV1的激活能增加產(chǎn)熱相關(guān)蛋白UCP1、骨形態(tài)發(fā)生蛋白-8b的表達(dá),同時(shí)Ca2+的內(nèi)流引起鈣調(diào)蛋白依賴激酶Ⅱ(Ca2+/calmodulin-activated protein kinase II,CaMKⅡ)、AMP活化激酶(AMP-activated kinase,AMPK)的磷酸化進(jìn)而促進(jìn)去乙酰化酶的表達(dá)以及增強(qiáng)其活性,從而促使白色脂肪棕色化增加機(jī)體產(chǎn)熱[31]。
辣椒素可激動(dòng)TRPV1發(fā)揮減肥作用,在動(dòng)物脂肪組織局部運(yùn)用辣椒素刺激TRPV1可引起脂肪因子和其他參與脂質(zhì)代謝的蛋白高表達(dá),從而引起脂肪細(xì)胞減小、體重降低[32]。另有研究表明,在運(yùn)動(dòng)的同時(shí)使用辣椒素激活TRPV1能額外增加能量消耗,減少脂肪積累,體重的下降更顯著[33]。除此之外在寒冷環(huán)境(17 ℃)和辣椒素刺激TRPV1的共同作用下,可以增強(qiáng)米色脂肪的生物學(xué)功能,增加產(chǎn)熱,在肥胖的治療和預(yù)防上均起顯著成效[34]。TRPV1的發(fā)現(xiàn),也為探索新型給藥方式的減肥藥物提供了理論基礎(chǔ)。表達(dá)TRPV1的神經(jīng)元主要分布在皮膚表面[35],由此為切入點(diǎn)而研制的減肥藥物或可通過(guò)透皮給藥方式治療肥胖,大大增加了減肥藥物使用的依從性和便捷性。
3.3.3 AMP依賴的蛋白激酶(adenosine 5′-monophosphate activated protein kinase,AMPK)及其激動(dòng)劑AMPK是一種調(diào)控能量穩(wěn)態(tài)的重要激酶,在機(jī)體處于低能量狀態(tài)時(shí)被激活,通過(guò)調(diào)節(jié)參與代謝分解相關(guān)酶的活性促進(jìn)脂質(zhì)、蛋白質(zhì)分解,增加ATP產(chǎn)生[36]。AMPK激動(dòng)劑二甲雙胍自1957年在英國(guó)批準(zhǔn)用于治療糖尿病以來(lái),陸續(xù)被發(fā)現(xiàn)可在心血管、肝臟、腎臟[37]疾病及相關(guān)腫瘤中發(fā)揮治療和預(yù)防作用 ,并因其減肥獲益在韓國(guó)批準(zhǔn)上市用于減肥治療,但并未受到各國(guó)的廣泛認(rèn)可。
近年來(lái),AMPK僅在ATP下降時(shí)被激活的傳統(tǒng)認(rèn)知受到了挑戰(zhàn)。林圣彩團(tuán)隊(duì)發(fā)現(xiàn),葡萄糖水平下降時(shí),溶酶體上的AMPK在ATP下降前就被激活,其中醛縮酶作為葡萄糖感受器發(fā)揮了重要作用[38-39]。該團(tuán)隊(duì)還篩選到了溶酶體醛縮酶特異性抑制劑“辟谷精”,可模擬葡萄糖水平下降時(shí)激活A(yù)MPK的場(chǎng)景,在動(dòng)物模型上發(fā)揮減肥效應(yīng),具有良好的應(yīng)用前景[40]。
3.4 同時(shí)作用于中樞和外周的相關(guān)靶點(diǎn)及藥物
3.4.1 擬交感神經(jīng)類藥物擬交感神經(jīng)類藥物在體內(nèi)發(fā)揮類似兒茶酚胺的功能,既能通過(guò)激活α-腎上腺素能受體發(fā)揮抑制食欲的作用,也可以激活β-腎上腺素能受體發(fā)揮刺激脂質(zhì)動(dòng)員的作用,均有助于達(dá)到減肥目的。在下丘腦的內(nèi)側(cè)區(qū),尤其在室旁核(paraventricular nucleus,PVN)或室旁核外側(cè),注射外源性的去甲腎上腺素能結(jié)合α2-腎上腺素能受體引起食欲的降低[41]。而β-腎上腺素能受體的三個(gè)亞型均參與脂質(zhì)動(dòng)員,其中β1-和β2-腎上腺素受體亞型主要參與全身脂質(zhì)動(dòng)員的調(diào)控[42],而β3-腎上腺素受體則在刺激棕色脂肪產(chǎn)熱方面作用顯著[43]。β2-腎上腺素能受體主要在皮下脂肪組織中表達(dá),是兒茶酚胺類物質(zhì)發(fā)揮脂質(zhì)降解作用的重要介質(zhì),且在能量的調(diào)節(jié)上發(fā)揮重要作用。
擬交感神經(jīng)類藥物可通過(guò)刺激下丘腦外側(cè)突觸前小泡釋放去甲腎上腺素(如芬特明),或者是通過(guò)阻止突觸前神經(jīng)元對(duì)去甲腎上腺素的再攝取(如多巴胺和去甲腎上腺素再攝取抑制劑安非他酮、5-HT和去甲腎上腺素再攝取抑制劑西布曲明等),引起突觸間隙內(nèi)的去甲腎上腺素水平升高來(lái)激動(dòng)受體;或者直接激動(dòng)腎上腺素能受體(如去甲麻黃堿等)。目前仍在市的此類藥物有芐非他明,以及芬特明(與托吡酯組成復(fù)方制劑),可用于肥胖的短期(≤ 12 周)治療。作為苯丙胺衍生物,這類藥物對(duì)體重的影響較為顯著,但長(zhǎng)期使用具有成癮性的風(fēng)險(xiǎn),屬于精神管控類藥品。除此之外,這些藥物還會(huì)導(dǎo)致失眠、口干、心悸和高血壓等不良反應(yīng),增加了心血管疾病的發(fā)病風(fēng)險(xiǎn)。因此作為減肥藥物建議短期和間歇性使用。
3.4.2 生長(zhǎng)分化因子15(growth differentiation factor 15,GDF15)及其受體膠質(zhì)細(xì)胞源性神經(jīng)營(yíng)養(yǎng)因子α樣受體(glial cell-derived neurotrophic factor receptor alpha-like,GFRAL)GDF15是TGF-β超家族的成員,在肝臟、腸道、腎臟和胎盤等組織器官中均有表達(dá)。研究發(fā)現(xiàn)過(guò)表達(dá)GDF15能引起實(shí)驗(yàn)動(dòng)物體重的下降,而GDF15敲除后可引起動(dòng)物體重的上升[44]。GDF15的減肥作用與其特異性受體——GFRAL相關(guān)[45]。GFRAL主要表達(dá)在腦干后側(cè)區(qū)與孤束核神經(jīng)元細(xì)胞上[45-46],GDF15與GFRAL結(jié)合之后再結(jié)合原癌基因酪氨酸蛋白激酶受體(Proto-oncogene tyrosine-protein kinase receptor,RET),形成的GFRAL-GDF15-RET復(fù)合物[47],引起細(xì)胞內(nèi)ERK1/2、AKT和PLCγ1的磷酸化,發(fā)揮后續(xù)抑制攝食、調(diào)節(jié)體重的作用[44]。除此之外,GDF15能上調(diào)棕色脂肪組織中產(chǎn)熱基因(UCP1、PGC1α、ECH1、Cox8b、Dio2、Cyc1、PGC1β、PPARα、Elvol3)以及白色脂肪組織、棕色脂肪組織中降脂基因(Adrb3、ATGL、HSL)的表達(dá)[48],增加脂肪組織中脂質(zhì)動(dòng)員與氧化代謝[49],通過(guò)增加產(chǎn)熱改善肥胖。
近年來(lái)圍繞GDF15-GFRAL軸作為減肥靶點(diǎn)的藥物研究很多,AMG-171作為GDF15類似物,可減少模型動(dòng)物對(duì)食物攝入,降低其體重,改善代謝特征[50],目前處于臨床Ⅰ期研究階段。此外,還有強(qiáng)生公司的JNJ-9090,諾和諾德公司的NN9215,均以GDF15為靶點(diǎn)開(kāi)展針對(duì)肥胖治療的臨床藥物研究。
3.4.3 白脂素(asprosin)及其受體白脂素最早是在一種罕見(jiàn)的遺傳性疾病——新生兒型類早衰綜合征中被發(fā)現(xiàn)的。除胃饑餓素外,絕大多數(shù)已知的能夠發(fā)揮影響食欲的激素都是厭食性激素,白脂素是為數(shù)不多的已知的促食欲激素之一[51]。白脂素由白色脂肪分泌,在外周可通過(guò)作用于肝臟中的嗅覺(jué)受體OLFR734[52]激活G蛋白-cAMP-PKA信號(hào)通路,引起肝糖原分解為葡萄糖快速釋放到升高血糖的效應(yīng)[53];在中樞白脂素可以穿過(guò)血腦屏障作用蛋白酪氨酸磷酸酶受體 δ(protein tyrosine phosphatase receptor δ,Ptprd)[54],通過(guò)依賴于cAMP的途徑直接激活促食相關(guān)神經(jīng)元釋放AgRP,最終引起攝食量增加[55]。而Ptprd基因的敲除可引起強(qiáng)烈的食欲抑制、消瘦,并阻斷了白脂素的促食欲作用[54]。動(dòng)物實(shí)驗(yàn)上使用白脂素抗體抑制白脂素可帶來(lái)降低空腹血糖[53]、減少攝食量并改善體重[55]的收益。
4 總結(jié)與展望
從19世紀(jì)末羊甲狀腺提取物用于減肥至今,減肥藥的研發(fā)已走過(guò)百年。隨著對(duì)肥胖的生理病理機(jī)制的不斷深入探索,越來(lái)越多與肥胖有關(guān)的靶點(diǎn)被發(fā)現(xiàn),但成功上市的藥物寥寥無(wú)幾。許多藥物雖然在動(dòng)物模型上獲得了良好的減肥效果,但在臨床試驗(yàn)上不盡如人意。嚙齒動(dòng)物單位質(zhì)量能量消耗更高,且棕色脂肪組織更多,因此減肥藥能夠更大范圍地動(dòng)態(tài)控制嚙齒動(dòng)物的食物攝入量,而人類使用減肥藥的最大療效會(huì)低2~4倍[56]。
近年來(lái),減肥藥物研發(fā)的思路也從單一靶點(diǎn)向多靶點(diǎn)聯(lián)合作用轉(zhuǎn)變,有效解決了單一靶點(diǎn)減肥效果不理想,不良反應(yīng)大等問(wèn)題。例如芬特明-托吡酯、納曲酮-安非他酮復(fù)方制劑,延長(zhǎng)了擬交感神經(jīng)藥物只能用作短期減肥治療的弊端。2022年1月的一項(xiàng)Meta分析表明,芬特明-托吡酯是現(xiàn)存在市最有效的減肥藥物之一[57],與之共享“最有效減肥藥“的另一種藥物是GLP-1受體激動(dòng)劑司美格魯肽(Semaglutide)。盡管單獨(dú)使用GLP-1受體激動(dòng)劑在減輕體重方面效果出眾,禮來(lái)研發(fā)的Tirzepatide作為一類雙重激動(dòng)劑可在激活GLP-1受體的同時(shí)激活另一類代謝相關(guān)靶點(diǎn)——葡糖糖依賴性促胰島素多肽受體(glucose-dependent insulinotropic polypeptide receptor,GIPR),最終達(dá)到減少體重22.5%的效果,并且激動(dòng)GIP受體可以減輕GLP-1受體激動(dòng)所引起胃腸道不良反應(yīng)。而另一種GLP-1R、GIPR以及胰高血糖素受體(glucagon receptor,GCGP)三受體激動(dòng)劑藥物L(fēng)Y3437943,也在減輕體重、改善血糖上取得良好效果[58],并完成了臨床Ⅱ期實(shí)驗(yàn)。
肥胖患者數(shù)量的逐年上升且僅有1%的藥物使用率都意味著肥胖藥物有著巨大的市場(chǎng)前景。國(guó)家藥品監(jiān)督管理局于2021年發(fā)布《體重控制藥物臨床試驗(yàn)技術(shù)指導(dǎo)原則》,藥物研發(fā)再次進(jìn)入公眾視野,也為我國(guó)自主研發(fā)減肥創(chuàng)新藥提出了要求和建議。隨著研究的進(jìn)展,將會(huì)有更多減肥相關(guān)的靶點(diǎn)被發(fā)現(xiàn),減肥藥物的研發(fā)也會(huì)越來(lái)越多元化。

