基于網絡藥理學分析蒼術-桂枝治療非酒精性脂肪性肝炎的作用機制
陶禹,劉文娟,馬茜茜*,付丹妮*
(1.內蒙古民族大學醫學院,內蒙古 通遼 028000;2.內蒙古自治區蒙藥心腦血管藥理學重點實驗室,內蒙古 通遼 028000)
現在生活和工作節奏不斷加快,人們的壓力也越來越大,造成很多人睡眠不均,飲食不規律,進而出現肝臟脂肪代謝異常,困倦乏力,面色發黃,食欲不振,惡心,厭油等一系列癥狀,最終演變為一種慢性疾病——非酒精性脂肪性肝炎(NASH)。NASH是現在常見的一種脂肪性肝病,進一步發展可能導致肝纖維化、肝硬化等肝臟的終末期疾病狀態[1],造成不可逆性損傷。近幾年,NASH的發病率逐年增加,已成為我國第一大肝病,但截至目前NASH的作用機理仍不明確,還需進一步研究。西醫對癥治療NASH的方法主要是保肝護肝、降低血脂、抗氧化等,具有見效快,服用方法簡便等特點,但普遍存在治療效果不明顯、毒副作用較大,還可能存在其他不良反應,對人體健康不利。中醫則不同,治療的目的在于調理機體,提高免疫力,運用整體觀念和辨證施治,治療方法多為保肝護肝調肝,在治療NASH上具有明顯療效;且從肝脾腎辨證論治入手,在痊愈率、有效率和改善肝功能等方面均明顯優于西藥[2];中藥治療也未發現嚴重不良反應。中藥又多配伍使用,復方治療效果更加顯著,是本病的治療方法之一。
中醫方面指出:肝郁,脾虛為本病的基本病理病機,痰濕、氣滯、血瘀、熱邪為本病的主要病理產物,又主要以痰濕為主。本病的病位主要在肝、脾胃,痰濕、氣滯等基本病理因素,熱邪在該病的發展過程中起著重要的作用,而該病日久不愈,遷延日久,瘀血內生,多種病理因素相互作用,相互影響,導致該病逐漸發展。
《金匱要略》云:“見肝之病,當先實脾”,因其相克之聯系,故保肝護肝多先健脾[3]。在中藥著作《神農本草經》《本草衍義》中,蒼術乃是一味化濕藥,味辛、苦,性溫,歸脾、胃、肝經,能補脾燥濕,祛風散寒,消食,明目,主要治療由脾胃濕熱引起的食欲不振,厭食,消化不良,惡心嘔吐,起到健脾祛濕的功效。氣機郁滯,肝氣郁結,最常見的原因是受情緒的影響,導致肝氣疏泄,進而出現胸悶氣短、兩脅脹痛、惡心、疲倦乏力,急躁焦慮抑郁等癥狀;或者出現口干、噯氣,便秘等病癥;或者影響脾胃消化的功能,從而出現了脾胃不適,偶有消化道出血,嚴重的會出現肝衰竭。于臟腑則表現為肝熱、肺熱、腸熱或者肝胃俱熱、胃腸俱熱等,形成內熱的核心機制,推動高血脂、脂肪肝的發生[4]。桂枝則是一味解表劑,辛、甘、溫,可發汗解肌,溫經通脈,止煩出汗,除風寒濕痹,另外可以助陽化氣,治腎虛痹證,平沖將氣。兩者都對NASH的治療有一定功效,但二者配伍使用的作用機理尚不明確。因此,討論蒼術-桂枝治療NASH的作用機理,加以運用,可以有效治療NASH。
近年來,網絡藥理學越來越多地被用于醫藥研究方面,尤其是中醫藥。一方面,網絡藥理學透徹地剖析單味中藥或者中藥方劑“多成分”“多途徑”的作用體系,展現出與特定疾病關聯的“成分-疾病-靶點-途徑”,明確中藥復方效用的物質過程及作用機制;另一方面,網絡藥理學注重提高藥物醫治效果,減小毒副作用,廣泛用于臨床新藥研發,節省藥物研發費用。因此,本次使用網絡藥理學的方法,主要探論蒼術-桂枝治療NASH的作用機理,為治療NASH提供參考。
1 資料與方法
1.1 蒼術-桂枝成分的收集分別以蒼術、桂枝為對象,在TCMSP中藥數據庫篩選蒼術、桂枝成分,參考 TCMSP數據庫使用指南,以“OB 值≥30%并且DL≥0.18”為基本條件[5],篩選蒼術和桂枝的有效活性成分。
1.2 蒼術-桂枝作用靶點的收集基于上述篩選得到的有效成分,收集蒼術、桂枝的潛在作用靶點,并在Uniport數據庫修正相關靶點簡稱,然后通過Swiss Target Prediction進一步補充蒼術、桂枝的靶點。
1.3 NASH靶點的收集以關鍵詞Nonalcoholic Steatohepatitis(NASH)在Gene Cards和OMIM疾病數據庫進行搜索,得到NASH的相關靶點信息。
1.4 預測蒼術-桂枝對抗NASH的作用靶點將蒼術、桂枝與NASH的靶點分別錄入到draw venn diagram中,繪制韋恩圖,得到蒼術與桂枝、蒼術-桂枝與NASH的交集靶點,即可能為蒼術-桂枝對抗NASH的作用靶點。
1.5 描繪“藥物-成分-疾病-靶點”網絡圖將蒼術-桂枝與NASH交集靶點導入到可視化軟件Cytoscape中,生成蒼術-桂枝與NASH關聯的“藥物-成分-疾病-靶點”網絡圖,對大小、形狀、顏色等進一步優化。
1.6 蛋白相互作用(PPI)網絡的構建String數據庫可以收集靶點并作出簡單的PPI網絡圖,輸入蒼術-桂枝與NASH交集靶點,獲取PPI網絡及數據信息,然后將數據導入 Cytoscape 可視化作圖軟件中,優化PPI網絡圖,分析關鍵靶點信息。
1.7 富集分析與分子對接利用DAVID富集分析平臺,分析蒼術-桂枝與NASH的主要BP、CC、MF和關鍵通路,得到蒼術-桂枝治療NASH的過程通路,并作出其通路分析氣泡圖和功能分析柱狀圖。
在化合物數據庫Pubchem得到交集靶點對應的活性成分的2D結構,制作分子對接的結構文件,把文件導入用PyMOL軟件,通過對核心組分和靶點的分子對接驗證,得到相關的結合能數據和分子對接圖像。
2 結果
2.1 蒼術-桂枝成分的收集在TCMSP中藥數據分析平臺,根據OB≥30%,同時 DL≥0.18 進行篩選, 共得到蒼術9個,桂枝7個(見表1),包括漢黃芩素(wogonin)、NSC63551、3β-乙酰氧基白術酮(3β-acetoxyatractylone)、β-胡蘿卜素(β-daucosterol_qt)、β-谷甾醇(β-sitosterol)、過氧麥角甾醇(Peroxyergosterol)、紫杉葉素(taxifolin)、表兒茶素(ent-Epicatechin)等。

表1 蒼術有效活性成分
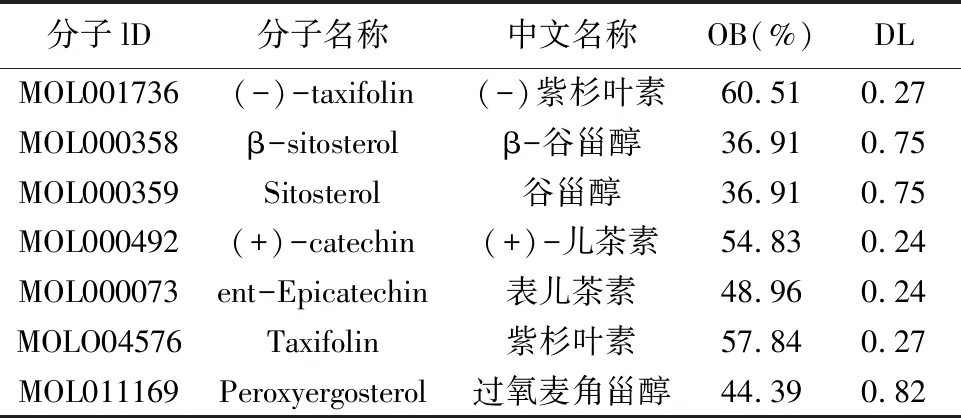
表2 桂枝有效活性成分表
2.2 蒼術-桂枝作用靶點的收集按照“2.1”項下篩選的有效活性成分,檢索其靶點信息,并通過Swiss Target Prediction數據庫預測補充,共得到蒼術靶點273個,桂枝靶點110個(去重后)。
2.3 NASH靶點的收集在Gene Cards和OMIM疾病數據庫共得到NASH的疾病靶點656個(去重后)(部分見表3)。
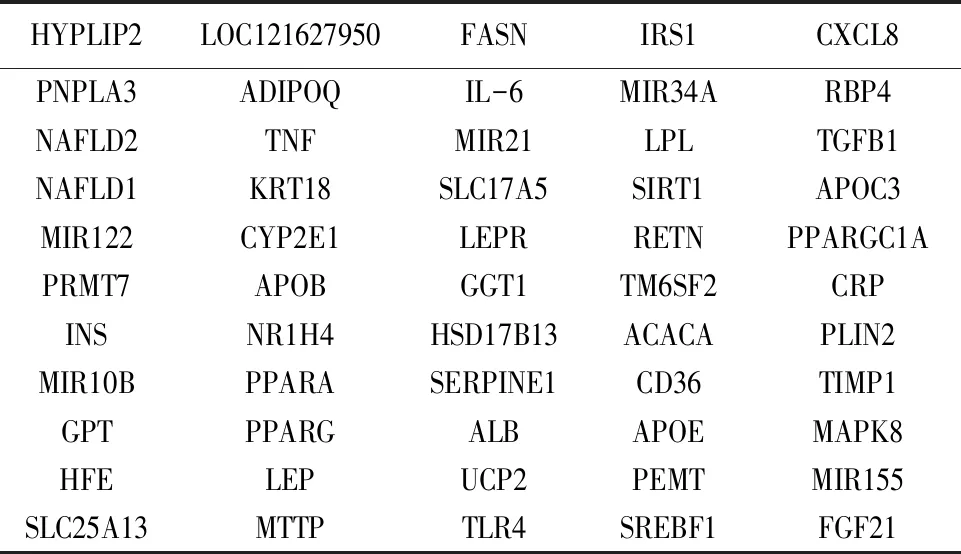
表3 NASH部分靶點
2.4 預測蒼術-桂枝對抗NASH的作用靶點將上述“2.2”和“2.3”項下得到的蒼術、桂枝、NASH的作用靶點分別輸入到draw venn diagram中,得到蒼術與桂枝交集靶點74個(見圖1),蒼術-桂枝與NASH的交集靶點77個(見圖2),其中的26個靶點可能為蒼術-桂枝對抗NASH的潛在作用靶點,如PPARD、HMGCR、NOS2、SLC6A4、PTPN1、RXRA、CYP2C19等。
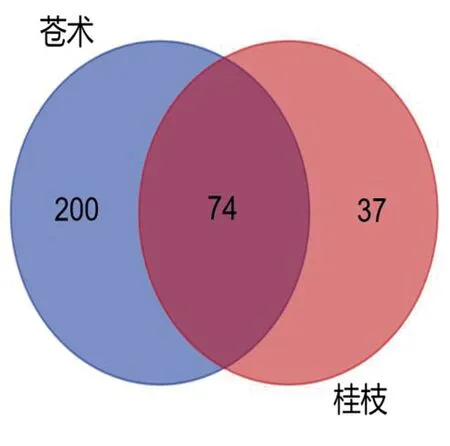
圖1 蒼術-桂枝交集靶點
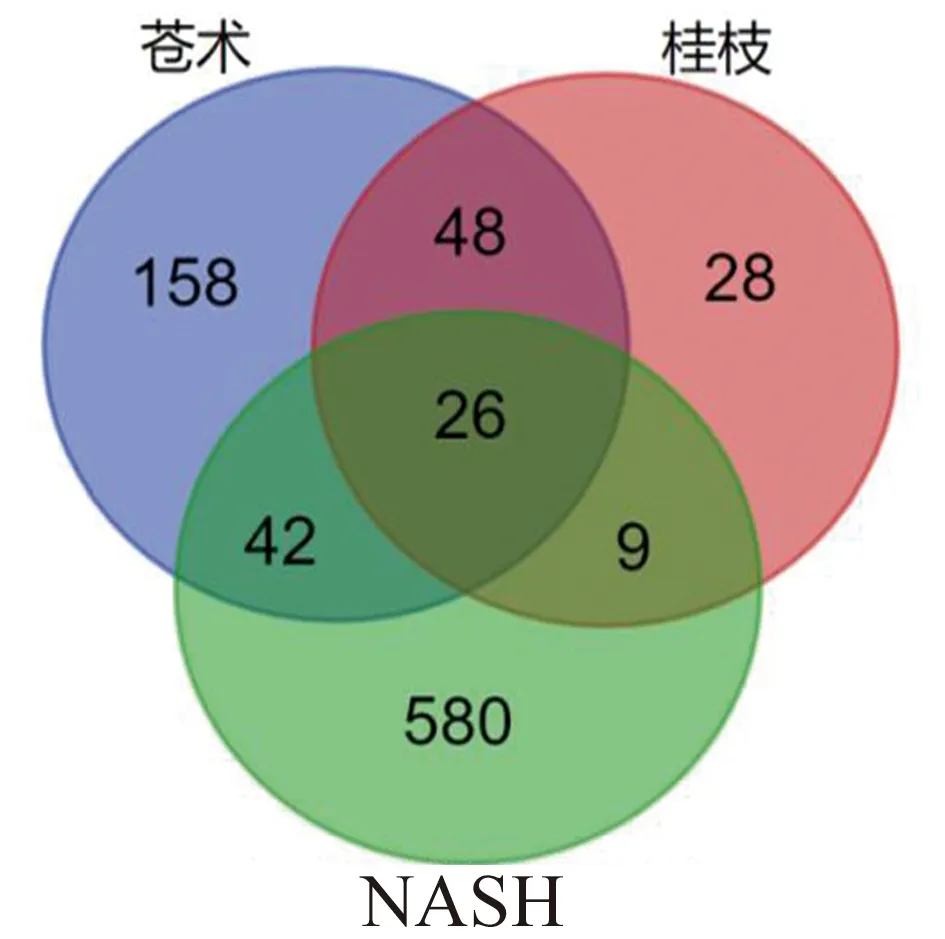
圖2 蒼術-桂枝與NASH的交集靶點
2.5 構建“蒼術-桂枝-成分-NASH-靶點”網絡圖在可視化軟件Cytoscape中導入有關文件,制作“蒼術-桂枝-成分-NASH-靶點”網絡圖(見圖3)。圖中共有91個點,191條邊,其中最中間的橙色菱形代表蒼術-桂枝與非酒精性脂肪性肝炎交集靶點,共26個,中間外圈紫色代表蒼術與NASH交集靶點,共42個,綠色代表藥物桂枝與NASH交集靶點,共9個,左側藍色圓圈代表蒼術與桂枝的有效成分,共11個,中間紅色為蒼術-桂枝藥對,最右側棕色為NASH。表明蒼術-桂枝的有效活性成分通過PPARD、HMGCR、NOS2、SLC6A4、PTPN1、RXRA、CYP2C19、NR1H3、CES2等靶點對治療NASH起作用。
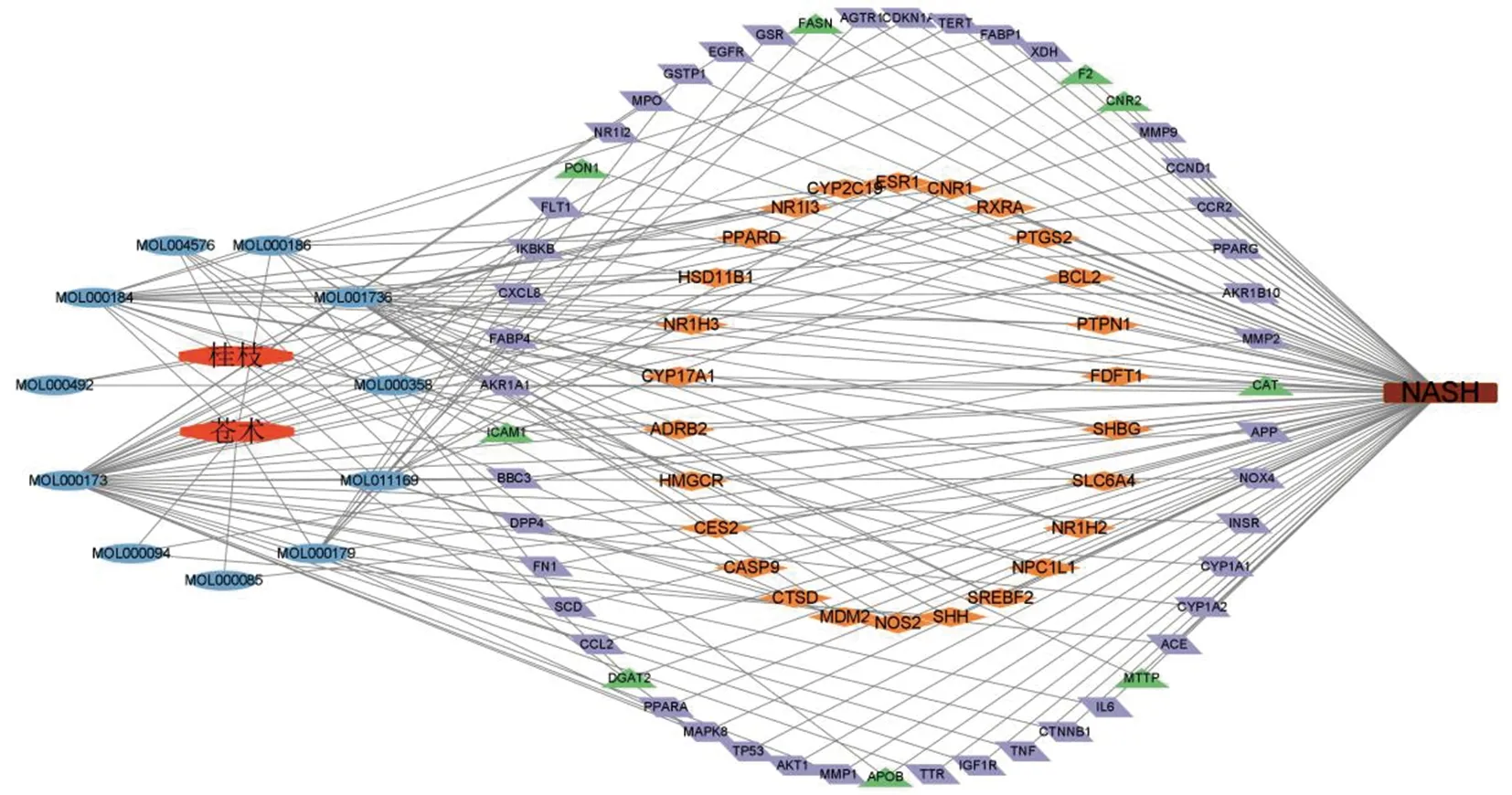
圖3 蒼術-桂枝與NASH的“藥物-成分-疾病-靶點”網絡圖
2.6 蛋白相互作用(PPI)網絡分析在String數據庫導入蒼術-桂枝與NASH的交集靶點信息,獲得PPI網絡,并把得到的相關數據導入Cytoscape可視化作圖軟件中,制作清晰明了的PPI網絡圖(見圖4),根據網絡分析各節點degree值,設置其大小、位置、顏色,degree值越大,字體,圖案越大,位置越靠近最里圈,顏色也越深,并根據Cytoscape軟件內的插件Centiscape 2.2依據Closeness、Betweenness、Degree篩選出蒼術-桂枝對抗NASH的關鍵靶點16個,分別是ACE、APOB、CAT、TP53、EGFR、PPARG、ESR1、PPARA、AKT1、PTGS2、FN1、IL-6、TNF、FASN、CTNNB1、RXRA。
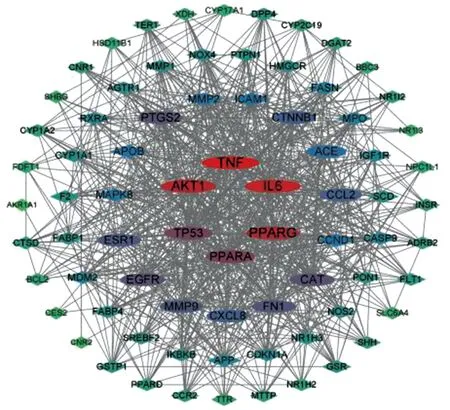
圖4 蒼術-桂枝與NASH交集靶點PPI網絡
2.7 富集分析將從韋恩圖得到的77個交集靶點導入David富集分析平臺進行富集分析,得到GO與KEGG數據。
2.7.1 富集分析根據P值<0.001篩選出:10種BP,10個CC,10個MF,并在微生信作圖網絡中作出其GO功能富集分析柱狀圖(見圖5)。其中炎癥反應[6]、膽固醇穩態[7]、細胞對脂多糖[8]的反應、膽固醇代謝過程、胰島素分泌的調節、炎癥反應[6]的積極調節;脂質顆粒、高分子絡合物;肝素[9]結合等,參與蒼術-桂枝治療NASH的過程。由此可見,蒼術-桂枝治療NASH的作用機制是由多種生物過程,多個細胞組分和多個分子功能相互協助,共同作用實現的。
同樣根據P<0.001篩選出13條信號通路,并利用微生信作出氣泡圖(見圖6),提示蒼術-桂枝可能主要通過這些通路對抗NASH,發揮作用,脂質與動脈粥樣硬化、內分泌抵抗、丙型肝炎、胰島素抵抗[10]、非酒精性脂肪肝[11]等,其中,有10個靶點落在胰島素抵抗的通路上,分別為:IKBKB、PTPN1、IL-6、MAPK8、NR1H2、INSR、NR1H3、AKT1、PPARA、TNF;有11個靶點落在非酒精性脂肪肝上,分別為:IKBKB、IL-6、MAPK8、RXRA、CXCL8、INSR、NR1H3、AKT1、PPARG、PPARA、TNF。綜上所述,蒼術-桂枝是通過以上多個通路治療NASH。
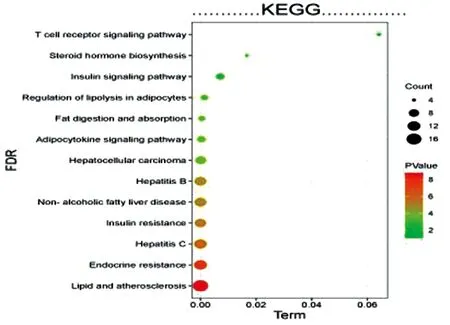
圖6 交集靶點KEGG通路富集分析氣泡
2.7.2 分子對接驗證結果將準備的結構文件導入用PyMOL分子對接軟件中運行得到成分與靶點的分子對接圖像(見圖7)和結合能信息(見表4),結果發現:蒼術的漢黃芩素與PTGS2有較強的結合能,能作用于上述通路發揮作用,很好的治療NASH。
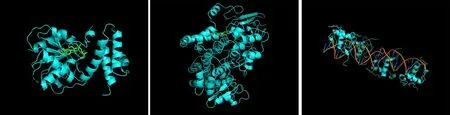
圖7 部分成分與靶點的分子對接圖像[從上到下分別為Taxifolin與APOB,Peroxyergostero與FASN,(+)-catechin 與RXRA]

表4 蒼術-桂枝與NASH部分成分-靶點對接結果
3 討論
本研究基于網絡藥理學和相關文獻分析蒼術-桂枝對抗NASH的作用機制,最終發現蒼術-桂枝可能通過漢黃芩素、β-胡蘿卜素、紫衫葉素、表兒茶素、β-谷甾醇等有效活性成分,作用于ACE、APOB、CAT、TP53、EGFR、PPARG、ESR1、PPARA、AKT1、PTGS2、FN1、IL-6、TNF、FASN、CTNNB1、RXRA等靶點,參與炎癥反應、膽固醇穩態、細胞對脂多糖的反應、膽固醇代謝過程、胰島素分泌的調節、炎癥反應的積極調節等生物過程,調控脂質與動脈粥樣硬化、內分泌抵抗、丙型肝炎、胰島素抵抗、非酒精性脂肪肝等信號通路,進而證明蒼術-桂枝在治療NASH方面起作用,分子對接結果也驗證本次研究數據的可靠性,但缺乏實驗證據,希望以后可以通過實驗證明。
4 結論
NASH的發病機制復雜,涉及脂質沉積、炎癥、氧化應激、纖維化、膽汁酸異常代謝、腸道菌群失調和易感基因變異之間復雜的相互作用[10],本次研究基于網絡藥理學的分析方法,剖析蒼術-桂枝治療NASH的作用機制,共得到16個有效活性成分。在蒼術的成分中,漢黃芩素[12]對炎癥反應起到抑制的作用;β-胡蘿卜素[13]具有抗氧化的作用,在桂枝的成分中,紫衫葉素[14]更是直接通過抵制炎癥從而治療NASH;表兒茶素[15]在對抗肝纖維化起到顯著作用。β-谷甾醇[16]既有抗炎作用又有抗氧化作用。383個潛在作用靶點,NASH有656個靶點,通過韋恩圖分析得知三者交集靶點共77個,進而猜測蒼術-桂枝是通過這些成分和靶點對NASH起到治療的作用。在PPI網絡分析中發現,degree值越大,越有可能起到治療作用,并根據Cytoscape軟件內的插件Centiscape 2.2依據Closeness、Betweenness、Degree篩選出14個關鍵靶點,進一步證明蒼術-桂枝藥對是通過多成分,多靶點醫治NASH[17-19]。
接下來為了進一步證明二者作用機制,又通過富集分析。結果顯示,二者聯合多種生物過程,細胞成分,分子功能,多種通路共同作用:上述成分和靶點參與炎癥反應、膽固醇穩態、細胞對脂多糖的反應、膽固醇代謝過程、胰島素分泌的調節、炎癥反應的積極調節等生物過程,調控脂質與動脈粥樣硬化、內分泌抵抗、丙型肝炎、胰島素抵抗、非酒精性脂肪肝等信號通路,表明蒼術-桂枝藥對確實對治療NASH起作用[20-22]。最后,分子對接驗證結果表明,蒼術的漢黃芩素與PTGS2有較強的結合能,桂枝的過氧麥角甾醇與FASN有較強的結合能,桂枝的(+)-兒茶素與RXRA有較強的結合能。這些結果更加說明蒼術與桂枝的核心活性成分與靶點之間具有較強聯系,通過多條通路調治NASH。

