新輔助化療聯(lián)合PD-1抑制劑治療三陰性乳腺癌的臨床療效
張曉宇 任悅 劉偉 苗彥玲 張輝 靳麗君 張恒樂 康曉寧 白杰 王遵義


摘要:目的 探討新輔助化療聯(lián)合PD-1抑制劑治療三陰性乳腺癌的臨床療效及其對免疫功能的影響。方法 將80例三陰性乳腺癌患者隨機分為對照組和觀察組,每組40例。對照組接受多柔比星脂質體+環(huán)磷酰胺+白蛋白紫杉醇(AC-T)序貫化療,觀察組在對照組的基礎上聯(lián)合PD-1抑制劑治療。所有患者完成免疫治療及新輔助化療3周后無手術禁忌證,均行乳腺癌改良根治術。比較2組患者的生活質量、臨床療效、手術時間、術中出血量、免疫指標及不良反應。結果 治療后,觀察組生活質量評分高于對照組(84.55±6.09 vs. 75.93±6.12,P<0.05)。治療8個周期后,觀察組完全緩解率(CRR)、CD4+、CD8+、CD4+/CD8+、IgG、IgA和IgM水平均優(yōu)于對照組(P<0.05)。觀察組手術時間[(43.25±6.85)min vs. (82.53±8.53)min]和術中出血量[(136.52±8.74)mL vs. (241.63±8.32)mL]均少于對照組(P<0.05);2組不良反應發(fā)生率差異無統(tǒng)計學意義(P>0.05)。結論 三陰性乳腺癌采用新輔助化療聯(lián)合PD-1抑制劑治療可以有效改善患者免疫功能和生活質量,保證臨床治療的安全性。
關鍵詞:免疫檢查點抑制劑;放化療,輔助;三陰性乳腺癌;生活質量;免疫,主動
中圖分類號:R737.9 文獻標志碼:ADOI:10.11958/20221554
Clinical efficacy of neoadjuvant chemotherapy combined with PD-1 inhibitor in the
treatment of triple negative breast cancer
ZHANG Xiaoyu REN Yue LIU Wei MIAO Yanling ZHANG Hui JIN Lijun ZHANG Hengle KANG Xiaoning BAI Jie ?WANG Zunyi
1 Department of Thyroid and Breast Surgery Ⅲ, Cangzhou Central Hospital, Cangzhou 061000, China; 2 Graduate School, Hebei Medical University; 3 Department of Ultrasound Ⅱ, Cangzhou Central Hospital
Corresponding Author E-mail:181176788@qq.com
Abstract: Objective To investigate the clinical efficacy of neoadjuvant chemotherapy combined with PD-1 inhibitor in the treatment of triple negative breast cancer and its effect on immune function. Methods Eighty patients with triple negative breast cancer were randomly divided into the control group and the observation group, with 40 cases in each group. The control group received sequential chemotherapy of doxorubicin liposome + cyclophosphamide + albumin paclitaxel (AC-T), and the observation group was treated with PD-1 inhibitor on the basis of the control group. The quality of life, clinical efficacy, operation time, intraoperative blood loss, immune function and adverse reactions were compared between the two groups. Results After treatment, the SF-36 score was significantly higher in the observation group (84.55±6.09) than that of the control group (75.93±6.12, P<0.05). After 8 courses of treatment, the complete response rate (CRR), CD4+, CD8+, CD4+/CD8+, immunoglobulin IgG, IgA and IgM levels were significantly better in the observation group than those in the control group (P<0.05). The operative time [(43.25±6.85) min vs. (82.53±8.53) min] and intraoperative bleeding [(136.52±8.74) mL vs. (241.63±8.32) mL] were significantly decreased in the observation group than those of the control group (P<0.05). There was no significant difference in the incidence of adverse reactions between the two groups (P>0.05). Conclusion Neoadjuvant chemotherapy combined with PD-1 inhibitor in the treatment of triple negative breast cancer can improve the immune function and quality of life of patients, and ensure the safety of clinical treatment.
Key words: immune checkpoint inhibitors; chemoradiotherapy, adjuvant; triple negative breast neoplasms; quality of life; immunity, active
三陰性乳腺癌(triple negative breast cancer,TNBC)占乳腺癌總數(shù)的15%~20%。往往發(fā)病比較早,且具有很強的侵襲性,尚缺乏有效的治療措施[1]。臨床流行病學調查顯示,TNBC較其他類型乳腺癌患者生存率低。程序性細胞死亡蛋白-1(PD-1)作為免疫球蛋白超家族的主要成員之一,是一種重要的免疫抑制分子。研究發(fā)現(xiàn),PD-1的免疫調節(jié)在對抗腫瘤、感染、自身免疫性疾病以及促進移植器官存活等方面發(fā)揮著重要作用[2]。PD-1配體(PD-L1)也可以作為靶標,參與免疫調節(jié)。PD-1和PD-L1是重要的免疫檢查點,共同啟動T細胞的程序性死亡,使腫瘤細胞免疫逃逸[3]。然而,鑒于多種原因,乳腺癌患者僅有10%~30%的患者接受PD-1/PD-L1抑制劑治療[4]。因此,如何進一步提高PD-1/PD-L1抑制劑的療效成為國內外的研究熱點。目前基于TNBC免疫治療的聯(lián)合治療研究相對較少。本研究旨在探討免疫治療和化療聯(lián)合治療能否增加單獨化療的抗腫瘤效應,同時觀察兩者聯(lián)合對免疫指標的影響,從而指導臨床治療。
1 對象與方法
1.1 研究對象
選取2019年5月—2022年2月滄州市中心醫(yī)院腫瘤外科經(jīng)病理及免疫組化染色證實均為TNBC的80例女性患者作為研究對象。按照隨機數(shù)字表法將其分為對照組和觀察組,每組40例。所有患者均經(jīng)病理活檢確診為乳腺癌,此前均未接受任何化療、激素治療或放療,常規(guī)檢查未見遠處轉移及器官損害。觀察組患者年齡44~57歲,平均(50.35±3.98)歲,病程1~1.6年,平均(1.28±0.16)年。對照組年齡43~58歲,平均(50.25±3.85)歲,病程0.9~1.8年,平均(1.33±0.23)年。2組年齡(t=0.114)、病程(t=1.129)差異均無統(tǒng)計學意義(P>0.05),具有可比性。
納入標準[5]:(1)均符合中國抗癌協(xié)會2008年版乳腺癌診斷標準,病理診斷為ⅡB期或Ⅲ期。(2)新輔助化療(NAC)前麥默通針或空心針活檢。(3)病理結果完整,腋窩淋巴結轉移。剔除標準:(1)嚴重心、肝、腎等器官功能障礙,急慢性傳染病及其他惡性腫瘤患者。(2)妊娠或哺乳期。(3)已有遠處轉移。(4)對研究藥物過敏或有使用禁忌證。(5)預估生存期小于3個月。(6)臨床資料不完整或不愿意簽署知情同意書。本研究得到了醫(yī)院倫理委員會的批準[倫理號:2021-134-02(z)],所有患者均簽署知情同意書。
1.2 研究方法
1.2.1 術前治療
對照組術前采用多柔比星脂質體+環(huán)磷酰胺+白蛋白紫杉醇(AC-T)新輔助序貫化療,觀察組在對照組基礎上聯(lián)合PD-1抑制劑治療。
AC-T序貫化療方案。AC:第1天,靜脈注射鹽酸多柔比星脂質體30 mg/m2,環(huán)磷酰胺600 mg/m2;21 d為1周期,連續(xù)治療4個周期。前4個治療周期完成后序貫T:第1天,靜脈滴注白蛋白紫杉醇,每3周給藥1次,每次260 mg/m2,21 d為1周期,連續(xù)治療4個周期;序貫T治療同期,觀察組患者進行PD-1抑制劑(特瑞普利單抗240 mg)靜脈滴注,21 d為1周期,共治療4個周期。如果患者有任何不適或不良反應,應及時報告上級醫(yī)師,并采取相應的治療措施。
1.2.2 手術治療
所有患者完成免疫治療及新輔助化療8個周期結束3周后,且無手術禁忌證情況下行乳腺癌改良根治術。所有手術均由同一組人員完成。
1.3 觀察指標
(1)比較2組治療前后的免疫指標。(2)利用SF-36量表評估2組患者的生活質量,滿分為100分,得分與生活質量成正比。(3)臨床療效:治療8個周期后,根據(jù)實體瘤療效評價標準,完全緩解(complete response,CR)定義為所有病灶完全消失并維持≥3周。(4)比較2組手術時間、術中出血量及胃腸道反應、白細胞減少、肝功能障礙、靜脈炎的發(fā)生率。
1.4 免疫指標檢測
分別于新輔助化療前和新輔助化療結束后3周(手術前)采用美國貝克曼庫爾特Epics XL型流式細胞儀以及配套試劑盒測定外周血T淋巴細胞亞群(CD3+、CD4+、CD8+、CD4+/CD8+)。使用日立008AS生化分析儀,采用免疫比濁法測定IgG、IgA、IgM。所有操作均嚴格按照說明書進行。
1.5 統(tǒng)計學方法
采用SPSS 27.0軟件處理數(shù)據(jù)。計量資料以均數(shù)±標準差(x±s)表示,組間比較采用成組t檢驗;計數(shù)資料以例(%)表示,組間比較采用χ2檢驗。P<0.05為差異有統(tǒng)計學意義。
2 結果
2.1 2組患者臨床療效比較
治療8個周期后,觀察組的完全緩解率(CRR)高于對照組,手術時間和術中出血量均低于對照組(P<0.01),見表1。
2.2 2組患者免疫指標比較
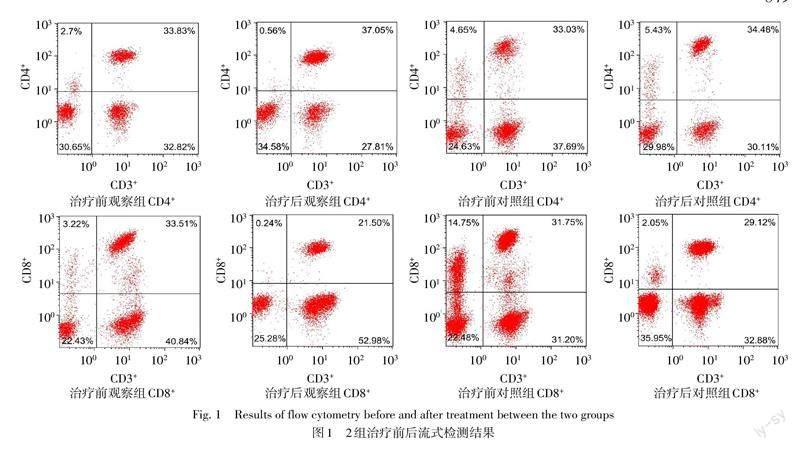
新輔助化療前2組患者CD4+、CD8+、CD4+/CD8+、IgG、IgA、IgM水平差異無統(tǒng)計學意義;新輔助化療8個周期結束后3周(手術前),觀察組前述指標均優(yōu)于對照組(P<0.05),見表2。流式細胞圖見圖1。
2.3 2組生活質量比較
治療前,2組生活質量評分差異無統(tǒng)計學意義;治療后,觀察組患者生活質量優(yōu)于對照組(P<0.01)。見表3。
2.4 2組不良反應發(fā)生情況比較
對照組患者術后并發(fā)胃腸道反應、白細胞減少、肝功能障礙及靜脈炎;觀察組無靜脈炎發(fā)生。2組不良反應發(fā)生率差異無統(tǒng)計學意義(52.5% vs. 40.0%,P>0.05)。見表4。
3 討論
3.1 TNBC的特點
TNBC具有惡性程度高、侵襲性強、內分泌治療和靶向治療效果差、易轉移和復發(fā)、預后差的特點[6-7]。由于乳腺癌主要發(fā)生在乳腺的腺上皮細胞中,并且乳腺不是支持人類生命活動的主要靶器官,因此乳腺原位腫瘤對人體的影響較小[8]。乳腺腫瘤細胞一旦失去正常的特性,就會導致細胞間連接的松弛和分裂,腫瘤細胞經(jīng)血液和淋巴流向全身并誘發(fā)轉移,危及患者的生命安全[9-10]。
3.2 乳腺癌手術的治療特點
目前,大多數(shù)乳腺癌患者采用保乳手術治療,該術式既彌補了改良根治術的缺陷,保留了患者正常的乳腺組織,又最大程度地減輕了患者的心理負擔[11]。相關研究表明,對于紫杉類+蒽環(huán)類+環(huán)磷酰胺治療后符合保乳適應證的晚期乳腺癌患者,保乳手術是一種安全可行的方法[12]。對于TNBC,保乳術前新輔助化療聯(lián)合AC-T序貫化療效果好,不良反應少。但保乳手術并不適合所有乳腺癌患者,仍有許多患者不能滿足保乳手術的適應證,因而改良根治術的應用仍然廣泛。乳腺癌的腫瘤細胞會通過血液循環(huán)轉移到身體的各個器官。因此,單一的手術治療不能完全殺死腫瘤細胞,術后轉移率和復發(fā)率仍然較高,這也是制約手術順利開展的主要因素。近年來,新輔助化療已廣泛應用于腫瘤的治療,其不僅可以治療局部晚期乳腺癌,還可用于乳腺癌手術治療的早期干預[13]。本研究結果也顯示治療8個周期后,觀察組CRR高于對照組,觀察組的手術用時、術中出血量均少于對照組。因此,這種潛在治療方法值得推廣。
3.3 免疫治療的特點
近年來,免疫治療已成為惡性腫瘤治療的一種新方法。結合傳統(tǒng)化療和放療的綜合治療策略已成為研究熱點[14]。PD-1/PD-L1作為一種免疫檢查點,具有免疫抑制因子的功能,可以抑制T淋巴細胞的活化和增殖,降低免疫系統(tǒng)的活性,該信號通路的激活是惡性腫瘤細胞逃避免疫殺傷的重要環(huán)節(jié)之一[15]。基于此,PD-1/PD-L1抑制劑可以靶向抑制PD-1/PD-L1活性,通過單克隆抗體及其受體結合抑制其負調控作用,恢復免疫系統(tǒng)活性,減少腫瘤的免疫逃逸[16]。研究發(fā)現(xiàn),免疫檢查點通路在腫瘤逃逸機制中起負向調節(jié)作用[17]。相關研究發(fā)現(xiàn)乳腺癌患者外周血T淋巴細胞亞群、CD3+、CD4+、CD8+及CD4+/CD8+水平均低于正常對照組,提示患者T淋巴細胞總數(shù)減少,免疫功能減弱[18]。T淋巴細胞總數(shù)的減少可促進腫瘤的增殖和生長。可見,乳腺癌的發(fā)生、發(fā)展及預后與患者的免疫功能密切相關。研究證實,阻斷PD-1/PD-L1信號通路可激活并上調CD8+T細胞的表達,提高其抗腫瘤活性,誘導腫瘤細胞表面主要組織相容性復合體分子表達,使更多腫瘤細胞暴露于免疫細胞[19]。本研究也顯示,觀察組采用新輔助化療聯(lián)合PD-1抑制劑治療后CD4+、CD8+、CD4+/CD8+均有所升高,且優(yōu)于對照組,表明新輔助化療聯(lián)合PD-1抑制劑治療TNBC能夠增強患者機體免疫力,抑制腫瘤細胞生長,從而縮小原發(fā)灶。此外,本研究也發(fā)現(xiàn),治療后觀察組生活質量優(yōu)于對照組,2組不良反應發(fā)生率無明顯差異。
綜上所述,TNBC采用新輔助化療聯(lián)合PD-1抑制劑治療可以有效提高患者免疫功能,改善患者生活質量,并保證臨床治療的安全性。相比單純新輔助化療,聯(lián)合PD-1抑制劑的抗腫瘤效應更高,為后續(xù)手術創(chuàng)造了條件,降低了手術難度,提高了手術效果,對TNBC的治療有較高的臨床應用價值。
參考文獻
[1] YIN L,DUAN J J,BIAN X W,et al. Triple-negative breast cancer molecular subtyping and treatment progress[J]. Breast Cancer Res,2020,22(1):61. doi:10.1186/s13058-020-01296-5.
[2] KWAPISZ D. Pembrolizumab and atezolizumab in triple-negative breast cancer[J]. Cancer Immunol Immunother,2021,70(3):607-617. doi:10.1007/s00262-020-02736-z.
[3] WON K A,SPRUCK C. Triple-negative breast cancer therapy:current and future perspectives (Review)[J]. Int J Oncol,2020,57(6):1245-1261. doi:10.3892/ijo.2020.5135.
[4] LEON-FERRE R A,HIEKEN T J,BOUGHRY J C. The landmark series:neoadjuvant chemotherapy for triple-negative and HER2-positive breast cancer[J]. Ann Surg Oncol,2021,28(4):2111-2119. doi:10.1245/s10434-020-09480-9.
[5] KEENAN T E,TOLANEY S M. Role of immunotherapy in triple-negative breast cancer[J]. J Natl Compr Canc Netw,2020,18(4):479-489. doi:10.6004/jnccn.2020.7554.
[6] EMENS L A. Breast cancer immunotherapy:facts and hopes[J]. Clin Cancer Res,2018,24(3):511-520. doi:10.1158/1078-0432.CCR-16-3001.
[7] BERGIN A R T,LOI S. Triple-negative breast cancer:recent treatment advances[J]. F1000Res,2019,8:F1000 Faculty Rev-1342. doi:10.12688/f1000research.18888.1.
[8] LYONS T. Targeted therapies for triple-negative breast cancer[J]. Curr Treat Options Oncol,2019,20(11):82. doi:10.1007/s11864-019-0682-x.
[9] ZHU Y,ZHU X,TANG C,et al. Progress and challenges of immunotherapy in triple-negative breast cancer[J]. Biochim Biophys Acta Rev Cancer,2021,1876(2):188593. doi:10.1016/j.bbcan.2021.188593.
[10] MARRA A,CURIGLIANO G. Adjuvant and neoadjuvant treatment of triple-negative breast cancer with chemotherapy[J]. Cancer J,2021,27(1):41-49. doi:10.1097/PPO.0000000000000498.
[11] NEDELJKOVI? M,DAMJANOVI? A. Mechanisms of chemotherapy resistance in triple-negative breast cancer-how we can rise to the challenge[J]. Cells,2019,8(9):957. doi:10.3390/cells8090957.
[12] GARRIDO-CASTRO A C,LIN N U,POLYAK K. Insights into molecular classifications of triple-negative breast cancer:improving patient selection for treatment[J]. Cancer Discov,2019,9(2):176-198. doi:10.1158/2159-8290.CD-18-1177.
[13] TARANTINO P,GANDINI S,TRAPANI D,et al. Immunotherapy addition to neoadjuvant chemotherapy for early triple negative breast cancer:a systematic review and meta-analysis of randomized clinical trials[J]. Crit Rev Oncol Hematol,2021,159:103223. doi:10.1016/j.critrevonc.2021.103223.
[14] SPORIKOVA Z,KOUDELAKOVA V,TROJANEC R,et al. Genetic markers in triple-negative breast cancer[J]. Clin Breast Cancer,2018,18(5):e841-e850. doi:10.1016/j.clbc.2018.07.023.
[15] WAKS A G,WINER E P. Breast cancer treatment:a review[J]. JAMA,2019,321(3):288-300. doi:10.1001/jama.2018.19323.
[16] CHAUDHARY L N,WILKINSON K H,KONG A. Triple-negative breast cancer:who should receive neoadjuvant chemotherapy?[J]. Surg Oncol Clin N Am,2018,27(1),141-153. doi:10.1016/j.soc.2017.08.004.
[17] POGGIO F,BRUZZONE M,CEPPI M,et al. Platinum-based neoadjuvant chemotherapy in triple-negative breast cancer:a systematic review and meta-analysis[J]. Ann Oncol,2018,29(7):1497-1508. doi:10.1093/annonc/mdy127.
[18] EMENS L A. Immunotherapy in triple-negative breast cancer[J]. Cancer J,2021,27(1):59-66. doi:10.1097/PPO.0000000000000497.
[19] BORRI F,GRANAGLIA A. Pathology of triple negative breast cancer[J]. Semin Cancer Biol,2021,72:136-145. doi:10.1016/j.semcancer.2020.06.005.
(2022-10-08收稿 2023-02-10修回)
(本文編輯 李鵬)

