桔梗皂苷D對(duì)大鼠急性腦梗死后神經(jīng)功能障礙和認(rèn)知功能障礙的改善作用
馮麗 賀慧敏 程林
缺血性卒中發(fā)生時(shí)因腦血流不足而引起的腦組織缺血性壞死。在當(dāng)下心腦血管疾病發(fā)病率不斷增加的的背景下缺血性卒中的發(fā)病率持續(xù)增高。由于腦對(duì)血液供給的敏感性,即使短期的血液閉塞也可導(dǎo)致對(duì)神經(jīng)元產(chǎn)生不可逆的損傷,并且大多數(shù)患者遭受隨之而來(lái)的神經(jīng)功能障礙和認(rèn)知功能障礙[1]。雖然美國(guó)食品藥品監(jiān)督管理局證明重組組織型纖溶酶原激活劑(tPA)可用于缺血性卒中治療中閉塞血管的再通,但tPA介導(dǎo)的有效溶栓治療窗較短,80%的患者因缺乏最佳溶栓治療而出現(xiàn)嚴(yán)重后遺癥甚至死亡[2]。此外,溶栓治療也增加了患者顱內(nèi)出血的風(fēng)險(xiǎn),極大地限制了其臨床應(yīng)用。目前,卒中的預(yù)防和治療仍然具有挑戰(zhàn)性,有必要找到與之相適應(yīng)的神經(jīng)保護(hù)藥物,確定合適和有效的治療策略,這對(duì)減輕腦缺血的神經(jīng)損傷具有重要意義。桔梗皂苷D(platycodin D,PLD),傳統(tǒng)中草藥的主要生物活性成分之一,是一種齊墩果烷型三萜皂苷,具有兩條糖鏈;在苷元的C-3位連接一個(gè)葡萄糖基,在C-28位連接其他4個(gè)糖殘基鏈[3]。已被證明調(diào)節(jié)許多涉及凋亡、炎癥、氧化應(yīng)激的生物過(guò)程[4]。先前的研究證明了預(yù)處理桔梗皂苷D降低了低氧/復(fù)氧誘導(dǎo)的H9c2心肌細(xì)胞的損傷[5]。然而,桔梗皂苷D在預(yù)防和治療腦缺血損傷中的功效仍不清楚。因此,為了進(jìn)一步確定桔梗皂苷D的用途,我們建立了局灶性腦缺血再灌注損傷模型,探討桔梗皂苷D的治療效果,并測(cè)定了神經(jīng)功能缺損評(píng)分、腦梗死面積、學(xué)習(xí)記憶能力、鐵死亡通路蛋白的表達(dá)。我們的發(fā)現(xiàn)為桔梗皂苷D在腦缺血再灌注損傷中的潛在應(yīng)用提供了線索。
1 材料與方法
1.1 儀器與試劑 研磨機(jī)、立體顯微鏡(南京江南永新光學(xué)有限公司,SZ6100)、水迷宮(上海新軟信息技術(shù)有限公司)、SDS-PAGE電泳設(shè)備(Bio-Rad,Mini Protean 3)、濕轉(zhuǎn)移膜儀器(Bio-Rad,170-3930)、脫色搖床(金壇醫(yī)療儀器,電化學(xué)發(fā)光成像系統(tǒng)(Tanon,180-5001)、BCA蛋白檢測(cè)試劑盒(Beyotime,P0010)、桔梗皂苷D(瑞芬思生物科技有限公司;純度≥99%)、抗MAP2/GPX4/FTH1/TfR1抗體(Abcam),以及HRP抗兔抗體(Beyotime,A0208)。
1.2 分組和動(dòng)物管理 60只雄性Sprague-Dawley(SD)大鼠(年齡8周;體重220~250 g)購(gòu)自上海Alac實(shí)驗(yàn)動(dòng)物有限公司(中國(guó)上海);許可證號(hào):SCXK(上海)2020-09。所有實(shí)驗(yàn)均按照《實(shí)驗(yàn)動(dòng)物飼養(yǎng)管理和使用指南》(美國(guó)國(guó)家研究委員會(huì))進(jìn)行,并經(jīng)本單位實(shí)驗(yàn)動(dòng)物使用倫理委員會(huì)批準(zhǔn)。所有的大鼠都喂以標(biāo)準(zhǔn)嚙齒動(dòng)物食物,無(wú)菌超純水可自由獲取,飼養(yǎng)在22%~25℃的環(huán)境中,濕度為40%~70%,光照-黑暗周期為12 h。正式實(shí)驗(yàn)前動(dòng)物適應(yīng)7 d。將總共60只SD大鼠隨機(jī)分成4組(n=15):偽手術(shù)組(SHAM)、急性腦梗死組(MCAO)、急性腦梗死低劑量桔梗皂苷D治療組(MCAO + 桔梗皂苷D 10 mg/kg, MCAO+PLD-L)、急性腦梗死高劑量桔梗皂苷D治療組(MCAO + 桔梗皂苷D 20 mg/kg, MCAO+PLD-H),并在后續(xù)研究中采取雙盲策略進(jìn)行檢測(cè)。桔梗皂苷D溶于無(wú)菌0.9%氯化鈉溶液水中。實(shí)驗(yàn)組大鼠每天腹腔注射10或20 mg/kg桔梗皂苷D,而假手術(shù)組和MCAO組每天給予相同體積的0.9%氯化鈉溶液,持續(xù)10 d。桔梗皂苷D劑量的選取參考自之前的研究[6]。
1.3 MCAO大鼠模型的建立 采用線栓法制備大鼠局灶性腦缺血再灌注損傷模型[7],首先通過(guò)腹膜內(nèi)注射1%戊巴比妥鈉然后固定在仰臥位。頸部被剃光并消毒,用于常規(guī)皮膚準(zhǔn)備。做一個(gè)中線頸部切口以分離右側(cè)頸總動(dòng)脈、頸外動(dòng)脈和頸內(nèi)動(dòng)脈,然后結(jié)扎頸外動(dòng)脈及其遠(yuǎn)端。暫時(shí)夾住頸總動(dòng)脈和頸內(nèi)動(dòng)脈的近端。在靠近頸總動(dòng)脈分叉處的頸外動(dòng)脈上做一個(gè)小切口,并插入涂有硅的縫合線。移除頸內(nèi)動(dòng)脈上的夾子,將縫合線通過(guò)頸外動(dòng)脈輕輕插入頸內(nèi)動(dòng)脈,直到大腦中動(dòng)脈的起點(diǎn)被堵塞。縫合線的長(zhǎng)度為18~20 mm。將縫合線收緊,移除頸總動(dòng)脈上的夾子。然后縫合頸部皮膚;缺血狀態(tài)后2 h,拆除縫線,使血液供應(yīng)再灌注。在假手術(shù)組,只解剖頸內(nèi)動(dòng)脈,不做任何其他手術(shù)。術(shù)后連續(xù)3 d肌內(nèi)注射10萬(wàn)U青霉素鈉預(yù)防感染。
1.4 TTC染色法 將TTC粉末(0.2 g)溶解在10 ml PBS中,制成2% TTC染料溶液。將每組大鼠斷頭,收集腦組織并在20℃冷凍30 min。冠狀切片是從額葉到半球背面(2 mm)制作的。將切片浸入TTC染料溶液中,在37℃培養(yǎng)箱中孵育20 min,每5分鐘翻轉(zhuǎn)1次并避光。清洗后,將切片在10%甲醛溶液中固定5~10 min,吸收多余的液體,將切片拍照。并記錄梗塞面積占總面積的百分比:梗塞面積百分比(%)=蒼白面積/腦切片面積。
1.5 神經(jīng)功能評(píng)估 采用Longa評(píng)分法對(duì)神經(jīng)功能進(jìn)行評(píng)分。評(píng)分標(biāo)準(zhǔn):0分,無(wú)神經(jīng)功能缺損;1分,左前肢不能完全伸展;2分,左轉(zhuǎn)圈;3分,走路時(shí)向左傾倒;4分,無(wú)法自行行走或意識(shí)喪失;5分,死亡。1~3分表示大鼠模型誘導(dǎo)成功。
1.6 學(xué)習(xí)和記憶評(píng)估 用桔梗皂苷D治療后,為評(píng)估大鼠學(xué)習(xí)和記憶能力的變化。給藥10 d后,大鼠接受Morris水迷宮訓(xùn)練5 d,并在第6天進(jìn)行測(cè)試,以評(píng)價(jià)它們的學(xué)習(xí)記憶能力。定位導(dǎo)航訓(xùn)練持續(xù)5 d。大鼠每天在固定時(shí)間接受1次訓(xùn)練。它們被依次放置在c、d、a和b象限的水中。將大鼠入水后120 s內(nèi)爬上平臺(tái)的時(shí)間記錄為該象限搜索平臺(tái)的潛伏期。如果大鼠不能在120 s內(nèi)爬上平臺(tái),將它們帶到平臺(tái),記錄潛伏期為120 s。所有大鼠完成第一象限訓(xùn)練后,依次開(kāi)始下一象限訓(xùn)練,直到所有大鼠完成所有象限的訓(xùn)練。訓(xùn)練結(jié)束時(shí),老鼠爬上或被帶到平臺(tái)上,休息30 s,然后回到它們的籠子里。記錄四象限潛伏期的平均值作為訓(xùn)練的逃避潛伏期。第6天空間探索實(shí)驗(yàn):拆除平臺(tái),將大鼠置于平臺(tái)與目標(biāo)象限相對(duì)的象限。在120 s內(nèi)記錄在目標(biāo)象限花費(fèi)的時(shí)間和大鼠穿過(guò)平臺(tái)所在目標(biāo)象限的次數(shù)。
1.7 蛋白質(zhì)印跡分析 通過(guò)斷頭處死大鼠,用剪刀取出海馬組織并放入勻漿器中。將1 mg組織加入10 ml裂解溶液中,將勻漿置于冰上30 min。將裂解的蛋白質(zhì)轉(zhuǎn)移到4℃的1.5 ml離心管中,并以10 000 r/min的速度離心15 min。將上清液轉(zhuǎn)移到Eppendorf管中,將提取的蛋白質(zhì)與上樣緩沖液以1∶4 的體積混合,然后置于金屬浴中,在100℃變性10 min。10% SDS-PAGE電泳后,將蛋白質(zhì)條帶轉(zhuǎn)移到PVDF膜上。室溫下用5%牛奶封閉緩沖液封閉膜1 h,用tris緩沖鹽水和吐溫20(TBST)洗滌3次,每次5 min,然后與目標(biāo)抗體(1∶1 000)在4℃下孵育過(guò)夜。用TBST洗滌3次(每次5 min)后,將膜與相應(yīng)的二抗(1∶5 000稀釋)在室溫下孵育1 h。用TBST洗滌3次(每次5 min)后,將膜與ECL檢測(cè)試劑一起孵育。使用化學(xué)發(fā)光成像儀拍攝圖像。Image J軟件用于定量分析蛋白質(zhì)條帶的光密度。
1.8 免疫熒光染色 將獲得的腦組織用4%多聚甲醛在室溫下固定24 h,并轉(zhuǎn)移到30%蔗糖溶液中。切成30 μm冰凍切片后用0.01 mol/L PBS洗滌5 min,用5%山羊血清,然后與針對(duì)MAP-2的一抗(1∶500)孵育過(guò)夜。洗滌后,將樣品與山羊抗兔Alexa-Fluor IgG二抗(1∶300)在室溫下反應(yīng)1 h。細(xì)胞核在室溫下用DAPI染色10 min。在高倍視野下觀察損傷海馬的圖像(放大倍數(shù)×200;奧林巴斯BX53)。
1.9 統(tǒng)計(jì)學(xué)分析 應(yīng)用SPSS 23.0統(tǒng)計(jì)軟件,使用方差分析(ANOVA)各組間差異。組間比較采用Tukey多重比較檢驗(yàn)。P<0.05為差異有統(tǒng)計(jì)學(xué)意義。
2 結(jié)果
2.1 桔梗皂苷D治療改善急性腦梗死引起的神經(jīng)功能缺陷 給藥10 d后,使用Longa評(píng)分法對(duì)大鼠的神經(jīng)功能缺損進(jìn)行評(píng)分。桔梗皂苷D組的神經(jīng)功能缺損評(píng)分低于MCAO組,劑量桔梗皂苷D組與MCAO組間均存在差異(P<0.05)。然而,高劑量組差異更明顯,這些發(fā)現(xiàn)表明用桔梗皂苷D治療可以改善急性腦梗死引起的神經(jīng)功能缺陷。見(jiàn)表1。
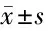
表1 桔梗皂苷D對(duì)急性腦梗死大鼠模型神經(jīng)功能缺損的影響 n=7,分,
2.2 桔梗皂苷D治療減少了腦梗死面積 為探討桔梗皂苷D治療對(duì)腦梗死的影響,用Image J分析并記錄MCAO大鼠的梗死面積。TTC染色圖像上的白色區(qū)域表示梗塞區(qū)域。與假手術(shù)組比較,MCAO模型組腦梗死面積明顯增加(P<0.01)。給藥10 d后,與MCAO組比較,高劑量桔梗皂苷D組梗死面積減小明顯減少;高劑量藥物組比低劑量藥物組降低更顯著(P<0.01)。見(jiàn)圖1,表2。
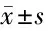
表2 桔梗皂苷D對(duì)急性腦梗死大鼠模型腦梗死面積的影響 n=8,%,
2.3 桔梗皂苷D治療減輕了急性腦梗死引起的空間認(rèn)知功能缺陷并促進(jìn)了功能恢復(fù) 為了評(píng)估桔梗皂苷D治療對(duì)存活神經(jīng)元和腦功能狀態(tài)的作用,使用Morris水迷宮評(píng)估大鼠的學(xué)習(xí)和記憶。定位導(dǎo)航實(shí)驗(yàn)中較長(zhǎng)的逃脫潛伏期和空間探索實(shí)驗(yàn)中較少的穿越平臺(tái)的情況表明學(xué)習(xí)和記憶能力的缺陷。訓(xùn)練5 d后,目標(biāo)象限中的平臺(tái)被移除后,假手術(shù)組在目標(biāo)象限中花費(fèi)的時(shí)間最長(zhǎng),而MCAO組最短。 桔梗皂苷D治療組花費(fèi)在目標(biāo)象限的時(shí)間顯著高于MCAO組。此外,假手術(shù)組大鼠穿越隱蔽平臺(tái)的次數(shù)最多,而MCAO組大鼠穿越隱蔽平臺(tái)的次數(shù)最少。 桔梗皂苷D組的平臺(tái)穿越次數(shù)明顯高于MCAO組,且以高劑量組效果最為明顯(P<0.05)。見(jiàn)表3,圖2。

圖2 桔梗皂苷D對(duì)MCAO大鼠模型水迷宮表現(xiàn)的影響
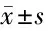
表3 桔梗皂苷D對(duì)急性腦梗死大鼠水迷宮學(xué)習(xí)認(rèn)知功能影響 n=7,
2.4 桔梗皂苷D治療上調(diào)了海馬中軸突蛋白的表達(dá) 對(duì)軸突蛋白MAP2進(jìn)行免疫熒光染色,結(jié)果顯示,與假手術(shù)組比較,MCAO海馬MAP2染色強(qiáng)度降低。與MCAO模型組比較,桔梗皂苷D低劑量組和高劑量組的MAP2表達(dá)明顯增加。見(jiàn)圖3。

圖3 桔梗皂苷D對(duì)MCAO大鼠模型海馬MAP2表達(dá)的影響(標(biāo)尺=100 μm)
2.5 桔梗皂苷D治療調(diào)節(jié)海馬鐵死亡相關(guān)蛋白的水平 通過(guò)蛋白質(zhì)印跡法測(cè)定鐵死亡相關(guān)蛋白,即GPX4、FTH1、和TfR1的表達(dá)水平。結(jié)果顯示,與假手術(shù)組比較,MCAO組的GPX4和FTH1水平顯著降低(P<0.001),桔梗皂苷D治療逆轉(zhuǎn)了這一趨勢(shì)。與假手術(shù)組比較,MCAO組的TFR1水平顯著升高(P<0.001),桔梗皂苷D低劑量組和高劑量組的TfR1表達(dá)明顯降低。與此一致的是,MCAO組海馬中鐵含量顯著增加,而桔梗皂苷D治療逆轉(zhuǎn)了這一趨勢(shì)。見(jiàn)圖4,表4。

圖4 桔梗皂苷D對(duì)MCAO大鼠模型鐵死亡相關(guān)通路蛋白表達(dá)的影響
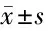
表4 桔梗皂苷D對(duì)急性腦梗死大鼠鐵死亡相關(guān)通路蛋白的定量分析 n=8,
3 討論
卒中是全球殘疾和發(fā)病的主要原因,全球有超過(guò)8 000萬(wàn)人患有卒中,卒中是204個(gè)國(guó)家和地區(qū)≥50歲成年人殘疾調(diào)整生命年的首要原因[8]。與此同時(shí),由于人口增長(zhǎng)和老齡化,中國(guó)年齡≥40歲的成年人卒中患病率亦一直增加[9]。腦卒中患者的神經(jīng)功能缺損和認(rèn)知障礙是卒中后認(rèn)知障礙的一個(gè)常見(jiàn)但被忽視的后果。研究表明,超過(guò)一半的卒中患者有認(rèn)知障礙[10]。且其治療方案獲得的治療效果有限。因此,進(jìn)一步明確卒中后病理生理的發(fā)展機(jī)制并開(kāi)發(fā)更有效的治療方案是非常必要的。
在缺血/再灌注開(kāi)始后,顯著的氧化應(yīng)激和炎癥被顯著觸發(fā)[7],鐵死亡是一種最近被認(rèn)識(shí)到的依賴于鐵和活性氧簇(ROS)的程序性細(xì)胞死亡形式,并被認(rèn)為參與了再灌注損傷。因此,鐵死亡為理解和治療許多疾病提供了新的途徑[11]。鐵死亡在缺血性損傷中的研究已經(jīng)在許多器官中進(jìn)行,包括心臟、腸和肝臟[12-14]。最近的研究揭示了鐵死亡和腦缺血的密切聯(lián)系,鐵死亡抑制劑成功地減少了腦的缺血性損傷[15]。抑制鐵死亡可能成為相關(guān)缺血性疾病的有效治療策略和起效方式。
缺血性卒中發(fā)生時(shí),由于向大腦供應(yīng)充足血液的動(dòng)脈阻塞,氧氣和營(yíng)養(yǎng)物質(zhì)的耗盡會(huì)激活過(guò)量的氧化應(yīng)激、引起線粒體損傷并最終導(dǎo)致細(xì)胞死亡[16]。鐵是平衡大腦組織能量代謝的一把雙刃劍:一方面,鐵對(duì)于正常大腦功能催化產(chǎn)生大量ATP是不可或缺的;另一方面,大腦極易受到鐵依賴的氧化應(yīng)激的影響[17]。鐵積累被廣泛的觀察到發(fā)生于缺血性卒中的臨床病例和動(dòng)物模型中的神經(jīng)元上[18]。另一方面,鐵螯合劑被發(fā)現(xiàn)在腦出血性卒中的過(guò)程中科研改善腦水腫、減少神經(jīng)元死亡并阻止腦萎縮[19]。因此,針對(duì)鐵死亡靶點(diǎn)的保護(hù)策略,可潛在用于治療缺血性卒中患者。
作為一種可逆轉(zhuǎn)多種氧化應(yīng)激損傷的單體物質(zhì),桔梗皂苷D已被發(fā)現(xiàn)在氧化應(yīng)激損傷中發(fā)揮作用[12,20]。在心肌細(xì)胞缺氧/復(fù)氧模型中。結(jié)果表明,桔梗皂苷D被發(fā)現(xiàn)可通過(guò)誘導(dǎo)Akt/Nrf2/HO-1通路的激活發(fā)揮其保護(hù)作用[11]。此外,在高糖刺激的糖尿病腎病細(xì)胞模型中,GPX4表達(dá)下調(diào),桔梗皂苷D可通過(guò)調(diào)節(jié)GPX4的表達(dá)抑制了鐵死亡[21]。桔梗皂苷D可通過(guò)增加海馬中的突觸發(fā)生增強(qiáng)了小鼠的認(rèn)知功能[22]。這些結(jié)果積極提示桔梗皂苷D可通過(guò)調(diào)節(jié)鐵死亡相關(guān)通路發(fā)揮對(duì)卒中模型的保護(hù)作用。因此,我們?cè)贛CAO大鼠卒中模型中觀察了桔梗皂苷D對(duì)卒中后神經(jīng)癥狀及認(rèn)知功能損傷的作用及鐵死亡相關(guān)蛋白水平的影響。正如預(yù)期的那樣,桔梗皂苷D顯著改善了卒中大鼠的神經(jīng)癥狀和認(rèn)知功能,并通過(guò)調(diào)節(jié)鐵死亡相關(guān)蛋白分子的表達(dá)參與了到了鐵死亡過(guò)程的調(diào)節(jié)中。桔梗皂苷D顯著逆轉(zhuǎn)了損傷導(dǎo)致的被抑制的FTH1和GPX4的表達(dá),并降低了海馬中的鐵含量,這將有效阻斷鐵死亡進(jìn)展。桔梗皂苷D治療可能部分地通過(guò)增加海緩解鐵死亡發(fā)生來(lái)促進(jìn)相關(guān)癥狀的恢復(fù)。
綜上,本研究表明,桔梗皂苷D的治療減輕了大鼠缺血性卒中后的神經(jīng)和認(rèn)知功能障礙,起到了明顯的神經(jīng)保護(hù)作用。我們的結(jié)果還證實(shí)桔梗皂苷D的作用是通過(guò)調(diào)節(jié)鐵死亡相關(guān)途徑的表達(dá)實(shí)現(xiàn)的。這些發(fā)現(xiàn)為開(kāi)發(fā)抗腦缺血和腦缺血/再灌注損傷的藥物提供了新的視角。
- 河北醫(yī)藥的其它文章
- 牙周炎和動(dòng)脈粥樣硬化共同危險(xiǎn)因素及相關(guān)機(jī)制研究進(jìn)展
- 唾液腺腺樣囊性癌嗜神經(jīng)侵襲微環(huán)境的研究進(jìn)展
- 基于互聯(lián)網(wǎng)模式的延續(xù)性干預(yù)對(duì)腦小血管病伴OSAHS認(rèn)知障礙患者精神狀態(tài)和生活質(zhì)量的影響
- 紅光照射聯(lián)合改良負(fù)壓封閉引流在糖尿病足潰瘍患者中的應(yīng)用
- 三位一體協(xié)同管理模式在預(yù)防骨科急癥內(nèi)固定術(shù)后患者圍術(shù)期血栓中的應(yīng)用
- 乳腺癌化療患者PICC并發(fā)癥預(yù)警模型的構(gòu)建及運(yùn)行效果評(píng)價(jià)

