例談玻爾原子理論中的量子化條件與應用
許冬保
(江西省九江第一中學 332000)
1 玻爾原子理論基本假設
玻爾理論是繼普朗克量子假說和愛因斯坦光子理論之后,向微觀研究領域跨出的重要一步,開創了原子現象研究的先河.玻爾理論中軌道量子化條件表明,普朗克常量在原子現象中起著十分重要的作用,它不僅決定了原子的大小、原子的能級結構,同時它也能很好地說明氫原子光譜.
1.1 現行高中教材的表述
在人教版物理教材中,在“氫原子光譜和玻爾的原子模型”一節中,介紹了玻爾原子理論的基本假設,其內容要點包括2方面內容,即:
(1)軌道量子化與定態:玻爾認為,原子中的電子在庫侖力的作用下,繞原子核做圓周運動……;電子運行的軌道半徑不是任意的,只有當半徑的大小符合一定條件,這樣的軌道才是可能的.也就是說電子的軌道是量子化的.
(2)頻率條件:當電子從能量較高的定態軌道(其能量記為En)躍遷到能量較低的定態軌道(能量記為Em,)時,會放出能量為hν的光子(h是普朗克常量),這個光子的能量由前后兩個能級的能量差決定,即hν=En-Em.
1.2 玻爾氫原子量子化條件
現行教材中,玻爾提到的軌道量子化,僅僅局限在文字描述的層面,未給出定量的表達式,存在明顯的缺陷,由此帶來學生知識結構的斷裂.玻爾量子化條件表述如下:
考察氫原子,若核外電子的質量為m,在半徑為r的圓周軌道上以速率v運動;普朗克常量為h,約化普朗克常量為?,則有

上式為玻爾量子化條件的數學表達式,n為量子數.
表達式中的“mv·r”是動量與半徑的乘積,為電子運動的角動量大小.
2 應用分析
補充了氫原子軌道量子化條件,完善了玻爾氫原子模型的認知結構,對于有關問題的分析便不再存在困惑.
2.1 玻爾軌道量子化條件與德布羅意波長之間的關系
例1 德布羅意指出:玻爾模型與電子的德布羅意波長之間存在著一個很有意思的關系,敘述并推導這個關系.
解析德布羅意認為,實物粒子也具有波動性,與實物粒子相聯系的波稱為德布羅意波或物質波.德布羅意發現,玻爾提出氫原子中電子的圓軌道模型,剛好能容納整數個電子的德布羅意波長,否則氫原子便是不穩定的.
設電子的德布羅意波長為λ,如上所述,對于氫原子核外電子,玻爾軌道量子化條件,表述為
2πr=nλ(n=1,2,3…)
該式的物理意義是:電子繞核運動周長等于其德布羅意波長的整數倍.
評述在歷史上,玻爾1913年提出氫原子理論.1924年德布羅意提出物質波的概念,至此,玻爾軌道量子化條件才具有較直觀的物理意義.
2.2 玻爾氫原子模型
例2設無限遠處氫原子體系的電勢能為零,已知電子電荷量為e,質量為m,普朗克常量為h,靜電力常量為k,試求量子數為n時:
(1)核外電子軌道半徑的表達式;
(2)氫原子處于基態時的電離能.

評述在推導氫原子核外電子軌道半徑及氫原子能級的過程中,依照經典電磁理論、牛頓運動定律及軌道量子化條件建立方程,其中,玻爾軌道量子化條件是量子論思想的表現,也是玻爾氫原子理論精髓之處.氫原子能級表達式也可由巴耳末公式導出.過程如下:

2.3 玻爾類氫離子模型
例3已知電子電荷量為e,質量為m,普朗克常量為h,靜電力常量為h.根據玻爾原子模型導出He+的能量表達式.
解析設電子電荷量為e,質量為m,運動速率為v,軌道半徑為r.由玻爾軌道量子化條件,有
在庫侖力作用下電子做圓周運動滿足的方程為
取無窮遠處電勢為零,He+具有的電勢能
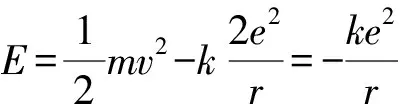
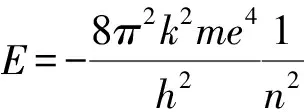
評述He+離子中原子核帶兩個單位的正電荷,核外一個電子,與氫原子結構相仿,稱為類氫離子,玻爾理論仍然成立.導出過程中所用的思維方法完全相同.
2.4 類氫原子模型
例4(清華大學2020年強基計劃測試題)氫原子核外電荷若被粒子μ-取代,已知它的質量是電子的207倍,電荷與電子相同,則與電子相比,其基態的能量、角動量、軌道半徑分別為原先的多少倍( ).


解析由例1知,處于基態的氫原子,其軌道半徑及能級分別為
取氫原子核質量為電子質量m的1836倍;氫原子核外電荷若被粒子μ-取代,則系統的約化質量μ為
設氫原子基態能量為EH.若氫原子核外電荷被粒子μ-取代,基態能量記為Eμ,有
由玻爾軌道量子化條件,有

當n=1時,基態角動量相等.
設氫原子基態軌道半徑為rH.若氫原子核外電荷被粒子μ-取代,基態軌道半徑記為rμ,得
綜上,正確選項是D.
點評分析μ-繞原子核的運動如同電子繞原子核的運動,分析中所使用的物理方法相同.基于玻爾氫原子模型的分析,氫原子核外電荷若被粒子μ-取代,則需要將電子的質量改為系統的約化質量.
2.5 奇特原子模型
例5 (2012清華保送生測試)物理學家在微觀領域發現了“電子偶素”這一現象.所謂“電子偶素”就是由一個負電子和一個正電子繞它們的質量中心旋轉形成的相對穩定的系統.已知正、負電子的質量均為m,電荷量大小均為e,普朗克常數h,靜電力恒量k.
(1)用玻爾模型推算“電子偶素”的基態半徑;
(2)求賴曼線產生光子的最高頻率.
解析(1)由牛頓運動定律,有


“電子偶素”系統具有的能量


評述奇特原子類似氫原子體系,通常由μ±子、τ±子、π±介子、D±介子、正電子、反質子、Σ±超子和Ω-超子等粒子組成,它們分別取代普通原子中的電子、原子核或取代兩者通過電磁作用形成的原子.其中原子核被取代的粒子稱為粒子素.不難發現,例4中的μ-子替換電子后,氫原子成為奇特原子.本例中的“電子偶素”即由正電子取代原子核而成,“電子偶素”可視為類氫原子,顯然玻爾理論仍適用.

