通量平滑度對肺癌放療物理劑量和生物劑量的影響
彭圣賢 龐 亞 劉 悅 王 東
(ThePracticalJournalofCancer,2023,38:0167~0171)
肺癌的發病率在全球居于首位,在我國也長期居于第一[1-2]。放射治療可以作為肺癌的一種重要治療手段。在調強放射治療優化系統中,計劃系統(treatment planning system,TPS)通過逆向優化迭代重建算法產生射束(beamlet)的通量,即“最優通量圖”。計劃復雜性可以描述為射束通量分布大小[3-4]。靶區和危及器官(organs at risk,OARs)越復雜的幾何形狀決定了更高的靶區適形度,并且越壓低OAR劑量,通量圖就越復雜;反之,對OAR劑量要求寬松,靶區適形度變差,通量復雜度就降低。在臨床工作中,一些復雜且苛刻的放療計劃會造成放療計劃系統運算時間長,執行計劃的機器跳數增加,給機器帶來負擔。當前多種計劃系統自帶通量平滑度選項[5],因此本研究以肺癌放療為例,基于Eclipse系統,比較靶區和OAR的劑量學和放射生物學在不同通量平滑參數時的參數差異。
1 資料與方法
1.1 通量平滑度
在調強優化系統中,當設定射野方向和定義靶區以及OAR的限制參數后,TPS通過逆向計劃優化算法產生射束的通量。通量平滑分為兩個方向,一個方向與MLC運動相向,另一個方向與MLC運動垂直。其中與MLC運動相向平滑值可以大大影響葉片運動的復雜性并降低機器跳數MU;與MLC運動垂直的平滑則影響MLC 的“凹凸槽”效應。通量平滑函數是優化罰分函數的一部分。系統在優化時不區分靶區和危及器官的罰分函數如(1)所示[6]。
式(1)中第四項為與通量平滑有關的罰分函數。
1.2 臨床資料
回顧性分析選取2019年6月至2019年12月在自貢市第一人民醫院腫瘤科治療的20例肺癌患者,使用碳纖維板、熱塑膜聯合枕頭固定患者,統一取仰臥位,在飛利浦CT模擬定位機下增強掃描。由副主任醫師按照ICRU83報告靶區和左右肺、心臟、脊髓等OAR。
1.3 計劃設計
對每個患者制定6組逆向調強計劃,第一組計劃使用默認的通量平滑值Smooth 40 30,即與MLC平行方向為40,與MLC垂直的方向平滑為30。本研究危及器官權重設定位100,依據通量平滑值與危及器官目標函數最大權重百分比制定其他五組逆向調強計劃。其他五組依次為Smooth 0 0、Smooth 20 10、Smooth 60 50、Smooth 80 70、Smooth 100 100。每個患者6組計劃均是設計固定野調強(fixed field Intensity Modulated Radiotherapy,ff-IMRT),射線均為6MV X射線,處方劑量均為66 Gy/33F。各組計劃優化條件一致,計劃系統為Eclipse v13.6,在Varian Trilogy加速器上治療。
1.4 計劃評估
1.4.1 劑量學參數 從放療計劃的劑量-體積直方圖(dose-volume histogram,DVH)來獲取放療計劃PTV和OAR的評估指標和各參數計算,參考國際輻射單位與測量委員會83號報告[7]。靶區的評估指標為:D2、平均劑量Dmean、D98,其中D2、D98分別為包圍PTV體積2%、98%的最低劑量;均勻性指數(homogeneity index, HI)定義為HI=(D2-D98)/Dmean,HI值越小,則PTV劑量越均勻。適形度指數(conformity index,CI)定義為CI=(VT,r/VT)×(VT,r/Vr),其中VT為PTV體積,VT,r為處方劑量所包繞的PTV體積,Vr為處方劑量所包繞的總體積,CI值上限為1,越大說明靶區越適形。各危及器官的劑量參數為肺V5、V20、V30;心臟V30、V40、Dmean,脊髓Dmax。此外,評估各計劃的機器跳數(monitor unit,MU)。
1.4.2 放射生物學參數 腫瘤控制概率(tumor control probability,TCP)和正常組織并發癥概率(normal tissue complication probability,NTCP)采用文獻的放射生物學模型[8]。等效均勻劑量(equivalent uniform dose,EUD)函數用于評價某一解剖結構受到不均勻劑量照射的生物學效應,如式(2)所示。該公式適用于腫瘤和正常組織。
式(2)中,N為靶區或者正常組織內總的體素個數,di為第i個體素的點劑量,a為不同組織的體積特性參數。基于EUD,TCP可以定義為式(3)[9-11]:
式(3)中,TCD50為腫瘤控制率為50%的劑量,γ50為腫瘤控制概率為50%時劑量響應曲線的斜率,為無量綱參數。基于EUD,對于正常組織,NTCP可以定義為式(4):
式(4)中,TD50為正常組織5年出現50%并發癥概率的耐受劑量。γ50為正常組并發癥概率為50%時劑量響應曲線的斜率。
1.5 統計學方法
應用SPSS v22.0軟件進行統計處理,經檢驗符合正態分布,數據以均值±標準差表示,對照組Smooth 40 30與其他組采用配對t檢驗,P<0.05為差異有統計學意義。
2 結果
2.1 劑量學參數結果
圖1所示是某個病例通量平滑為6組計劃的靶區劑量分布圖。表1所示是6組通量平滑靶區PTV的劑量學參數。與對照組Smooth 40 30相比,Smooth 0 0、Smooth 20 10通量組的D2有統計學差異(P<0.05);所有組CI和D98均有統計學差異(P<0.05);Smooth 0 0、Smooth 100 100通量組的Dmean有統計學差異(P<0.05);Smooth 100 100通量組的HI有統計學差異(P<0.05)。從表2中OAR劑量學看出,通量平滑值在Smooth 40 30以上,OAR受量增加。與Smooth 40 30相比,只有Smooth 100 100危及器官受量指標有統計學差異(P<0.05),其他大部分指標無統計學差異(P>0.05)。
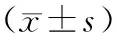
表1 靶區劑量學參數比較
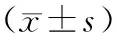
表2 危及器官劑量學參數比較
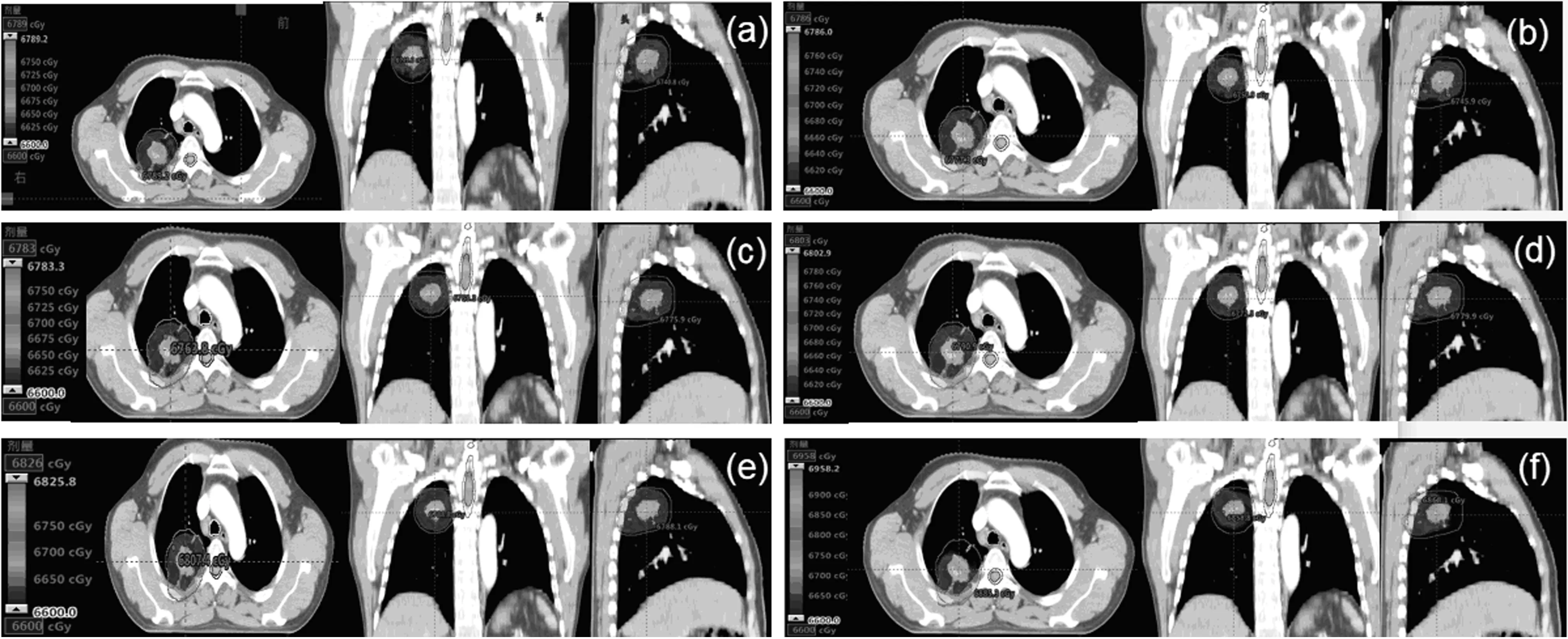
注:a為Smooth 0 0;b為Smooth 20 10;c為Smooth 40 30;d為Smooth 60 50;e為Smooth 80 70;f為Smooth 100 100。圖1 六組計劃的靶區劑量分布圖
圖2是機器跳數(MU)的平均值隨通量平滑變化的趨勢圖。與Smooth 40 30相比,其他通量平滑組MU均有統計學差異(P<0.05)。從圖中看出,隨著通量平滑值,MU顯著減小。
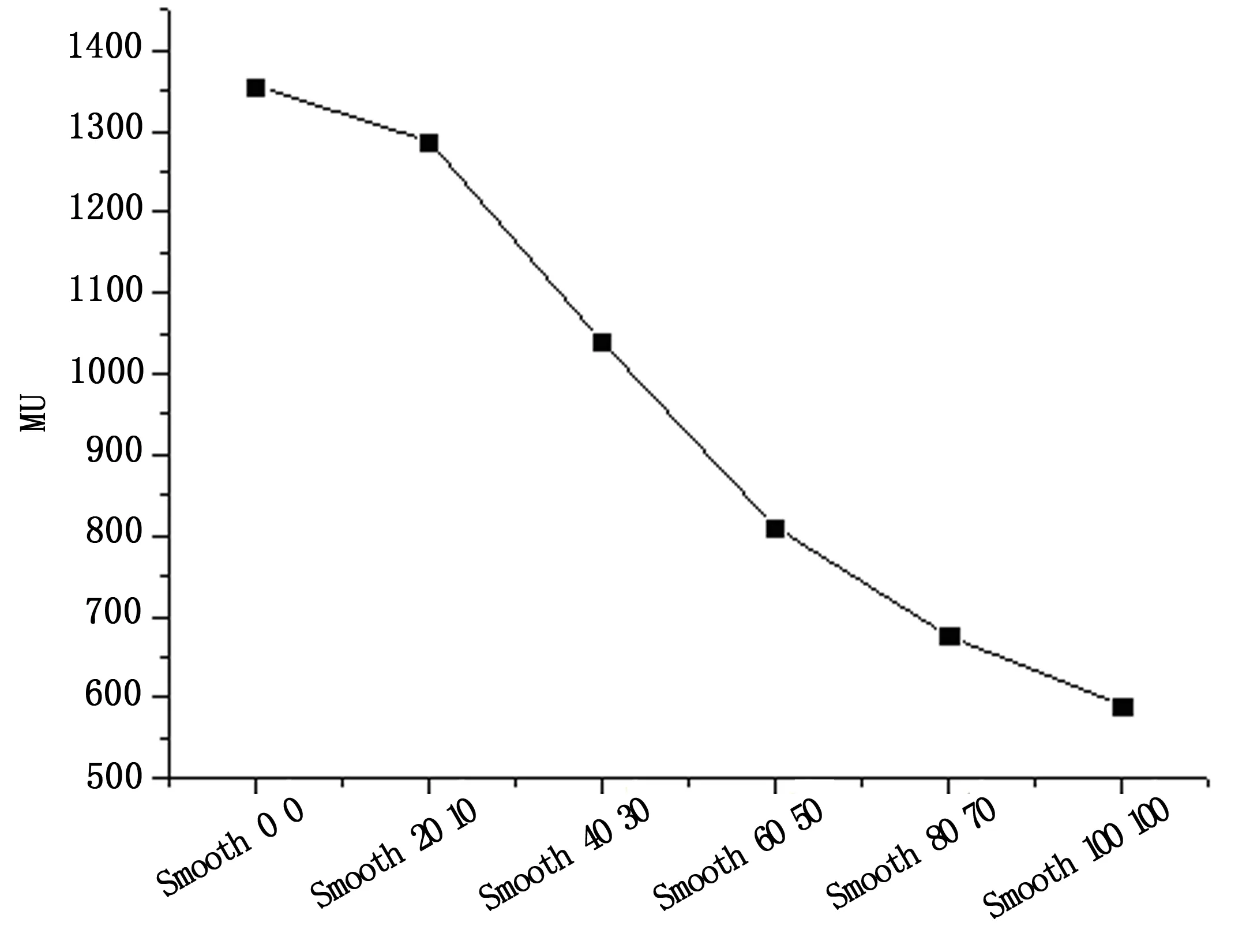
圖2 MU隨通量變化
2.2 放射生物學參數結果
在Eclipse計劃系統中以0.1 Gy為間隔導出txt格式的DVH圖,利用Matlab程序[12]計算TCP和NTCP。對于PTV,TCD50=36.5,γ50=0.72,a=-13,α/β=10,危及器官肺TD50=24.5,γ50=2,a=3,α/β=3;心臟TD50=50,γ50=3,a=3,α/β=2;脊髓TD50=66.5,γ50=4,a=13,α/β=2。計算所需的相關參數來自參考文獻[13-15]。
圖3所示為PTV靶區 TCP平均值,正常肺,脊髓和心臟的NTCP平均值隨通量平滑變化圖。與Smooth 40 30通量組相比,其他通量組TCP均無統計學意義(P>0.05);正常肺NTCP除Smooth 0 0,Smooth 20 10外、其他通量組有統計學意義(P<0.05)。脊髓和心臟的NTCP無統計學差異(P>0.05)。
3 討論
以往的報道多數是僅針對劑量學依據[16-18],少數以生物劑量為依據報道[19]。本研究結合物理劑量和生物劑量評估肺癌放療計劃通量平滑值的影響。
本研究參考部分文獻[20-21],選取不同的通量平滑值,以劑量學和典放射生物學參數為依據,選出最佳的通量平滑值。早期有學者[20]報道了Eclispe系統通量平滑對前列腺癌和頭頸部腫瘤放療計劃的影響,發現通量平滑值對葉片因子、劑量學參數有影響。Broderick等[22]報道了通量平滑可以降低機器跳數和危及器官的劑量,Matuszak[23]和Giorgia[24]報道了通量平滑值的增加對劑量投照的準確性有影響。如今成熟的商用計劃系統自帶了通量平滑[5,17-18],Elipcse計劃系統的通量平滑值范圍從0~1000,本研究參考其他文獻選取兩個方向通量范圍為0~100。通量平滑值越大,機器跳數越小,機器跳數增加反映了計劃的復雜性變大。賈曉斌等[17]報道了不同通量平滑值下頭頸部腫瘤放療劑量學影響,結論是通量平滑太大,靶區覆蓋率會受影響并且危及器官劑量提高,這與本研究結論一致,本研究OAR在Smooth 60 50及以上時,OAR受量增加。潘香等[18]比較了Monaco計劃系統低、中、高3種通量平滑在左側乳腺調強放療中的劑量學,通量平滑度增加會減少機器跳數,這些結論與本研究基本一致。機器跳數MU在Smooth 40 30及以下時,MU較高,給臨床工作帶來負擔。
早期,有許多計算放射生物學參數的數學模型和工具[12,25],Gay等[12]提供了Matlab程序用于計算TCP和NTCP,本研究采用其推薦的程序基于EUD模型計算肺癌的TCP和NTCP 。TCP及NTCP與通量平滑值的變化趨勢基本穩定,因此,通量平滑值變化對放射生物學參數影響不大。此外,由圖1看出Smooth 100 100時OAR受量較高,靶區均勻性較差,臨床實用性較差,因此本研究沒有考慮Smooth 100 100以上的通量平滑值。
基于臨床需求和硬件條件,考慮劑量學和放射生物學參數及機器跳數,在肺癌固定野調強放療計劃中建議選取通量平滑值為Smooth 60 50。

