壓強平衡常數的考查特點及典例解析
尉言勛
(安徽省碭山第四中學 235300)
1 壓強化學平衡常數表達式的考查
例1(2021年·全國甲卷·28節選)二氧化碳催化加氫制甲醇,有利于減少溫室氣體二氧化碳.二氧化碳加氫制甲醇的總反應可表示為:

合成總反應在起始物n(H2)/n(CO2)=3時,在不同條件下達到平衡,設體系中甲醇的物質的量分數為x(CH3OH),在t=250℃下的x(CH3OH)~p、在p=5×105Pa下的x(CH3OH)~t圖像如圖1所示.
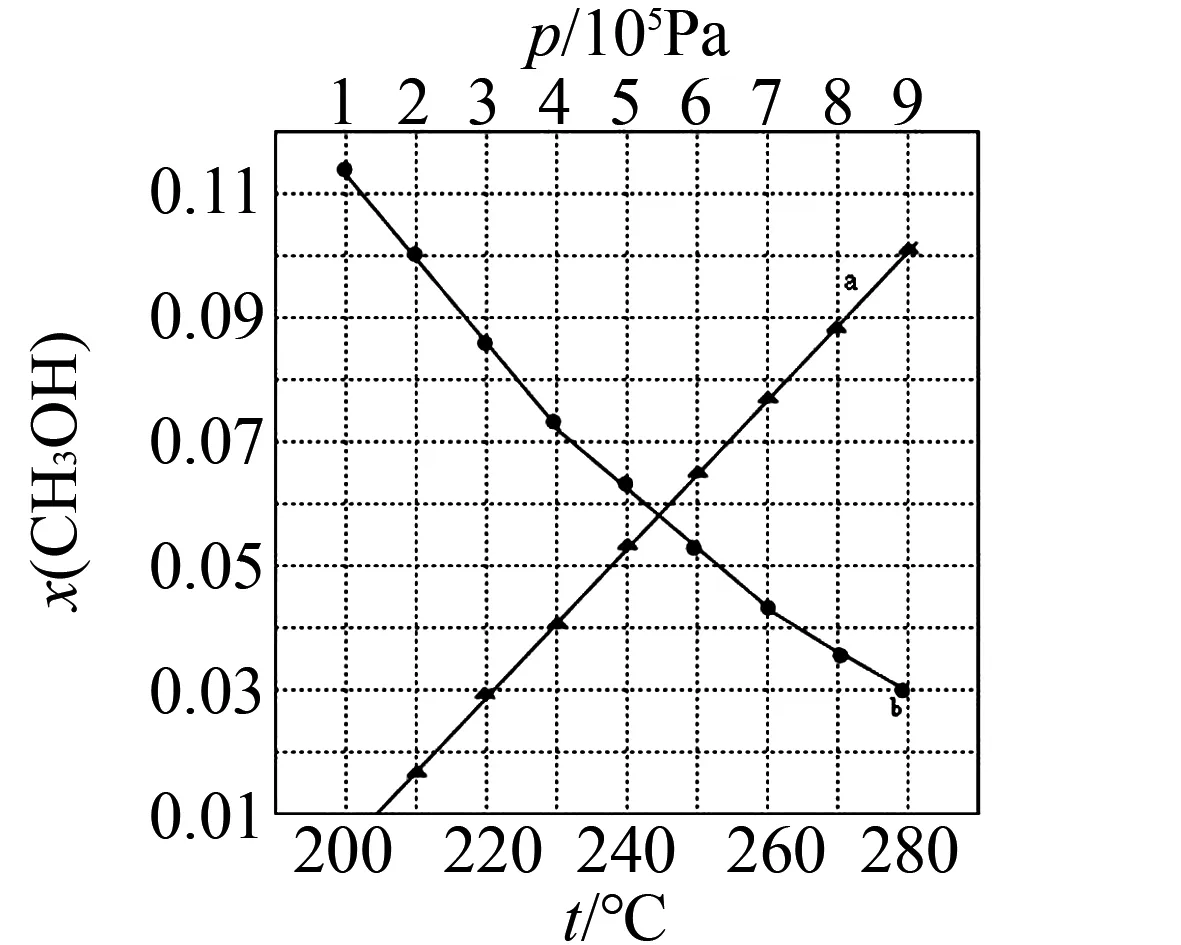
圖1
用各物質的平衡分壓表示總反應的平衡常數,表達式Kp=____;
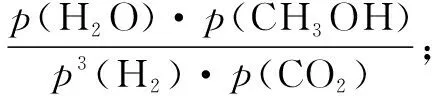
解析由題意可得二氧化碳加氫制甲醇的總反應為:

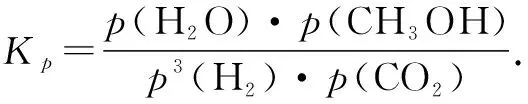
點評本題注重情境的選擇,H2與CO2反應制備燃料甲醇,有利于減少溫室氣體;用平衡分壓(分壓=總壓×物質的量分數)代替平衡濃度,壓強平衡常數表達式與濃度平衡常數表達式相同.Kp的計算只需要列出表達式,在計算能力要求上難度降低.
2 考查壓強平衡常數的計算式,以及通過lgKp推測反應焓變的大小
例2(2021·全國乙卷·28節選)一氯化碘(ICl)是一種鹵素互化物,具有強氧化性,可與金屬直接反應,也可用作有機合成中的碘化劑.回答下列問題:

(2)McMorris測定和計算了在136~180℃范圍內下列反應的平衡常數Kp.
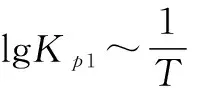
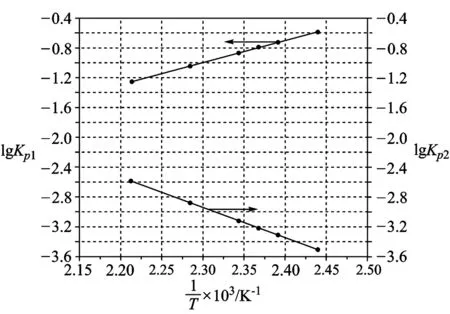
圖2
①由圖可知,NOCl分解為NO和Cl2反應的ΔH____0(填“大于”或“小于”)
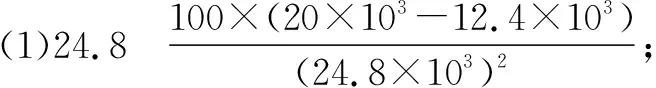

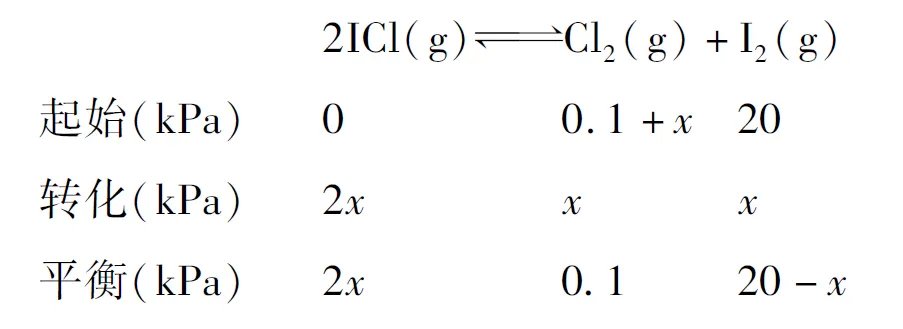
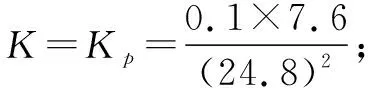
(2)①由圖可知,lgKp2隨著溫度的升高而增大,說明升高溫度,平衡正向移動,則NOCl分解為NO和Cl2反應為吸熱反應,ΔH大于0;
點評本題巧妙地將兩個反應平衡常數的對數與溫度的倒數繪制成線性關系圖,側重考查學生的信息加工能力、邏輯推理能力和歸納論證能力,注意題目中箭頭的方向,上面的斜線代表對于左側的縱坐標,下面的斜線對應右側的縱坐標.對于第(3)題第2問,解題的關鍵是從圖上信息獲知平衡常數與溫度內在關系,并在此基礎上通過提供兩個反應的平衡常數與溫度的關系,推導出一氯化碘分解反應是吸熱還是放熱.
3 拓展呈現形式,考查標準平衡常數
例3(2021·湖南高考·16題節選)氨中氫含量高,是一種優良的小分子儲氫載體,且安全、易儲運,可通過下面兩種方法由氨得到氫氣.

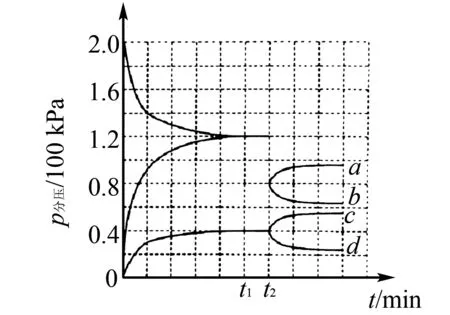
圖3
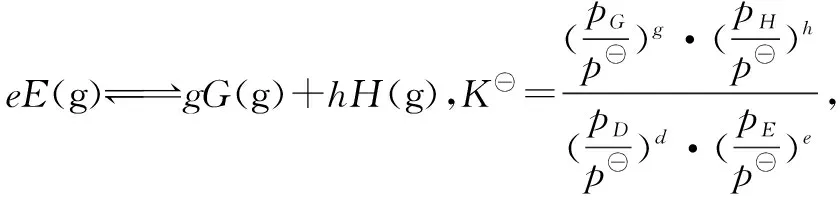
答案:0.48
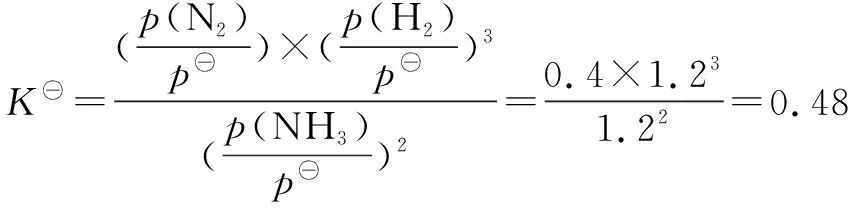
點評在壓強平衡常數呈現形式上繼續拓展,考查標準平衡常數K?的計算.題目以信息呈現的形式給予了K?的表達形式,學生通過圖像可得三種氣體的平衡分壓.代入表達式即可得標準平衡常數.
4 結合圖形,根據相對壓力平衡常數考查平衡轉化率
例4(2021廣東卷·19節選)我國力爭于2030年前做到碳達峰,2060年前實現碳中和.CH4與CO2重整是CO2利用的研究熱點之一.該重整反應體系主要涉及以下反應:


ΔH2


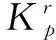
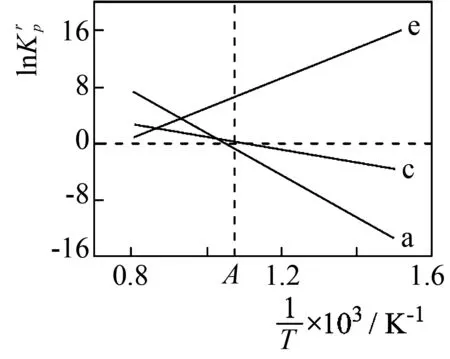
圖4

②在圖中A點對應溫度下、原料組成為n(CO2)∶n(CH4)=1∶1、初始總壓為100 kPa的恒容密閉容器中進行反應,體系達到平衡時H2的分壓為40kPa.計算CH4的平衡轉化率,寫出計算過程____.
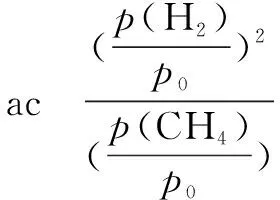
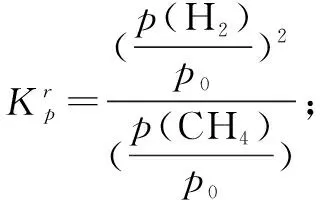
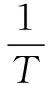
5 給予表格信息,以連續反應形式考查Kp的計算
例5(2018新課標Ⅰ卷·28節選)采用N2O5為硝化劑是一種新型的綠色硝化技術,在含能材料、醫藥等工業中得到廣泛應用,回答下列問題:
F. Daniels等曾利用測壓法在剛性反應器中研究了25℃時N2O5(g)分解反應:
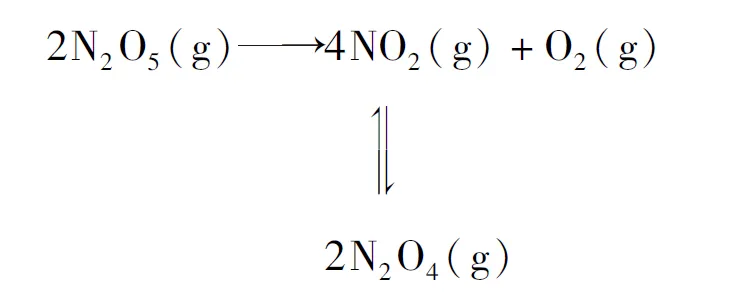
其中NO2二聚為N2O4的反應可以迅速達到平衡,體系的總壓強p隨時間t的變化見表1(t=∞時,N2O4(g)完全分解).
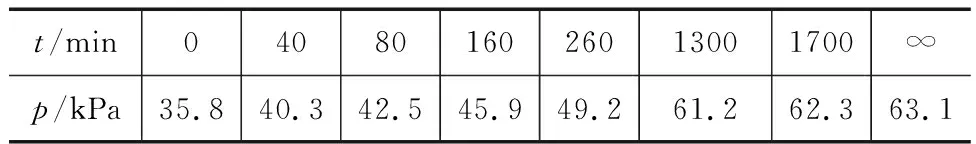
表1


設生成的p(N2O4)=xkPa,可得

開始(kPa) 71.6 0
變化量(kPa) 2xx
平衡量(kPa) 71.6-2xx

答案:13.4.
點評本題以表格形式呈現信息,考查連續反應的壓強平衡常數,培養學生的變化觀念與平衡思想,引導學生多角度的認識化學反應.題目對學生的能力要求較高,在提取有效信息的基礎上,利用“三段式”的解題模型有效解題.

