高性能高鎳三元正極材料的合成條件
李 翔 ,戴林杉 ,彭金星 ,隋邦傑*
(1.武漢理工大學汽車工程學院,湖北 武漢 430070;2.清華四川能源互聯網研究院電化學能源材料與器件研究所,四川 成都 610213)
高鎳三元正極材料LiNi0.8Co0.1Mn0.1O2因具有能量密度高和成本低的特點,成為近年來的研究重點[1]。鎳含量的提高會帶來陽離子混排、表面殘堿與電解液發生副反應等問題[2],但可通過優化燒結工藝,在一定程度上進行緩解。
以往的研究聚焦于如燒結溫度、升溫速率等[1]單一因素對三元材料性能的影響,并不全面。本文作者采用高溫固相法合成LiNi0.8Co0.1Mn0.1O2正極材料,系統研究燒結溫度、燒結時間和過鋰量對高鎳三元材料合成的影響,以期為進一步優化高鎳三元正極材料的合成工藝提供參考。
1 實驗
1.1 三元正極材料LiNi0.8Co0.1Mn0.1O2 的制備
將NiSO4·6H2O(四川產,AR)、CoSO4·7H2O(四川產,AR)和MnSO4·H2O(四川產,AR)按物質的量比8 ∶1 ∶1混合,配制成濃度為2.2 mol/L 的Ni0.8Co0.1Mn0.1SO4溶液,緩慢滴加到55 ℃的恒溫反應釜中,同時,用蠕動泵通入10 mol/L 氨水(四川產,AR)作為絡合劑,通入10 mol/L NaOH(四川產,AR)溶液作為沉淀劑,在pH 值為11、轉速為800 r/min 的條件下反應24 h,在第二反應釜中陳化4 h 后過濾,并用蒸餾水清洗,至濾液中無法檢出SO2-4,得到Ni0.8Co0.1Mn0.1(OH)2三元前驅體。將三元前驅體在空氣氣氛中、105 ℃下干燥24 h,再與LiOH·H2O(四川產,AR)混合,在氧氣氣氛中燒結。升溫速率為5 ℃/min,降溫速率為10 ℃/min,在480 ℃下預燒5 h,氧氣流量為0.1 L/min。
研究設計17 組實驗,各組實驗條件及變量如表1 所示。
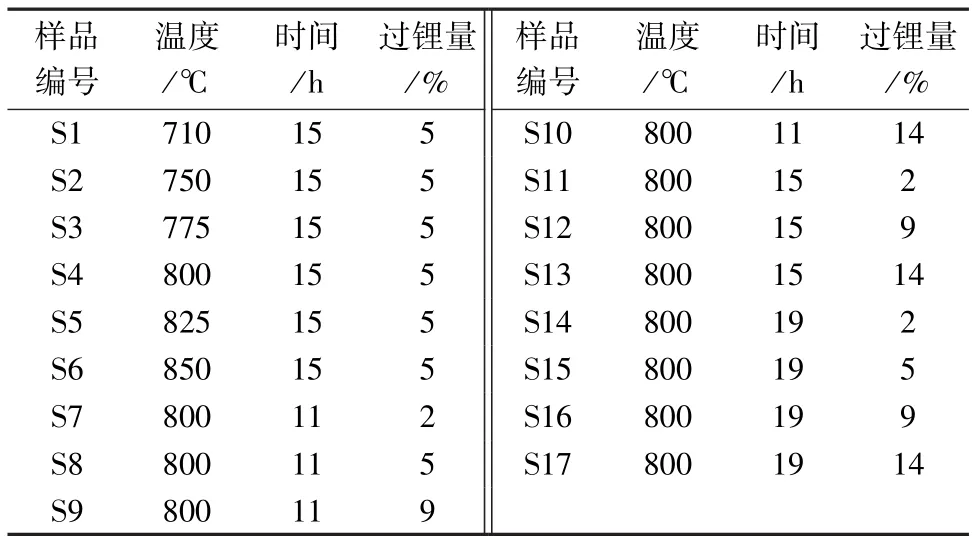
表1 LiNi0.8Co0.1Mn0.1O2 的合成條件Table 1 Synthesis conditions of LiNi0.8Co0.1Mn0.1O2
1.2 材料的分析
用STA449F3 型綜合熱分析儀(德國產)分析樣品的熱特性,升溫速率為5 ℃/min,溫度為30~1 000 ℃;用Mini Flex600 型X 射線衍射儀(日本產)分析樣品的物相結構,CuKα,λ=0.154 059 nm,管壓40 kV、管流15 mA,掃描速度為0.06(°)/s,步長為0.01°;用BT-9300ST 型激光粒度分析儀(遼寧產)分析正極材料的粒度分布;用JSM-IT 500 型掃描電子顯微鏡(日本產)觀察正極材料的微觀形貌。
1.3 電化學性能測試
將正極材料、乙炔黑(瑞士產,電池級)和聚偏氟乙烯(安徽產,電池級)按8 ∶1 ∶1的質量比混合,以N-甲基吡咯烷酮(四川產,AR)為溶劑制漿,涂覆在18 μm 厚的鋁箔(四川產,AR)上,在125 ℃下干燥12 h,輥壓后,裁切成19 mm×44 mm 的正極片,活性物質面密度為0.004 2 g/cm2。
以Celgard 2400 膜(日本產)為隔膜,1 mol/L LiPF6/EC+DEC+PC(體積比1 ∶1 ∶1,安徽產)為電解液,在氬氣保護的手套箱中組裝軟包裝單體電池,尺寸為30.0 mm×55.0 mm×0.9 mm,額定容量為6.6 mAh。用CT-4008 型電池充放電測試系統(深圳產)進行首次充放電、循環及倍率性能等測試。
首次充放電性能測試:以0.1C恒流充電至3.65 V,進行化成,擱置1 min 后,以0.2C恒流充電至4.30 V,轉恒壓充電30 min,擱置10 min 后,以0.2C放電至2.50 V。
循環性能測試:化成后,以1.0C恒流充電至4.30 V,轉恒壓充電10 min,擱置10 min 后,以1.0C放電至2.75 V,擱置10 min 后,開始下一次循環,共循環100 次。
倍率性能測試:化成后,依次以0.2C、0.5C、1.0C、2.0C、4.0C和0.2C的電流恒流充電至4.30 V,轉恒壓充電10 min,擱置10 min 后,以相同的電流放電至2.75 V,擱置10 min 后,開始下一次循環,每種電流循環5 次。
2 結果與討論
2.1 TG/DTG 及DSC 測試結果分析
對Ni0.8Co0.1Mn0.1(OH)2與LiOH·H2O 的混合粉體進行綜合熱分析實驗。熱重(TG)/微分熱重(DTG)及差示掃描量熱(DSC)測試結果見圖1。
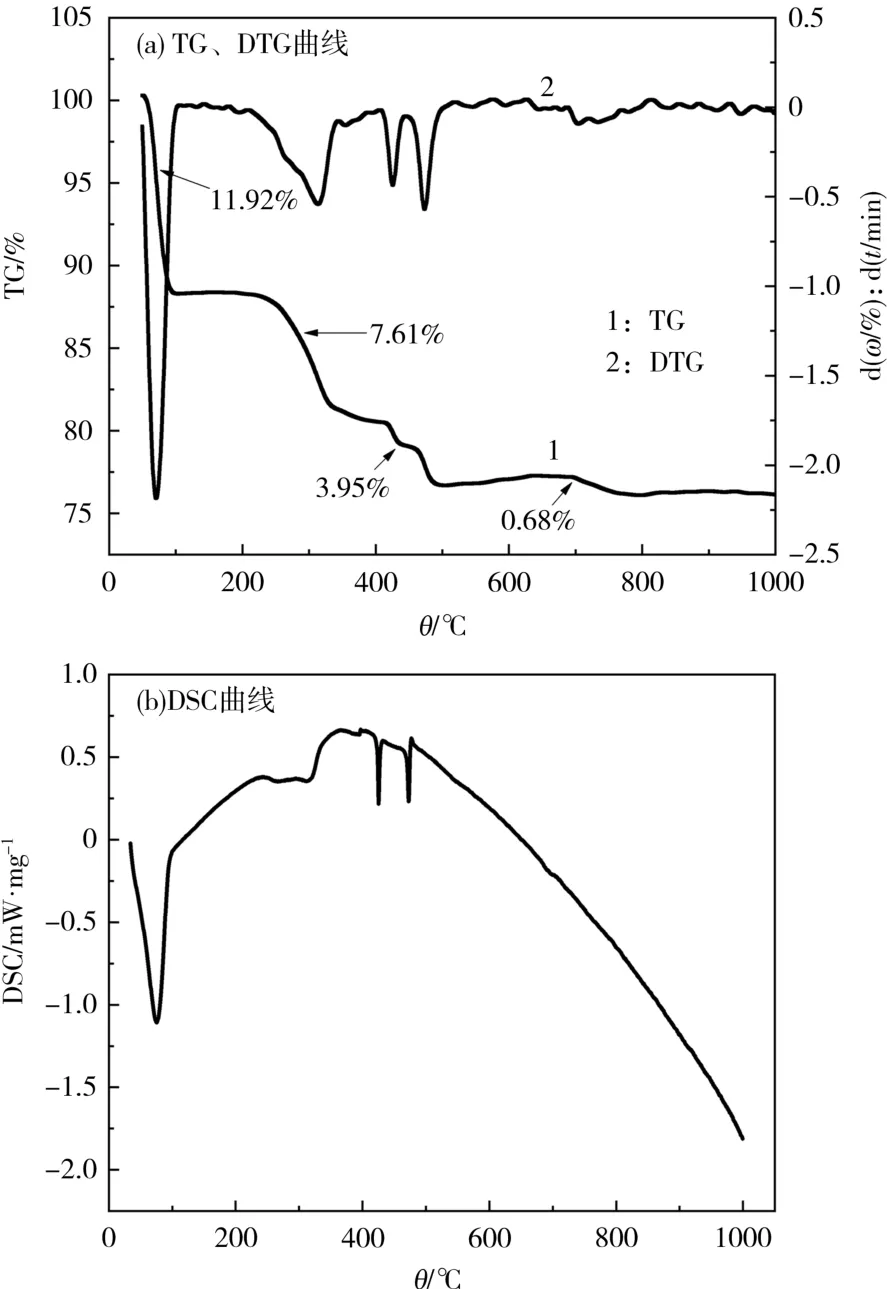
圖1 Ni0.8Co0.1Mn0.1(OH)2 與LiOH·H2O 混合粉體的TG/DTG 及DSC 曲線Fig.1 Thermogravimetry(TG)/differential thermal gravity(DTG)and differential scanning calorimetry(DSC) curves of Ni0.8Co0.1Mn0.1(OH)2 and LiOH·H2O mixed powder
從圖1 可知,反應第一階段為35~100 ℃,混合粉體失重率為11.92%,吸熱峰溫度為75.3 ℃,對應的反應是LiOH·H2O 失去結晶水。反應第二階段發生在220~330 ℃,混合物失重7.61%,對應DSC 曲線上較寬的一段吸熱峰,對應Ni0.8Co0.1Mn0.1(OH)2前驅體脫水生成Ni0.8Co0.1Mn0.1O 及H2O。反應第三階段為420~480 ℃,混合物失重為3.95%,425 ℃及472 ℃處兩個明顯的吸熱峰,均對應LiOH 水解生成Li2O。反應第四階段為500~750 ℃,失重0.68%,此階段Ni0.8Co0.1Mn0.1O 和Li2O 在氧氣氛圍中固溶生成LiNi0.8Co0.1Mn0.1O2。DSC 曲線在700 ℃附近有一個微小的吸熱峰,意味著LiNi0.8Co0.1Mn0.1O2三元正極材料的合成基本完成[3]。在700 ℃以后,隨著溫度的上升,混合物的質量緩慢下降,原因是高溫下晶體分解及Li+的蒸發。根據以上測試結果可知,隨著溫度的升高,反應分多階段緩慢進行,為了給脫水及相變反應預留充分的時間,應采用兩步燒結法進行實驗。將預燒溫度設置為500 ℃,并保溫5 h。
2.2 燒結溫度對LiNi0.8Co0.1Mn0.1O2 的影響
圖2 是樣品S1~S6 的XRD 圖。
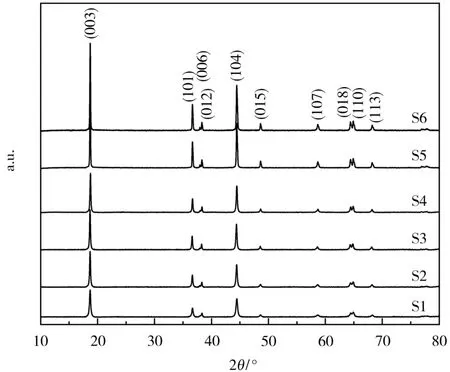
圖2 不同燒結溫度下合成的LiNi0.8Co0.1Mn0.1O2 的XRD 圖Fig.2 XRD patterns of LiNi0.8Co0.1Mn0.1O2 synthesized at different sintering temperatures
從圖2 可知,6 個溫度下所合成樣品均為純相,各衍射峰特征符合α-NaFeO2層狀結構,且都屬于六方晶系,空間群為R3m。隨著燒結溫度的提高,(006)/(012) 峰和(018)/(110)峰的分裂愈加明顯,反映了層狀結構愈加有序。
瑞豐生態(集團)營銷中心總監胡學敏表示,瑞豐生態將會以土壤修護研究院為核心,打造中國規模最大的基層土壤修護服務體系,通過項目建設、技術指導和現場服務的方式,憑借以產品為核心的服務體系解決土壤和種植問題,幫助傳統經銷企業轉型成為經銷服務商,實現企業、經銷商和農民等多方的融合共贏。
各樣品的晶胞參數、(003)峰強度I(003)與(104)峰強度I(104)之比及代表材料六方結構有序程度的R值[計算公式見式(1)]列于表2。

式(1)中:I(012)、I(006)和I(101)分別為(012)、(006)和(101)峰的強度。
表2 中的c/a反映了晶體層狀結構發育的完善程度。各樣品的c/a均大于4.95,說明層狀結構較好。高鎳正極材料合成時易發生鋰鎳混排現象,造成容量損失。I(003)/I(104)常用于衡量鎳鋰混排的嚴重程度,當比值大于1.20 時,可認為鎳鋰混排程度較低。隨著燒結溫度的提高,I(003)/I(104)呈先增大、后減小的趨勢,在800 ℃時達到最大值,且均超過1.20。燒結溫度繼續提高,會造成更嚴重的鎳鋰混排,原因是高溫下氧的溢出導致更多的Ni3+轉變成Ni2+。R越小,材料的六方有序結構越好。在燒結溫度800 ℃時,R達到最小值。晶粒尺寸通過Scherrer 公式計算[4]。隨著燒結溫度的提高,晶粒尺寸不斷增大,在800 ℃后增速明顯加快。一次顆粒的增大,導致Li+遷移路徑變長,電池內阻及極化增大。
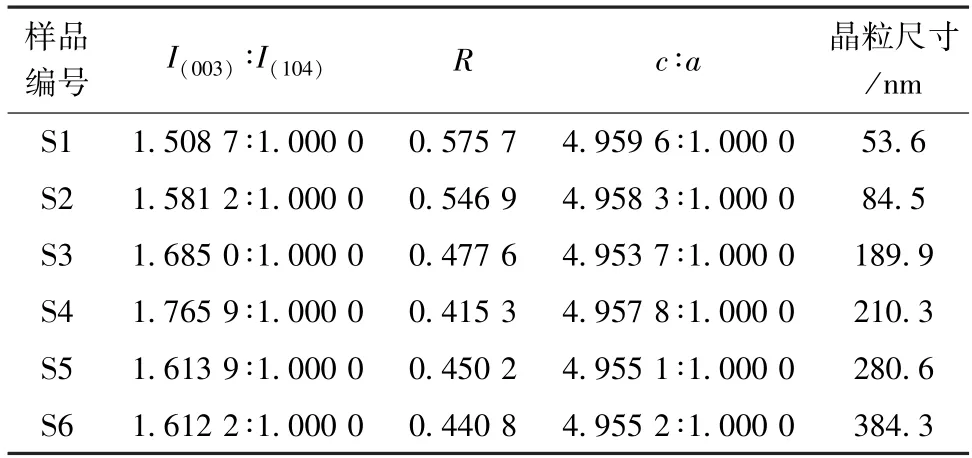
表2 不同燒結溫度下合成的LiNi0.8Co0.1Mn0.1O2 的晶胞參數Table 2 Cell parameters of LiNi0.8Co0.1Mn0.1O2 synthesized at different sintering temperatures
不同燒結溫度下合成的LiNi0.8Co0.1Mn0.1O2的粒徑分布見圖3。
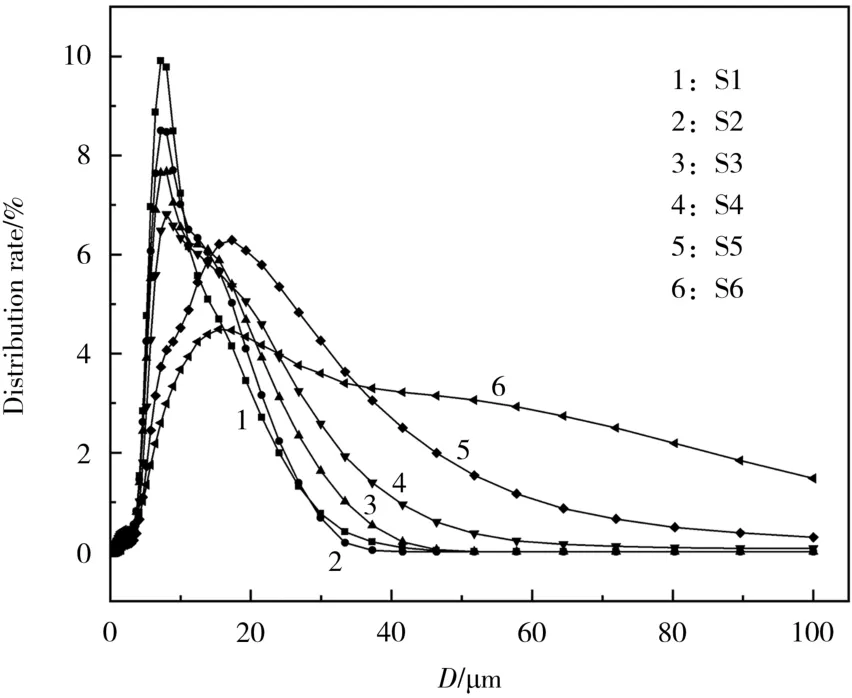
圖3 不同燒結溫度下合成的LiNi0.8Co0.1Mn0.1O2 的粒徑分布Fig.3 Particle size distribution of LiNi0.8Co0.1Mn0.1O2 synthesized at different sintering temperatures
從圖3 可知,隨著燒結溫度的提高,三元材料的粒徑逐漸增大,分布范圍逐漸變寬。當溫度超過800 ℃后,粒徑增大情況加劇,異常大尺寸的顆粒數量急劇上升。
圖4 是不同燒結溫度下合成的LiNi0.8Co0.1Mn0.1O2單顆粒及聚集情況的SEM 圖。
從圖4 可知,隨著燒結溫度的提高,三元材料表面一次顆粒尺寸不斷增加,且團聚情況不斷惡化。圖4(g)顯示,燒結溫度達到850 ℃時,出現熔融現象,導致粒度測試中粒徑分布不服從正態分布。三元材料粒徑和一次顆粒尺寸的增大及顆粒之間的黏連熔融現象,導致Li+的傳輸路徑變長,電池極化增大,使倍率性能降低。電池材料在嵌脫鋰過程中,電極顆粒內部電勢分布不均勻,會產生不均勻的應力,而完整的球形有利于三元材料克服這種應力帶來的損害[5]。

圖4 不同燒結溫度下合成的LiNi0.8Co0.1Mn0.1O2 單顆粒及聚集情況的SEM 圖Fig.4 SEM photographs of single particle and aggregation of LiNi0.8Co0.1Mn0.1O2 synthesized at different sintering temperatures
綜上所述,S4 樣品具有最低的陽離子混排程度、最好的晶體結構、較好的粒度分布及微觀形貌。
各樣品的首次充放電曲線見圖5。
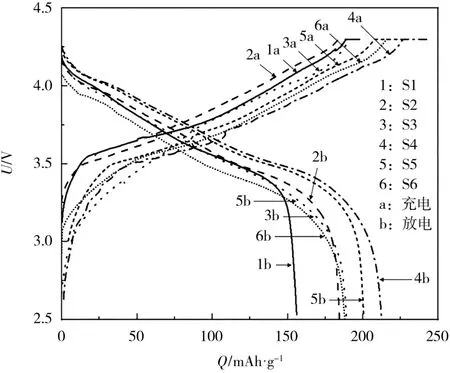
圖5 不同燒結溫度下合成的LiNi0.8Co0.1Mn0.1O2 的首次充放電曲線Fig.5 Initial charge-discharge curves of LiNi0.8Co0.1Mn0.1O2 synthesized at different sintering temperatures
從圖5 可知,隨著燒結溫度的升高,材料的放電比容量先增大、后減小,其中S4 樣品的首次放電比容量最大,達到了212.2 mAh/g。過高的燒結溫度會導致放電起始電壓下降,原因是30 min 的恒壓充電不足以消除由一次顆粒生長、二次顆粒的熔融所帶來的極化。
各樣品的循環性能及倍率性能見圖6。
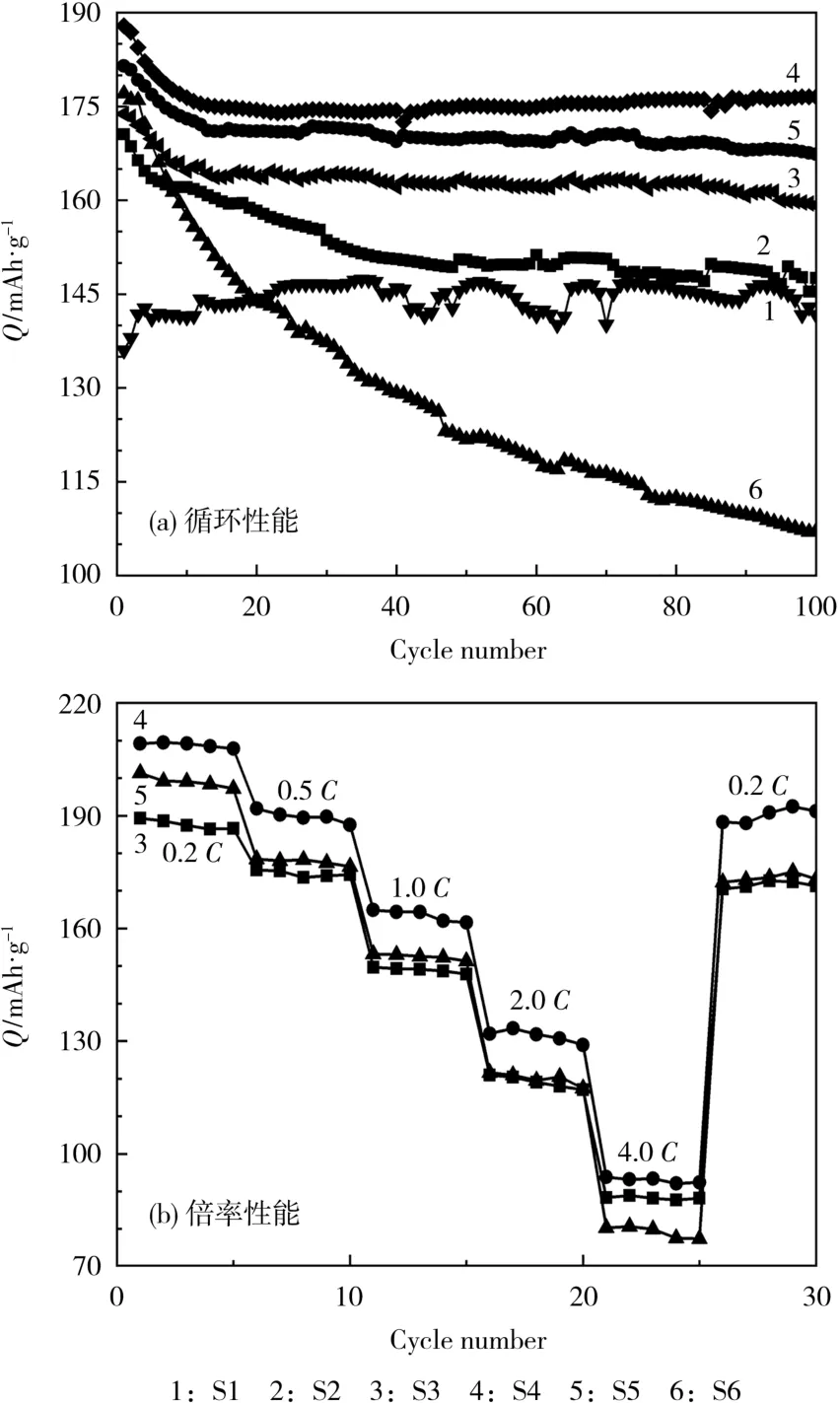
圖6 不同燒結溫度下合成的LiNi0.8Co0.1Mn0.1O2 的循環性能及倍率性能Fig.6 Cycle performance and rate capability of LiNi0.8Co0.1 Mn0.1O2 synthesized at different sintering temperatures
從圖6 可知,S4 樣品的放電比容量由187.9 mAh/g 下降到176.6 mAh/g,容量保持率為94.0%,不僅具有最高的比容量,還具有最高的容量保持率,大部分衰減發生在前20 次循環中。S6 樣品不僅初始容量較低,循環穩定性也很差,容量保持率僅為60.5%,可能是循環過程中不規則球體不斷破碎所致。可以看出,各樣品在高倍率下的容量衰減趨勢一致,燒結溫度越低,在高倍率下的容量衰減程度就越低,但是在不同倍率下,比容量最高的均是S4 樣品。由此可知,800 ℃是LiNi0.8Co0.1Mn0.1O2正極材料的最佳燒結溫度。
2.3 燒結時間及過鋰量對LiNi0.8Co0.1Mn0.1O2 的影響
燒結時間的延長會導致Li+的蒸發,燒結時間及過鋰量呈強相關性,為了得到最優燒結工藝,進行了表1 中的實驗。不同燒結工藝所制備LiNi0.8Co0.1Mn0.1O2正極材料的晶胞參數及首次充放電數據列于表3。
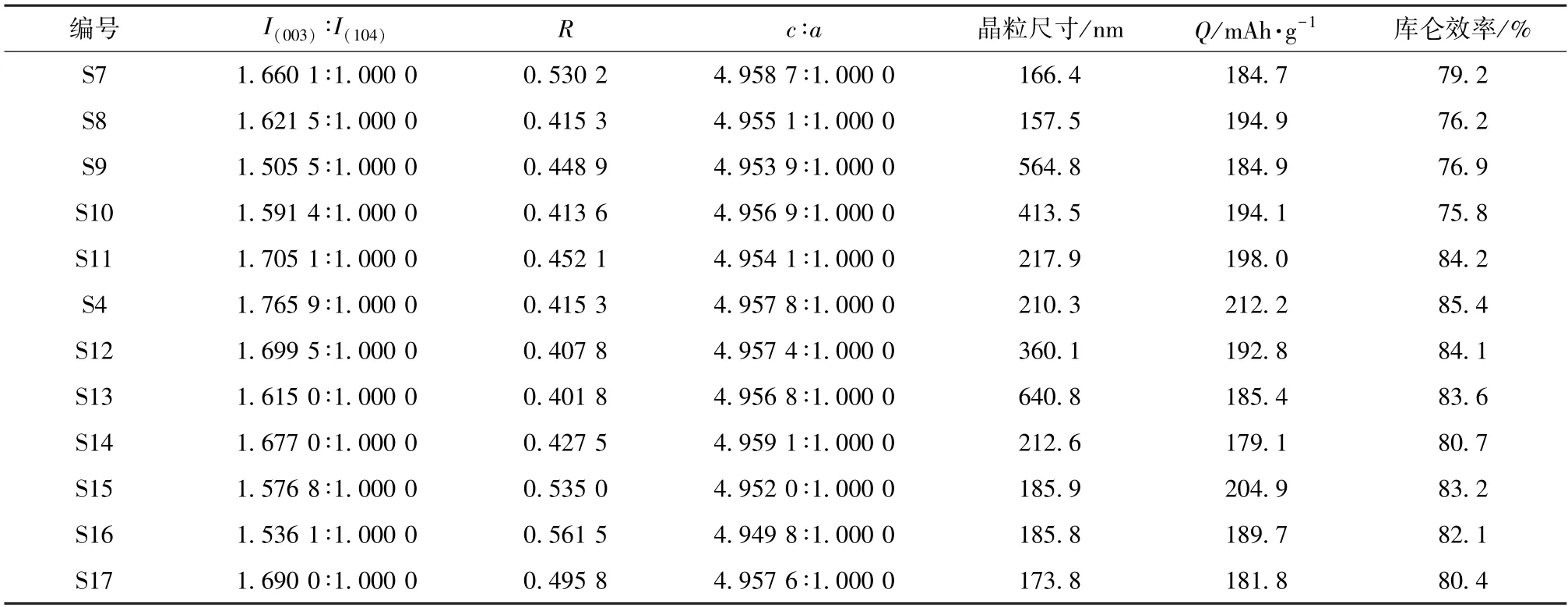
表3 不同燒結時間及過鋰量的LiNi0.8Co0.1Mn0.1O2 的晶胞參數和首次充放電數據Table 3 Cell parameters and initial charge-discharge data of LiNi0.8Co0.1Mn0.1O2 synthesized with different sintering time and excess lithium amout
從表3 可知,在過鋰量相同的情況下,隨燒結時間的延長,鎳鋰混排程度基本上呈先減小、后增大的趨勢,原因是:燒結11 h,時間過短,不足以使材料形成穩定的晶體結構;而燒結19 h,時間過長,造成過多的Li+蒸發,使Ni3+還原成Ni2+,加劇鎳鋰混排。隨著燒結時間的延長,R值基本上呈先減小、后增大的趨勢。一次顆粒的大小主要受過鋰量的主導,當過鋰量不高于5%時,一次顆粒較小,極化現象相對輕微。各樣品的c/a均大于4.95,形成了良好的層狀結構。
從表3 可知,首次充放電性能最好的是S4 樣品,放電比容量和首次庫侖效率最高。燒結時間為11 h 的S7~S10 樣品,首次放電比容量和庫侖效率均較低,原因是燒結時間過短,不足以讓材料的晶體結構充分發育,造成可逆容量的降低。燒結時間為19 h 的S14~S17 樣品,比容量和庫侖效率略差于15 h 時的樣品,主要是由Li+蒸發帶來的鎳鋰混排惡化現象引起的。在燒結時間相同的情況下,過低的過鋰量不足以補償高溫燒結帶來的Li+蒸發損失;過高的過鋰量則會導致一次顆粒尺寸的增加,造成更為嚴重的極化,導致表面殘堿增加,加劇電解液與正極材料的反應,造成電池材料阻抗增加,首次充放電庫侖效率降低。
3 結論
本文作者系統研究了燒結溫度、燒結時間及過鋰量對高鎳正極材料LiNi0.8Co0.1Mn0.1O2的晶體結構、形貌及電化學性能的影響。結果表明:在燒結溫度為800 ℃、燒結時間為15 h,過鋰量為5%的條件下合成的LiNi0.8Co0.1Mn0.1O2正極材料,具有最好的電化學性能,以0.2C的電流在2.50~4.30 V充放電,首次放電比容量為212.2 mAh/g;第100 次循環的比容量從首次循環的187.9 mAh/g 下降至176.6 mAh/g,容量保持率為94.0%。

