抗PD-1免疫治療聯(lián)合放療在鼻咽癌患者中的應(yīng)用效果及對腫瘤標志物的影響
藍清華 曾慶芳 詹濤 鐘建明
鼻咽癌(NPC)主要來自鼻咽部上皮細胞,多位于頭頸部,是常見的惡性腫瘤之一。放療是鼻咽癌的主要治療方法,能改善鼻咽癌局部控制和患者的總生存期(OS)[1-2]。T 細胞免疫療法和免疫檢查點抑制為臨床治療腫瘤提供新的思路,免疫治療已經(jīng)成為治療腫瘤的新興方式[3]。程序性死亡受體1(PD-1)/程序性死亡受體配體1(PD-L1)單抗是免疫檢查點抑制劑中的關(guān)鍵,具有顯著的抗腫瘤作用,且在臨床中已經(jīng)得到廣泛的使用[4-6]。Zeng 等[7]發(fā)現(xiàn)PD-1 免疫檢查點抑制劑治療腫瘤方面取得新的突破。本研究探討抗PD-1 免疫治療聯(lián)合放療在鼻咽癌患者的臨床療效及對腫瘤標志物的影響,現(xiàn)報道如下。
1 資料與方法
1.1 一般資料 選取2018 年1 月-2022 年1 月贛州市腫瘤醫(yī)院內(nèi)科三區(qū)收治的鼻咽癌患者113 例患者為研究對象,納入標準:(1)經(jīng)過CT、MRI、血清中EB 病毒相關(guān)抗體檢測,參照文獻[8]《中醫(yī)耳鼻喉科學(xué)》確診;(2)愿意接受放療;(3)思維清晰。排除標準:(1)精神障礙或者依從性較差;(2)近1 個月內(nèi)接受化療或者其他治療方法;(3)嚴重肝腎功能障礙;(4)慢性病處于發(fā)作期;(5)拒絕接受抗PD-1 治療或者終末期。依據(jù)治療方式的不同分為觀察組(n=57)和對照組(n=56),本研究經(jīng)過醫(yī)院倫理委員會批準。患者簽署知情同意書。
1.2 方法 所有患者均給予單抗PD-1 治療,方法:靜滴特瑞普利單抗注射液[生產(chǎn)廠家:蘇州眾合生物醫(yī)藥科技有限公司,批準文號:國藥準字S20180015,規(guī) 格:240 mg(6 mL)/ 瓶] 用 法:240 mg/次,21 d 為一療程。對照組單用PD-1 抑制劑,連續(xù)用藥一直到腫瘤進展或者患者出現(xiàn)不可耐受的現(xiàn)象。觀察組在此基礎(chǔ)上均給予放療。患者取仰臥位,熱塑面罩固定頭頸部位,然后進行CT 檢查。然后將掃描的資料上傳到三維治療系統(tǒng),由專業(yè)醫(yī)師畫出靶區(qū),鼻咽腫瘤體積(GTVnx)為70.06 Gy、頸部淋巴體積(GTVnd)為65.28 Gy,原發(fā)腫瘤2~2.3 Gy,分割次數(shù)為33 次,5 次/周,依據(jù)患者治療協(xié)作組(RTOG)0615 和RTOG0225 的情況評估危及器官限制劑量和計劃。
1.3 觀察指標及評價標準 1 個月后進行指標評價。(1)客觀緩解率:經(jīng)過CT 影像學(xué)檢測,采用面積軟件確定腫瘤的大小,取其平均值。依據(jù)患者腫瘤大小確定臨床療效。完全緩解(CR):1 個月后經(jīng)過影像CT 檢查,所有腫瘤目標已經(jīng)消失。部分緩解(PR):1 個月后經(jīng)過影像CT 檢查,所有目標腫瘤消失50%以上。穩(wěn)定(SD):1 個月后經(jīng)過影像CT 檢查腫瘤無任何變化;進展(PD):1 個月后經(jīng)過影像CT 檢查腫瘤增加25%以上,且出現(xiàn)新的腫瘤。客觀緩解率(ORR)=(CR+PR)例數(shù)/總例數(shù)×100%。(2)腫瘤標志物:分別采用治療前后清晨空腹血4 mL,以3 500r/min 離心5 min,置于4~5 ℃冰箱保存,采用免疫化學(xué)夾心法檢測鱗狀細胞癌相關(guān)抗原(SCC),以SCC 大于等于2.5 ng/mL 為陽性標準。CEA 測定結(jié)果以0~10 ng/mL 為標準,采用CEA 定量檢測試劑盒進行檢測,試劑盒由新產(chǎn)業(yè)生物醫(yī)學(xué)工程有限股份公司提供,具體操作參照說明書。(3)外周血T 細胞表面PD-1、CD8+、自然殺傷(NK 細胞)表達水平:分別于治療前后清晨空腹肘部靜脈采血4 mL,采用流式細胞儀檢測患者CD8+、NK 細胞、PD-1。(4)生活質(zhì)量:分別于治療前后采用鼻腔鼻竇結(jié)局測試-20(SNOT-20)量表中文版和癌癥患者生命質(zhì)量測定量表(QLQ-C30)對患者的生活質(zhì)量進行評估。SNOT-20 中文版:包括鼻腔部癥狀、鼻竇炎癥狀、睡眠障礙和情感障礙4 個領(lǐng)域,包含有20 個項目。每個項目0~3 分,分數(shù)越低,則表示患者的生活質(zhì)量越好[9]。QLQ-C30量表:包含軀體、心理、社會功能、認知方面及角色5 個方面,分數(shù)為0~100 分,分數(shù)越高則表示生活質(zhì)量越好[10]。
1.4 統(tǒng)計學(xué)處理 采用SPSS 27.0 軟件進行統(tǒng)計學(xué)分析,定性資料采用率(%)表示,計量資料以()表示,以χ2進行非連續(xù)性變量檢驗,以t檢驗進行連續(xù)性數(shù)據(jù)組間比較,P<0.05 表示差異有統(tǒng)計學(xué)意義。
2 結(jié)果
2.1 兩組一般資料比較 觀察組男29 例,女28 例;年齡31~75 歲,平均(46.58±10.26)歲;臨床分期:Ⅰ期10 例,Ⅱ期12 例,Ⅲ期16 例,Ⅳ期19 例。對照組男28 例,女28 例;年齡30~76 歲,平均(46.63±10.52)歲;臨床分期:Ⅰ期12 例,Ⅱ期15 例,Ⅲ期14 例,Ⅳ期15 例。兩組一般資料比較,差異均無統(tǒng)計學(xué)意義(P>0.05),具有可比性。
2.2 兩組客觀緩解率比較 治療后觀察組ORR 為80.70%,明顯高于對照組的64.29%(χ2=4.345,P=0.037),見表1。

表1 兩組客觀緩解率比較[例(%)]
2.3 兩組腫瘤標志物比較 治療前,兩組SCC、CEA 水平比較,差異均無統(tǒng)計學(xué)意義(P>0.05);治療后兩組SCC、CEA 水平均降低,且觀察組均低于對照組(P<0.05)。見表2。
表2 兩組腫瘤標志物比較[ng/mL,()]
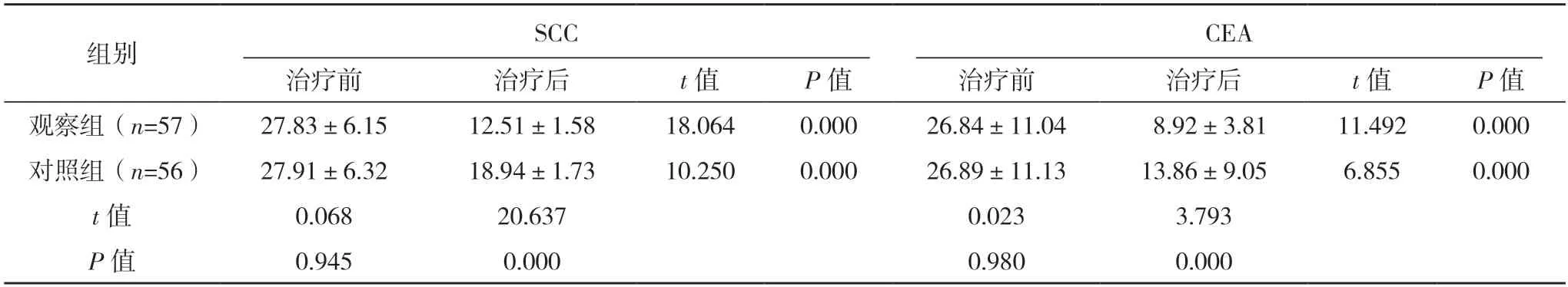
表2 兩組腫瘤標志物比較[ng/mL,()]
2.4 兩組外周血T 細胞表面PD-1、CD8+、NK 細胞表達水平比較 治療前,兩組PD-1、CD8+、NK細胞表達水平比較,差異均無統(tǒng)計學(xué)意義(P>0.05);治療后,兩組PD-1、CD8+表達水平均明顯升高(P<0.05),觀察組PD-1、CD8+均高于對照組(P<0.05),兩組治療后NK 細胞與治療前比較,差異均無統(tǒng)計學(xué)意義(P>0.05);兩組治療后NK 細胞比較,差異無統(tǒng)計學(xué)意義(P>0.05)。見表3。
表3 外周血T細胞表面PD-1、CD8+、NK細胞表達水平比較[%,()]
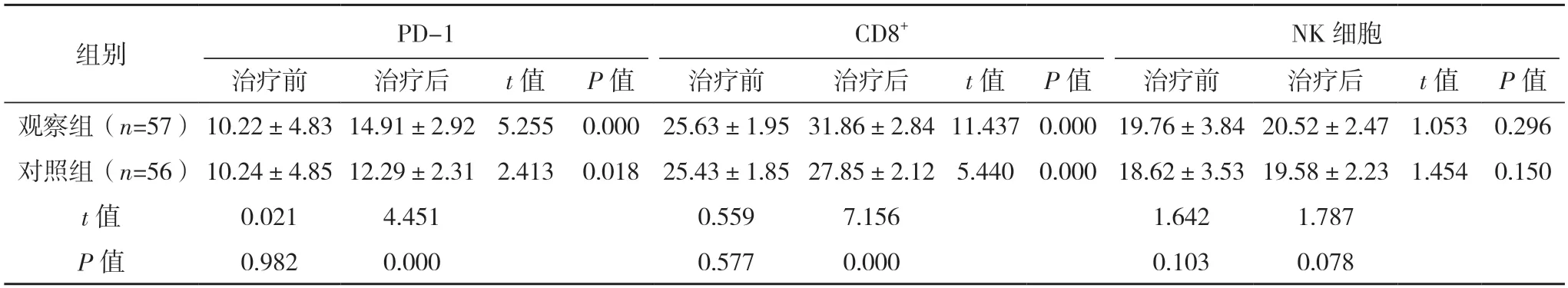
表3 外周血T細胞表面PD-1、CD8+、NK細胞表達水平比較[%,()]
2.5 兩組生活質(zhì)量比較 治療前,兩組SNOT-20、QLQ-C30 評分比較,差異均無統(tǒng)計學(xué)意義(P>0.05);治療后,兩組SNOT-20 評分均降低,觀察組低于對照組(P<0.05),兩組QLQ-C30 評分均升高,且觀察組高于對照組(P<0.05)。見表4。
表4 兩組生活質(zhì)量比較[分,()]
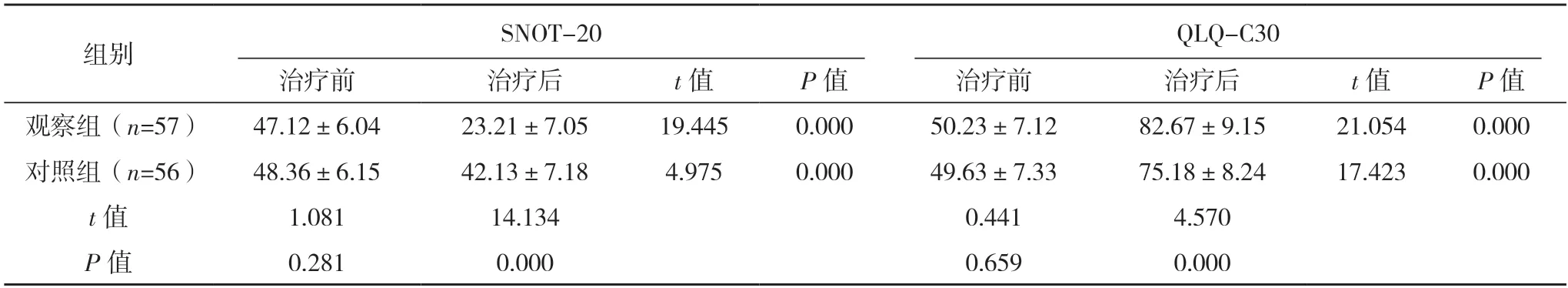
表4 兩組生活質(zhì)量比較[分,()]
3 討論
鼻咽癌是多發(fā)生于頭頸部的惡性腫瘤,經(jīng)過調(diào)查顯示,我國每年鼻咽癌的發(fā)病率占全球的80%~85%[11]。鼻咽癌早期患者無明顯的癥狀,一旦確診則為中晚期,給臨床治療帶來嚴重的困難,且鼻咽癌是一種低分化鱗癌,大部分患者對放療較為敏感,還會損傷正常組織細胞,并且治療后患者還容易出現(xiàn)皮膚潰爛、疼痛、口腔黏膜炎等并發(fā)癥。目前,抗PD-1 免疫治療聯(lián)合放療是臨床治療鼻咽癌的首選方式。腫瘤組織中PD-1 表達、微衛(wèi)星不穩(wěn)定(MSI)及腫瘤組織的突變負荷(TMB)均已經(jīng)成為預(yù)測免疫治療的指標,但是其預(yù)測效果尚未明確。PD-1 主要表達在T/B 淋巴細胞、單核細胞、間充至細胞及NK 細胞。其主要配體是PD-L1,人類重組蛋白(APCs)、造血細胞和上皮細胞均有表達,但是在腫瘤細胞存在過表達的現(xiàn)象[12]。腫瘤細胞殺傷機制是腫瘤細胞和免疫效應(yīng)細胞的相互表達過程中,其腫瘤細胞表面PD-L1 結(jié)合免疫效應(yīng)細胞表面的PD-1,表達出免疫抑制信號[13]。PD-1 抑制劑是隔斷PD-1/PDL1 通路,使腫瘤細胞產(chǎn)生免疫作用,進而對腫瘤細胞起到殺傷作用。若免疫治療產(chǎn)生作用,則抗PD-1 治療可以活化免疫細胞和效應(yīng)T 細胞下游細胞會產(chǎn)生相應(yīng)的變化[14]。
本研究結(jié)果顯示,觀察組患者的客觀緩解率高于對照組,治療后兩組SCC、CEA 水平均降低,且觀察組均低于對照組,表明抗PD-1 免疫治療聯(lián)合放療可改善鼻咽癌患者臨床療效,抑制腫瘤細胞,改善預(yù)后。夏念等[15]研究表明,化療藥物用于腫瘤細胞的亞致死損傷時,對細胞DNA 的修復(fù)起到抑制作用,且同步腫瘤細胞,提高放射治療的敏感性。腫瘤標志物是臨床治療鼻咽癌患者常用的輔助檢查手段[16]。CEA 是人胚胎特異性抗原,腫瘤的療效、進展和轉(zhuǎn)移與CEA 的動態(tài)變化密切相關(guān)。鄧偉明等[17]研究發(fā)現(xiàn),鼻咽癌組織中大量存在CEA,其細胞的凋亡與脫落,均可以檢測到。SCC 指標也是臨床常檢測的腫瘤標物,且與多種腫瘤存在一定的相關(guān)性[18]。PD-1 屬于CD28 類的一種,其中主要表達位于表面CD4+細胞和CD28+細胞。Miyake等[19]發(fā)現(xiàn)PD-1 表達水平越高,則表明PD-1 抑制作用越好。CD8+細胞是一種具有細胞毒T 細胞,其主要效應(yīng)抗腫瘤免疫[20]。NK 細胞具有直接殺傷靶細胞效應(yīng),在抗腫瘤免疫和阻止病毒感染中起著重要的作用[21]。本研究發(fā)現(xiàn),觀察組臨床治療后PD-1、CD8+表達水平與治療前比較均升高,提示抗PD-1 免疫治療聯(lián)合放療能改善鼻咽癌患者的免疫功能[22]。PD-1 抗體阻斷PD-1 的識別過程且恢復(fù)部分T 淋巴細胞的功能和數(shù)量,進而使腫瘤細胞具有免疫耐受能力[23-24]。本研究結(jié)果顯示,治療后兩組SNOT-20 評分、QLQ-C30 評分均明顯改善,觀察組改善程度更加明顯,表明抗體PD-1 免疫治療聯(lián)合放療在鼻咽癌患者中臨床效果更加顯著,改善患者的生活質(zhì)量[25]。
綜上所述,抗PD-1 免疫治療聯(lián)合放療治療鼻咽癌患者臨床效果顯著,降低腫瘤標志物水平,改善機體免疫功能和生活質(zhì)量,在臨床有良好的應(yīng)用價值。

