MnO-C負極材料的制備及其電化學性能研究
李博陽,張三峽,李佳豪
(1.武漢工程大學湖北省等離子體化學與新材料重點實驗室,湖北 武漢 430205;2.武漢工程大學,湖北 武漢 430205)
鋰離子電池由于其高能量密度、長壽命和無記憶效應,在電動汽車和電子智能設備的應用中發揮著至關重要的作用[1]。由于商用石墨陽極的理論容量較低(372 mAh·g-1),鋰離子電池很難滿足日益增長的高能量密度需求[2]。因此,各個方面的研究主要集中在有前途的鋰離子電池陽極材料上,如過渡金屬氧化物[3]、金屬硫化物[4]、硅基[5]和錫基材料[6]。由于理論容量高且易于制備,過渡金屬氧化物尤其具有吸引力。在這些陽極中,MnO 因其較高的理論容量和豐富的資源而成為最有前景的陽極材料之一[7]。然而,由于充放電過程中固有的低導電性和大體積膨脹,MnO 材料通常具有低倍率性能和較差的循環性能,因此其商業應用受到阻礙[8]。
為了克服上述問題,人們做出了各種努力來提高MnO 基陽極材料的電化學性能。其中,利用高導電性的碳材料和MnO 形成納米復合材料是另一種成功的方法,可以有效地提高電化學性能。這是由于MnO 基碳復合材料可以提高電子導電性和MnO表面介導的反應動力學,復合材料中的介孔提供了緩沖的空間,緩解了MnO 在電池循環過程中的體積膨脹和破裂脫落[9]。
本文提出了一種簡便且低成本的策略,以構建獨特的納米復合結構,即通過高錳酸鉀、過氧化氫和葡萄糖的一步熱解策略在碳網絡中負載MnO。在制備過程中,使用高錳酸鉀作為錳源、廉價的葡萄糖作為碳源。碳材料不僅提供彈性碳框架防止MnO顆粒聚集,并適應循環過程中的體積膨脹,而且還提供了促進快速離子轉移的空穴和增強電荷轉移的電子傳輸通道。因此,復合陽極在0.3 A·g-1的電流密度下循環50 圈后保持384.2 mAh·g-1的可逆容量,體現出了良好的循環性能。
1 實驗部分
1.1 實驗材料
高錳酸鉀、葡萄糖、過氧化氫、導電炭黑、氫氧化鉀、電解液以及聚偏氟乙烯,均為市售,分析純;實驗所使用的水均為去離子水。
1.2 MnO-C 復合材料的制備
制備流程示意圖如圖1所示。稱取1.58 g 高猛酸鉀、0.61 g 氫氧化鉀、3 mL 過氧化氫、1 g 葡萄糖加入到水熱中超聲分散30 min,然后攪拌上述混合溶液,2 h 后將混合溶液放入烘箱內烘干得到均勻的混合粉末。最后,先將混合粉末在300 ℃氬氣中熱處理4 h,然后分別在500、600、700 ℃氬氣中退火 2 h,得到樣品 MnO-C500、MnO-C600、MnO-C700,加熱速率為5 ℃·min-1。
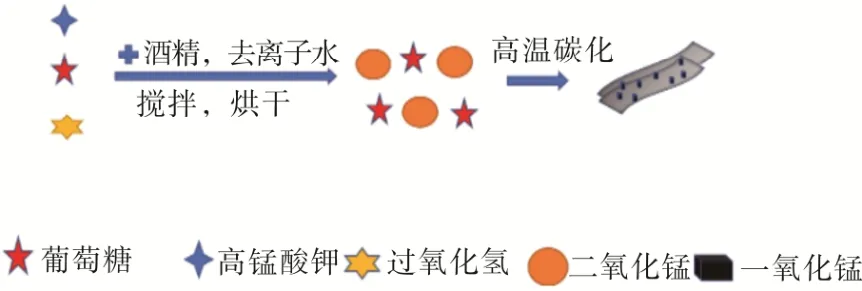
圖1 制備流程示意圖
將80 mg 電極材料與10 mg 導電劑和10 mg 黏合劑分散在0.8 mL 超純水中,制成黏稠的漿液。將該漿液均勻地涂敷在集流體(銅箔,0.02 mm)上,干燥后得到電極片。集流體上活性材料的負載量約為0.95 g·cm-2。使用鋰片作為對電極,在真空手套箱中組裝為扣式半電池后,對半電池進行電化學性能分析。
1.3 材料表征及電池性能測試
采用X 射線衍射(XRD,布魯克公司的D8 型X 射線粉末晶體衍射儀,CuKαλ=0.154 06 nm)、場發射掃描電子顯微鏡(Gemini SEM 300)對材料的晶體結構、微觀形態和結晶性能等各種參數進行表征和測試。
恒流充放電(窗口0.01~3 V,電流密度0.1 C)和倍率充放電(窗口0~3 V)分析在Land 電池測試系統(武漢藍電電子股份有限公司)上進行,電化學阻抗譜(EIS)在電化學工作站(Princeton 4000)上進行測試,測試頻率范圍在0.01~100 000 Hz。
2 結果與討論
2.1 XRD 表征與分析
圖1表現了此負極材料的制備過程,由高錳酸鉀、過氧化氫和葡萄糖的一步熱解方法制備而成。然后對樣品的晶體結構進行了分析,圖2為不同溫度下碳化的樣品的XRD 圖譜。由圖2可以看出,前驅體在氬氣環境下碳化后均顯示出與純MnO 相同的衍射峰,對應的晶面(111)、(200)、(220)、(311)(222)與MnO 吻合,表明在高溫炭化的過程中高錳酸鉀反應產生的MnO2被還原為MnO。
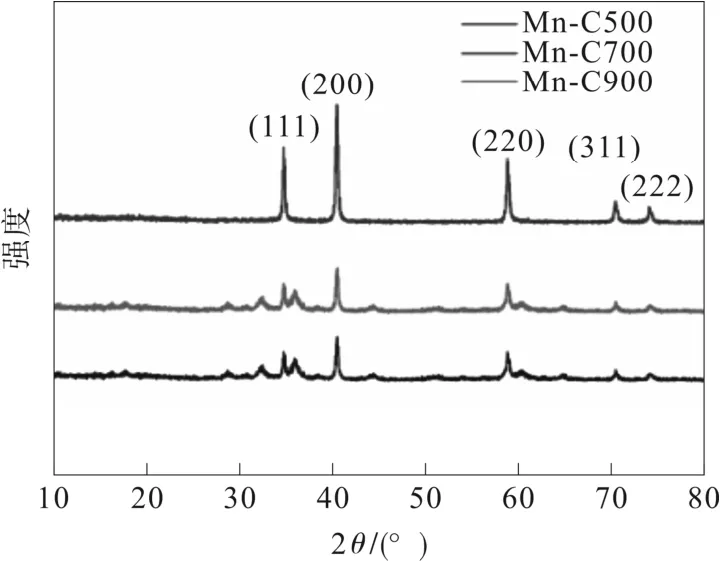
圖2 不同溫度處理后樣品XRD 圖譜
2.2 SEM 表征與分析
圖3為MnO-C600 為的掃描電鏡圖片,可以觀察到MnO 納米顆粒均勻分散在碳材料基底上,并沒有大范圍的團聚。同時由于葡萄糖在高溫碳化時官能團的脫去和與MnO2發生氧化還原反應在碳材料表面造成了不規則的缺陷,由于這種結構使得MnO納米顆粒不會大量團聚,同時在作為負極材料的循環過程中起到保護和緩沖作用。

圖3 MnO-C600 的SEM 圖象
2.3 BET 表征與分析
為了進一步研究材料的內部結構,測定了樣品MnO-C600 的吸附/解吸等溫線,得到了材料的比表面積和孔徑分布,結果如圖4所示。基于BET 法,計算了材料MnO-C600 的比表面積和孔體積分別為561.898 m2·g-1和0.199 cm3·g-1,同時還呈現了較寬的孔徑分布范圍,1~40 nm。這樣的孔徑分布有利于促進電解質的滲透和離子的快速傳輸,高比表面積提供了更多的活性點位,從而產生了優異的倍率性能和較高的容量。
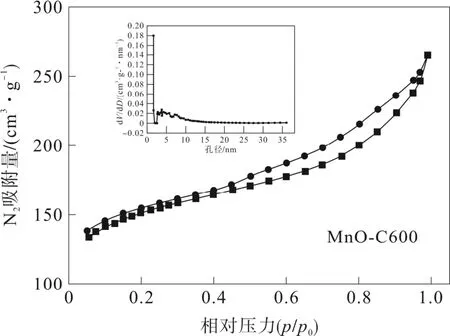
圖4 MnO-C600 氮氣吸附-解吸等溫線機孔徑分布
2.4 電化學性能分析
為了評估樣品的電化學性能,對對不同樣品進行了恒流充放電測試和倍率測試,結果如圖5和圖6所示。由圖5和圖6圖可以看出,MnO-C600的循環和倍率性能最優,在0.3 A·g-1的電流密度下循環50 圈后保持384.2 mAh·g-1的可逆容量,在1 C的電流密度下仍保持329.3 mAh·g-1的可逆容量。這說明復合材料中多孔碳材料有效地緩解了在鋰離子電池循過程中MnO 的膨脹和破裂,從而提高了材料的循環和倍率性能。其中在600 ℃碳化的樣品展現出最好的性能,可能是由于500 ℃時溫度過低,碳化不完全,沒有造成豐富的孔結構,而隨著溫度持續升高到700 ℃,材料原本的缺陷結構又在高溫下發生坍塌,所以造成性能下降。

圖5 MnO-C500、MnO-C600、MnO-C700 的充放電曲線

圖6 MnO-C500、MnO-C600、MnO-C700 的倍率曲線
2.5 材料阻抗譜分析
圖7為MnO-C500、MnO-C600、MnO-C700 負極材料的EIS 阻抗圖譜。圖中曲線高頻區與X軸的第一個交點為電池的溶液阻抗(Rs),半圓弧的直徑對應于材料的電荷轉移阻抗(Rct)[10]。其中MnO-C600 的Rct最小為73.6 Ω,表明了MnO-C600電極材料具有更好的反應性和更快的鋰離子轉移[11]。這也表明MnO-C600 樣品具有更好的孔結構,同時MnO 納米顆粒分散得更加均勻,碳材料起到的緩沖作用更好。

圖7 MnO-C500、MnO-C600、MnO-C700 的EIS 阻抗譜
3 結 論
本文提出了一種簡單且低成本的策略,通過高錳酸鉀、過氧化氫和葡萄糖的一步熱解法,在碳網絡中構建碳包裹MnO 納米顆粒的獨特納米結構。獨特的納米復合結構不僅提供空穴以促進快速離子傳輸和導電網絡以促進電荷轉移,還提供緩沖空間以適應體積變化。因此,MnO-C600 半電池的陽極顯示出在0.3 A·g-1的電流密度下循環50 圈后保持384.2 mAh·g-1的可逆容量,在1 C 的電流密度下仍保持329.3 mAh·g-1的可逆容量。這種簡便、低成本的方法和獨特的納米結構設計有望推廣到其他復合陽極材料,包括多孔摻氮碳片、金屬氧化物和用于LIBs 的三維碳網絡。

