連續流動條件下硝酮的光化學合成在本科實驗教學中的應用探索
宣俊,金偉偉,李磊,廉笑,張瓊,劉晨江,*
1安徽大學化學化工學院,合肥 230601
2新疆大學化學學院,烏魯木齊 830046
利用可見光作為綠色能源引發的有機化學轉化已成為合成化學中的前沿研究領域之一[1]。由于該類反應具有反應條件溫和、化學選擇性優異等優點,使其在現代合成有機化學及化學生物學等研究中具有良好的應用前景。但隨著反應規模的擴大,光無法有效地穿透溶液至反應中心而導致反應效率下降明顯。提高光照強度又可能會導致反應物過度照射而引發副產物的產生。近年來,流動化學的出現為解決光反應中的這些問題提供了一條有效的途徑[2]。流動化學,也稱作連續流化學,它的主要特征是在連續流動的流相中完成化學反應的發生。與在燒瓶等容器中進行的傳統反應相比,流動化學通過對混合、加熱和停留時間等關鍵反應參數的調控,可以更好地控制反應,從而提高反應效率。另外對于放熱量大的反應,使用流動化學反應裝置可以增強實驗的安全性。
另一方面,硝酮是有機合成中最重要的合成子之一,常被用作1,3-偶極子參與環加成反應來構建具有重要生理、藥理活性的雜環化合物[3]。近年來化學家們相繼開發出了多種合成硝酮的方法,其中N-單取代羥胺與醛或酮的縮合反應是制備硝酮最有效的方法之一,但這些反應往往需要使用脫水試劑或在高溫條件下才能進行[4]。仲胺、亞胺以及N,N-二取代羥胺的氧化是合成硝酮的另一有效方法,但通常需要消耗化學計量的氧化劑,產生的廢棄物較多,不符合綠色化學理念[5]。
隨著有機化學新反應、新方法和新合成技術的不斷涌現,針對本科生的有機化學實驗教學不能只滿足于傳統的知識傳授和常規有機實驗技能的培養,如蒸餾、分餾、重結晶等[6]。通過設計操作簡便的有機合成新實驗,將學科前沿研究熱點有效融合于本科生實驗教學中,不僅可以讓學生接觸到有機合成新方法,還可以拓寬他們的學術視野和知識面,激發本科生學習有機化學的興趣。
1 實驗目的
本實驗將流動化學與有機光化學結合,實現硝酮化合物的綠色合成。與已知文獻報道的硝酮合成方法相比,該反應具有反應條件綠色溫和、無需催化劑及添加劑以及副產物少等優勢。同時我們希望用本實驗設計實現:(1) 讓本科生熟悉硝酮類化合物的合成方法,拓展現階段本科有機化學教學實驗開設的范圍;(2) 掌握微量有機反應中薄層分析法、柱層析及相關儀器的操作,并將所學的核磁共振氫譜/碳譜的理論知識運用到實際分析中;(3) 通過讓學生搭建簡易流動光化學反應裝置,從本質上理解流動化學的特點和優勢,鍛煉動手能力;(4) 讓學生了解學科前沿研究熱點,對有機光化學和連續流動化學有初步認識,了解綠色化學的原理及核心概念,提高環保意識[7]。
2 實驗原理
如圖1所示,苯基重氮酸酯1在藍色LED燈照射下可以產生卡賓中間體[8],隨后亞硝基苯中親核性氮原子對卡賓加成得到兩性離子中間體4,進而異構為結構更加穩定的硝酮產物3。用TLC監測反應過程,反應結束后柱層析提純目標化合物。
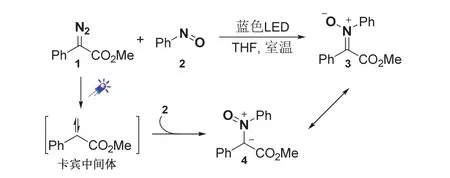
圖1 硝酮3的光化學合成路線
3 儀器與試劑
3.1 實驗儀器
磁力攪拌器(IKA)、旋轉蒸發儀(IKA)、電子天平(梅特勒)、核磁共振波譜儀(德國Bruck公司)、ZF-1型三用紫外燈、藍色LED燈(武漢格奧化學技術有限公司)、自組裝的簡易流動光化學反應器(配件:藍色LED燈帶、風扇、循環泵和流動軟管均為網上購買)。
3.2 主要試劑
苯乙酸甲酯(薩恩化學技術有限公司)、對甲苯磺酰疊氮(薩恩化學技術有限公司)、1,8-二氮雜雙環[5.4.0]十一碳-7-烯(DBU)(畢得醫藥)、亞硝基苯(畢佳索)、乙腈(上海麥克林生化科技有限公司)、四氫呋喃(天津市大茂化學試劑廠)、無水硫酸鈉(天津市大茂化學試劑廠)、氯化銨溶液(10%) (國藥基團化學試劑有限公司)、飽和氯化鈉溶液(天津市大茂化學試劑廠)、石油醚(成都市科隆化學品有限公司)、乙酸乙酯(成都市科隆化學品有限公司),均為國產分析純試劑。
4 實驗步驟
4.1 反應底物苯基重氮酸酯1的制備
苯基重氮酸酯1可由實驗教師預先制備,其合成路線如圖2所示。該反應為文獻已知過程,產物為供體-受體型重氮化合物,性質穩定,使用安全,低溫下可較長時間存放。向50 mL圓底燒瓶中依次加入苯乙酸甲酯(10 mmol,1.5 g),TsN3(12 mmol,2.4 g)和20 mL CH3CN。待溶解均勻后向溶液中逐滴滴加DBU (14 mmol,2.3 g),將所得溶液于室溫下攪拌,通過TLC點板監測反應。反應結束后(約3 h),加入水淬滅反應,并用乙酸乙酯進行萃取(10 mL × 3次)。合并的有機相分別用配制好的10% NH4Cl溶液和飽和氯化鈉溶液洗滌,最后用無水硫酸鈉進行干燥。用旋轉蒸發儀除去溶劑,通過快速柱層析獲得目標產物1 (洗脫劑:石油醚:乙酸乙酯 = 60 : 1-30 : 1 (體積比);紅色油狀物,1.6 g,產率:91%)。

圖2 苯基重氮酸酯1的合成路線
4.2 硝酮3的光化學合成:微量反應
如圖3所示,在室溫下向兩個10 mL Schlenk反應管中分別加入苯基重氮酸酯1 (0.2 mmol,35.2 mg)、亞硝基苯2 (0.1 mmol,10.7 mg)、1.0 mL無水四氫呋喃以及攪拌子。將其中一個Schlenk反應管放置在24 W藍色LED燈照射下攪拌1 h,另一個Schlenk反應管用錫箔紙包裹完全后置于黑暗條件下攪拌1 h。反應結束后,通過旋轉蒸發儀除去溶劑,粗產品通過柱層析分離純化(洗脫劑:石油醚:乙酸乙酯 = 20 : 1-5 : 1)。

圖3 硝酮3的微量光化學合成路線
4.3 硝酮3的光化學合成:放大量反應
4.3.1 常規玻璃瓶中硝酮的放大量合成
如圖4所示,室溫下向50 mL圓底燒瓶中分別加入苯基重氮酸酯1 (2.0 mmol, 352 mg)、亞硝基苯2 (1.0 mmol,107 mg)、10 mL無水四氫呋喃以及攪拌子。隨后將圓底燒瓶放置在藍色LED下照射下攪拌4 h。反應停止后,通過旋轉蒸發儀除去溶劑,將所得的粗產品進行柱層析分離純化(洗脫劑:石油醚:乙酸乙酯 = 20 : 1-5 : 1)。

圖4 圓底燒瓶中硝酮3的放大量光化學合成路線
4.3.2 連續流動條件下硝酮的放大量合成
搭建流動光化學反應器所需的零部件主要有:藍色LED燈帶、風扇、循環泵和流動軟管,如圖5所示。這些主要零部件均可以通過網上購買,價格也合適于本科實驗開展(注:搭建一套簡易流動光化學反應器大約需人民幣300元,具體購買信息及價格見本論文的補充材料部分)。

圖5 簡易流動光化學反應器主要部件
室溫下向50 mL圓底燒瓶中分別加入苯基重氮酸酯1 (2.0 mmol,352 mg)、亞硝基苯2 (1.0 mmol,107 mg)、10 mL無水四氫呋喃以及攪拌子。隨后將反應體系放置于流動光化學反應器中反應4 h (流速約2.5 mL·min?1)。反應停止后,通過旋轉蒸發儀除去溶劑,將所得的粗產品進行柱層析分離純化(洗脫劑:石油醚:乙酸乙酯 = 20 : 1-5 : 1)。
5 結果與討論
5.1 對微量反應
如表1所示,對硝酮的微量光化學合成反應,藍光照射下反應1 h后的體系顏色呈亮黃色,TLC點板顯示有明顯新產物生成,經柱層析分離純化得硝酮產物3 (黃色固體,收率:79%)。黑暗條件下攪拌1 h后的反應體系顏色為淺綠色,TLC點板顯示無新產物生成,黑暗條件下反應并未發生。由此可以得出實驗設計的硝酮光化學合成方案可行,且藍色LED燈照射是本實驗必不可少的條件。

表1 微量反應結果
5.2 對放大量反應
如表2所示,對于放大量反應而言,在普通圓底燒瓶中光照下攪拌4 h后的反應體系顏色為淺綠色,TLC點板顯示有新產物生成,但新產物點較淺,經柱層析分離純化得硝酮產物3 (黃色固體,收率:23%)。而在流動光化學反應器中反應4 h后的體系顏色呈亮黃色,TLC點板顯示有明顯新產物生成,經柱層析分離純化得硝酮產物3 (黃色固體,收率:70%)。兩組數據對比可知,對于放大量的光化學合成反應,由于使用的溶劑量增多,直接在圓底燒瓶中光照反應時,光吸收效果差導致反應產率下降明顯。而在流動光化學反應器中的放大量反應,基本維持了和微量反應差不多的反應效果,僅有略微的產率下降。反應效果明顯優于普通圓底燒瓶中光照下攪拌。

表2 放大量反應結果
5.3 產物分析與表征
如圖6所示,產物硝酮3的結構通過核磁共振氫譜(1H NMR)以及核磁共振碳譜(13C NMR)表征確定。核磁譜圖的出峰位置、相對峰積分面積和峰裂分均與文獻報道一致。并且譜圖上基本沒有雜質峰,表明通過柱層析方法分離得到的硝酮產物具有很高的純度。
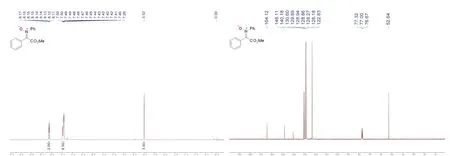
圖6 硝酮3的核磁譜圖
1H NMR (400 MHz, CDCl3, 300 K):δ= 8.17-8.11 (m, 2H), 7.49 (m, 2H), 7.46-7.39 (m, 6H), 3.52 (s,3H);13C NMR (100 MHz, CDCl3, 300 K):δ= 164.1, 148.1, 140.2, 130.6, 129.9, 128.9, 128.8, 128.3,128.2, 122.8, 52.6。
6 實驗組織
本實驗總時長大約6-8 h,無需使用無水無氧等特殊實驗操作,適合本科生在基礎實驗室中操作完成。建議以綜合設計實驗形式,面向大學三年級下學期或四年級上學期學生開設。目前,本設計實驗已組織我校本科生在實驗室進行了多輪重復,數據重復性好,具有在本科生基礎有機實驗室中開展的潛力。
7 結語
本實驗將流動化學與有機光化學結合,實現硝酮化合物的綠色合成。通過將連續流動化學和光化學合成融合運用于本科實驗教學,拓展現階段本科有機化學教學實驗的開設范圍。通過本實驗可以讓學生掌握微量有機反應中薄層分析法、柱層析及相關儀器的操作,并將所學的核磁共振氫譜/碳譜的理論知識運用到實際分析中。另外,還可以讓學生了解學科前沿研究熱點,對有機光化學和連續流動化學有初步認識,了解綠色化學的原理及核心概念,提高環保意識。自實驗開設以來,教研相長,教師和學生均對有機光合成和流動化學產生了濃厚的學習興趣。

