基于美國FAERS數據庫的利那洛肽不良事件信號挖掘與分析
王浩,陽麗,劉小英,陳力(. 成都市新都區人民醫院藥劑科,成都 60500;2. 四川大學華西第二醫院藥學部,成都 6004;3. 四川大學華西第二醫院循證藥學中心,成都 6004;4. 出生缺陷與相關婦兒疾病教育部重點實驗室,成都 6004)
腸易激綜合征(IBS)是一種全球范圍內常見的、以腹痛/腹脹或腹部不適為主要癥狀的功能性腸病,排便后癥狀多有改善,常伴有排便習慣(頻率和/或性狀)的改變[1]。若腹部癥狀+便秘反復不斷,則很有可能是IBS 的一種主要亞型便秘型腸易激綜合征(IBS-C)[2]。我國IBS 患病率為6.5%[1],其中IBS-C 占比達15.1%[3]。利那洛肽是一種鳥苷酸環化酶C 受體(GC-C)激動劑,它與腸道GC-C 結合后,一方面使細胞內和細胞外環磷酸鳥苷(cGMP)濃度升高,可刺激腸液分泌,加快胃腸道蠕動,從而增加排便頻率;另一方面細胞外cGMP 濃度升高可降低痛覺神經信號傳導,緩解腹痛癥狀[4-5]。2013年2月,利那洛肽在美國獲批準上市,用于IBS-C 和慢性特發性便秘患者的治療。作為全球首個獲批用于便秘治療的鳥苷酸環化酶C 激動劑,它的上市填補了IBS-C 患者僅能選擇癥狀改善類藥物而無針對性治療藥物的空白。2019年1月 15日國家藥品監督管理局(NMPA)批準該藥正式在中國上市。作為我國專門治療成人IBS-C 的處方藥物,將填補我國成人IBS-C 治療的空白,為廣大國內患者帶來福音。隨著利那洛肽的廣泛使用,真實世界的藥物不良事件(ADE)報告也逐漸增多。本文通過對美國FDA ADE 報告系統(FAERS)收集到的數據進行挖掘和篩選,分析利那洛肽可疑的ADE 信號,以期為國內臨床安全合理用藥提供參考。
1 資料與方法
1.1 數據來源
選取FAERS 數據庫中2016年第一季度至2021年第二季度共22 個季度的數據,用MySQL進行分析,去重處理后得到首要懷疑藥物為利那洛肽的ADE 報告。
1.2 數據篩選
以利那洛肽的通用名“Linaclotide”和商品名“LINZESS”為關鍵檢索詞在數據庫中進行檢索,得到包括人員信息、藥物信息、ADE 和原發疾病等數據資料,刪除重復和存疑數據,形成研究ADE 的原始數據。
1.3 數據處理
采用《國際醫學用語詞典》 MedDRA 23.0 更新版(MedDRA)中藥物不良反應(ADR)術語集的首選系統器官分類(SOC)和首選術語(PT)對ADE 進行分類和表達,并完成相應的中英文映射。
1.4 數據分析
選用在ADE 監測中廣泛應用的比值失衡測量法中的報告比值比法(ROR)[6]和綜合標準法(MHRA)[7]分別計算ROR 值和比例報告比值(PRR),篩選潛在信號(見表1、2)。目標藥物相關風險信號的檢測閾值設定為ROR 中95%的可信區間(95%CI)下限大于1 且報告數不少于3 例,以及MHRA 中PRR ≥2、χ2≥4 且報告數不少于3 例[8]。
1.5 嚴重ADE
嚴重ADE 系指使用藥物引起下列情況之一:導致死亡;危及生命;致畸、致癌、致缺陷;導致顯著或永久的人體傷殘或器官功能損傷;導致住院或住院時間延長;導致其他重要醫學事件,如不進展治療可能出現上述情況(如成癮性)。
2 結果
2.1 ADE 報告的基本情況
2016年第一季度至2021年第二季度的ADE背景信號共22 137 402 個,其中經刪除重復數據后得到首要懷疑藥物為利那洛肽的ADE 報告共16 730 份,報告數1088 個。在6560 例患者的報告中,可發現女性占大多數(61.20%),患者主要為18 歲及以上人群(34.59%),而美國是報告數最多的國家(94.38%),2016 至2020年每年報告數差距不大,具體報告基本信息見表1。

表1 利那洛肽相關ADE 報告基本信息Tab 1 Basic information of linaclotide ADE reports
2.2 不良反應信號分析結果
對利那洛肽為首要懷疑藥品的ADE 信號進行篩選,經ROR 法和MHRA 法篩選后最終獲得的利那洛肽ADE 信號數為102 個,報告總計數為11 623 份,經刪除存疑信號后,得到ADE 相關信號75 個,報告總計數為7577 份。在有信號的PT 中,以報告數排序的前50 位如表2所示。其中,較為常見的未在說明書中提及的ADE 為腹瀉(1943 例)、腹脹(434 例)、腹痛等(318 例)等。
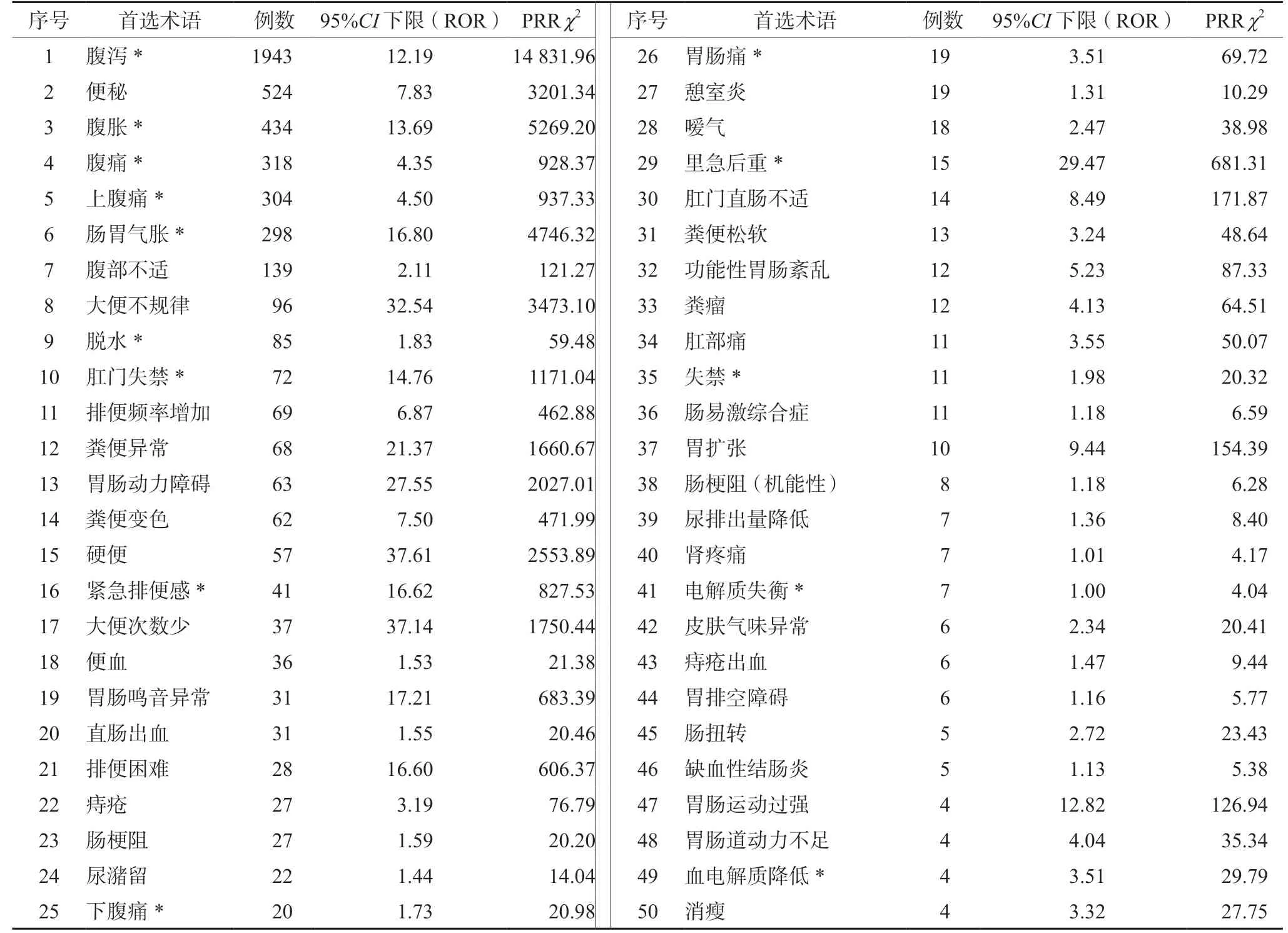
表2 利那洛肽報告數排名前50 位的ADE 信號Tab 2 Top 50 ADE signals of linaclotide in descending order of reports
2.3 SOC 分類ADE 報告及信號分類
根據MedDRA 對有信號的PT 進行SOC 分類排序,可發現有信號的SOC 11 個,具體見圖1。其中,胃腸系統疾病(64.99%)、全身性疾病及給藥部位各種反應(32.04%)的報告例數相對較多。
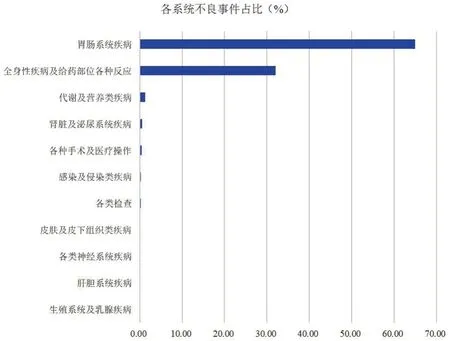
圖1 各SOC 項下不良事件信號的報告例數占比Fig 1 Percentage of ADE signal detection of each SOC
2.4 嚴重的ADE
嚴重的 ADE 主要體現在胃腸系統和腎臟及泌尿系統兩大類。其中在胃腸系統主要表現為肛門失禁、便血、直腸出血、腸梗阻等,而在腎臟及泌尿系統疾病主要表現為尿潴留、失禁等(見表3)。
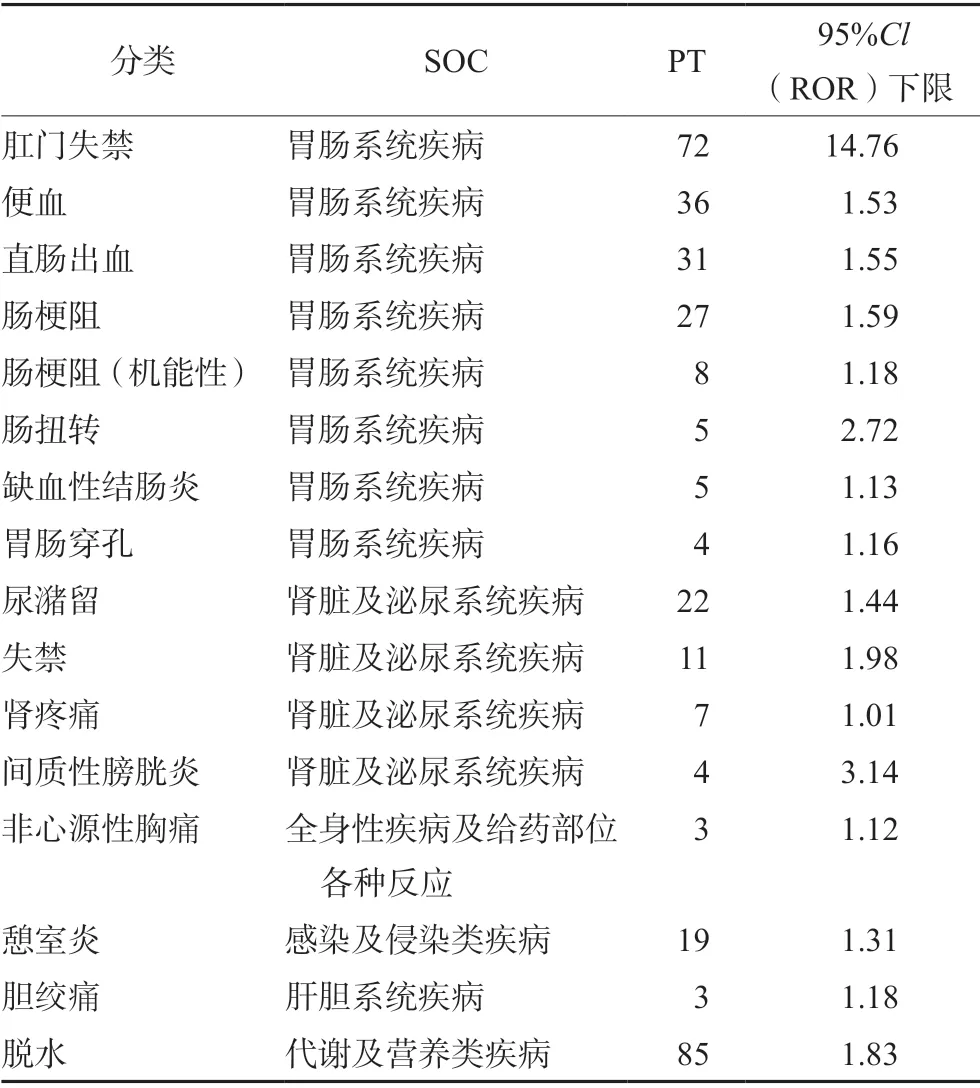
表3 嚴重的 ADE 信號Tab 3 Severe ADE signal
3 討論
通過ROR 法和MHRA 法挖掘到的ADE 信號與利那洛肽說明書記錄及用藥警示信息基本一致,主要表現為胃腸系統疾病、全身性疾病及給藥部位各種反應。
3.1 常見的ADE 信號
一項關于利那洛肽治療IBS-C 的meta 分析發現利那洛肽的主要不良反應為胃腸道反應,以腹痛、腹瀉較為常見[9]。結合表2和圖1可發現,胃腸系統疾病這一SOC 的ADE 報告數占比最高,主要信號包括腹瀉、腹脹、腹痛等。在慢性便秘患者的兩項大型Ⅲ期試驗中,最常見和劑量相關的ADE 是腹瀉,導致兩個利那洛肽治療組中 4% 的患者停止治療[10]。一項利那洛肽在對合并便秘的IBS 患者的Ⅱb 期研究中發現有至少3%的利那洛肽使用者發生了腹瀉,且腹瀉發生率跟劑量成正相關,大多數為輕度或中度,也有部分患者出現較為嚴重的腹瀉,從第一次服用研究藥物到首次出現腹瀉的中位天數為4 d[11],可能與利那洛肽主要作用于胃腸道有關,提示臨床使用過程中如果發生持續(如超過1 周)或重度腹瀉,應考慮暫停利那洛肽直至腹瀉緩解,同時因持續性或嚴重腹瀉可能導致水、電解質紊亂,對有水、電解質紊亂傾向及耐受性差的患者(如老年人、心血管疾病患者、糖尿病和高血壓)應謹慎使用。一項為期12 周的臨床隨機對照試驗發現,有7 例接受利那洛肽的患者在治療結束時血清碳酸氫鹽水平低于正常下限,但這些患者均未報告腹瀉為或其他被認為與低碳酸氫鹽水平有關的不良反應[12],提示利那洛肽使用者雖未出現腹瀉但依然有酸堿失衡的風險。對于上述情況,應考慮檢查電解質及酸堿平衡。除說明書記載的常見胃腸道不良反應,此次研究還檢測到糞便變色、胃腸鳴音異常、腸梗阻、便血、腸扭轉、胃腸穿孔等少見的胃腸道ADE 信號,提示在治療過程中發生此類疾病需考慮是否具有相關性,在存在高危因素尤其有腸梗阻的患者應避免使用。而僅次于胃腸系統疾病的全身性疾病及給藥部位反應,主要信號包括藥物無效、對非適應證用藥無效、治療反應減弱,提示臨床在使用過程中注意觀察藥品效應,出現上述情況應考慮重新調整用藥方案。
3.2 其他少見的ADE 信號
雖然在安全性上,利那洛肽幾乎不進入血液循環,與其他藥物基本無相互作用[13],但在本次研究中發現尚有少量非胃腸系統的新的 ADE 信號的報告,主要包括尿排出量降低、腎疼痛、皮膚氣味異常等,具體原理和機制尚不明確。說明書中病毒性胃腸炎、頭暈、頭痛是常見的ADE,但在本次研究前50 位中卻未被發現,此處與說明書提示存在差異,臨床需注意。
3.3 嚴重的ADE 信號
通過表3可以發現利那洛肽嚴重ADE 信號中肛門失禁、脫水較其他嚴重ADE 信號計數多,可能是因腹瀉是利那洛肽常見的ADE,嚴重腹瀉及腹瀉持續時間較長時容易導致患者肛門失禁、脫水,且肛門失禁信號強度較大,提示于藥物使用的相關性較強。此外,其他嚴重ADE 雖然發生較少但可能會導致患者住院或危及生命,提示在使用過程中應密切監測,出現以上嚴重 ADE時應立即停藥,并做相應處理。
3.4 小結
即使有如此大樣本的數據,本研究仍存在一定的局限性。首先,由于FAERS 是自發呈報系統,存在漏報、錯報等情況;其次,盡管ROR 法和MHRA 法兩種方法同時使用,但仍不能完全排除假陽性信號的出現;另外,在使用MedDRA術語集時,使用比PT 更高級別的術語可能出現統計上不同的結果[14];最后,定量信號檢測方法產生的ADE 信號是基于報告的數量關聯而非生物學關聯[15]。綜上,本研究無法精確定義利那洛肽的ADE 真實發生率,最終結果仍需進一步的研究證實。
4 結論
基于美國 FAERS 數據庫,利用ROR 法和MHRA 法對利那洛肽上市后的ADE 進行分析,挖掘出更加真實完整的藥品安全信息,發現了如便秘、大便不規律、胃腸動力障礙、糞便變色、硬便、便血、胃腸鳴音異常、直腸出血、腸梗阻、尿潴留、憩室炎、噯氣、胃擴張、尿排出量降低、腎疼痛、皮膚氣味異常等新的ADE,同時還觀察到利那洛肽在胃腸系統、全身性疾病及給藥部位各種反應方面的ADE 相對較多,這在一定程度上彌補了藥品上市前臨床試驗的不足,可為臨床合理用藥提供參考。當然,利那洛肽的ADE 還需在真實世界中不斷地被探索和研究,以更好地為患者的生命健康保駕護航。