血清HBV RNA預測慢性乙型肝炎患者停藥后復發(fā)的meta分析
張琪 王余彥 秦波
乙型肝炎病毒(hepatitis B virus, HBV)感染是一個全球性問題[1]。肝內共價閉合環(huán)狀DNA(covalently closed circular DNA, cccDNA)是導致HBV感染慢性化的主要原因[2]。而肝內cccDNA的清除被認為是慢性乙型肝炎(CHB)完全治愈[3-4]。但無論是核苷類似物NAs還是干擾素IFN均無法直接作用于肝內cccDNA,因而完全治愈幾乎無法實現(xiàn)。目前各種指南及專家共識多將功能性治愈暨臨床治愈[4-7]作為CHB治療的理想終點,而未對肝內cccDNA水平進行監(jiān)測。肝內cccDNA的存在,使得這些經過長期抗病毒治療、甚至是實現(xiàn)了功能性治愈的患者,停藥后仍面臨著復發(fā)的風險。
肝內cccDNA水平的測定需進行有創(chuàng)性肝穿刺,臨床上難以普及。因而,亟待找尋一種可反映肝內cccDNA水平的無創(chuàng)性新型血清學標志物。血清HBV RNA就是近年研究的熱點之一[8]。已有學者證實血清HBV RNA實際上是由前基因組RNA(pregenomic RNA, pgRNA)及其剪切變異體形成的病毒樣顆粒或衣殼抗體復合物[9-11]。PgRNA由肝內cccDNA直接轉錄形成,因而血清HBV RNA在反映肝內cccDNA存在及活性方面都具有優(yōu)勢[12-14]。
最近,一些研究[15-20]開始關注停藥時血清HBV RNA狀態(tài)與停藥后復發(fā)之間的關系。本meta分析將探討停藥時血清HBV RNA狀態(tài)與停藥后復發(fā)情況之間的內在聯(lián)系,為今后尋找指導安全停藥的新型血清學標志物提供依據(jù)。
資料與方法
一、 文獻檢索
檢索PubMed、Embase、Web of science、Cochrane library以及網站https://clinicaltrials.gov/,搜集2016至2020年期間發(fā)表的關于血清HBV RNA與CHB患者停藥后復發(fā)之間關系的相關英文文獻。檢索詞為血清HBV RNA和CHB的英文(具體如下: “HBV RNA” or “HBV pgRNA” or “HBV pregenomic RNA” or “hepatitis B virus RNA” or “hepatitis B virus pgRNA” or “hepatitis B virus pregenomic RNA”和“hepatitis B, chronic” or “chronic hepatitis B” or “chronic hepatitis B virus Infection” or “hepatitis B virus infection,chronic”)。同時進行手工檢索。以PubMed為例,具體檢索策略見圖1。本研究在注冊前進行了預檢索,相關中文研究數(shù)量少,以綜述為主,基本無符合納入標準的文獻;因而著重檢索了英文文獻。(PROSPERO網站注冊號: CRD42020208267)。
二、 納入與排除標準
(一) 納入標準 (1)研究對象為長期接受抗病毒治療并停藥的CHB患者;(2)文章提供所需數(shù)據(jù);(3)隊列研究;(4)英文文獻。
(二) 排除標準 (1)研究對象不符合前述條件;(2)文章無法提供所需數(shù)據(jù);(3)非隊列研究;(4)其他語種文獻,重復文獻,不能進行meta分析的文獻。
三、 文獻篩選與數(shù)據(jù)提取
嚴格按照納入及排除標準進行文獻篩選。對于最終納入本meta分析的文獻,研究者將提取以下信息:(1)作者、發(fā)表年份、國家及研究類型;(2) 目標人群基本特征(包括人數(shù)、患者基本情況);(3)停藥時血清HBV RNA狀態(tài)、隨訪時間、停藥后復發(fā)情況;(4)血清HBV RNA檢測為陰性的標準、具體的停藥標準及復發(fā)的定義。兩位研究者分別獨立進行數(shù)據(jù)提取,出現(xiàn)任何分歧都將進行討論后達成共識或者通過咨詢第三位研究者來解決。
四、 結局指標 分析所有納入文獻的特點,由于文獻的描述廣泛,故大致考慮復發(fā)標準如下:(1)臨床復發(fā):停藥后出現(xiàn)血清丙氨酸轉氨酶(ALT)異常升高;(2) 病毒學復發(fā):停藥后血清HBV DNA水平異常升高。并從最終納入的文獻中提煉出復發(fā)的具體定義。
五、 納入文獻的質量評價 由于納入的研究均為隊列研究,因而使用紐卡斯爾渥太華量表(NOS)23來評估每項研究的質量。大于6分為高質量文獻。
六、 統(tǒng)計分析 所有統(tǒng)計學分析均采用Revman 5.3軟件進行。通過計算風險比(RR)和95%CI來確定停藥時血清HBV RNA狀態(tài)與停藥后復發(fā)之間的關系。總效應采用Z檢驗,如果P<0.05,則認為組間差異有統(tǒng)計學意義。緊接著將進行異質性檢驗,如果存在顯著的異質性(I2>50%),使用隨機效應模型;如果異質性較小(I2<50%)則采用固定效應模型。為了探尋導致異質性的潛在原因,將對存在顯著異質的研究進行亞組分析。最后進行敏感性分析評估此次meta分析的結果是否穩(wěn)健可靠。若有10項以上的研究納入本meta分析,將使用漏斗圖來評估發(fā)表偏倚。
結 果
一、 文獻檢索結果
初步檢索共得到599篇文獻,其中Web of science檢索到159篇文獻,Pubmed檢索到104篇文獻,Embase檢索到240篇文獻, Cochrane library檢索到91篇文獻,Clinical trials共檢索到13個相關研究,但均未提供相關數(shù)據(jù)結果或處于研究未完成狀態(tài),因而未納入;同時手工檢索到5篇文獻。首先排除267篇重復文獻,然后通過閱讀標題和摘要排除314篇文獻,最后通過閱讀全文排除14篇文獻。最后,來自4篇文章[17-20]的6項獨立研究被納入本次meta分析,為了區(qū)分來自同一篇文章的不同研究,采用”作者名字1”和”作者名字2”來區(qū)分。所有納入研究均為隊列研究,在2016年至2020年間以英文發(fā)表。具體文獻篩選流程如圖1所示。
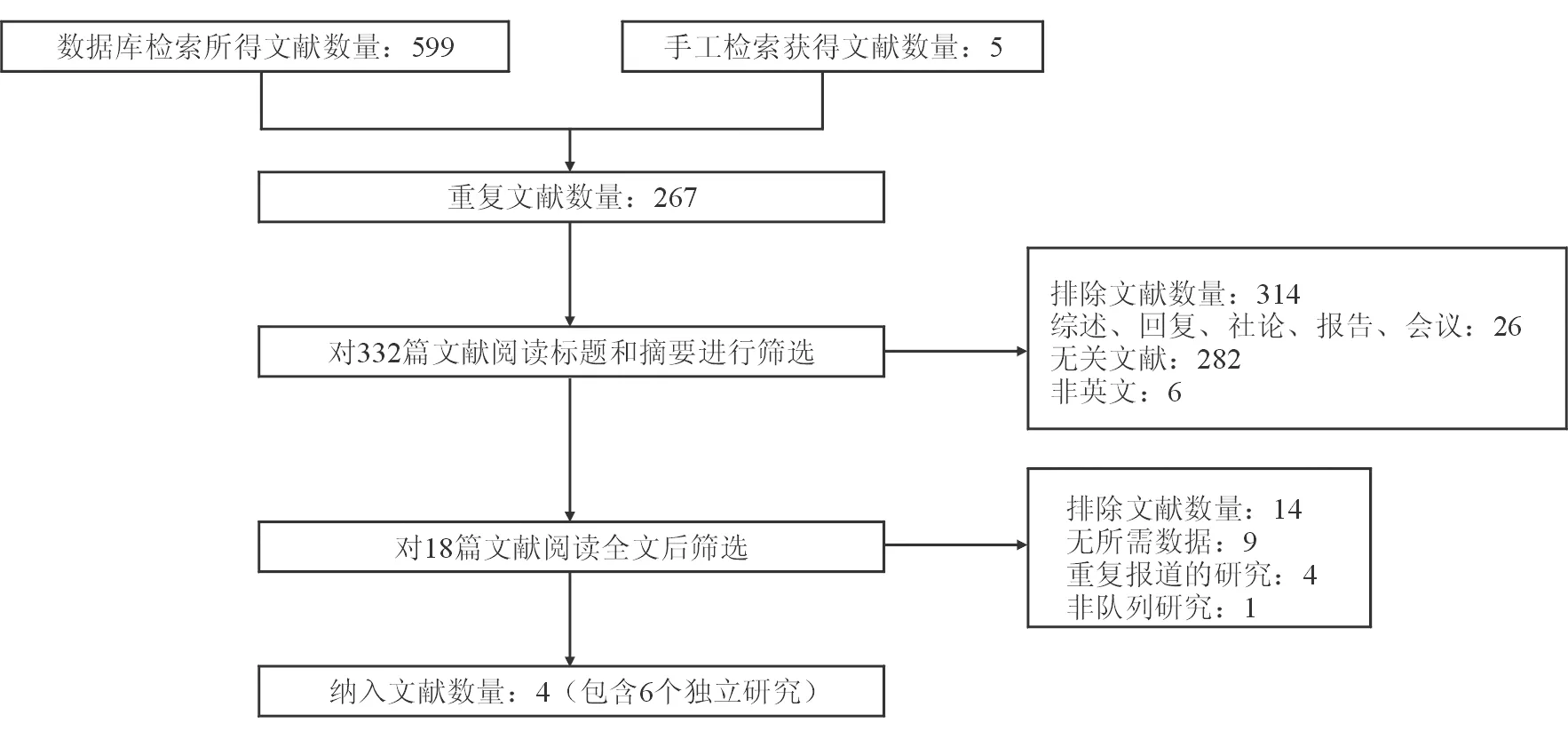
圖1 文獻篩選流程圖
二、納入文獻基本特征及質量評價
表1總結了最終納入研究的特點及NOS評分。

表1 文獻基本特征及質量評價表
三、meta分析結果
(一) 臨床復發(fā)情況 來自3篇文章中的4項研究[16-18]報道了停藥后的臨床復發(fā)情況。根據(jù)患者停藥時HBV RNA狀態(tài),將患者分為HBV RNA陽性組和HBV RNA陰性組。其中HBV RNA陽性組共133例患者,有49例患者在停藥后出現(xiàn)了臨床復發(fā);而HBV RNA陰性組71例患者中僅有8例在停藥后出現(xiàn)臨床復發(fā)。研究之間的異質性較小(Chi2=3.41,P=0.33,I2=12%),因而采用固定效應模型進行分析。meta分析結果顯示,停藥時血清HBV RNA陽性患者在停藥后出現(xiàn)臨床復發(fā)的風險更高(RR=2.98, 95%CI=1.55~5.72,P=0.001,圖2)。
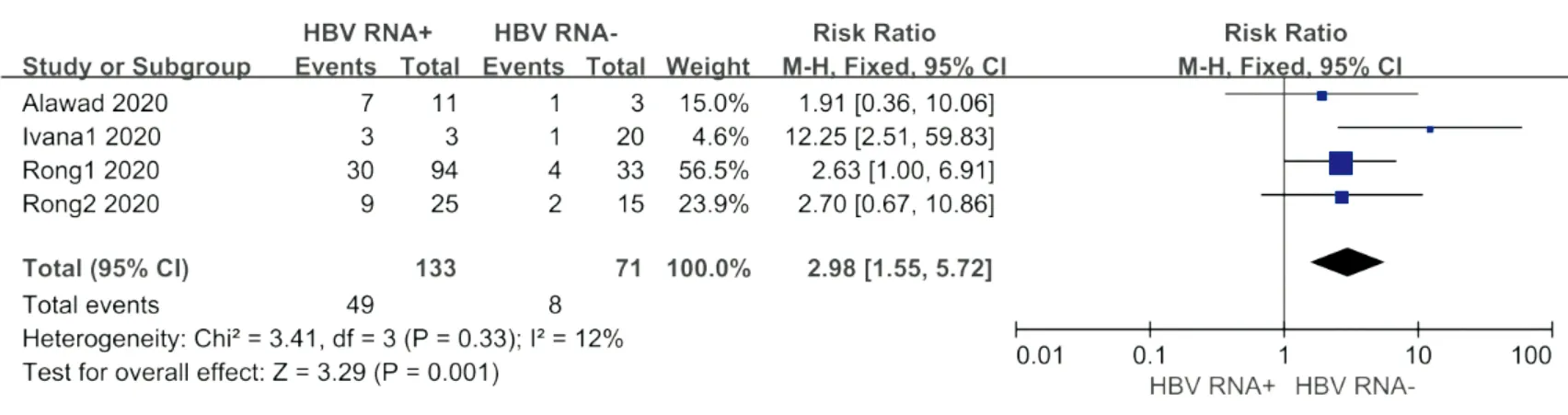
圖2 臨床復發(fā)情況
(二) 病毒學復發(fā)情況 來自4篇文章的6項研究[15-18]報告了停藥后的病毒學復發(fā)情況。此項分析共納入256例患者,其中HBV RNA陽性患者156例,HBV RNA陰性患者100例。研究之間存在顯著的異質性(Chi2=34.11,P<0.01,I2=85%),故采用隨機效應模型進行分析。結果顯示,相比于血清HBV RNA陽性患者,血清HBV RNA陰性患者停藥后病毒學復發(fā)率較低(39%, 39/100 vs 67.3%, 105/156,P=0.07,見圖3),但差異并無統(tǒng)計學意義。
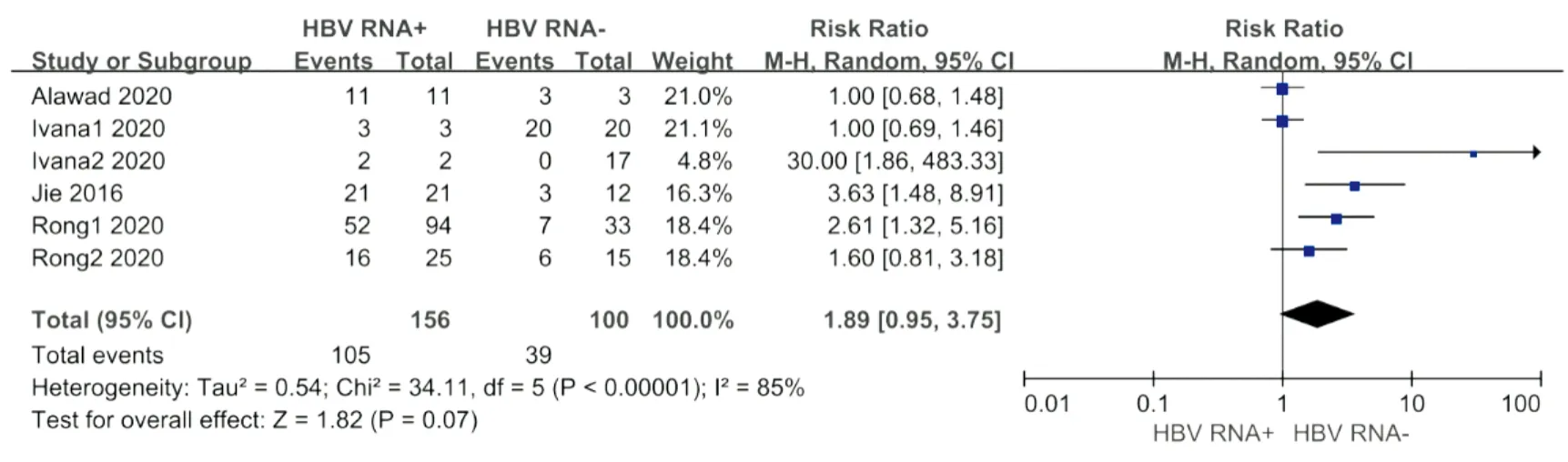
圖3 病毒學復發(fā)情況
(三) 異質性檢驗 為探討報道病毒學復發(fā)的研究之間異質性的可能原因,對以下四個方面進行亞組分析,包括樣本人數(shù)、隨訪時間、血清HBV RNA檢測為陰性的標準、病毒學復發(fā)的定義。亞組分析的結果顯示,小樣本數(shù)量(樣本人數(shù)<30Chi2=9.44,P=0.009,I2=79% vs樣本人數(shù)>30Chi2=2.27,P=0.32,I2=12%))和病毒學復發(fā)定義的不同(HBV DNA>20 iu/mLChi2=25.03,P<0.01,I2=92% vs HBV DNA>2000 IU/mLChi2=1.05,P=0.31,I2=5%)可能是造成研究間顯著異質性的原因。而隨訪時間的不同(隨訪時間<3年Chi2=25.03,P<0.01,I2=92% vs隨訪時間>3年Chi2=11.79,P=0.003,I2=83%)、血清HBV RNA檢測為陰性的標準不一致(HBVR RNA低于LLOQChi2=10.52,P=0.001,I2=90% vs HBV RNA 檢測不到Chi2=17.89,P=0.0005,I2=83%)不能解釋異質性。
(四) 敏感性分析 采用逐一排除文獻法。在本meta分析中,排除任何一項研究都不會過度影響異質性,因而考慮本次meta分析結果相對穩(wěn)健。但對于報道臨床復發(fā)的4項研究[18-20](所有納入研究之間異質性較小I2=12%),必須提到的是,在排除Ivana1 2020這項研究之后,異質性(P=0.94,I2=0%)消失了。進一步研究后發(fā)現(xiàn),該研究對于臨床復發(fā)標準的定義較其他研究更具包容性,即ALT>10 ULN(檢測上限)時才認為臨床復發(fā),遠遠高于多種指南中常用的ALT水平。但總的來說,敏感性分析顯示了本次meta分析結果的穩(wěn)定性。
(五) 發(fā)表偏倚 由于在本meta分析中只有不到10項研究,使用漏斗圖來評估發(fā)表偏倚是非常受限的,因而未采用漏斗圖評估發(fā)表偏倚。但本次meta分析的發(fā)表偏倚是可以合理推斷的,因為大多數(shù)納入的研究都是在2020年發(fā)表的,且未對灰色文獻進行專門的檢索。
討 論
肝內cccDNA的持續(xù)存在使CHB患者停藥后仍面臨復發(fā)風險。臨床工作中,肝內cccDNA的監(jiān)測因有創(chuàng)性肝活檢而受限。血清HBV RNA與肝內cccDNA有良好的相關性,在一定程度上可以反映肝內cccDNA的存在。因而本meta分析探討了停藥時血清HBV RNA狀態(tài)與停藥后復發(fā)之間的關系。
本meta分析結果顯示,停藥時血清HBV RNA陽性的患者停藥后出現(xiàn)臨床復發(fā)的風險更高(RR=2.98, 95%CI=1.55~5.72,P=0.001)。研究間異質性較小,采用固定效應模型。敏感性分析表明,雖然存在一定的異質性,但結果是穩(wěn)健可靠的。同時,本meta分析發(fā)現(xiàn),相比于HBV RNA陽性患者,停藥時血清HBV RNA陰性患者病毒學復發(fā)率較低(39% vs 67.3%,P=0.07),但差異無統(tǒng)計學意義。有研究表明,停藥后病毒學復發(fā)情況的研究間存在顯著的異質性,因而研究者進行了亞組分析,結果表明產生異質性的主要原因是樣本數(shù)量和病毒學復發(fā)定義的不同。
抗病毒藥物如NAs或IFNs不能清除肝內cccDNA。所以即使達到了理想的治療終點——功能性治愈之后再停止治療,患者也有可能出現(xiàn)復發(fā)。這一點在本meta分析中得到了部分證實,那些在停藥時血清HBV RNA為陽性的患者,或者換句話說,其cccDNA仍處于激活狀態(tài)的患者在停藥后更有可能出現(xiàn)臨床復發(fā)。另一方面,停藥時血清HBV RNA陰性的患者病毒學復發(fā)率確實更低,但在本meta分析中差異無統(tǒng)計學意義。這一結論看起來似乎與臨床實踐不符。因此研究者進一步行亞組分析以探討原因。結果表明,樣本量和病毒學定義的不同可能是造成這些研究之間顯著異質性的原因。
綜上,血清HBV RNA對于預測CHB患者停藥后復發(fā)有重要意義。本meta分析首次系統(tǒng)探討了血清HBV RNA在預測CHB患者停藥后復發(fā)方面的意義,為進一步尋找安全停藥的新指標提供了依據(jù)。但本meta分析仍然有一些局限性。首先,納入本次meta分析中的研究是非常有限的,灰色文獻沒有被專門搜索,這可能會導致發(fā)表偏倚,影響結果的穩(wěn)定性。第二,結局指標的定義和停藥的標準雖然相似,但并不完全一致,盡管研究者已經進行了亞組分析以減少由此引起的異質性。第三,目前相關研究總體較少,此次meta分析研究總量少于10例,可能造成研究的局限性。
綜上所述,血清HBV RNA是協(xié)助預測停藥后臨床復發(fā)的重要生物標志物。未來還需進一步深入研究。

