激動劑長方案中兩種促排卵藥物對患者助孕結局的比較
張小玉 張興興 邊曉露 趙淑芹
[摘要] 目的 比較兩種促排卵藥物在促性腺激素釋放激素激動劑(GnRH-a)長方案中的應用,探討其對輔助生殖(ART)患者助孕結局的影響。 方法 回顧性分析2019年4月至2020年6月于棗莊市婦幼保健院生殖醫學中心IVF-ET/ICSI-ET長方案助孕患者新鮮周期的臨床資料共374周期,按照其應用外源性促性腺激素藥物(Gn)的不同分為兩組:使用國產重組人促卵泡激素(r-hFSH,金賽恒)進行控制性超促排卵(COH)176周期(A組),使用進口重組人促卵泡素β(r-hFSH,普利康)進行COH198例(B組)。分別比較兩組患者的一般情況、用藥情況、實驗室各指標及最終臨床結局。 結果 兩組患者的平均年齡、平均不孕年限、體質量指數(BMI)、抗苗勒試管激素(AMH)值、基礎卵泡刺激素(b-FSH)值等比較,差異均無統計學意義(P>0.05);兩組Gn量、Gn天數、HCG日子宮內膜的厚度、受精率、可移植胚胎率、優質胚胎率、無可移植胚胎周期率、移植胚胎數、妊娠率、著床率、早期流產率等比較,差異均無統計學意義(P>0.05);B組患者較A組患者有更多的獲卵數[(13.78±4.37)枚 vs.(10.41±3.87)枚],差異有統計學意義(P<0.05)。 結論 在GnRH-a長方案超促排卵中,應用國產重組人促卵泡激素注射液和進口重組促卵泡素β注射液均可以獲得滿意的臨床結局。
[關鍵詞] 控制性超促排卵;GnRH激動劑長方案; 妊娠結局;促排卵藥物
[中圖分類號] R771.7? ? ? ? ? [文獻標識碼] B? ? ? ? ? [文章編號] 1673-9701(2022)14-0058-04
Comparison of two kinds of ovulation induction drugs in agonist long protocol on pregnancy outcome of patients
ZHANG Xiaoyu? ?ZHANG Xingxing? ?BIAN Xiaolu? ?ZHAO Shuqin
Reproductive Medicine Center, Maternity and Child Health Care of Zaozhuang in Shandong Province,Zaozhuang 277100,China
[Abstract] Objective To observe and compare the application of two kinds of ovulation induction drugs in gonadotropin-releasing hormone agonist (GnRH-a) long protocol and explore its effect on assisted pregnancy outcomes in patients with assisted reproductive technology (ART). Methods The clinical data of 374 fresh IVF-ET/ICSI-ET long protocol assisted pregnant patients in the Reproductive Medicine Center of Maternity and Child Health Care of Zaozhuang from April 2019 to June 2020 retrospectively analyzed and divided into two groups according to their application of exogenous gonadotropins(Gn).Domestic recombinant human follicle-stimulating hormone (r-hFSH) (Jinsaiheng) was used for 176 cycles of controlled ovarian hyperstimulation (COH)( group A).Imported recombinant human follicle-stimulating hormone β(r-hFSH ) (Plikang) was used for COH in 198 cases (group B).The general conditions, medication, laboratory parameters, and final clinical outcomes of patients in two groups were compared. Results There was no significant difference in the mean age,mean duration of infertility, body mass index (BMI),anti-Mullerian hormone (AMH) value,and basal follicle-stimulating hormone (b-FSH) value between group A and group B(P>0.05). There was no significant difference in Gn amount, Gn days,endometrial thickness on HCG day,fertilization rate, transferable embryo rate,high-quality embryo rate,non-transferable embryo cycle rate, number of transferred embryos, pregnancy rate,implantation rate, and early abortion rate(P>0.05). Patients in group B had more oocytes ([13.78±4.37] Pieces vs. [10.41±3.87] Pieces) than those in group A,and the difference was statistically significant(P<0.05 ). Conclusion Both domestic recombinant human follicle-stimulating hormone injection and imported recombinant follicle-stimulating hormone β injection in long protocol GnRH-a ovarian hyperstimulation can obtain satisfactory clinical outcomes.3DC19304-5FFB-4E5C-862B-B3170A3FEE0A
[Key words] Controlled ovarian hyperstimulation; GnRH agonist long protocol; Pregnancy outcome; Ovulation induction drugs;
控制性超促排卵(controlled ovarian hyperstimulation,COH)是利用促排卵藥物在可控的范圍內,誘發超過正常生理狀態的卵泡發育和成熟[1],以此基礎而獲得較多的胚胎,進而提高臨床妊娠率,它是輔助生殖技術中不可缺少的重要環節。現臨床上常用的COH藥物重組人促卵泡素(recombinant human follicle-stimulating hormone,r-hFSH)因其高純度和高生物效價的特點而深受生殖醫師的青睞。r-hFSH按藥物產地可分為國產藥與進口藥。是否此類藥物不論國產或是進口都能使不孕患者的個體化治療達到最滿意的療效?為比較國產藥物與進口藥物的不同,本研究通過回顧性分析,將對金賽恒和普利康的療效和臨床結局進行對比分析,以期對臨床治療進行更好的指導,并為患者合理用藥提供依據,現報道如下。
1 資料與方法
1.1 一般資料
選取2019年4月至2020年6月在棗莊市婦幼保健院生殖醫學中心接受體外受精-胚胎移植(in vitro fertilization and embryo transfer,IVF-ET)、卵胞質內單精子顯微注射-胚胎移植(intracytoplasmic sperm injection and embryo transfer,ICSI-ET)治療的患者。本研究為回顧性研究,所有患者行輔助生殖助孕前均常規簽署相關知情同意書并獲得醫院醫學倫理委員會審查和同意。
納入標準:①促排卵方案為促性腺激素釋放激素激動劑(gonadotropin-releasing hormone agonist,GnRH-a)長方案;②促排卵藥物為金賽恒或普利康。
排除標準[2]:①重度腺肌癥、子宮畸形、子宮內膜異位癥、子宮肌瘤較大影響內膜者;②復發性流產者;③宮腔粘連或結核患者;④甲狀腺、腎上腺及其他內分泌疾病者;⑤男女一方或雙方染色體異常者。
分組:長方案促排卵過程隨機選擇使用藥物,根據促排卵過程中選用促性腺激素(gonadotropin,Gn)藥物不同分為兩組:A組176例(國產重組人促卵泡激素注射液:金賽恒,75 U/支,長春金賽藥業,中國);B組198例(進口重組促卵泡素β注射液:普利康,300 U/支或600 U/支,默沙東,美國)。
1.2 控制性超促排卵方案
本中心常用長方案為短效長方案,具體方法為:于前次月經周期的黃體中期B超檢測卵巢無囊腫開始皮下注射醋酸曲普瑞林(達必佳,0.1 mg/支,輝凌制藥,德國)0.1 mg連用7 d后,改為0.05 mg繼續使用7~11 d。降調14~18 d后晨起空腹抽血,內分泌激素測定采用貝克曼化學發光法檢測。當內分泌達到垂體降調的標準:血卵泡生成素(follicle-stimulating hormone,FSH)<5 mIU/ml、黃體生成素(luteinizing hormone,LH)<3 mIU/ml、雌二醇(estradiol,E2)<50 pg/ml時根據患者基礎情況的不同給予金賽恒注射液或普利康注射液(150~300) U/d促排卵直至扳機(human chorionic gonadotrophin,HCG)日。
B超提示至少1個優勢卵泡平均直徑≥18 mm或至少2~3個卵泡平均直徑≥16 mm時肌注注射用絨促性素(HCG,2000IU,珠海麗珠,中國)6000~10 000 IU,34~36 h后行陰道B超引導下穿刺取卵。取卵后常規體外受精/卵胞漿內單精子顯微注射、胚胎培養,新鮮周期評估患者的激素水平、內膜情況、胚胎情況等,若各方面均無明顯影響胚胎著床的因素存在時,選擇1~2枚優質胚胎移植,移植后常規黃體支持。剩余可用胚胎進行冷凍保存;若存在任何可能干擾成功妊娠的因素存在則選擇全胚冷凍(優質胚胎與囊胚)后再行凍融胚胎解凍復蘇移植。
移植后第14天,患者通過檢測血清人絨毛膜促性腺激素(human chorionic gonadotrophin,β-hCG)判斷是否懷孕,懷孕者于移植后35 d給予B超檢查,見到孕囊者為臨床妊娠。
1.3 胚胎質量標準的評判
Ⅰ級:胚胎形態完整,發育正常,卵裂細胞大小均勻,碎片<5%;Ⅱ級:發育稍遲緩,卵裂球細胞大小均勻,碎片5%~20%;Ⅲ級:發育遲緩1~2 d,卵裂球大小不均勻,碎片21%~50%;Ⅳ級:發育遲緩(2 d以上);碎片大于50%。Ⅰ級、Ⅱ級胚胎及3BC以上囊胚為本中心可移植的優質胚胎[3]。
1.4 統計學方法
采用SPSS 20.0統計學軟件進行數據分析。對各計量資料進行正態性分析,呈正態分布的計量資料以均數±標準差(x±s)表示,采用t檢驗;計數資料以[n(%)]表示,采用χ2檢驗,P<0.05為差異有統計學意義。
2 結果
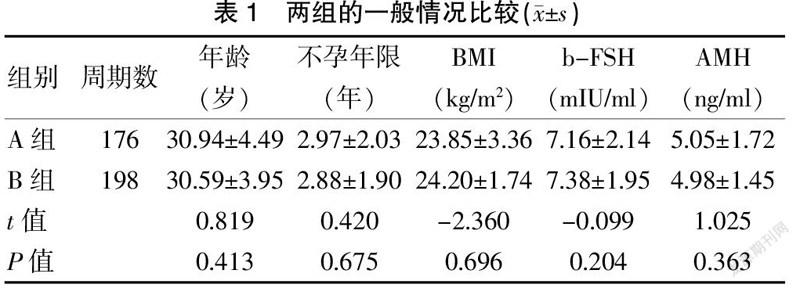
2.1 兩組的一般情況比較
兩組患者的平均年齡、平均不孕年限、體質量指數(body mass index,BMI)、抗苗勒試管激素(anti-mullerian hormone,AMH)值、基礎卵泡刺激素(b-FSH)值比較,差異均無統計學意義(P>0.05)。見表1。
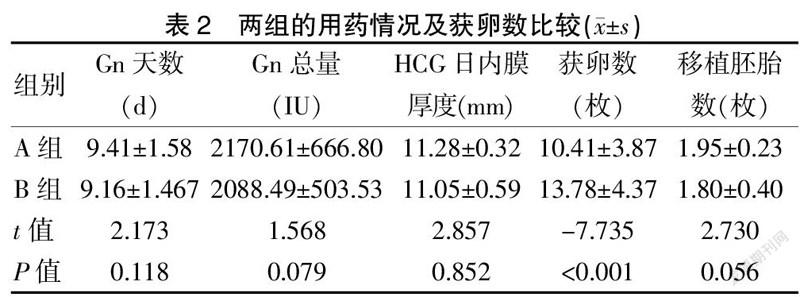
2.2 兩組的用藥情況及獲卵數比較
兩組患者的Gn天數、Gn總量、HCG日子宮內膜厚度、移植胚胎數比較,差異均無統計學意義(P>0.05)。B組患者獲卵數較A組患者多,差異有統計學意義(P<0.05)。見表2。3DC19304-5FFB-4E5C-862B-B3170A3FEE0A
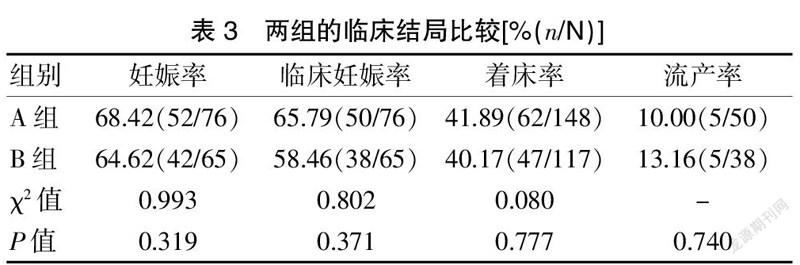
2.3 兩組的實驗室指標及臨床結局比較
兩組的各實驗室指標及最終臨床結局比較,差異均無統計學意義(P>0.05)。其中A組共有76例患者行移植術,89例患者行全胚冷凍,11例患者無可移植胚胎;B組共有65例患者行移植術,123例患者行全胚冷凍,10例患者無可移植胚胎。見表3~4。
3 討論
促性腺類激素(Gn)藥物自應用于不孕癥治療以來,其重要性不言而喻[4-8]。隨著輔助生殖技術的迅速發展,Gn藥物的種類,從最初的絕經期婦女的尿中提取的人絕經期Gn到現在臨床中廣泛應用的r-hFSH,未來也必將有更多、更新的Gn藥物投入到臨床應用中來。r-hFSH來源于哺乳動物細胞,無FSH人蛋白,無LH活性。有許多臨床試驗顯示r-hFSH較其他種類的Gn藥物能夠更有效促進多卵泡發育,累積妊娠率更高且更經濟[9-11]。目前臨床上常用的r-FSH有國產和進口兩大類。雖然產地、來源、制備工藝等諸多不同,但臨床應用目的一致:最少的花費、獲得合適數量的優質卵子以達到最好的妊娠結局。金賽恒是國內研制出的首個r-hFSH藥物,藥物說明其與進口r-hFSH具有相同的表達細胞和基因,因此具有一致的活性及分子結構均一性[12-14]。本研究回顧性分析臨床上最常用的長方案中使用國產r-hFSH金賽恒和進口r-hFSH普利康兩種促排卵藥,比較兩種藥物是否具有差異性。
本研究中,兩組患者的平均年齡、不孕年限、BMI、基礎FSH值、AMH值等比較,差異均無統計學意義(P>0.05),說明兩組患者的基礎條件、卵巢功能等大致相同,兩種藥物的臨床應用效果具有可比性。兩組患者的Gn天數、Gn總量、HCG日子宮內膜的厚度、受精率、可移植胚胎率、優質胚胎率、周期取消率、平均移植胚胎數、著床率、妊娠率、早期流產率等比較,差異均無統計學意義(P>0.05),說明國產r-hFSH與進口r-hFSH具有相似的藥物效能,在改善胚胎質量、提高臨床妊娠率等方面均具有較好療效,本研究結果與既往的臨床研究數據是一致的[4,15]。
GnRH-a長方案因其具有較高的臨床妊娠率,現在依然是大多數生殖中心的主流方案[16],但長方案由于降調時間長,垂體抑制深,卵巢對外源性卵泡刺激素的閾值窗窄,促排卵時容易多卵泡發育發生卵巢過度刺激綜合征(ovarian hyperstimulation syndrome,OHSS)。本研究兩組中均未出現中、重度卵巢過度刺激綜合征患者的原因是隨著拮抗劑方案的廣泛臨床應用[17-19],本中心多囊卵巢綜合征的患者、潛在卵巢高反應的患者在進周期時,筆者更傾向性選擇OHSS發生風險更低[20]、更為安全的拮抗劑方案[21],因此統計期間兩組均未出現中、重度卵巢過度刺激綜合征患者;B組患者平均獲卵數較A組患者多[(13.78±4.37)枚 vs.(10.41±3.87)],差異有統計學意義(P<0.05)。獲卵數偏高,說明此種藥物可能具有更高的卵泡募集效能。長方案超促排卵臨床應用重組卵泡刺激素β藥物時,臨床醫師需要評估患者的基礎狀態,更加謹慎地選擇Gn啟動劑量,根據卵泡發育個數和激素變化及時調整用量,以免升高OHSS發生風險;對于卵巢功能減退、低反應的患者,重組卵泡刺激素β較國產重組卵泡刺激素來說,可能更多地增加可用卵子的數量,但最終能否提高臨床妊娠率,需要進一步研究觀察。
綜上所述,根據本研究結果,兩種藥物的臨床治療均有較好的效果,生殖臨床醫生可根據治療方案,結合患者的基礎情況進行自由的用藥選擇。由于本文所述研究為本院生殖醫學中心的回顧性研究,樣本量小且患者存在地域集中性,與既往研究結果的不同之處可能與研究對象的地域差異性、各中心促排卵方法的不同有關。研究結果存在少量偏差,后期會繼續研究、觀察、隨訪,以期為患者臨床促排卵提供更為合理的指導。
[參考文獻]
[1]? ?Huime JA,Lambalk CB,van Loenen AC,et al.Contemporary pharmacological manipulation in assisted reproduction[J].Drugs,2004,64:297-322.
[2]? ?楊蕊,梁曉燕,朱依敏,等.國產重組人促卵泡激素在輔助生殖技術控制性超促排卵的臨床應用[J].中華生殖與避孕雜志,2021,41(2):113-119.
[3]? ?Veeck LL.An atlas of human gametes and conceptuses:An illustrated reference for assisted reproductive technology[M]. Parthenon Publishing Group,1999:46-51.
[4]? ?鄭波,戴芳芳.控制性促排卵中三種促性腺激素使用4天后血FSH值及助孕結局分析[J].生殖醫學雜志,2020, 29(1):33-37.
[5]? ?王天琪,孫振高.不同類型Gn對IVF患者獲卵及胚胎結局的初探[J].中國優生與遺傳雜志,2017,25(5):123-125.
[6]? ?劉雪竹,陳玉文.兩種促排卵藥物臨床應用比較研究[J].當代醫學,2020,26(6):26-27.
[7]? ?張若梅,張曉慶.三種促排卵藥物在體外受精-胚胎移植/卵胞質內單精子注射中對治療結局的影響[J].安徽醫藥,2020,24(9):1855-1858.
[8]? ?趙偉娥,梁曉燕.不同促性腺激素釋放激素類似物對垂體反應性的作用[J].生殖醫學雜志,2017,26(11):1067-1070.3DC19304-5FFB-4E5C-862B-B3170A3FEE0A
[9]? ?Daya S.Updated meta analysis of recombinant follicle stimulating hormone (FSH) versusurinary FSH for ovarian stimulation in assisted reproduction[J].Fertil Steril,2002, 77(4):711-714.
[10]? Barriere Paul,Porcu-Buisson Géraldine,Hamamah Samir.Cost-effectiveness analysis of the gonadotropin treatments HP-hMG and rFSH for assisted reproductive technology in France:A markov model analysis[J].Applied Health Economics and Health Policy,2018,16(1): 65-77.
[11]? 姚琳琳,王華莉,李璐.重組人促卵泡激素治療對多囊卵巢綜合征患者血清激素水平、排卵及妊娠的影響[J].內科,2020,15(3):285-288.
[12]? 郝鵬,金磊.rhFSH工程細胞株的篩選及表達條件的優化[D].長春:吉林大學,2008.
[13]? 陳寧,金磊.重組人促卵泡激素的質量研究[D].長春:吉林大學,2008.
[14]? 劉慧娟,裴瑾.重組人促卵泡激素的純化及鑒定[D].長春:吉林大學,2007.
[15]? 蘇艷華.基因重組卵泡刺激素對PCOS不孕患者促排卵治療的療效觀察[J].福建醫藥雜志,2008,30(2):27,37,47.
[16]? 聶玲,趙琰.早卵泡期長方案治療中促性腺激素時長對多囊卵巢綜合征患者體外受精-胚胎移植助孕治療結局的影響[J].中華生殖與避孕雜志,2018,38(4):274-278.
[17]? 沈秀珍,沈新光,王芳敏.促性腺激素釋放激素激動劑聯合小劑量人絨毛膜促性腺激素雙扳機在卵巢高反應患者拮抗劑促排卵周期中的應用效果[J].中國性科學,2021,30(6):84-87.
[18]? 彭露,劉玲,湯鮮,等.GnRH拮抗劑方案和GnRH激動劑長方案對IVF-ET/ICSI患者療效及安全性的影響[J].中國婦幼保健,2021,36(8):1805-1808.
[19]? 朱潔茹,歐建平,邢衛杰,等.GnRH激動劑長方案與GnRH拮抗劑方案在不同年齡組、不同反應人群中的新鮮周期臨床結局比較[J].中山大學學報(醫學科學版),2017,38(5):738-745.
[20]? 蔡文元,張學紅. 拮抗劑方案與改良超長方案在卵巢高反應人群中應用的比較[J].生殖醫學雜志,2020,28(2):134-139.
[21]? 劉博文,楊菁.拮抗劑方案和長方案促排卵對PCOS患者妊娠結局影響的meta分析[J].生殖醫學雜志,2020, 29(4):512-520.
(收稿日期:2021-09-09)3DC19304-5FFB-4E5C-862B-B3170A3FEE0A

