κ-卡拉膠/魔芋葡甘聚糖/羧甲基淀粉復合膜及空心膠囊制備
張陽,張慶,趙祎,鄧利玲,鐘耕*
1(西南大學 食品科學學院,重慶,400715)2(重慶市生物技術研究所有限責任公司,重慶,401121)
膠囊作為藥物中的常見劑型,方便服用且可提高藥物穩定性。當前,明膠膠囊已成為市面上應用最廣和加工技術最成熟的膠囊產品[1],明膠具有良好的成膜性,但該分子中含的各種活性基團容易與醛、多酚、還原糖和維生素C等交聯,影響膠囊的崩解和穩定性[2]。明膠主要通過牛、豬等動物皮骨中提取的骨膠、皮膠發酵得到,由于宗教信仰,動物源性明膠膠囊受素食主義者和伊斯蘭教等人群的抵制[3]。隨著養殖業濫用藥品的增加,以及激素的大量使用,動物產品的安全性越來越受到人們的質疑。國內“毒膠囊”事件的爆發影響和威脅著人們的健康,也讓明膠膠囊的研制及應用雪上加霜。因此,尋求質量可控、安全可靠且成本低廉的植物原料制備膠囊代替傳統的明膠膠囊具有重要意義。
羧甲基淀粉具有優良的成膜性和崩解性[4];魔芋葡甘聚糖(konjac glucomannan,KGM)是安全可食用的天然多糖,它具有優良的凝膠性、成膜性和生物可降解性,逐漸成為食品和藥品包裝中重要的包裝材料[5-6]。膠囊所需囊材的必要條件是能形成熱可逆凝膠,雖然羧甲基淀粉具有優良的成膜性和崩解性,但是不能形成熱可逆凝膠。因此將κ-卡拉膠與羧甲基淀粉共混,由于分子間的相互協同作用,可形成熱可逆凝膠,在此基礎上加入KGM,使混合后形成的凝膠效果更好,兼具KGM凝膠的高彈性和κ-卡拉凝膠的高強度。囊材的成膜性是其制備膠囊的重要依據,膜的制備工藝也相比膠囊制備工藝簡單,更易操作,且機械性和阻隔性等性能易于準確測定。因此,可以通過研究膜的性能來預判膠囊的性能,從而確定制備膠囊的配方和工藝條件,并減少膠囊在制備過程中出現問題的幾率。
目前已出現少量以變性淀粉或魔芋膠與卡拉膠混合制備膠囊的專利,但是,對不同原料復配等性能報道較少。在復配體系中,組分的比例影響其成膜性,以及各組分之間的相容性,進而影響膠囊的性質。因此,本試驗以κ-卡拉膠/KGM/羧甲基淀粉制備復合膜作為研究對象,研究了混合膠(κ-卡拉膠與KGM等質量混合)與羧甲基淀粉不同配比(質量比:10∶0、9∶1、8∶2、7∶3、6∶4、5∶5、4∶6與3∶7)對復合膜機械性能、阻隔性能和溶解性的影響;并用透光率、紅外光譜、X-射線衍射與掃描電鏡等評估復合膜的相容性,分析了各成分對膜特性的影響;最后基于復配體系成膜特性的基礎,確定2種配比,參照明膠膠囊生產工藝,以這2種配比制備植物基空心膠囊,并研究產品的溶出性與穩定性。研究結果有助于為新型植物膠囊的研制提供理論依據,為羧甲基淀粉、KGM的應用提供新的途徑。
1 材料與方法
1.1 實驗材料
羧甲基淀粉,參照張運芳[7]的方法,以玉米淀粉為原料實驗室自制,取代度為(0.677±0.012)%;魔芋葡甘聚糖(食品級),康家客食品有限公司;卡拉膠(食品級),上海北連生物科技有限公司;KCl,(食品級),河南強利化工產品有限公司;甘油(食品級),國藥集團化學試劑有限公司。西咪替丁,重慶科瑞制藥(集團)有限公司;明膠膠囊,市售。
1.2 儀器和設備
FA2004A型電子分析天平,上海橫平科學儀器有限公司;DHG-9070A型鼓風干燥箱,上海齊欣科學儀器有限公司;XLW(G)-PC智能電子拉力機、CHY-CA型薄膜厚度測量儀,濟南蘭光機電技術有限公司;HCJ-4C磁力攪拌水浴鍋,常州恩培儀器制造有限公司;Spectrum 100紅外光譜儀,美國Perkin Elmer公司;STA 449 F3同步熱分析儀,德國耐馳公司;D8 Advance型X射線衍射儀,德國布魯克公司;S-4800場發射掃描電子顯微鏡,日本日立公司;NDJ-5S 型旋轉黏度計,上海越平儀器有限公司。LB-881B六管崩解儀,無錫科達儀器廠;RCZ-6B型溶出儀,上海黃海藥檢儀器廠;MMI001千分尺,上海明寶工具有限公司。
1.3 實驗方法
1.3.1 不同配比復合膜制備
由于分子間的相互協同作用,κ-卡拉膠與KGM復配比例不同,復配體系性能不同,從而影響復合膜的性能。因此,本研究通過預實驗測定κ-卡拉膠/KGM成膜性、凝膠性,固定了κ-卡拉膠與KGM質量比為5∶5,配成混合膠。制備:混合膠在加入了0.1%的KCl(占總物質質量百分比,下同)、0.1%的甘油(占固體物質量百分比,下同)的去離子水中攪拌混勻,配成1%(質量百分比,下同)的溶液;羧甲基淀粉在加入了1‰的KCl、10%的甘油的去離子水中攪拌混勻,配成4%的溶液。前者溶脹30 min(80 ℃),并補充散失的水分,后者靜置1 h(25 ℃)。將混合膠與羧甲基淀粉在80 ℃下按不同的比例混合,配成質量比分別為10∶0、9∶1、8∶2、7∶3、6∶4、5∶5、4∶6、3∶7、2∶8和1∶9的膠液,充分攪拌均勻,離心脫氣后,倒入培養皿流延成膜,50 ℃干燥24 h,冷卻后揭膜,在室溫下相對濕度為43%的硝酸鎂飽和溶液環境中保存3 d以上。
1.3.2 復合膜性能的測定
1.3.2.1 厚度測定
在均勻待測膜的中心與邊緣區隨機取點,選取至少10個不同點用測厚儀測定,結果取平均值,單位以mm表示[8]。
1.3.2.2 機械性能測定
取完整、薄厚均勻的膜,裁剪大小為100.0 mm×15.0 mm(長×寬),使用智能電子拉力機進行測定。測試條件:上下探頭間距為(60.0±0.5) mm,拉伸速率50 mm/min,拉伸強度(tensile strength,TS)、斷裂伸長率(elongation at break,EAB)和楊氏模量(e-modulus,EM)按公式(1)~公式(3)計算[8-9]。
(1)
式中:F,最大斷裂應力,N;S,膜樣品橫截面積,mm2。
(2)
式中:L,試樣原始標線距離,mm;ΔL,試樣斷裂時標線距離-試樣原始標線距離,mm。
(3)
式中:EM,楊氏模量,應力與應變的比值,表示材料抵抗變形的能力,MPa;σ,應力,單位面積上所受到的力(F/A,其中A表示面積),MPa;ε:應變,在外力作用下的相對形變(相對伸長ΔL/L)。
1.3.2.3 水蒸氣透過率(water vapor permeability,WVP)測定
擬杯子法測定:稱取2.0 g無水CaCl2(0%相對濕度)于稱量瓶中,用待測膜將瓶口密封以做成透濕杯,稱重。然后將其置于底部放有飽和CaCl2溶液(75%相對濕度)的干燥器中,每隔24 h稱重,最后計算WVP[10],如公式(4)所示:
(4)
式中:m,透濕杯的增重,g;d,膜厚度,mm;A,試樣的透過面積,m2;t,時間變化,d;P,水蒸氣透過膜兩側的蒸汽壓差,kPa。
1.3.2.4 氧氣透過率測定
將15 g新鮮大豆油倒入錐形瓶,用薄厚均勻的待測膜密封瓶口,并在培養箱中陳化7 d,測定大豆油的過氧化值[11],用過氧化值的大小評價膜的阻氧性。
1.3.2.5 溶解率
將膜在相對濕度為0%的干燥器中貯存10 d后,選取完整、厚度均勻的膜,裁剪大小相近,質量約0.25 g,放入裝有100 mL蒸餾水的三角瓶中,37 ℃振蕩水浴10 min(50 r/min),抽濾分離膜未溶解部分,100 ℃烘干至恒重[11]。膜的溶解率按公式(5)計算:
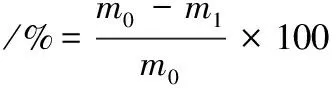
(5)
式中:m0,樣品溶解前質量,g;m1,樣品烘干后質量,g。
1.3.3 復合膜相容性研究
1.3.3.1 透光率分析
裁剪大小為5.0 cm×1.0 cm的膜,將其緊貼于比色皿一側,以空皿為對照,在400~800 nm下測定透光率。
1.3.3.2 紅外光譜分析
選取完整、厚度均勻的膜,將其在4 000~400 cm-1內掃描,記錄膜的紅外光譜圖。
1.3.3.3 X-射線衍射分析
選取完整、厚度均勻、大小一致的膜。實驗條件:X-射線源為Cu-Kα線,掃描角度 3~45°,掃描速度為4 °/min。
1.3.3.4 掃描電鏡分析
選擇完整、厚度均勻的膜,裁剪為2.5 mm×2.5 mm,固定在樣品臺上,在真空狀態下鍍金,觀察復合膜的表面,放大倍數為10 000倍。
1.3.4 復合膜熱重分析
樣品用量為5~10 mg,升溫速率為10 ℃/min,掃描范圍為室溫到500 ℃。
1.3.5 膠囊的制備工藝流程
本試驗依照膠囊傳統蘸膠法制備膠囊,工藝流程如下:
配料→溶膠→保溫→蘸膠→干燥→脫殼、切割→成品
工藝要點:選取復合膜性能良好的膠液配比,80 ℃混膠30 min,膠液脫氣,55 ℃保溫30 min。將膠囊模具豎直緩慢沒入膠液,4~8 s后勻速拔出,再連續翻轉數次,50 ℃干燥2~2.5 h。將干燥好的樣品取出冷卻回濕,用膠囊鉗拔下,再將囊坯截成規定的長度。
1.3.6 膠囊性能檢測
根據2015版《中國藥典》中對明膠膠囊的要求,對制備膠囊的松緊度、脆碎度、崩解時限、干燥失重與灼燒殘渣進行測定[12]。
1.3.7 膠囊溶出性能
選擇西咪替丁作為模型藥物,根據2015版《中國藥典》四部通則0931中溶出度測定第一法——藍法測定。
1.3.8 膠囊穩定性試驗
1.3.8.1 高溫下質量變化
稱取一定量的膠囊樣品,置于密封潔凈的廣口瓶中,60 ℃下保存,于第5天、第10天取樣,記錄其質量變化。
1.3.8.2 高溫下溶出度變化
將西咪替丁裝入準備好的膠囊中,高溫下放置,于第5天、第10天取樣,按1.3.7測其溶出性能,并以0 d測定結果作為對照[13]。
1.3.9 數據處理
采用Origin 9.1 作圖,SPSS 24.0對實驗數據進行分析處理。
2 結果與分析
2.1 不同配比復合膜的性能
2.2.1 不同配比復合膜的機械性能
由圖1可知,隨著羧甲基淀粉占比增加,復合膜的抗拉強度和楊氏模量逐漸增加,當混合膠與羧甲基淀粉質量比為7∶3時,抗拉強度最高,楊氏模量最大,隨后呈降低趨勢。由此說明,添加適量羧甲基淀粉可提高膜的拉伸性能。混合膠與羧甲基淀粉質量比從9∶1到4∶6,復合膜的抗拉強度一直強于κ-卡拉膠/KGM膜(即混合膠與羧甲基淀粉質量比為10∶0,下同)。說明在一定范圍內,這3種組分分子之間具有良好的相容性,羧甲基淀粉與二者充分混溶,使得κ-卡拉膠/KGM共混物的結構在一定程度上重新排列,產生了協同效應使得分子間的聯結更加致密[14];也可能是卡拉膠中具有強陰離子性的半硫酸酯基能與羧甲基淀粉中的Na+相互作用[15],從而提高了復合膜的抗拉強度。但隨著羧甲基淀粉用量繼續增加,抗拉強度和楊氏模量降低,是由于羧甲基淀粉分子之間的氫鍵作用要強于其與κ-卡拉膠及與KGM之間的氫鍵作用,在復配膜結構中表現微觀的相分離[16],從而導致了復配膜抗拉強度的下降,抵抗形變的能力降低。當混合膠與羧甲基淀粉質量比為9∶1、8∶2時,復合膜的斷裂伸長率受羧甲基淀粉含量影響較小,當混合膠與羧甲基淀粉質量比在8∶2之后,隨著羧甲基淀粉的增加,復合膜的斷裂伸長率緩慢下降,二者比例在6∶4后,下降趨勢明顯。一方面可能是由于加入的羧甲基淀粉分別與κ-卡拉膠、KGM 2種分子相互作用,各組分分子之間相互纏繞,網絡結構更加緊密,相互約束阻礙了聚合物鏈的活動[17];另一方面,羧甲基淀粉單獨成膜有硬而脆的特點,韌性低[18],因此較多的羧甲基淀粉會使復合膜的斷裂伸長率下降。

a-抗拉強度;b-斷裂伸長率;c-楊氏模量圖1 不同配比對復合膜機械性能的影響Fig.1 Effect of compound proportion on mechanical properties of blend films
2.2.2 不同配比復合膜的阻隔性能
水蒸氣透過率和氧氣透過率越低說明膜的阻隔性能越好。由圖2可知,隨著羧甲基淀粉用量的增加,復合膜的水蒸氣透過率和氧氣透過率先降低后升高,當混合膠與羧甲基淀粉質量比為7∶3時,二者降到最低值。此外,混合膠與羧甲基淀粉質量比從9∶1到2∶8,復合膜的阻隔性能一直優于κ-卡拉膠/KGM膜。由于羧甲基淀粉的加入,讓各組分分子之間的相互作用更強,結構更加緊密,且相互纏繞導致復合膜中孔隙變得更曲折,一定程度上會對水分子在膜中的擴散起到阻礙作用[19],從而降低水蒸氣透過率與氧氣的透過率。但是隨著羧甲基淀粉進一步增加,羧甲基淀粉分子之間的氫鍵作用要強于其與κ-卡拉膠及KGM之間的氫鍵作用,在復配膜結構中表現微觀的相分離[16],從而導致復配膜的水蒸氣透過率與氧氣透過率上升,這與上文復合膜的抗拉強度的解釋一致。

圖2 不同配比對復合膜阻隔性能的影響Fig.2 Effect of compound proportion on barrier properties of blend films
2.2.3 不同配比復合膜的溶解度
崩解性表示膠囊在溶液中溶解快慢的程度,是膠囊性能中的關鍵指標。膜的溶解度又與膠囊的崩解性能正相關。因此,可通過測定復合膜的溶解度間接反映膠囊崩解性能。由圖3可知,隨著羧甲基淀粉用量的增加,復合膜溶解度逐漸增加,原因是卡拉膠一般在溫度為70 ℃以上時才能充分溶解[20],室溫下不易溶于冷水[21],而羧甲基淀粉的水溶性好,當復合膜中羧甲基淀粉占比增加,卡拉膠占比減少,復合膜的溶解性就呈上升趨勢。當混合膠與羧甲基淀粉質量在7∶3以后,復合膜溶解性表現較好,如6∶4溶解度87.76%,5∶5溶解度89.22%。此外,在試驗中發現,復合膜不是直接溶于水中,而是在水中先溶脹后變軟,網絡結構被破壞后再發生溶解。
綜合考慮機械性能、阻隔性能和溶解性,選取混合膠與羧甲基淀粉質量比為6∶4和5∶5進行膠囊制備研究。

圖3 不同配比對復合膜溶解度的影響Fig.3 Effect of compound proportion on the solubility of blend films
2.2.4 復合膜相容性研究
2.2.4.1 透光率分析
材料在可見光區的高透明性對于其應用非常重要,通常用透光率來評價復合材料的相容性,若復合材料組分之間有良好的相容性,則透光率較高;反之,當光透過膜時,會出現光的散射或反射,透光率較低[22]。由圖4可知,κ-卡拉膠/KGM膜透光率在76%左右,顯示出較高的透明性,一方面是因為κ-卡拉膠和KGM本身具有很高的透明度,另一方面與其膜內部分子之間強的相互作用有關,從而透光率較高。隨著羧甲基淀粉用量的增加,復合膜的透光率逐漸降低,但混合膠與羧甲基淀粉質量比從9∶1到4∶6降低程度較小,3∶7與2∶8透光率降低程度較大,這主要與羧甲基淀粉本身的透光率有關[23]。由前期試驗測得羧甲基淀粉溶液透光率為37.4%,當羧甲基淀粉比例增加時,復合膜的透光率下降。但9∶1到2∶8復合膜的透光率仍遠高于羧甲基淀粉溶液的透光率,說明復合膜各組分之間有較好的相容性。

圖4 不同配比對復合膜透光率的影響Fig.4 Effect of compound proportion on the transparency of blend films
2.2.4.2 紅外光譜分析



圖5 不同配比復合膜紅外光譜圖Fig.5 FTIR patterns of blend films with compound proportion
2.2.4.3 X-射線衍射分析
X-射線衍射可以用來表示膜的相容性,研究分子間的相互作用。若復合膜中各組分之間有較強的相互作用,衍射譜圖則將表現為某些聚合物組分的特征衍射峰消失[27-28]。由圖6可知,所有復合膜都無強衍射峰,不存在結晶區,是典型的無定型結構[29]。10∶0復合膜在15°附近有一個衍射峰,20°左右有一個較寬的衍射峰。當羧甲基淀粉加入到復合膜后,隨著用量增加,復合膜在15°處的衍射峰強度逐漸減弱甚至消失,是因為羧甲基淀粉與κ-卡拉膠、KGM間存在較強的相互作用,從而打破了κ-卡拉膠/KGM膜原有的穩定結構,對其結構性能產生影響,與宋彥志等[30]、劉穎[31]的結果一致,進一步說明羧甲基淀粉添加后復合膜各組分間呈現出良好的相容性[32-33]。

圖6 不同配比復合膜X-射線衍射圖譜Fig.6 X-ray patterns of blend films with compound proportion
2.2.4.4 掃描電鏡分析
由圖7可知,在相同的放大倍數(10 000倍)下,10∶0膜表面的微觀結構明顯粗糙,膜表面有一些塊狀突起。隨著羧甲基淀粉比例的增加,復合膜表面更加光滑均勻且平整,沒有裂隙和小孔,所有的復合膜樣品均未出現相分離現象,說明κ-卡拉膠、KGM與羧甲基淀粉三者之間存在較強的相互作用,使得膜的結構變得緊密,三者有良好的相容性[34],這與紅外光譜、X-射線衍射等試驗結果一致。

a-10∶0;b-9∶1;c-7∶3;d-5∶5;e-3∶7圖7 不同配比復合膜的掃描電鏡圖Fig.7 SEM images of blend films with compound proportion
2.2.5 熱重分析
由圖8可知,復合膜熱失重過程分為2個階段:第1階段在50~120 ℃,由復合膜內的水分隨溫度升高蒸發所致,對應的微商熱重(differential thermos gravimetry,DTG)曲線表現一個小峰[35],第2階段在250~400 ℃,熱重(thermos gravimetry , TG)曲線急劇下滑,在該階段內復合膜發生失重量顯著,主要是復合膜各組分的熱降解反應,相應的DTG曲線則出現一個大峰[36]。由TG、DTG曲線可得到相應的熱分解數據,其中10∶0膜的初始失重溫度和最大失重速率溫度分別為251.3和274.4 ℃,600 ℃時的殘炭為32.3%;與10∶0復合膜相比,加入羧甲基淀粉后的復合膜的初始失重溫度與最大失重速率溫度均得到了提高,例如:9∶1復合膜的初始失重溫度和最大失重速率溫度分別為253.6、277.1 ℃,在600 ℃時的殘炭為32.39%;7∶3復合膜分別是258.6、279.3 ℃,在600 ℃時的殘炭為32.99%;5∶5復合膜分別為266.4、281.8 ℃,在600 ℃時的殘炭為33.60%。這種總體趨勢向高溫方向移動的現象說明羧甲基淀粉的加入使復合膜的熱穩定性提高,且κ-卡拉膠、KGM與羧甲基淀粉三者之間存在氫鍵相互作用[22]。

a-TG;b-DTG圖8 不同配比復合膜的TG曲線和DTG曲線Fig.8 TG and DTG curves of blend films with compound proportion
2.2.6 膠囊性能檢測
混合膠與羧甲基淀粉質量比為6∶4和5∶5時,復合膜綜合性能良好,因此選擇它們作為膠囊制備的研究,制備出6∶4膠囊、5∶5膠囊,同時制備未加入羧甲基淀粉的膠囊(10∶0膠囊),并購買明膠膠囊與兩者對比性能差異。
2.2.6.1 外觀、氣味及尺寸檢測
自制膠囊圖片見圖9,膠囊外觀光潔、色澤均勻無軟癟變形和黑點,符合藥典標準。自制2種膠囊的尺寸、氣味等性能指標見表1,自制膠囊在氣味、尺寸方面符合藥典標準。

a-6∶4膠囊;b-5∶5膠囊圖9 膠囊圖片Fig.9 Picture of capsule

表1 膠囊尺寸和氣味Table 1 Size and smell of capsule
2.2.6.2 性能指標檢測
(1)松緊度試驗結果均無漏粉現象,符合藥典標準。
(2)脆碎度試驗結果無膠囊破裂,符合藥典標準。
(3)崩解時限試驗中,6∶4與5∶5膠囊符合藥典標準,而未加羧甲基淀粉的10∶0膠囊,遠高于標準,說明羧甲基淀粉在膠囊崩解性能中起著關鍵作用,羧甲基淀粉占比越高,膠囊崩解時限越短。
(4)干燥失重試驗結果符合藥典標準。
(5)灼燒殘渣試驗結果符合藥典標準。
具體見表2。
2.2.7 溶出性能
由圖10可知,西咪替丁藥物溶出時間在2~10 min,明膠膠囊的溶出性能高于6∶4與5∶5膠囊。因為明膠膠囊在3 min之內快速溶脹,并開始崩解,6 min時,快速崩解,藥物從膠囊中快速溶出;而自制膠囊在2~6 min時,處于溶脹階段,未出現明顯崩解,當溶出時間超過6 min后,膠囊開始崩解,藥物從膠囊中快速溶出。自制膠囊在2~6 min時溶出慢的原因可能是KGM、κ-卡拉膠的加入增強了膜的網絡結構,從而降低了膠囊的溶解性能。此外,自制膠囊在溶解時容易在藥物表面形成一層黏稠狀的液體,部分藥物被包裹在里面,不能及時釋放出來,從而也降低了藥物的溶出。但是當溶出時間為15 min時,6∶4膠囊、5∶5膠囊和明膠膠囊中西咪替丁的累積溶出百分率分別達到了87.70%、89.45%和93.62%,完全符合藥典的規定(在20 min時,西咪替丁累積溶出百分率達到75%及以上)。此外,5∶5膠囊溶出性能優于6∶4膠囊,說明羧甲基淀粉有利于增強膠囊的溶出性能。當溶出時間超過20 min時,3種膠囊的累積溶出百分率幾乎相同,都達到95%以上。

表2 膠囊性能指標檢測Table 2 Properties test of capsule
2.2.8 穩定性試驗
2.2.8.1 高溫下質量變化
由表3可知,所有膠囊在高溫下(60 ℃)質量略有下降,且自制膠囊比明膠膠囊失重少,失重都在5%之內,說明這些膠囊在高溫下穩定[20]。

圖10 西咪替丁膠囊溶出曲線Fig.10 The dissolution curve of cimetidine capsules

表3 膠囊在高溫下失重結果Table 3 Results of capsule in high temperature
2.2.8.2 高溫下溶出度變化
由圖11可知,對于自制6∶4、5∶5膠囊,在高溫條件下放置時間越長,藥物溶出時間越短,但不影響藥物的最終溶出量,說明高溫對自制膠囊的影響不大。而明膠膠囊隨著高溫時間延長,藥物的溶出量減少,從而導致最終溶出量降低,這可能與明膠膠囊在高溫下容易發黏有關。由此可得自制膠囊的高溫穩定性優于明膠膠囊。

a-6∶4膠囊;b-5∶5膠囊;c-明膠膠囊圖11 西咪替丁膠囊在高溫下的溶出曲線Fig.11 The dissolution curve of cimetidine capsules in high temperature
3 結論
本試驗采用流延法制備可降解的κ-卡拉膠/KGM/羧甲基淀粉復合膜,測定了不同配比復合膜的機械性能、阻隔性能和溶解性。用紅外光譜、X-射線衍射、掃描電鏡等儀器研究復合膜的相容性,并分析了復合膜熱穩定性。根據明膠硬膠囊的生產工藝,制備空心膠囊。主要結論如下:
(1)對不同配比的復合膜的性能研究發現,添加適量的羧甲基淀粉可以改善復合膜的機械性能和阻隔性能,提高溶解度,當混合膠與羧甲基淀粉質量比為6∶4和5∶5時,復合膜綜合性能良好。
(2)透光率、紅外光譜、X-射線衍射結果表明,κ-卡拉膠/KGM/羧甲基淀粉復合膜的組分間存在氫鍵相互作用,微觀形貌結果表明復合膜具有均勻、致密的結構,熱重分析表明加入羧甲基淀粉可以提高復合膜的熱穩定性。綜上,在復合膜中κ-卡拉膠、KGM與羧甲基淀粉三者之間通過氫鍵相互作用,使復合膜表現出良好的相容性,適合作為膠囊囊材。
(3)根據中國藥典的規定,對自制6∶4,5∶5膠囊進行了性能檢測,自制2種膠囊成品的外觀光滑,無味,松緊度、脆碎度、崩解時限、干燥失重及灼燒殘渣均符合藥典標準,以10∶0膠囊作對比,可得羧甲基淀粉在膠囊崩解性能中起關鍵作用,羧甲基淀粉比例越高,膠囊崩解時限越短。
(4)以明膠膠囊作對比,西咪替丁作為模型藥物,當溶出時間到達15 min時,6∶4膠囊、5∶5膠囊中西咪替丁的累積溶出百分率分別達到了87.70%、89.45%,完全符合國家藥典標準。自制膠囊高溫穩定性優于明膠膠囊,在高溫后藥物溶出時間提前,并不影響最終溶出量。

