典型聚乙烯、聚丙烯、聚苯乙烯廢塑料共熱解初期反應特性的ReaxFF分子模擬研究
賀興處 ,陳德珍
(同濟大學 熱能與環境工程研究所,上海多源固廢協同處理和能源化工程技術研究中心,上海 200092)
城市生活垃圾中含有六種常見的塑料組分,包括高密度聚乙烯(HDPE)、低密度聚乙烯(LDPE)、聚丙烯(PP)、聚苯乙烯(PS)、聚氯乙烯(PVC)和聚對苯二甲酸乙二醇酯(PET)[1],其中,典型塑料組分PE/PP/PS是生產液態烴的原料。隨著近年來城市生活垃圾的分類實施,塑料垃圾有條件單獨收運或者廢塑料可以容易地從干垃圾中分離獲得。廢塑料的回收利用方法主要分為物理和化學回收,由于物理回收技術的局限性,實際只有聚對苯二甲酸乙二醇酯(PET)和聚乙烯(PE)實現了物理回收和再循環,而且當塑料混合物的組成非常復雜時,再生塑料的使用性能會受到影響。化學回收是通過熱解或化學分解等技術將廢塑料中的有機成分轉化成小分子烴等石油化工原料[2]。熱解作為一種廢塑料的化學回收技術,不僅可以解決廢棄塑料對環境的污染,同時還可生產出具有極高經濟價值的燃料油和其他化工原料[3],實現塑料垃圾的減量化、無害化和資源化利用,并且混合廢塑料的熱解是回收石化工業原料的一種經濟有效的方法[4],并得到了廣泛的關注。表1為PE/PP/PS的主要來源以及溫度對熱解產品分布的影響,可見低溫熱解主要以較大分子石蠟等產品為主,隨著溫度升高,產生更多的輕質油和氣體小分子產品。
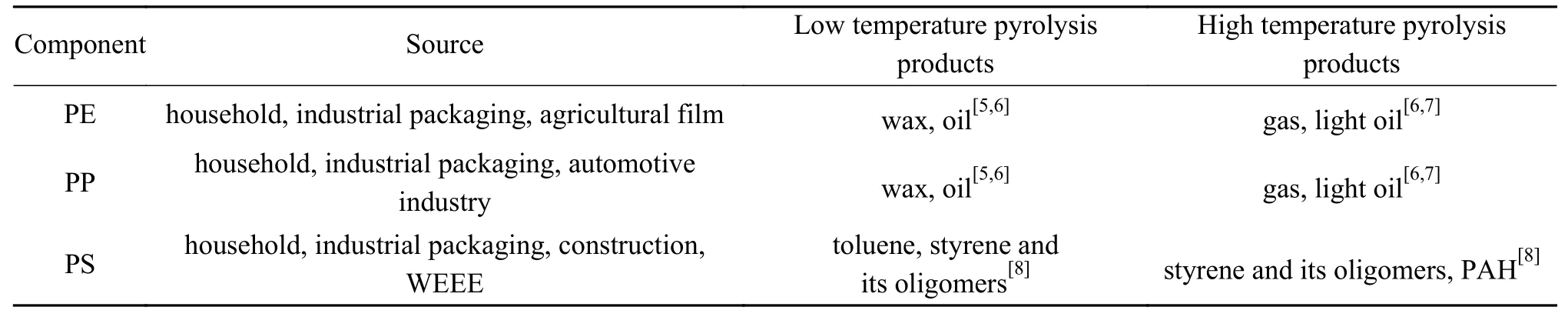
表 1 廢塑料典型組分主要來源及其熱解產品分布Table 1 Main sources of typical plastics and their pyrolysis products at low and high temperatures
Predel等[9]采用流化床反應器進行PE/PP/PS混合廢塑料在510 ℃下的熱解實驗,通過Py-GC/MS等方法進行熱解產物分析,結果表明,有價值的產物主要是從聚烯烴中得到的脂肪族蠟,同時也探究了不同混合比例在熱解過程中的相互作用。Williams等[1]對混合塑料進行700 ℃下固定床熱解研究,發現PE和PP熱解所獲得的油產品主要由烷烴、烯烴和烷二烯等脂肪族有機物組成,PS熱解的油產品具有更多的芳香族成分,同時發現與PS混合的塑料比單一塑料熱解具有更高的產氣率和更低的產油率。Jin等[10]考慮到塑料的高黏度和低導熱性,選用降膜熱解反應器對PE/PP/PS在650 ℃下的快速共熱解過程進行了研究,分析了三種組分在不同比例下的熱解油氣產率和熱解產物組成,詳細探討了共熱解特性。
近年來,隨著反應分子動力學(Reactive Force Field Molecular Dynamics, ReaxFF MD)的迅速發展,基于原子層面的廢塑料熱解機理的研究也越來越深刻。ReaxFF MD是由 Van Duin 和Goddard共同發展的、將反應力場(ReaxFF)和分子動力學(MD)相結合、以描述復雜體系中分子鍵的斷裂和生成的模擬算方法方法[11]。ReaxFF MD 已被廣泛用于聚烯烴等的熱分解過程的反應機理研究[12-14]。Liu等[12]將ReaxFF MD 應用于 HDPE 模型體系研究,通過分析模擬軌跡獲取了PE熱解的詳細反應機理和氣體分子生成途徑,證明了應用 ReaxFF MD有助于建立對聚合物熱解系統原子層面的機理理解。賀興處等[14]采用ReaxFF MD 從原子層面詳細揭示了CaO和H2O對PE熱解過程的影響,揭示了CaO對碳鏈斷裂的作用機理和H2O對產品品質的影響途徑。但是目前關于ReaxFF MD探究PE/PP/PS混合熱解機理的相關研究報道極少,而在實際工程中一般都是混合塑料共熱解,要獲得理想產品,研究其共熱解機理非常重要。
鑒于PE/PP/PS在塑料垃圾中占比50%-70%的事實,本研究以PE/PP/PS為研究對象進行混合廢塑料共熱解機理研究,采用ReaxFF MD模擬手段,借助一款反應分子動力學模擬結果自動分析與可視化軟件AutoRMA(automatic reaction mechanism analyzer)[15]探究原子層面共熱解行為。AutoRMA基于LAMMPS[16]進行ReaxFF MD計算輸出的鍵級文件和軌跡文件自動探測詳細分子信息和化學反應信息,并以可視化的方式呈現分析結果。在用活化能驗證模擬過程正確的基礎上、分析不同混合比例和溫度下熱解產物分布,以了解混合塑料共熱解與單一塑料熱解的區別、及不同混合比例對熱解產物的影響,便于產物的調節。
1 模擬方法
1.1 模型構建
模擬中首先使用Materials Studio(MS)[17]建立PE、PP、PS單鏈模型,然后利用Amorphous Cell模塊構建周期性模擬盒子,體系密度設置為1.0 g/cm3,不同模擬體系添加分子的種類和數量如表2所示,其相對分子質量比例保持與Jin等[10]實驗研究相同,綜合考慮計算耗時與模擬精度,總原子數量控制在8000-10000。而后利用MS的Forcite模塊對構建的模擬盒子進行幾何構型優化和退火計算。
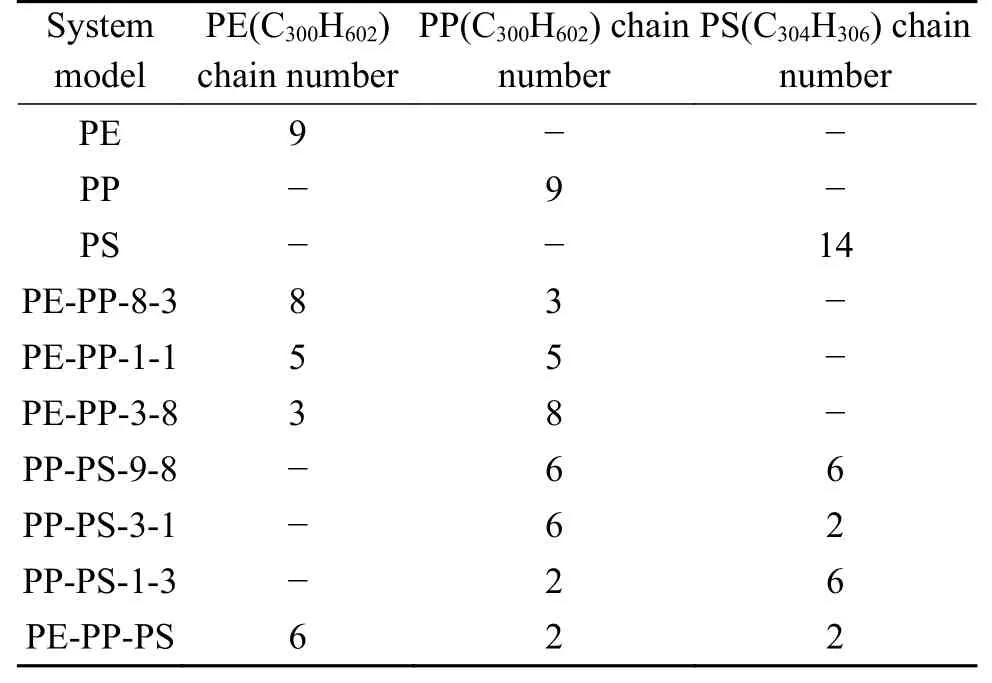
表 2 模擬體系分子構成Table 2 Molecular composition of simulation system
PE-PP-PS模擬盒子共有8436個原子(C3008H5428),圖1為其在MS中進行幾何優化和退火后計算后的構象。
1.2 模擬方法
利用LAMMPS的REAX包進行ReaxFF MD計算,所用力場參數[18]已用于聚合物的熱解模擬[12,14,19]。當模擬體系較大時,ReaxFF MD極其耗時,已有研究[12,20-22]證明,在ReaxFF MD模擬中提高反應溫度僅影響反應速率,對反應機制幾乎無影響,因此,可以通過提高模擬溫度以縮短反應所需的時間而不降低模擬精度[2]。因此,本研究進行了2400、2600、2800和3000 K一系列恒溫模擬以研究共熱解特性。所有計算采用NVT系綜和周期性邊界條件,時間步長為0.25 fs,cutoff為0.25。
2 結果與討論
根據已有研究[23,24],熱解產物按照碳原子數可分為炭(C41+)、油(C5-40)和可燃氣(C0-4),油產物又可分為輕油(C5-13)和重油(C14-40)。由于各體系總原子數量不一致,因此,不同熱解體系中可燃氣分子的絕對數量缺乏對比性,因此,本文定義NR(Number ratio)為各氣體分子數量與主要氣體分子總數量的比值來進行對比,即:
2.1 共熱解動力學分析
固相分解的單步動力學方程如式(2)所示,式(3)為反應速率的Arrhenius表達式,通過積分轉換,可以將反應動力學函數f(α)表示為積分形式G(α), 進而在不同溫度T下測定速率常數k(Ti),根據式(5)獲得速率常數k(Ti)的Arrhenius圖可以估計出活化能Ea和指前因子A。
式中,α為固體轉化率,本研究中α的上限為0.9。R為理想氣體常數。
由于廢塑料熱解反應主要包括碳鏈的斷裂和重組以及自由基的解離和加成,C–C鍵(包括芳香鍵、單鍵、雙鍵及三鍵)和C–H鍵的斷裂對熱解反應起著決定性作用,因此,可嘗試C–C鍵和C–H鍵解離的動力學參數來表征整個熱解體系的動力學參數。C–C鍵和C–H鍵斷裂的反應速率常數k可通過式(6)求出[16,25]:
式中,N0為初始狀態(t= 0)鍵數量,Nt為平衡狀態(t=tequilibrium)鍵數量。進而利用Arrhenius方程式可求得活化能Ea和指前因子A。
整個體系活化能可通過體系中C–C鍵和C–H鍵的活化能加權求和進行計算,即為Bonds方法,在體系剛開始熱解過程沒有H–H鍵變化,因此,不進行H–H鍵相關計算。
采用RTP(reduced time plots)方法對體系在2400、2600、2800和3000 K下進行熱解計算結果進行分析,可獲得廢塑料熱解過程的動力學參數。圖2為2400-3000 K下PE-PP-PS體系等溫熱解過程C–C鍵和C–H鍵的數量變化及動力學計算,其中,TG、Bonds和Char Bonds分別表示按照固體轉換率α在0.9之前的失重速率、根據體系中炭油氣三項產物中總化學鍵斷裂速率和只根據體系炭產物中化學鍵斷裂速率進行統計計算。
圖2(c)為在不同溫度下體系熱解250 ps過程中的失重變化,隨著熱解過程進行,失重率迅速增大并趨于平衡,另外隨著溫度的升高,體系在熱解后期會出現失重率降低的情況,這是由于在熱解模擬計算過程中沒有實時去除揮發分產生結焦現象,導致部分揮發分重新結合形成焦炭。如圖2所示,隨著溫度升高,C–C鍵和C–H鍵的斷裂速率逐漸增大。在相同溫度下,Bonds(統計整個體系中的化學鍵)方法比Char Bonds(只統計炭產物中的化學鍵)方法計算具有更大的鍵斷裂速率,說明在熱解初期炭裂解為小分子的同時,該小分子會進一步裂解為更小分子,并且由于C–C鍵和C–H鍵的數量隨時間具有一致的變化趨勢,因此,小分子形成的主要方式是碳鏈的斷裂和C–H生成H自由基和H2。根據圖2中C–C鍵及C–H鍵數量變化可以發現,C–C鍵和C–H鍵斷裂速率在16 ps之前較16 ps之后更大,形成較為明顯的兩個變化趨勢,尤其是2800和3000 K溫度條件下;另外,在16 ps左右,2800和3000 K下體系中C–C鍵和C–H鍵數量變化均達到一個3 ps左右的短暫平衡態,此時熱解體系中C–C鍵和C–H鍵數量第一次趨于穩定, 稱之為第一次達到平衡狀態。由于模擬過程在高溫下進行,之后產物的二次反應大量發生,所以此穩定狀態非常短暫。由于本文研究目的是探討PE/PP/PS共熱解初期的相互作用機理,暫不考慮二次反應,因為二次反應與所處的反應條件有關,不適用于分析不同廢塑料共熱解的相互作用機制與動力學參數;為確保二次反應沒有大量發生,并保證反應率α不大于0.9,選擇C–C鍵和C–H鍵斷裂速率一致的反應區域進行計算[26],可獲得更能揭示PE/PP/PS共熱解本質的動力學參數而不受二次反應的干擾,因此,選擇tequilibrium=16 ps作為計算時間以保證所有計算溫度下反應率α從開始到該時間的一致性。下一步再采用類似文獻[27]的研究方法進行二次裂解和炭產品相關分析。采用Char Bonds方法計算結果如圖2(f)所示,其與文獻[10]實驗結果基本一致,并且Bonds方法較TG方法更接近實驗值,因此,熱解過程C–C鍵和C–H鍵解離的動力學參數可以準確表征整個體系的動力學參數,故其余體系采用化學鍵數量變化方法進行動力學參數計算。
圖3為不同溫度下PE/PP/PS單獨熱解及以典型混合比共熱解過程C–C鍵和C–H鍵的數量變化,其中,Char-Bonds-C-C和Char-Bonds-C-H是基于Char Bonds方法統計的C–C鍵和C–H鍵的數量變化,Bonds-C-C和Bonds-C-H是基于Bonds方法統計的C–C鍵和C–H鍵的數量變化。可見,隨著溫度升高,整個體系的C–C鍵和C–H鍵數量迅速降低,碳鏈的解離速度明顯加快。在相同溫度下,C–C鍵的減少程度大于C–H鍵,這是由于在熱解初期,碳鏈斷裂主導整個過程,·H自由基的脫離稍晚于碳鏈的斷裂,炭產物中C–C鍵和C–H鍵的變化趨勢一致也表明,·H自由基尚未大量脫離。
PE/PP/PS典型混合比例體系共熱解的動力學參數計算結果如表3所示,其中,實驗值來自Jin等[10]對廢塑料典型組分在降膜熱解反應器中的共熱解特性試驗研究,模擬時間取體系第一次達到平衡狀態的時間16 ps,可見活化能的模擬值與實驗值的誤差僅為 ± 3.86%。
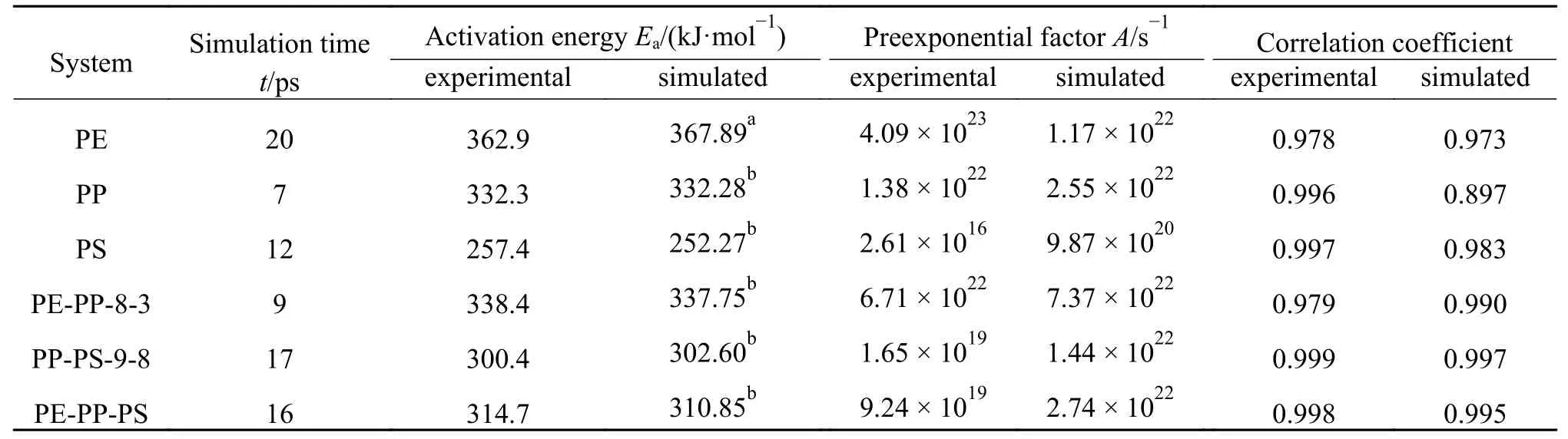
表 3 PE/PP/PS廢塑料單獨熱解及共熱解過程動力學參數Table 3 Pyrolysis kinetic parameters of PE, PP, PS and mixtures of PE-PP, PP-PS and PE-PP-PS
由表3可以看出,除PE體系外,采用Char Bonds方法可以得到與實驗相符的活化能,而采用Char Bonds方法計算純PE體系熱解20 ps得到的活化能是532.63 kJ/mol,明顯大于實際熱解活化能,這是由于PE沒有支鏈結構,在熱解初期長鏈斷裂的同時,熱解產生的中間產物的分解對整個反應有較大影響,因此,采用Bonds方法進行計算更符合實際熱解過程。
2.2 共熱解特性分析
2.2.1 PE/PP共熱解特性
圖4為3000 K下PE/PP混合熱解過程三相產物的產率變化,所有體系在20-40 ps均達到90%以上的轉化率,混合熱解的轉化率在PE和PP單獨熱解平均轉化率之間,產物油和氣的質量比分別在60%和40%左右,與Williams等[1]和Jin等[10]實驗結果相符。由于PP具有支鏈結構,PP熱解開始時間較PE早,但其構成單體丙烯C3H6分子碳原子數大于PE構成單體乙烯C2H4分子,因此,在初始階段PP的固體轉換率變化低于PE。所有體系在20 ps左右,焦油產量達到最大,一次裂解基本完成,之后隨著二次反應的進行,焦油分子進一步分裂,產生更多的氣體分子。
在一次裂解主導階段,隨著PP摻量的增加,轉換速率逐漸變緩,過多的PP摻量會導致期間焦油產量減少,而增加產物炭比率。但在二次反應開始后,隨著PP比例的增加,體系中焦油產率逐漸增加,而氣體產率逐漸減少,這也主要是由于構成單體碳原子數的影響。因此,以油為目標產物的熱解中,增加PP/PE中PP的比例可以提高熱解油的產率,而增加PP/PE中PE的比例可以提高不凝氣體的產率。但在較短停留時間工況下,需要根據焦油性質確定合適的PP摻量。
圖5為不同比例PE/PP在3000 K混合熱解80 ps后油品中重油和輕油的相對比率,油產品中輕質油組分比例大于重油組分,少量PP的加入不影響油的組分,但隨著PP摻量的增加,重油組分逐漸增多,而輕油組分減少。因此,以輕質油為產品的廢塑料熱解,PP摻量需要進行適當控制。
圖6為不同比例PE/PP在3000 K下混合熱解80 ps的主要氣體分布,隨著PP摻量的增加,H2和CH4產量呈上升趨勢,這是由于PP具有支鏈結構,在熱解過程更易脫落形成·CH3和·H自由基,形成類似PE無支鏈結構,因此,造成C2H4相對含量的下降和C2H6相對含量的相對平穩。
2.2.2 PP/PS共熱解特性
與PE/PP共熱解類似,如圖7所示,PP/PS共熱解油產率隨熱解時間的延長均呈現先上升后隨著二次裂解發生出現下降趨勢,并且摻有PS的體系中,由于PS熱解過程推遲,熱解到80 ps尚未達到完全平衡。在40-60 ps之后,體系熱解炭的產率開始上升,這是因為在熱解過程中,沒有將揮發分分離,產生了結焦現象。由于本研究主要分析熱解油和氣產品,因此,取第一次平衡態60 ps的模擬結果進行產物分析即可,不影響分析結果。隨著體系中PS摻量的增加,熱解產品中炭和油的產率升高,而氣體產率降低。
圖8為不同比例PP/PS在3000 K下混合熱解60 ps后油品中重油和輕油的相對比率,由于PS單體為苯乙烯C8H8,分子量較大,因此,PS參與的混合熱解體系更傾向于產生更多的油,而且油產物中重油組分的比例也較高。隨著PS摻量增加,油產物中重油組分逐漸增多,輕油組分產率逐漸減少,但在PP∶PS比例達到1∶1后其比率變化較小。
圖9為不同比例PP/PS在3000 K下共熱解80 ps后的主要氣體分布,隨著PS相摻量增加,H2含量呈上升趨勢,這是由于混合熱解中PS會大量產生·H自由基,而CH4呈下降趨勢。另外適量的PS可以促進PP裂解為其單體C3H6,但是過量會呈現抑制作用。
2.2.3 PE/PP/PS共熱解特性
分別取PE-PP-PS混合體系在不同溫度下第一次達到平衡狀態時的計算結果研究溫度對熱解的影響,2400、2600、2800和3000 K下的等溫模擬第一次達到平衡狀態的時間分別為250、120、95和45 ps,圖10為不同溫度下PE-PP-PS體系熱解主要產物的產率及固體轉化率,不同溫度下轉化率均能達到93%以上,溫度為2400-2600 K,轉化率迅速升高了4.78%,但是隨著溫度繼續升高,轉化率開始降低,這是由于在混合熱解過程中發生了結焦。高溫有利于重油裂解為輕油,隨著溫度的升高,重油和輕油的相對含量發生明顯變化,輕油的相對含量從2400 K的44.77%升高到3000 K的56.18%。圖11為PE-PP-PS體系在2400-3000 K不同溫度下熱解產品氣主要組分,隨著溫度升高,H2和CH4的產率逐漸上升,但C2H4和C3H6的產率先上升后降低,這是由于高溫會促使烴類小分子進一步裂解生成相對更小分子產物,但如前所述,過高的溫度會造成結焦而不是進一步裂解,因此,促進聚合物大量分解為其單體結構需要選擇適當的溫度。
2.3 共熱解機理分析
表4為PE/PP/PS混合模擬體系在典型比例、3000 K下化學反應進程追蹤結果,兩條反應進程分別表示碳鏈的斷裂和塑料單體及小分子的生成時間順序,其中,R–CH3表示不包含CH4的氣體小分子。
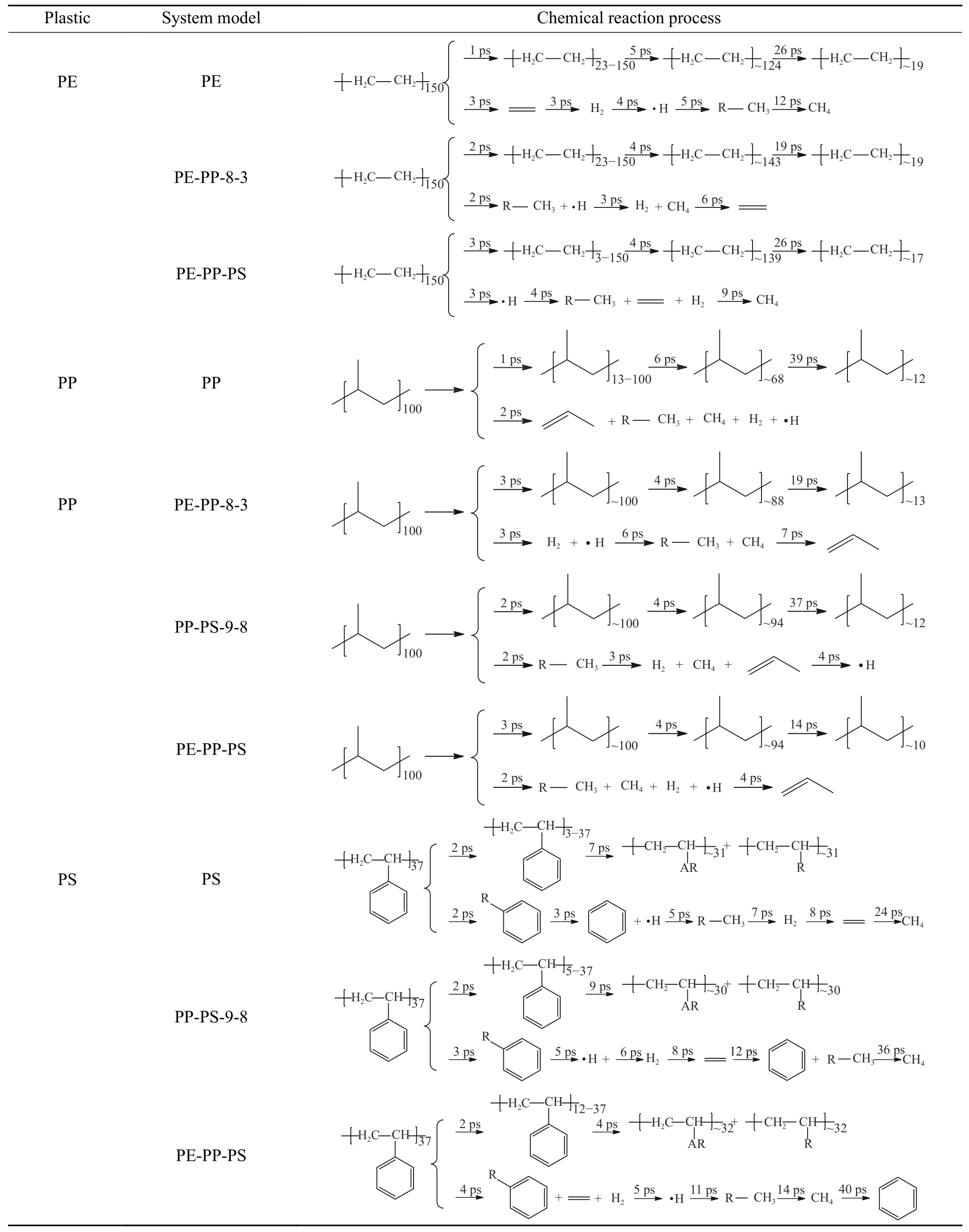
表 4 3000 K下PE/PP/PS在等溫混合熱解化學反應進程Table 4 Chemical reaction process during isothermal co-pyrolysis of PE/PP/PS at 3000 K
碳鏈斷裂順序三個時間節點分別表示開始反應時間、碳鏈全部參與反應時間和轉換率達到95%的反應時間,由于PS熱解過程會產生結焦現象,無法達到95%以上的轉換率,因此,只有前兩個時間節點。如表4所示,相比單一塑料熱解,共熱解初始反應時間延遲,但總體反應時間縮短,說明不同塑料之前具有相互促進作用,能夠加快反應速率,這與Li等[28]報道一致。并且產物更傾向于為較小分子,共熱解加劇了反應物之間的相互作用。PE和PP單獨熱解時,首先生成其構成單體分子,繼而生成烷烴和小分子氣體,但混合熱解過程呈現相反趨勢:首先生成烷烴和小分子氣體,而后生成其單體。PS熱解首先產生苯乙烯和苯,繼而生成小分子氣體,但在混合熱解體系中,苯的產生時間明顯延遲,這是由于苯乙烯較穩定,而且PE和PP產生的含碳自由基傾向于和·H自由基結合,因此,PS在熱解過程中更傾向于提供·H自由基,從而減弱了苯環和乙烯基之間碳碳鍵的斷裂,如圖9在PP/PS混合體系中,隨著PS摻量的增加,乙烯的產量不增甚至有微弱下降,也是因此原因。
PE/PP/PS混合熱解反應在2-4 ps開始產生H2和·H自由基,因此,表3中活化能的計算若只根據C–C鍵斷裂速率進行計算會導致結果偏低,加權C–C鍵和C–H鍵活化能更符合實際熱解過程,可以獲得更準確的動力學參數。
3 結 論
本研究利用ReaxFF進行了廢塑料典型組分PE/PP/PS共熱解特性研究,利用AutoRMA進行產物演變分析,從動力學、熱解產物及熱解過程三方面揭示了原子層面的共熱解特性。研究結論如下:
PE/PP/PS共熱解的動力學參數可通過C–C鍵和C–H鍵斷裂的活化能加權求和獲得,與實驗數據接近。
增加PP-PE體系中PP的含量可以提高油和可燃氣的產率,增加PP-PS體系中PS的含量可以提高炭和油產率。
在PE-PP-PS體系中,高溫利于重油裂解為輕油,同時高溫也會促使烴類小分子進一步裂解生成更小分子,隨熱解溫度升高,H2和CH4的產率明顯上升,但C2H4和C3H6的產率先上升后降低。相比單獨熱解,混合熱解開始反應時間有所延遲,但達到第一次平衡的總反應時間縮短,并且更傾向于生成較小分子產物。
PE和PP單獨熱解時,首先生成其單體,繼而生成烷烴和小分子氣體,但兩者共熱解過程中首先生成烷烴和小分子氣體,而后生成其單體;另外在共熱解中PS更傾向于提供·H自由基從而與PE和PP生成的自由基結合,形成小分子烷烴或H2。
上述研究結果為混合廢塑料共熱解產物的控制奠定基礎。

