X射線調(diào)強(qiáng)放療與電子線放療對(duì)早期乳腺癌保乳術(shù)后血清腫瘤標(biāo)志物和T細(xì)胞亞群的影響*
梁巧媚, 鄭報(bào), 張曉葳, 陳磊
(安徽醫(yī)科大學(xué)附屬阜陽(yáng)醫(yī)院 腫瘤放療科, 安徽 阜陽(yáng) 236000)
乳腺癌的患病率約為10%,多見于育齡期女性,可嚴(yán)重影響患者的生活質(zhì)量[1]。保乳術(shù)及術(shù)后放療是早期乳腺癌的有效治療方式之一,可有效清除微小病灶,降低腫瘤的復(fù)發(fā)及轉(zhuǎn)移,提高患者生存率[2-3],目前臨床對(duì)放療的瘤床補(bǔ)量方式存有爭(zhēng)議。電子線放療及X射線調(diào)強(qiáng)放療都是臨床常見瘤床補(bǔ)量方式,電子線放療方案照射劑量分布不均勻、多集中于心臟及患側(cè),而X射線調(diào)強(qiáng)放療靶區(qū)劑量分布均勻[4-5]。有研究報(bào)道電子線及X射線調(diào)強(qiáng)放療在乳腺癌局部腫瘤控制率的效果相當(dāng),但臨床關(guān)于2種瘤床補(bǔ)量方式在乳腺癌患者術(shù)后血清腫瘤標(biāo)志物、T細(xì)胞亞群及副反應(yīng)上存在一定差異[6-7]。基于此,本研究探討X射線調(diào)強(qiáng)放療與電子線放療對(duì)乳腺癌術(shù)后血清腫瘤標(biāo)志物、T細(xì)胞亞群及副反應(yīng)的影響,為改善乳腺癌預(yù)后提供參考,報(bào)告如下。
1 資料和方法
1.1 一般資料
選取2018年9月—2021年1月在本院進(jìn)行X射線調(diào)強(qiáng)放療的早期乳腺癌術(shù)后患者48例為觀察組,另按照年齡、手術(shù)方式為配伍原則,收集同期行電子線放療的早期乳腺癌術(shù)后患者42例為對(duì)照組。入選標(biāo)準(zhǔn):(1)符合《中國(guó)抗癌協(xié)會(huì)乳腺癌診治指南與規(guī)范》[8]、且經(jīng)病理學(xué)確診者;(2)均為女性單側(cè)乳腺癌、且接受乳腺癌保乳術(shù)治療者;(3)臨床分期Ⅰ~Ⅱ期;(4)患者或家屬均知情同意者。排除標(biāo)準(zhǔn):(1)重要臟器功能不全者;(2)存在精神障礙;(3)有其他惡性腫瘤病史;(4)有免疫系統(tǒng)疾病;(5)有血液系統(tǒng)疾病者。觀察組中,年齡38~52歲,平均(42.05±5.12)歲;體質(zhì)量指數(shù)(BMI)19~28 kg/m2,平均(23.54±2.18)kg/m2。對(duì)照組中,年齡36~54歲,平均(41.26±4.76)歲;BMI 19~28 kg/m2,平均(23.36±2.52)kg/m2。本研究獲醫(yī)院醫(yī)學(xué)倫理委員會(huì)批準(zhǔn),批準(zhǔn)文號(hào)為2019(17)。
1.2 方法
兩組患者均行乳腺癌保乳術(shù)治療,完整切除腫瘤后,放療前均行表阿霉素或紫杉醇為主的化療方案。保乳術(shù)后1個(gè)月內(nèi)對(duì)患者進(jìn)行全乳照射50 Gy/25次,若患者出現(xiàn)腋窩淋巴結(jié)轉(zhuǎn)移,進(jìn)行同側(cè)鎖骨上下淋巴引流區(qū)照射,放療劑量(DT)=50 Gy/25次。對(duì)照組瘤床補(bǔ)量行電子線放療:以手術(shù)切口向外延伸20 mm為瘤床靶區(qū),并確保90%劑量線在胸壁上;同時(shí)設(shè)置固定的源皮距照射,在皮膚表面垂直照射8~10 MeV電子線,劑量為10~16 Gy/5~8次。觀察組瘤床行X射線調(diào)強(qiáng)放療:將CT圖像術(shù)中標(biāo)記、手術(shù)瘢痕及術(shù)后勾畫的改變區(qū)設(shè)為瘤床靶區(qū),以瘤床區(qū)域向外延伸3 mm,后界不超過(guò)胸肌前緣為計(jì)劃靶區(qū),處方劑量為10~16Gy/5~8次。
1.3 觀察指標(biāo)
1.3.1照射劑量 (1)瘤床靶區(qū),95%、105%、110%以上的相應(yīng)處方劑量射線照射瘤床體積百分比V95%、V105%、V110%;(2)心臟、患側(cè)肺照射劑量。
1.3.2腫瘤標(biāo)志物 于放療前、放療后1個(gè)月、3個(gè)月時(shí)抽取患者靜脈血3 mL, 3 000 r/min離心10 min,分離血清檢測(cè)癌胚抗原(CEA,采用放射免疫法)及糖類抗原15-3(CA153,采用化學(xué)發(fā)光法)。
1.3.3T細(xì)胞亞群 于放療前、放療后1個(gè)月、3個(gè)月采用SC流式細(xì)胞儀(美國(guó),貝克曼)測(cè)定患者的CD3+、CD4+、CD4+/CD8+值。
1.3.4副反應(yīng) 放療期間觀察患者惡心嘔吐、口腔黏膜炎、放射性皮膚損傷、放射性食管炎、放射性肺炎、心臟毒性、血液毒性等。毒副反應(yīng)以WHO不良反應(yīng)分級(jí)為標(biāo)準(zhǔn)[9]:0級(jí),未出現(xiàn)不良反應(yīng);Ⅰ級(jí),不良反應(yīng)為輕度;Ⅱ級(jí),不良反應(yīng)為中度;Ⅲ級(jí),不良反應(yīng)為重度;Ⅳ級(jí),嚴(yán)重不良反應(yīng)。
1.4 統(tǒng)計(jì)學(xué)處理
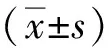
2 結(jié)果
2.1 一般資料
兩組患者一般資料比較差異無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05)。見表1。

表1 兩組乳腺癌患者一般資料比較Tab.1 Comparison of general data of breast cancer patients between two groups
2.2 照射劑量
兩組患者靶區(qū)V95%比較,差異無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05);但觀察組靶區(qū)V105%、V110%量、心臟及患側(cè)肺照射劑量均低于對(duì)照組(P<0.05)。見表2。

表2 兩組乳腺癌患者術(shù)后瘤床補(bǔ)量照射劑量比較Tab.2 Comparison of postoperative tumor bed supplemental radiation doses between two groups
2.3 腫瘤標(biāo)志物水平
結(jié)果顯示,放療前兩組患者CEA及CA153水平比較,差異無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05);放療后,兩組CEA及CA153水平均隨放療時(shí)間延長(zhǎng)而降低,但觀察組均低于對(duì)照組(P<0.05)。見表3。
2.4 T細(xì)胞亞群
結(jié)果顯示,放療前兩組患者CD3+、CD4+及CD4+/CD8+比較,差異無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05);放療后,兩組患者CD3+、CD4+及CD4+/CD8+均隨放療時(shí)間延長(zhǎng)而降低,但觀察組均高于對(duì)照組(P<0.05)。見表4。

表4 兩組乳腺癌手術(shù)患者放療前后T細(xì)胞亞群比較Tab.4 Comparison of T cell subsets before and after radiotherapy between two groups
2.5 副反應(yīng)
兩組乳腺癌手術(shù)后患者瘤床放療補(bǔ)量治療后,惡心嘔吐、口腔黏膜炎、放射性皮膚損傷、放射性食管炎、放射性肺炎及心臟毒性等毒副反應(yīng)多集中發(fā)生在Ⅰ~Ⅱ級(jí)患者中,且兩組患者毒副反應(yīng)比較,差異無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05)。見表5。
3 討論
近年來(lái)乳腺癌的發(fā)病率不斷提升,乳房疼痛、乳腺腫塊、乳頭溢液是其常見癥狀,若未及時(shí)進(jìn)行治療可嚴(yán)重影響患者的生活質(zhì)量及健康[10]。保乳術(shù)后放療加瘤床補(bǔ)量方案對(duì)乳腺癌的治療效果已得到臨床證實(shí),其可有效殺死殘留病灶,降低術(shù)后復(fù)發(fā)及轉(zhuǎn)移率,提高患者預(yù)后[11]。臨床資料顯示,瘤床靶區(qū)劑量的均勻分布是瘤床補(bǔ)量的關(guān)鍵,其可進(jìn)一步提高乳腺癌患者的腫瘤控制率[12-13]。電子線瘤床補(bǔ)量雖對(duì)乳腺癌患者的治療效果確切,但由于乳腺組織厚度不均、表面呈曲線形變化,瘤床位于乳房邊緣時(shí)可影響電子線照射劑量的不均勻分布,可能對(duì)靶區(qū)正常組織、患側(cè)肺及心臟造成損傷[14-15];X射線調(diào)強(qiáng)放療屬于精確放療技術(shù),其劑量分布均勻且穿透性強(qiáng),對(duì)位置較深、形狀不規(guī)則的瘤床靶區(qū)補(bǔ)量治療有效[16]。本研究中,觀察組靶區(qū)V105%、V110%量、心臟及患側(cè)肺照射劑量均顯著低于對(duì)照組,提示X射線調(diào)強(qiáng)放療靶區(qū)劑量均勻性分布優(yōu)于電子線放療,且其對(duì)正常組織的照射劑量少,降低了放射過(guò)程中正常組織的損傷。

表5 兩組乳腺癌手術(shù)患者瘤床補(bǔ)量治療后副反應(yīng)比較[n(%)]Tab.5 Comparison of side effects after tumor bed supplementation therapy between two groups[n(%)]
血清腫瘤標(biāo)志物水平與乳腺癌疾病的發(fā)展密切相關(guān)[17]。CEA為糖蛋白,主要存在于腫瘤細(xì)胞表面,研究指出,乳腺癌患者CEA水平較高,可參與淋巴及血液循環(huán),且黏附能力強(qiáng)[18]。CA153是乳腺癌特異性標(biāo)志物,其不僅可減低細(xì)胞黏附性,促使癌細(xì)胞脫落轉(zhuǎn)移,且其含量變化與乳腺癌治療效果密切相關(guān)[19]。本研究中,放療前兩組患者CEA、CA153水平均較高、放療后均降低,但觀察組低于對(duì)照組,提示X射線調(diào)強(qiáng)放療對(duì)癌細(xì)胞的殺滅作用更明顯,可降低CEA的分泌,可用于乳腺癌預(yù)后狀況的監(jiān)測(cè)。
減少對(duì)瘤床靶區(qū)正常組織及心臟的照射劑量,以降低患者正常組織放射性損傷是保乳術(shù)后放療的重要目的[20-21]。放療對(duì)機(jī)體的負(fù)向損傷作用雖不可避免,但如何降低放療造成的放射性損傷仍是臨床研究的重點(diǎn)[22]。本研究中的兩組乳腺癌手術(shù)患者放療補(bǔ)量治療后血液CD3+、CD4+及CD4+/CD8+均隨放療時(shí)間延長(zhǎng)而降低,提示放療的免疫抑制效果顯著高于腫瘤消失對(duì)機(jī)體免疫抑制的解除效果,且觀察組患者的CD3+、CD4+及CD4+/CD8+高于對(duì)照組,提示X線調(diào)強(qiáng)放療對(duì)患者免疫功能的影響較電子線電放療小,分析原因可能與X線調(diào)強(qiáng)放療瘤床靶區(qū)劑量的均勻分布及正常組織放射性損傷少有關(guān)。
放療過(guò)程中會(huì)不可避免的對(duì)機(jī)體造成負(fù)向損傷,兩組乳腺癌手術(shù)患者放療補(bǔ)量治療后惡心嘔吐、口腔黏膜炎、放射性皮膚損傷、放射性食管炎、放射性肺炎及心臟毒性等毒副反應(yīng)多集中發(fā)生在Ⅰ~Ⅱ級(jí)的乳腺癌患者中,該結(jié)果與國(guó)內(nèi)外較多報(bào)道相符[23-25],提示X線調(diào)強(qiáng)放療與電子線放療對(duì)乳腺癌患者的毒副作用均較小,這可能與放療技術(shù)的相對(duì)成熟及放療中不良反應(yīng)的預(yù)防有關(guān)。
 貴州醫(yī)科大學(xué)學(xué)報(bào)2022年2期
貴州醫(yī)科大學(xué)學(xué)報(bào)2022年2期
- 貴州醫(yī)科大學(xué)學(xué)報(bào)的其它文章
- 進(jìn)展期胃癌手術(shù)患者術(shù)前兩種化療方案對(duì)治療效果的影響*
- 胸部CT對(duì)慢性阻塞性肺疾病合并肺動(dòng)脈高壓的分級(jí)診斷價(jià)值*
- 2016—2020年《貴州醫(yī)科大學(xué)學(xué)報(bào)》期刊影響力及論文作者特征的相關(guān)因素*
- TrkB抑制劑對(duì)前列腺癌細(xì)胞生物學(xué)效應(yīng)及VEGF表達(dá)的影響*
- Caspase12和Caspase3在內(nèi)質(zhì)網(wǎng)應(yīng)激介導(dǎo)的HCC細(xì)胞凋亡中的作用*
- 綠茶有效組分固定劑量聯(lián)合對(duì)牙周炎大鼠的治療效果*
