深層熱療聯合化療治療結直腸癌肝轉移療效觀察*
陳春橋,陸玉松,潘 旻,唐桂艷,黃明月,夏 燕,黃 輝
(桂林市人民醫院腫瘤放療科,廣西 桂林 541002)
直腸癌發生率在中國惡性腫瘤中排名第三,死亡率在世界惡性腫瘤中排名第二[1]。據統計,在診斷時15%~25%的結直腸癌患者已處于晚期[2],即使接受手術治療仍有大約50%的可能性發展為復發和轉移性結直腸癌。據統計顯示,大約25%的結腸癌患者有肝轉移,超過60%的患者有異時性肝轉移[3]。這種疾病的治療通常采用手術切除和術后化療,但患者預后并不好,80%~90%的結直腸癌肝轉移患者在初診時就錯過了手術治療的機會。因此,尋找合適的治療方法是改善此類患者預后的關鍵。目前,化療與靶向療法相結合已延長了轉移性結直腸癌患者的生存期,但其客觀反映率太低,無進展生存期尚未得到延長[4]。近年來,熱療逐漸發展成為結直腸癌綜合治療的重要手段。有研究表明,除自身良好的抗腫瘤作用外,熱療還可提高化療的療效[5]。目前,很少有關于熱療聯合化療在結直腸癌肝轉移患者中的應用研究。本研究觀察了射頻深層熱療聯合化療治療結直腸癌肝轉移的療效和不良反應,現報道如下。
1 資料與方法
1.1資料
1.1.1一般資料 選取2018年1月至2020年3月本院的結直腸癌肝轉移患者60例,分為研究組和對照組,每組30例。2組患者性別、年齡、病理類型、體力狀況(PS)評分、腫瘤分化程度、腹腔積液情況、腫瘤大小等一般資料比較,差異均無統計學意義(P>0.05)。見表1。本研究已通過本院醫學倫理學委員會審核批準。
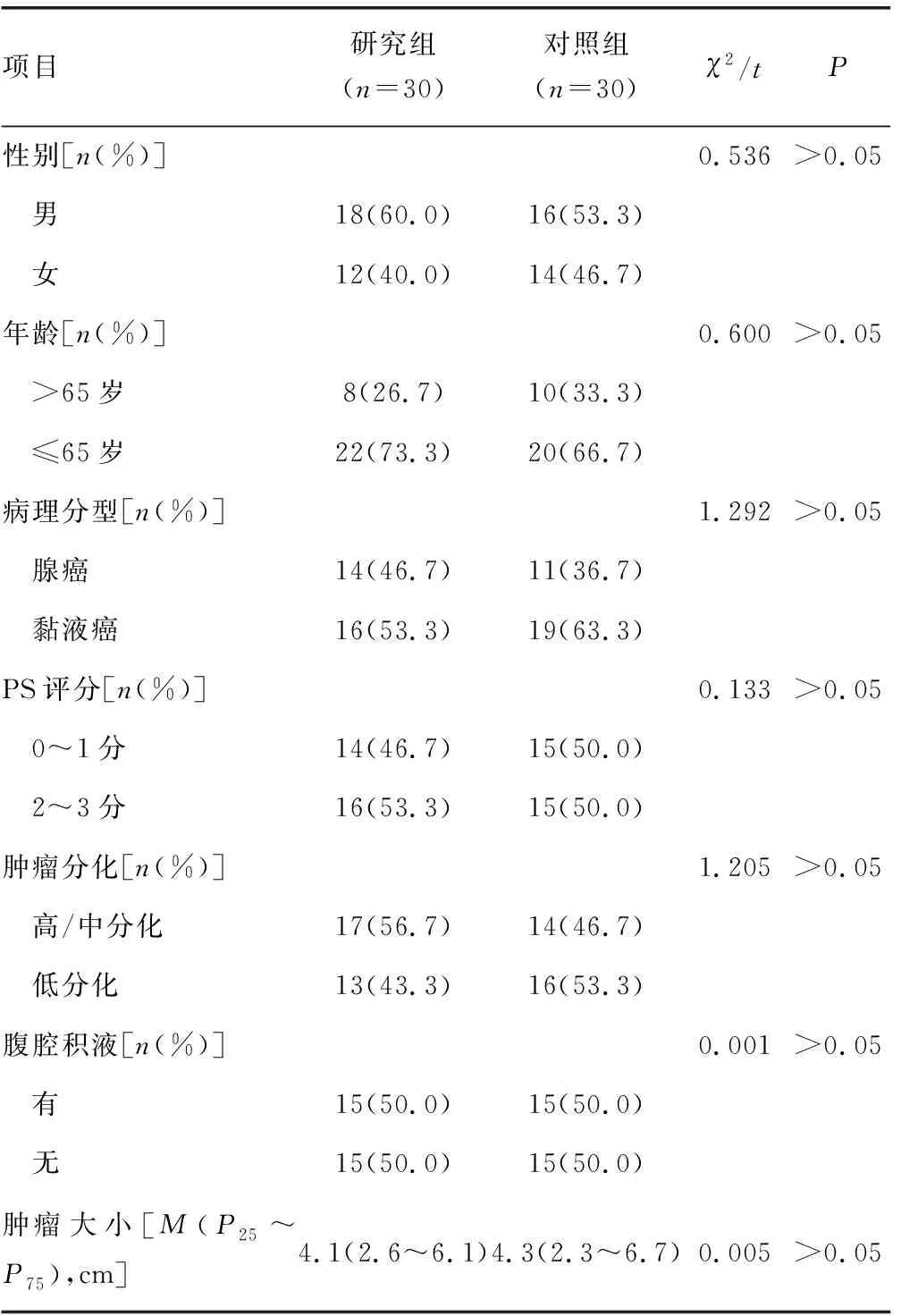
表1 2組患者一般資料比較
1.1.2納入標準 (1)經組織病理學檢查診斷為結直腸癌并有肝轉移;(2)通過相關影像學檢查為T3-4N0M0或任何T、N+M1(Ⅱ/Ⅲ期);(3)無化療、熱療禁忌證;(4)預計生存時間大于6個月;(5)無腸梗阻,可以進食;(6)告知本研究目的與風險后簽署知情同意書。
1.1.3排除標準 (1)年齡大于75歲;(2)體內有金屬植入物;(3)嚴重肝、腎、心功能不全;(4)嚴重感染;(5)有出血傾向;(6)溫度調節和(或)感知干擾障礙。
1.1.4退出標準 (1)出現嚴重藥物不良反應需減少或更換藥物;(2)由于各種原因未按要求完成治療過程,在治療中途放棄或失訪者;(3)因患者要求而非醫療原因而終止治療者。
1.2方法
1.2.1治療方案
1.2.1.1對照組 僅采用奧沙利鉑聯合卡培他濱方案化療:靜脈輸注奧沙利鉑130 mg/m2,第1天;口服卡培他濱850~1 000 mg/m2,每天2次,第1~14天;1個化療周期持續3周,完成8個化療周期。
1.2.1.2研究組 在采用奧沙利鉑聯合卡培他濱方案化療基礎上進行深層腫瘤熱療。化療方法與對照組相同。熱療方法:采用吉林邁達NRL-002內源性腫瘤熱療儀,向患者及家屬說明禁忌證和適應證,簽署熱療同意書。熱療的執行時間為放療的第1天,第二時間間隔72 h,依此類推。治療區域主要在骨盆(CT模擬器位于熱療中心),設定電壓為170~180 V,電流為570~580 mA,治療時間設定為60 min,預設溫度為41.5~42.5 ℃(直腸溫度),使用Ⅰ號主機(左右電極板)和Ⅱ號主機(前后電極板)加熱肝臟腫瘤,用0.45%鹽水袋隔離防止皮膚灼傷并在5 min后達到預設溫度進行治療。深層熱療治療時間在化療第1、4、8、12天,實施4次為1個周期。
1.2.2療效判定標準 根據國際實體瘤療效反映評價標準[6]判定療效:(1)完全緩解(CR)為所有靶病變消失;(2)部分緩解(PR)為基線病變長度減少30%及以上;(3)病變進展(PD)為病變長徑基線總和增加20%及以上或出現新的病變;(4)病變穩定(SD)為病變長徑基線總和減少但未達到PR或增加但未達到PD。總有效率=(CR例數+PR例數)/總例數×100%。
1.2.3觀察指標
1.2.3.1肝轉移情況 2組患者完成3個周期化療后進行上腹部磁共振、增強檢查以評估肝轉移情況。
1.2.3.2不良反應 定期檢查2組患者血常規和肝、腎功能。根據WHO抗癌藥物不良反應0~Ⅳ度標準[7]對治療期間發生的不良反應進行分級。分為血液學和非血液學毒性。
1.2.3.3生活質量 根據美國東部合作腫瘤小組建立的PS評分標準評估2組患者治療后生活質量改善情況[8]。
1.2.4隨訪 觀察2組患者治療后短期療效,隨訪至2020年8月31日,共隨訪0~26個月,中位11個月。2組患者中均為失訪者。
2 結 果
2.12組患者臨床療效比較 研究組患者總有效率明顯高于對照組,差異有統計學意義(P<0.05)。見表2。
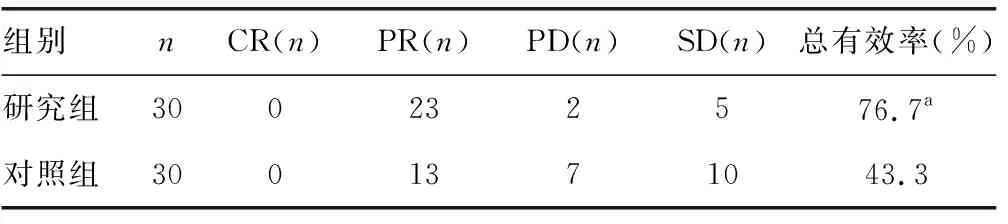
表2 2組患者臨床療效比較
2.22組患者肝轉移情況比較 研究組患者治療后肝轉移均明顯萎縮,一些病變甚至轉變為接近正常組織,明顯優于對照組。見圖1。
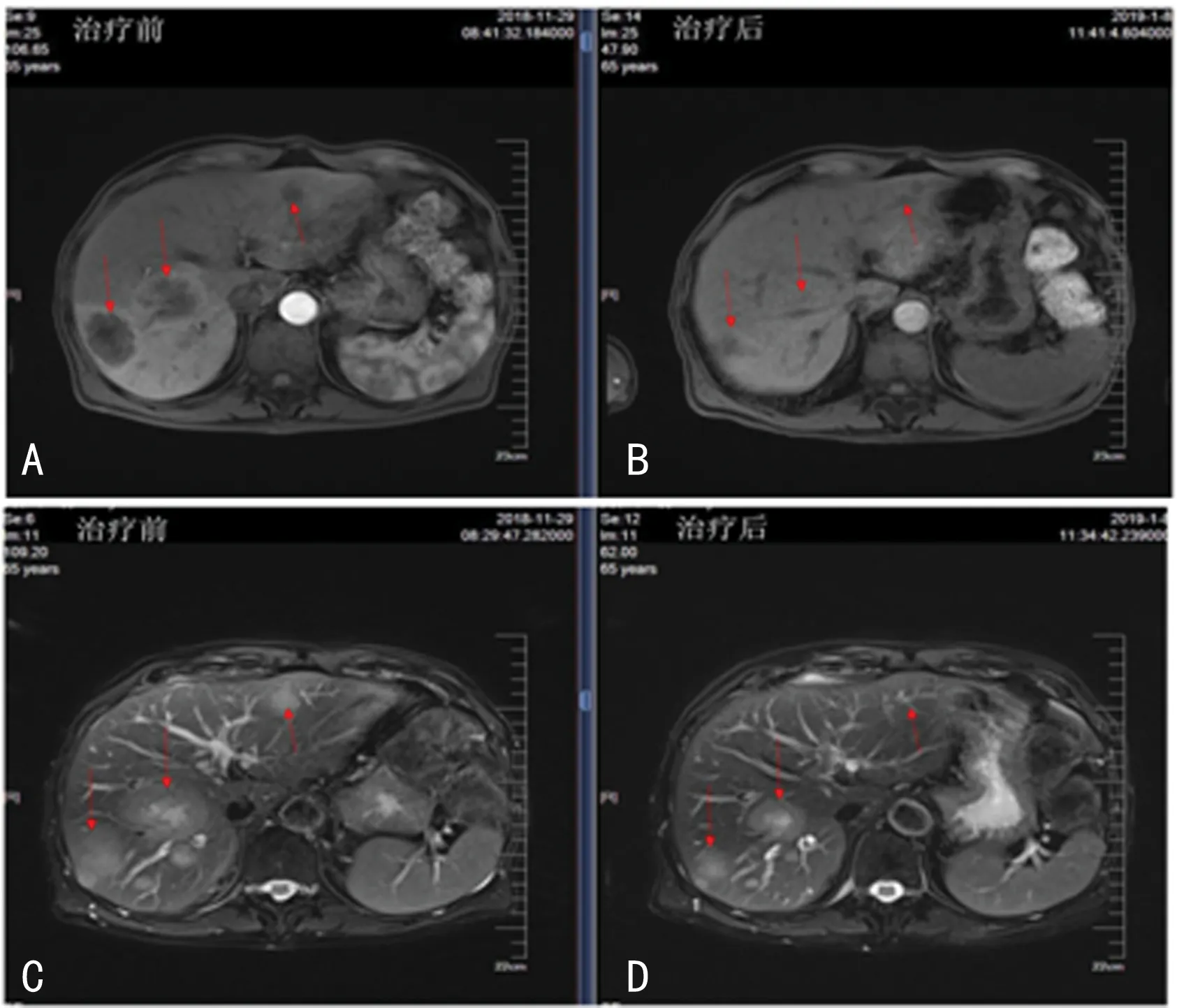
注:A.患者1治療前肝轉移灶;B.患者1治療后肝轉移灶情況; C.患者2治療前肝轉移灶; D.患者2治療后肝轉移灶情況。
2.32組患者不良反應發生情況比較 研究組患者粒細胞下降、肝腎毒性不良反應發生率均明顯低于對照組,差異有統計學意義(P<0.05);2組患者胃腸道反應、周圍神經不良反應發生率比較,差異均無統計學意義(P>0.05)。見表3。2組患者中出現皮疹者無需治療即可自發緩解。
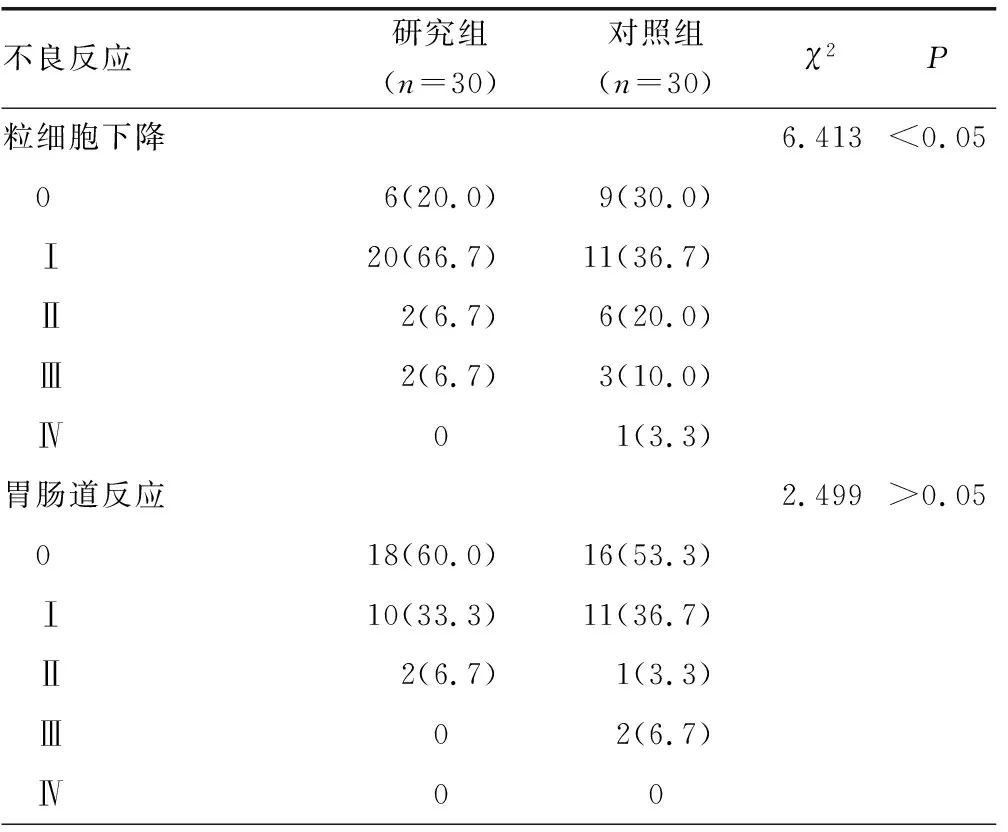
表3 2組患者不良反應發生情況比較[n(%)]
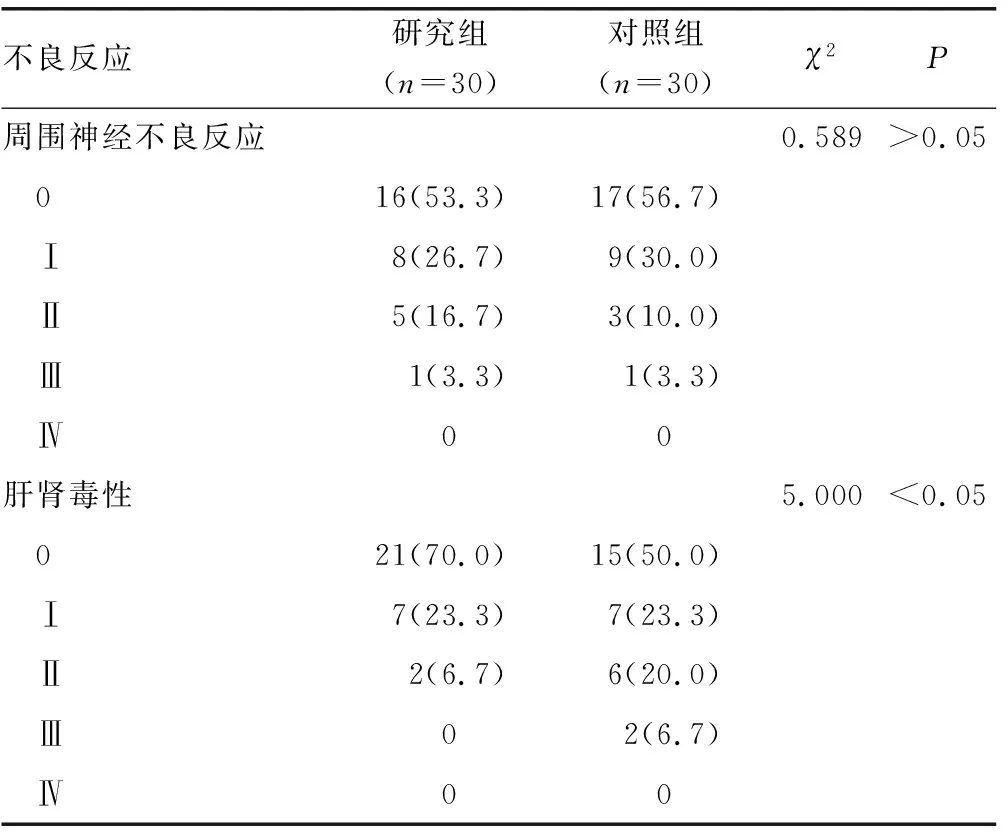
續表3 2組患者不良反應發生情況比較[n(%)]
2.42組患者治療后PS評分改善情況比較 研究組患者中治療后PS評分降低11例(36.67%),對照組患者中治療后PS評分降低5例(16.67%)。研究組患者生活質量改善率明顯高于對照組,差異有統計學意義(χ2=7.200,P<0.05)。
3 討 論
有研究表明,肝轉移在大腸癌患者中更為普遍,初診時8%~25%的大腸癌患者出現肝轉移;20%的患者在治療原發性腫瘤后出現[9]。肝臟的解剖學特征決定了其非常容易成為惡性腫瘤轉移和侵襲的靶標。對無法切除的結直腸癌肝轉移患者標準化綜合治療是目前臨床治療中的首選方法,包括化療、分子靶向藥物治療和熱療。
熱療不僅具有抗腫瘤作用,而且可加強化療的療效。因高溫可改善腫瘤組織血液供應和氧氣供應,所以,可逆轉某些化療藥物的耐藥性,還可增強化療藥物對細胞增殖的作用并通過調節腫瘤壞死因子相關凋亡誘導配體、腫瘤壞死因子和腫瘤壞死因子配體等促進細胞凋亡[4]。熱療作為一種結直腸癌綜合治療的新興方法,通常與放療或化療結合或3種方法結合使用。有研究發現,腫瘤細胞比正常細胞對熱損傷更敏感,對放療不敏感的腫瘤細胞通常處于S期或缺氧環境,對熱療高度敏感,熱療聯合化療具有協同的抗腫瘤作用[5]。熱療可改善人體對腫瘤細胞的免疫反應[7];熱療也會影響腫瘤相關基因如血管內皮生長因子表達,減少腫瘤的轉移和復發[10]。另外,高熱能通過影響腫瘤細胞中理化因子的作用增加腫瘤細胞中化療藥物的濃度,從而逆轉耐藥性[11]。當前包含納米粒子的高頻磁場熱療可增強化療藥物對腫瘤細胞的殺傷效果[12]。
本研究結果顯示,研究組患者總有效率(73.33%)明顯高于對照組(43.33%),治療后肝轉移性病變的影像學表現明顯改善,表明深部高溫療法與化療相結合提高了療效,其機制可能與溫度升高有關,當熱療治療時局部轉移灶細胞內鈣離子流入增加,鈣離子增加使膜流動性增高,從而影響細胞對藥物的滲透性[13]。同時,聯合治療也降低不良反應發生率。本研究結果顯示,研究組患者粒細胞下降、肝腎毒性不良反應發生率均明顯低于對照組;與對照組比較,研究組患者生活質量得到明顯改善。一方面熱療可增加免疫原性表面受體(如膜表面主要組織相容性復合物Ⅰ類鏈相關分子A、主要組織相容性復合物Ⅰ等)數量,進而增強自然殺傷細胞和CD8+細胞的作用和功能,提高患者自身免疫[14];另外熱療還可通過熱效應擴大腫瘤周圍正常組織血管,促進局部組織微循環和代謝活動,加速炎癥因子,如內皮素、白細胞介素-1、白細胞介素-6、緩激肽、腫瘤壞死因子-α、轉化生長因子的代謝,改善組織供氧,以達到止痛作用[15];并改善患者生活能力。患者癥狀的改善又可顯著改善患者睡眠質量,消除患者焦慮、緊張感,從而增加患者認知功能,如注意力集中,最終改善了患者的生活質量。本研究觀察2組患者不良反應發生情況時從血液學毒性角度看,2組患者均主要是Ⅰ級骨髓抑制。熱療和化療的結合并沒有加重結直腸癌肝轉移患者骨髓抑制程度。2組患者非血液學毒性——周圍神經不良反應、胃腸道反應(惡心、嘔吐、腹瀉等)發生率比較,差異均無統計學意義(P>0.05),表明熱療并沒有明顯增加化療不良反應。
綜上所述,深層熱療和化療相結合比單獨使用化療具有更好的效果。綜合治療是腫瘤療法未來發展的必然趨勢。在以往的研究中熱療被多次證實能增強化療的療效,本研究結果也符合該結論。而值得注意的是,本研究中一些接受熱療的患者肝轉移灶明顯縮小或有所減少,提示熱療可能可作為評價化療方案敏感性的依據,指導術后化療方案的選擇,如降低化療藥物的劑量或減少沒有必要的手術;同時,對一些接受熱療治療的患者也為化療提供了窗口期,以觀察有無新的或無法切除的轉移灶出現。另一方面,熱療結合輔助化療可能改善了患者的預后,本研究結果顯示,聯合熱療不會增加化療的不良反應,可減輕患者損傷且臨床癥狀也得到明顯改善。表明化療治療結直腸癌肝轉移患者時聯合深部熱療是一種選擇,可改善患者的臨床癥狀并減輕患者痛苦。